用于在内窥镜图像中显示肿瘤位置的方法与流程
相关申请的交叉引用
本申请要求2019年1月30日提交的美国临时专利申请第62/798,854号的权益和优先权,其全部公开内容通过引用并入本文。
背景技术:
相关技术的描述
随着技术的进步,外科医生已经开始用微创技术(诸如腹腔镜和胸腔镜手术)代替传统的开放式手术技术,以尽量最小化对周围组织的创伤,减轻疼痛,减少疤痕,以及缩短患者的住院时长。微创手术(诸如19世纪中期开创的胸腔镜手术)涉及使用小切口(一到数个),通常不超过3至10毫米。最初使用膀胱镜进行,医学技术的进步开发了在胸腔中使用的专用器械,例如胸腔镜,以在进行外科手术时观察胸腔内的解剖结构。在20世纪后期,发展了视频辅助胸外科手术(vats),其利用光纤内窥镜进一步减小执行手术所需的切口尺寸,并且提供了更清晰、更明确的胸腔图像。
同时,医学成像的进步使得临床医生能够更准确地描绘患者的解剖结构,从而更准确地识别疾病和任何患病组织的位置。这些进步使得临床医生能够更有效地利用微创外科技术,诸如上述胸腔镜手术。使用医学成像,诸如ct(包含x射线ct、计算机轴向断层摄影(cat)扫描、正电子发射断层扫描(pet)和单光子发射ct(spect)),临床医生能够准确地识别病变或其他医学状况,而不需要侵入性手术(诸如开放手术或开胸手术)。然而,由于现代成像模式能够识别越来越小的病变,这些病变可能是粘膜下的,并且在胸腔镜捕获的图像上不容易识别(例如,在胸腔镜图像上不可见),外科医生必须依靠用手指触诊组织来确定组织内病变的精确位置。可以理解,在微创手术期间用手指触诊组织不合期望的,因为需要附加的端口使外科医生的手指可以通过其来触诊组织。
为了缓解这个问题,重要的研究和开发集中在能够远程触诊的器械、识别组织内病变位置的算法、能够在器械靠近病变时通知外科医生的触觉反馈系统等。然而,这种系统依靠视觉以外的感官来识别病变相对于外科器械的位置。
技术实现要素:
本公开涉及一种显示手术部位内的感兴趣区域的方法,其包括对患者肺部进行建模,识别患者肺部模型内的感兴趣区域的位置,使用与内窥镜相关联的第一摄像头、光源和结构化光图案源来确定患者肺部的表面的形貌,在与内窥镜相关联的监视器上显示由与内窥镜相关联的第二摄像头捕获的患者肺部的实时图像(第二摄像头具有视场),使用所确定的患者肺部的表面的形貌将患者肺部的实时图像与患者肺部的模型配准,以及在患者肺部的实时图像上叠加指示患者肺部内感兴趣区域位置的标记,其中当第二摄像头的视场改变时,所述标记在患者肺部内保持静止。
在各方面,所述方法可以包含当感兴趣区域在第二摄像头的视场之外时,显示指示感兴趣区域相对于第二摄像头的视场所处方向的信息。
在某些方面,所述方法可以包含在患者体腔内推进内窥镜。
在其他方面,对患者肺部进行建模可以包含获取患者肺部的计算机断层摄影(ct)数据。
在某些方面,对患者肺部进行建模可以包含获取患者肺部的组织数据。
在各方面,所述方法可以包含将软件应用存储在与计算机相关联的存储器中,所述计算机具有配置为执行所述软件应用的处理器,所述软件应用在被执行时基于所述ct数据和所述组织数据创建患者肺部的模型。
在本公开的另一方面,提供了一种用于显示手术部位内的感兴趣区域的系统,所述系统包括计算机和与计算机和内窥镜相关联的监视器,所述计算机具有配置为执行软件应用的处理器,所述软件应用在被执行时创建患者肺部的模型。监视器配置为显示由与具有视场的内窥镜相关联的第一摄像头捕获的患者肺部的实时图像。处理器配置为确定患者肺部的形貌,使用所确定的患者肺部的表面的形貌将患者肺部的实时图像与患者肺部的模型配准,并且在患者肺部的实时图像上叠加指示患者肺部内感兴趣区域的所处位置的标记。当第一个摄像头的视场改变时,标记在患者肺部内保持静止。
在各方面,计算机可以包含存储器,用于存储与患者肺部相关联的计算机断层摄影(ct)数据和组织数据。
在某些方面,处理器可以配置为当感兴趣区域在第一摄像头的视场之外时,在监视器上显示指示感兴趣区域相对于第一摄像头的视场所处方向的信息。
在其他方面,内窥镜可以配置为在患者体腔内推进。
在各方面,处理器可以配置为获取患者肺部的计算机断层摄影(ct)数据。
在其他方面,计算机可以配置为获取患者肺部的组织数据。
在某些方面,内窥镜可以包括第二摄像头。在各方面,内窥镜可以进一步包括光源。在其他方面,内窥镜可以进一步包括结构化光图案源。
在其他方面,可以使用第二摄像头、光源和结构化光图案源来确定患者肺部的形貌。
根据本公开的又一方面,提供了一种显示手术部位内的感兴趣区域的方法,其包含指示与计算机相关联的处理器执行软件应用(所述软件应用在被执行时创建患者肺部的模型),在与计算机相关联的监视器上显示由与内窥镜相关联的第一摄像头捕获的患者肺部的实时图像(所述第一摄像头具有视场),以及指示处理器确定患者肺部的形貌,使用所确定的患者肺部的形貌将患者肺部的实时图像与患者肺部的模型配准,并且在患者肺部的实时图像上叠加指示患者肺部内感兴趣区域的所处位置的标记,其中当第一摄像头的视场改变时,标记在患者肺部内保持静止。
在各方面,所述方法可以包含当感兴趣区域在第一摄像头的视场之外时,在监视器上显示指示感兴趣区域相对于第一摄像头的视场所处方向的信息。
在其他方面,确定患者肺部的形貌可以包含使用与内窥镜相关联的第二摄像头、光源和结构化光图案源来确定患者肺部的形貌。
在某些方面,指示与计算机相关联的处理器执行软件应用可以包含获取患者肺部的计算机断层摄影(ct)数据和组织数据。
附图说明
下文参考附图描述本公开的各个方面和特征,其中:
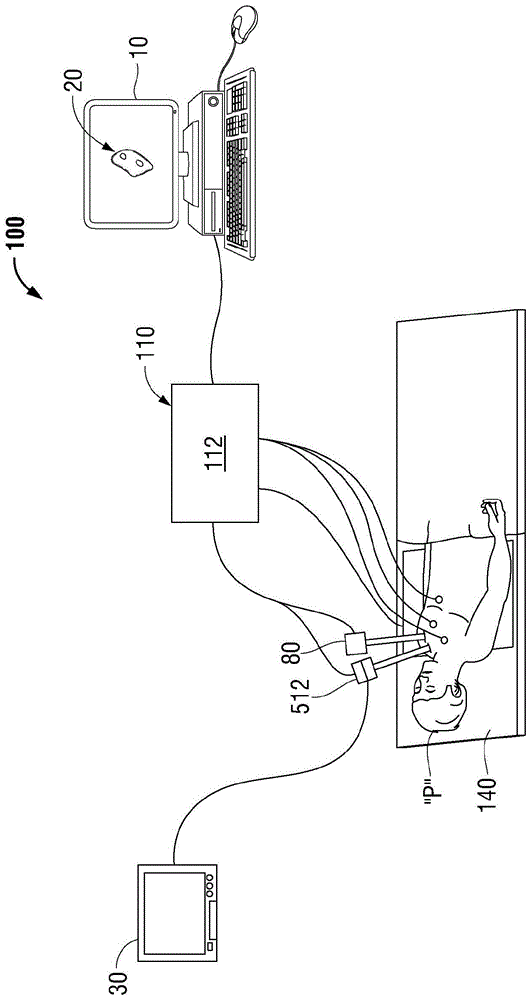
图1是根据本公开提供的系统的透视图,其配置为用于对肺部进行建模和治疗肺部内的感兴趣区域;
图2是示出根据本公开的对肺部进行建模和执行外科手术的方法的流程图;
图3a是患者肺部的3d模型的剖视图,示出了感兴趣区域以及高和低对比度密度细节;
图3b是患者肺部的3d模型的剖视图,示出了已经被区分和分组在一起的高和低对比度密度细节;
图3c是患者肺部的3d模型的剖视图,示出了已经被部分区分的高和低对比度密度细节;
图4是患者胸腔的3d模型的剖视图,示出了肺部和附着在其上的粘连;
图5是患者肺部的3d模型的剖视图,示出了其上应用有生成的网格的模型;
图6是患者肺部的3d模型的剖视图,示出了塌陷状态下的肺部;
图7是根据本公开提供的胸腔镜的透视图,其上设置有结构化光扫描仪;
图8是患者胸腔的侧剖视图,示出了推进其中的图7的胸腔镜;
图9a是图1的系统的用户界面的图示,显示了塌陷状态下的患者肺部,其上覆盖有塌陷肺部的3d模型;
图9b是图1的系统的用户界面的图示,显示了塌陷状态下的患者肺部,其上覆盖有塌陷肺部的另一个3d模型;
图9c是图1的系统的用户界面的图示,显示了塌陷状态下的患者肺部,其上覆盖有塌陷肺部的又一3d模型;
图10是图1的系统的用户界面的图示,示出了从图7的胸腔镜观看的摄像头视图;
图11是图1的系统的用户界面的图示,显示了患者胸腔的3d模型的剖视图,示出了肺部和附着在其上的粘连;
图12是图1的系统的用户界面的图示,示出了由图7的胸腔镜捕获的患者肺部的实时视图,并且图示了由叠加在患者肺部的实时视图上的标记指示的感兴趣区域;
图13是图1的系统的用户界面的图示,示出了由图7的胸腔镜捕获的患者肺部的实时视图,并且图示了叠加在患者肺部的实时视图上的箭头,所述箭头指示感兴趣区域相对于胸腔镜视场的所处方向;
图14是图1的系统的用户界面的图示,示出了临床医生操作患者肺部时从图7的胸腔镜观看的摄像头视图;以及
图15是根据本公开配置使用的机器人手术系统的示意图。
具体实施方式
本公开涉及用于显示手术部位内感兴趣区域的位置的方法和系统。如本文所描述,使用先前获得的患者肺部的计算机断层摄影(ct)数据来生成患者肺部的三维(3d)模型。使用任何合适的ct设备对患者进行成像,并且将数据存储在与计算机相关联的存储器中。存储在存储器中的软件应用由计算机执行,以使临床医生能够检查图像数据。通过检查图像数据,临床医生能够识别指示肺部疾病的感兴趣区域,并且确定其在患者的肺部内的位置。一旦临床医生识别出感兴趣区域和其位置,软件应用就处理图像数据,并且生成ct图像的3d重建或模型。可以理解,在胸腔镜手术过程中,有必要对患者肺部的一部分放气,以便在胸腔内为操作手术工具提供必要的空间。软件应用能够使用分割算法对塌陷状态下的患者肺部进行建模以界定各种类型组织的边界,并且基于它们的密度、连续性等将相似类型的组织分组在一起。以这种方式,增强患者肺部的3d重建的准确性,使得临床医生能够制定比通常可能使用的标准技术更准确的术前计划。
当开始外科手术时,临床医生使用套管针或任何其他合适的进入设备穿透患者胸部,并且除了诸如胸腔镜的第二手术工具之外,推进诸如镊子、外科缝合器等外科器械,以在外科手术期间捕获患者解剖结构的实时图像。胸腔镜包含能够将图案扫描到胸腔内的患者解剖结构上的结构化光扫描仪。此外,胸腔镜包含能够检测ir光的红外(ir)摄像头,以检测由结构化光扫描仪扫描到患者解剖结构上的图案。使用胸腔镜收集的信息,软件应用生成患者塌陷肺部的3d表面模型。以这种方式,软件应用能够更新塌陷肺部模型,并且提供塌陷状态下的患者肺部的更准确的模型。可以设想,软件应用可以向临床医生显示患者肺部的各种生成的3d模型,并且使临床医生能够选择最准确地描绘塌陷状态下的患者肺部的模型。附加地,不是将肺部的3d模型与结构化光扫描仪获得的扫描进行比较,而是预期3d模型可以与由胸腔镜获得的临床医生的实时视图进行比较。
使用由ir摄像头获得的位置数据,在结构化光扫描仪数据中检测各种特征点或基准点,诸如裂缝、韧带附件、粘连等。使用这一数据,3d模型可以与塌陷状态下的患者肺部的实时视图相关联或配准。以这种方式,感兴趣区域和其他结构可以叠加在患者肺部的实时视图上,以使临床医生能够更准确地治疗感兴趣区域并且避开位于患者肺部内的关键结构。感兴趣区域可以由标记(诸如红点,其叠加在患者肺部的实时视图上)表示,使得临床医生可以在体腔内和患者肺部内操纵外科器械的同时连续观察感兴趣区域的位置。在实施例中,标记可以叠加在患者肺部内,而不是其表面上,以更准确地描绘患者肺部内感兴趣区域的位置。
当临床医生相对于感兴趣区域操作胸腔镜时,标记保持位于感兴趣区域。以这种方式,当操作胸腔镜并且与胸腔镜相关联的摄像头的视场改变时,标记在患者肺部内保持静止。然而,如果临床医生操作胸腔镜,使得感兴趣区域不再在摄像头的视场内,软件应用将箭头或其他指示符叠加在患者肺部的实时视图上,指示感兴趣区域相对于摄像头的视场的所处方向。可以理解,箭头可以叠加在患者肺部的实时视图内的右、左、中、外、上、下位置。
尽管这里详细描述的系统和方法通常是针对肺部描述的,但是可以设想,以下系统和方法可以应用于肝脏、脾脏或任何其他器官。
现在参考附图详细描述本公开的实施例,其中在几个视图的每一个中,相同的附图标记表示相同或相应的元件。如本文所使用,术语“临床医生”指的是医生、护士或任何其他护理提供者,并且可以包括支持人员。在整个说明书中,术语“近端”指的是设备或其部件更靠近临床医生的部分,术语“远端”指的是设备或其部件更远离临床医生的部分。附加地,在附图和随后的描述中,诸如前、后、上、下、顶、底和类似方向术语的术语仅仅是为了描述方便而使用的,而不旨在限制本公开。尽管本文通常被描述为由临床医生执行的各种确定和/或选择步骤,但是可以设想,本文描述的确定和/或选择步骤可以由软件应用或者临床医生和软件应用输入的组合来执行。可以理解,在某些情况下,软件应用程序可能需要做出某些确定,而在其他情况下,临床医生可能需要做出某些确定。在实施例中,软件应用可以做出确定并且将所述确定呈现给临床医生以供选择和/或确认。在其他实施例中,软件应用可能需要向临床医生提供关于临床医生的决定的后果的提示或其他警告,或者向临床医生提供替代选择,或者其组合。在以下描述中,没有详细描述众所周知的功能或结构,以避免在不必要的细节中模糊本公开。
如图1中所示,下文描述的方法利用包含导航系统的系统100,所述导航系统能够将胸腔内的手术工具80和患者“p”的肺部“l”导向感兴趣区域“aoi”。导航系统包含跟踪系统110,其配置为与手术工具80一起使用,并且能够监视手术工具80的远端部分的位置和方向。系统100进一步包含计算机10和显示在与计算机10或合适的监视设备30(例如,视频显示器)相关联的显示器上的用户界面20。下文将进一步详细描述具有本文所述方法的系统100的作用和用途。
参考图2中描绘的流程图,描述了一种使用计算机断层摄影(ct)数据采用患者“p”的肺部“l”的生成模型来治疗患者的方法。最初,在步骤s100中,使用任何合适的ct设备(未示出),诸如x射线ct、计算机轴向断层摄影(cat)扫描、正电子发射断层摄影(pet)和单光子发射ct(spect)对患者“p”成像,并且成像数据存储在耦合到计算机10的存储器(未示出)中(图1)。存储器可以包含用于存储可由处理器(未示出)执行的数据和/或软件的任何非暂时性计算机可读存储介质,例如固态、易失性、非易失性、可移动和不可移动的。可以理解,图像可以经由有线或无线连接被存储在与诸如分布式网络或因特网的远程计算机或网络(未示出)相关联的存储器内,以用于向其他源发送数据和从其他源接收数据。可以进一步设想的是,图像可以存储在一个或多个可移动存储设备(未示出)上,诸如光盘、存储卡、zip盘或软盘、磁盘包、磁带、usb闪存驱动器、外部硬盘驱动器等。
在对患者成像之后,在步骤s102中,存储在存储器中的软件应用由与计算机相关联的处理器执行,以能够检查图像数据。这种应用的一个实例是美敦力plc目前销售的
参考图3a,结合图2,在步骤s106中,在步骤s100期间获得的图像数据由软件应用处理,并且使用本领域已知的任何合适的方法生成ct图像的3d重建。可以理解,在诸如下文所描述的胸腔镜手术过程中,有必要对患者肺部的一部分放气(例如,诱发肺部不张),以便在胸腔内为手术工具的操作提供必要的空间。如上文所描述,3d重建必然是完全充气的肺部的重建。因此,一旦外科手术开始,肺部的几何形状就会发生变化,导致在肺部和胸腔内所识别的感兴趣区域“aoi”的位置发生变化。因此,如下文详细描述的那样制定的术前计划必须补偿外科手术过程中改变的肺部几何形状。
为了补偿这种改变的几何形状,在步骤s108中,软件应用对塌陷状态下的患者“p”的肺部“l”进行建模。具体而言,软件应用使用分割算法来界定各种类型组织的边界,并且基于它们的密度和连续性以及其他因素将类似类型的组织分组在一起(图3b)。可以设想,软件应用可以利用任何合适的分割算法,诸如二元掩蔽、确定分离组织和背景的最佳阈值、自适应区域生长、波前传播等。
可以理解,软件应用可能无法区分所有不同的组织类型(图3c)。这样,软件应用能够选择性地切换动脉、静脉、支气管等,以校正任何不准确性。以此方式,软件应用将每个分割的组呈现为不同的颜色或不同的透明度级别,临床医生可以选择性地调整这些颜色或透明度级别,以便使临床医生能够更好地识别每个分割的或区分的组,或者在实施例中,可以将识别的结构呈现为不透明的,将未识别的结构呈现为半透明的,反之亦然。
为了进一步提高塌陷肺部重建的准确性,软件应用调整3d重建以考虑重力的影响(例如,患者在手术台140上的方向)和患者的脊柱在冠状面或额状面(例如,将患者“p”的身体分成腹侧和背侧部分的平面)中的曲率。胸腔内的其他结构(诸如粘连、病变等)影响肺部体积和肺部在患者胸腔内的位置(图4)。软件应用通过先前获得的患者“p”的肺部“l”的图像识别这些结构,并且在存在粘连的情况下通过迫使肺部“l”位于胸腔中更高的位置,通过将粘连固定到胸廓的固定边界并且应用弹性模型来确定位移或其组合来将这些结构的存在考虑在内。在替代方案中,软件应用可以识别粘连的去除,或者粘连的去除可以由临床医生手动输入合成器,并且软件应用将相应地重新调整模型(例如,肺部“l”将朝向肺门位于更远的位置)。
可以预见,软件应用可以估计更可能的肺部放气水平,因为肺部组织的弹性特性将受到常见肺部状况(诸如copd、患者的年龄、患者的吸烟状况等)的影响。附加地,软件应用可以考虑患者“p”可能经历的会影响整体肺部容积的先前外科手术。在识别肺部“l”内的各种结构之后,软件应用使用有限元分析(fea)算法来对肺部“l”进行建模,并且在显示器20上向临床医生呈现塌陷的肺部模型(图5和图6)。塌陷肺部的最终3d模型形成计算肺部模型(clm),所述模型是在术前规划、术中辅助和术后检查期间在显示器20或与计算机110相关联的监视设备上显示给临床医生的3d模型。
参考图7和图8,在已经开发了clm之后,在步骤s110中,临床医生可以通过使用套管针(未示出)或其他合适的进入设备穿透患者“p”的胸部来开始期望的过程,外科器械400(例如,镊子、外科缝合器、电外科器械、夹具施放器等)通过所述进入设备推进到患者“p”的体腔中。可以理解,第二手术工具在患者“p”的体腔内推进,以在外科手术过程中捕获患者的解剖结构的实时图像。在一个非限制性实施例中,第二手术工具是胸腔镜510或诸如内窥镜或腹腔镜的其他合适的设备,其能够在患者“p”的胸腔内推进,并且其上设置有结构化光扫描仪512(图7)。可以设想的是,胸腔镜510可以包含本领域已知的任何合适的结构化光扫描仪512,诸如发光二极管“led”或led红外激光器,或可见光led激光器,其以合适的方式设置在胸腔镜510上,以通过旋转镜、分束器或衍射光栅扫描图案(例如,线、网格、点等),或者可以是数字光处理(dlp)投影仪。在一个非限制性实施例中,结构化光扫描仪512是具有准直光的led激光器。胸腔镜510进一步包含设置在其上的ir摄像头514(图7),其能够检测ir光。可以设想的是,ir摄像头514可以是本领域已知的任何热成像摄像头,诸如铁电体、硅微测辐射热计、非制冷焦平面阵列(ufpa)等。可以进一步设想的是,设置在胸腔镜510上的各种传感器可以是具有相关联的硬件和/或软件的独立且不同的部件,或者可以是诸如
在步骤s112中,使用由胸腔镜510收集的信息,软件应用生成患者“p”的塌陷肺部“l”的3d表面模型。所述塌陷肺部的3d表面模型由软件应用用来更新clm并且提供塌陷状态下的患者“p”的肺部“l”的更准确的模型。在步骤s114(图9a-图9c),软件应用通过用户界面20向临床医生显示多个生成的患者肺部的3d表面模型。在步骤s116中,软件应用使临床医生能够选择最准确地描绘塌陷状态下的患者“p”的肺部“l”的肺部放气模型(图9a-图9c)。例如,图9a示出了塌陷状态下叠加在患者肺部扫描上的clm。图9b示出了在塌陷状态下最准确匹配患者肺部扫描的选定clm。图9c示出了临床医生使用手势来改变clm的形状和旋转,以更紧密地匹配塌陷状态下的患者肺部的扫描。在实施例中,临床医生可以实时改变clm的形状和旋转。以此方式,临床医生可以实时调节肺部的充气或放气量,调节肺部在胸腔内沿x、y和z轴中的每一个的旋转量等。
参考图10,可以进一步设想,在步骤s118中,不是将clm与由结构化光扫描仪512获得的扫描进行比较,而是可以将clm与由胸腔镜510获得的患者“p”的塌陷肺部“l”的临床医生的实时视图进行比较。以此方式,胸腔镜510包含摄像头516或设置在其远端部分的用于捕获视频图像的其他合适设备。可以理解,胸腔镜510可以是能够在视频辅助胸腔镜手术(vats)过程、图像引导视频辅助胸腔镜手术(ivats)过程或机器人辅助胸腔镜手术(rats)过程中使用的任何合适的胸腔镜。在实施例中,摄像头516可以是诸如数字光处理(dlp)系统的光学扫描系统(未示出),可以用于准确地确定塌陷状态下的患者“p”的肺部“l”的尺寸。
在步骤s120中,使用由ir摄像头514或光学扫描系统获得的位置数据,在结构化光扫描仪数据中检测各种特征点或基准点,诸如裂缝、韧带附件、粘连“a”、患者“p”的肺部“l”的表面高度或位于胸腔内的任何其他合适的特征点(图11)。在步骤s122中,一旦特征点被识别,计算这些检测到的特征点相对于塌陷clm中相应特征点的偏移。可以设想的是,可以使用任何合适的特征匹配算法来计算结构化光扫描仪数据和clm数据之间的特征点偏移,诸如尺度不变特征变换(sift)、旋转不变特征变换(rift)、广义鲁棒不变特征(g-rif)、加速鲁棒特征(surf)、主成分分析sift(pca-sift)、梯度位置定向直方图(gloh)、高斯-sift等。软件应用使用计算出的特征点偏移并且再生成clm以更准确地反映患者“p”的塌陷肺部“l”的观察状态。可以理解,当胸腔镜510在胸腔内相对于患者“p”的肺部“l”推进时,clm可以实时再生成。以此方式,合成器300的软件应用监视视觉陆标的位置,诸如裂缝、病变等,或者可以使用内部陆标,诸如结节(通过使用病变检测技术可识别)或基准点(未示出),这些基准点先前已经放置在患者“p”的肺部“l”中。在实施例中,软件应用可以检测患者“p”的肺部“l”中的病变,并且将病变作为自然基准点来处理,使得患者“p”的肺部“l”中的关键结构可以在clm中被识别。
在步骤s124中,当胸腔镜510在胸腔内推进时,视频图像被捕获并且传输到与计算机10或监视设备30(图1)相关联的监视器,提供患者“p”的塌陷肺部“l”的实时视图。在步骤s126中,在将clm与由胸腔镜510获得的患者“p”的塌陷肺部“l”的实时视图相关联或配准之后,感兴趣区域“aoi”和肺部“l”内的其他结构叠加在患者“p”的肺部“l”的实时视图上,以使临床医生能够更准确地治疗感兴趣区域“aoi”并且避开位于肺部“l”内的关键结构(图12)。在实施例中,感兴趣区域“aoi”可以由诸如红点的标记600(图12)表示,其叠加在患者“p”的肺部“l”的实时视图上,使得临床医生可以在体腔内和患者“p”的肺部“l”内操纵外科器械400的同时连续观察感兴趣区域“aoi”的位置。可以设想,标记600可以叠加在患者“p”的肺部“l”内,而不是叠加在患者“p”的肺部“l”的表面上,以更准确地描绘感兴趣区域“aoi”在患者“p”的肺部“l”内的位置。
在步骤s128中,可以设想当临床医生相对于感兴趣区域“aoi”操作胸腔镜510时,标记600保持位于感兴趣区域“aoi”。以此方式,当操作胸腔镜510并且胸腔镜510的摄像头516的视场改变时,标记600在患者“p”的肺部“l”内保持静止。然而,如果临床医生操作胸腔镜510使得感兴趣区域“aoi”不再在胸腔镜的摄像头516的视场内,则在步骤s130,软件应用将箭头610或其他指示符叠加在肺部“l”的实时视图上,指示感兴趣区域“aoi”相对于胸腔镜的摄像头516的视场的所处方向(图13)。可以理解,箭头610可以叠加在肺部“l”的实时视图中的右、左、中、外、上、下位置处。
可以进一步设想的是,clm可以反映由临床医生对肺部“l”的操作。如图14中所示,当临床医生使用任何合适的外科器械90(例如,手术钳等)操作肺部“l”的一部分时,可以更新clm以反映肺部“l”在胸腔内的当前位置。以此方式,可以更新肺部“l”和感兴趣区域“aoi”内的结构的位置,并且特别是更新代表感兴趣区域“aoi”的标记600(图12),以基于临床医生如何操作肺部“l”来反映它们的真实位置。
诸如本文所描述的内窥镜、计算设备和系统100的其他部件的外科器械也可以配置为与机器人外科系统和通常称为“远程外科手术系统”的系统一起工作。这种系统使用各种机器人元件来帮助外科医生,并且允许外科器械的远程操作(或部分远程操作)。各种机器人臂、齿轮、凸轮、滑轮、电动和机械马达等可以用于此目的,并且可以设计有机器人手术系统,以在手术或治疗过程中帮助外科医生。这种机器人系统可以包含远程操控系统、自动柔性手术系统、远程柔性手术系统、远程铰接手术系统、无线手术系统、模块化或选择性可配置的远程操作手术系统等。
机器人手术系统可以与一个或多个控制台一起使用,控制台靠近手术室或位于远程位置。在这种情况下,一队外科医生或护士可以为患者做手术准备,并且用本文公开的一个或多个器械配置机器人手术系统,而另一个外科医生(或外科医生组)通过机器人手术系统远程控制器械。可以理解,高技能外科医生可以在多个位置执行多个手术,而不离开他/她的远程控制台,这对于患者或一系列患者来说既具有经济优势又有利。
手术系统的机械臂通常通过控制器耦合到一对主手柄上。外科医生可以移动手柄,以产生任何类型的外科器械(例如,端部执行器、抓紧器、刀、剪刀、内窥镜等)的工作端的相应运动,这可以补充本文描述的一个或多个实施例的使用。主手柄的运动可以缩放,使得工作端的相应运动不同于、小于或大于由外科医生的操作手所执行的运动。缩放因子或传动比可以调节,以便操作者可以控制外科器械的工作端的分辨率。
可以设想,本文描述的系统可以由机器人系统定位,并且内窥镜的精确位置被传送到计算机,以构建扫描的器官或手术区域的3d图像。机器人系统具有自主扫描手术区域并构建所述区域的完整3d模型的能力,以帮助外科医生引导机器人臂或为机器人系统提供必要的3d信息,从而进一步自主地进行手术步骤。在内窥镜包含彼此独立的摄像头和结构化光源的实施例中,机器人系统可以分别引导摄像头和结构化光源。机器人系统提供了对结构化光和摄像头视图中的点进行三角测量以构建手术区域的3d表面所需的各个内窥镜之间的相对坐标。以此方式,机器人系统具有能够自主地将结构化光源定位到摄像头或摄像头内窥镜的视场上的特定优势。附加地或者可替代地,在机器人控制摄像头位置(或其他部件位置)的情况下,机器人可以移动摄像头(或其他部件)以扩大扫描的解剖结构的尺寸(例如,扫描的量),从而为用户(例如,外科医生)创建更大的视图而无需用户的输入或知识。
主手柄可以包含各种传感器,以向外科医生提供与各种组织参数或条件相关的反馈,例如,由于操作、切割或其他处理引起的组织阻力、器械对组织的压力、组织温度、组织阻抗等。可以理解,这些传感器向外科医生提供模拟实际操作条件的增强触觉反馈。主手柄还可以包括各种不同的致动器,用于精细的组织操作或治疗,进一步增强了外科医生模拟实际操作条件的能力。
参考图15,医疗工作站通常被示出为工作站1100,并且通常可以包含多个机器人臂1102、1103;控制设备1104;和与控制设备1104耦合的操作控制台1105。操作控制台1105可以包括显示设备1106,所述显示设备可以被设置为特别显示三维图像;和手动输入设备1107、1108,借助于这些手动输入设备,人(未示出)(例如,外科医生)能够在第一操作模式下远程操作机械臂1102、1103。
根据本文公开的几个实施例中的任一个,机器人臂1102、1103中的每一个可以包括通过关节连接的多个构件,以及附接设备1109、1111,例如,支撑端部执行器1120的手术工具“st”可以附接至这些附接设备。
机器人臂1102、1103可以由连接到控制设备1104的电驱动器(未示出)驱动。控制设备1104(例如,计算机)可以被设置成激活驱动器,特别是借助于计算机程序,以此方式使得机械臂1102、1103、它们的附接设备1109、1111以及因此手术工具(包含末端执行器1120)根据由手动输入设备1107、1108限定的运动来执行期望的运动。控制设备1104也可以以此方式设置使得其调节机器人臂1102、1103和/或驱动器的运动。
医疗工作站1100可以配置为用于躺在病床1112上的患者“p”,患者“p”将通过端部执行器1120以微创方式进行治疗。医疗工作站1100还可以包含两个以上的机器人臂1102、1103,附加的机械臂同样连接到控制设备1104,并且可以通过操作控制台1105远程操作。医疗器械或手术工具(包括末端执行器1120)也可以附接到附加的机器人臂。医疗工作站1100可以包含数据库1114,特别是与控制设备1104耦合的数据库,其中存储例如来自患者/活体为“p”的术前数据和/或解剖图谱。
虽然在附图中已经示出了本公开的几个实施例,但并不意味着本公开局限于此,因为意图是使本公开的范围与本领域所允许的一样宽,并且同样地阅读说明书。因此,上述描述不应被解释为限制,而仅仅是特定实施例的范例。
- 还没有人留言评论。精彩留言会获得点赞!