口服递送剂型水凝胶、其制备方法和使用方法与流程
口服递送剂型水凝胶、其制备方法和使用方法
相关申请
1.本技术要求2019年8月29日提交的美国临时专利申请62/893,529的优先权,其全部内容通过引用并入本文。
背景技术:
2.本公开主要涉及可水解降解的交联聚合物凝胶(也称为崩解水凝胶)用作能够封装和向有需要的患者口服递送用于营养、药物和/或兽医学目的的营养成分和/或治疗成分的口服剂型的用途。
3.环境响应性水凝胶先前已用于许多目的,包括但不限于药物递送(us9644039b2)、三维细胞培养基(p.m.kharkar,k.l.kiick,&a.m.kloxin,chem.soc.rev.,2013,42,7335)、地下采油(us20070281870a1,us20070277981a1)和固化环氧树脂(us10214479b2)。环境响应性聚合物也被设计用于靶向药物递送目的(us20090220615a1)(c.dingels,s.s.m
ü
ller,t.steinbach,c.tonhauser,h.frey,biomacromolecules 2013,14,448)。
4.能够对环境条件做出响应的交联剂的化学性质取决于应用和响应的相应时间尺度。生命科学领域中使用的化学物质的示例包括甲硅烷基醚、季戊四醇、原甲酸三甲酯和作为端基共价结合到甲基丙烯酸羟乙酯上的缩酮官能团(us20070281870a1;us20070277981a1;s.kim、o.linker、k.garth,k.r.carter.polym.degrad.stab.2015,121,303)、作为端基结合到胺上并通过二环氧化物交联的缩酮官能团(us10214479b2)、缩酮交联多羟基聚合物,例如聚乙烯醇、聚甲基丙烯酸羟乙酯和使用醛、酮、缩醛和/或乙烯基醚的多糖(us9644039b2)、具有额外短键如苄基或羟乙基的海藻糖二丙烯酸酯(m.burek,s.waskiewicz,a.lalik,i.wandzik,polym.chem.2018,9,3721)、通过巯烯点击化学法(k.wang,j.lu,r.yin,l.chen,s.du,y.jiang,q.yu,mater.sci.eng.c 2013,33,1261;k.wang,n.a.n.zhang,j.lu,r.yin,j.u.n.nie,q.yu,j.polym.mater.2014,31,89)或自由基聚合法交联(s.kaihara,s.matsumura,j.p.fisher,macromolecules 2007,40,7625)的环状缩醛、用丙酮形成的二羟乙基甲基丙烯酰胺缩酮(v.t.huynh,s.binauld,p.l.de souza,m.h.stenzel,chem.mater.2012,24,3197)或苯甲醛衍生物(us7056901 b2;n.murthy,y.x.thng,s.schuck,m.c.xu,j.m.j.fr
é
chet,j.am.chem.soc.2002,124,12398)、二羟乙基丙烯酸酯丙酮缩酮(y.wang,j.zheng,y.tian,w.yang,j.mater.chem.b 2015,3,5824;s.luan,y.zhu,x.wu,y.wang,f.liang,s.song,acs biomater.sci.eng.2017,3,2410)以及与丙烯酸二羟乙酯结合的甲硅烷基醚(m.c.parrott,j.c.luft,j.d.byrne,j.h.fain,m.e.napier,and j.m.desimone,j.am.chem.soc.2010,132,17928)。研究还证明了合成含有甲硅烷基醚官能团的聚合物(未交联)能够酸催化水解将聚合物降解为更小的聚合物(p.shieh,h.v.t.nguyen and j.a.johnson,nature chem.2019,11,1124)。
技术实现要素:
5.本公开涉及交联聚合材料(称为水凝胶)的化学组合物、制备方法和用作向有需要的患者口服递送具有营养、治疗作用和/或兽医学价值的化合物的口服剂型的用途,包括但不限于补充剂、基于细胞的治疗剂和活性药物成分。水凝胶包含两个主要成分:主链和连接或交联它们的可水解降解的键。这种设计独特地促进了(1)负载材料(例如食品级或药物级材料)在主链之间的水凝胶孔隙空间内机械化学稳定地封装,以及(2)通过可降解的键在酸性和/或中性流体(包括但不限于胃和胃肠道的胃肠液)中的降解(通过酸催化水解或酶催化裂解)实现水凝胶的快速崩解。水凝胶是通过聚合可水解降解的交联剂而产生的,该交联剂含有共价结合到可聚合基团的可降解键,在聚合反应完成时,该可聚合基团转化为主链。为了本公开的目的,可水解降解的交联剂(有时仅称为交联剂)被定义为一种含有可水解降解的键(有时仅称为键)的多功能化学品,其是一种含有一个或多个可水解降解的官能团的化学成分,其中该官能团与两个或多个可聚合的官能团共价结合。在键降解后,将其连接到交联剂的可聚合官能团的共价键得以保持。因此,主链由交联剂的可聚合官能团以及在聚合反应过程中存在于溶液中的任何其他可聚合单体(也简称为单体)形成。交联剂的键组分及其水解降解产物的亲水性质使得具有接枝/梳状结构的水溶性聚合物与水凝胶孔的负载材料一起释放。重要的是,交联剂化学成分包括生物相容性化学成分,例如但不限于聚乙二醇(也称为peg),以确保低毒性。如果主链还包含疏水性烷基链,例如丙烯酸十八烷基酯,则释放的梳状聚合物将具有表面活性剂的特性,这将有助于提高水凝胶的负载物的溶解度,特别是药物和/或食品级物质。
附图说明
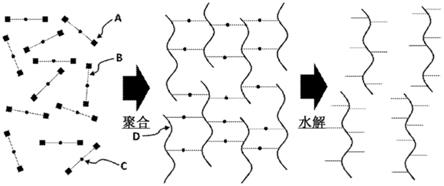
6.图1是本文所述的崩解水凝胶的聚合和随后的水解反应的示意图。
7.图2是崩解水凝胶内负载物的载药和药物释放的示意图。
8.图3是以不同的载药水平封装在由按体积计25%的缩醛交联剂组成的水凝胶中的维生素e(生育酚)在0.1m hcl溶液(ph=1)中的溶出曲线。维生素e最终浓度与固有溶解度的比值(x_sat)随载药水平的不同而变化。
9.图4是封装在由按体积计20%的缩醛交联剂和按体积计0%、15%或10%的表面活性剂组成的水凝胶中的非诺贝特在0.1m hcl溶液(ph=1)中的溶出曲线。
10.图5是封装在由按体积计20%的缩醛交联剂和按体积计15%或10%的表面活性剂组成的水凝胶中的孕酮在0.1m hcl溶液(ph=1)中的溶出曲线。
11.图6是几种不同载药水平的苯芴醇从由按体积计25%的乙缩醛交联剂组成的崩解水凝胶片剂释放到模拟胃液中的浓度的溶出曲线,与纯结晶苯芴醇进行比较(标记为“在缓冲液中”)。为了进行比较,该图还包括纯结晶苯芴醇释放到预崩解水凝胶片剂在模拟胃液中的溶液(标记为“聚合物溶液”)中的溶出曲线。
12.图7是二氟尼柳作为纯结晶材料释放与在低载药水平和高载药水平下从由按体积计25%的缩醛交联剂组成的崩解水凝胶释放相比,释放后二氟尼柳在模拟胃液中的浓度的溶出曲线。
13.图8是氯法齐明作为纯结晶材料释放与从由按体积计25%的缩醛交联剂组成的崩解水凝胶中释放相比,释放后氯法齐明在模拟胃液中的浓度的溶出曲线。
14.图9是视黄酸作为纯材料释放与在低载药水平和高载药水平下从由按体积计25%的缩醛交联剂组成的崩解水凝胶释放相比,释放后视黄酸在模拟胃液中的浓度的溶出曲线。
15.图10是辅酶q10作为纯结晶材料释放与从由按体积计25%的缩醛交联剂、按体积计0.7%的甲基丙烯酸甲酯、按体积计2.2%的甲基丙烯酸二甲氨基乙酯和按体积计1.1%的甲基丙烯酸丁酯组成的崩解水凝胶释放相比,释放后辅酶q10在模拟胃液中的浓度的溶出曲线。
16.图11是阿苯达唑作为纯结晶材料释放与从由按体积计25%的缩醛交联剂和按体积计30%的甲硅烷基醚交联剂组成的崩解水凝胶释放相比,释放后阿苯达唑在模拟胃液中的浓度的溶出曲线。
17.图12是两性霉素b作为纯结晶材料释放与从由按体积计25%的缩醛交联剂和按体积计30%的甲硅烷基醚交联剂组成的崩解水凝胶释放相比,释放后两性霉素b在模拟胃液中的浓度的溶出曲线。
18.图13是二十碳五烯酸作为纯材料释放与从由按体积计25%的缩醛交联剂组成的崩解水凝胶释放相比,释放后二十碳五烯酸在模拟胃液中的浓度的溶出曲线。
19.图14是阿托伐他汀作为纯结晶材料释放与从由按体积计25%的缩醛交联剂组成的崩解水凝胶释放相比,释放后阿托伐他汀在模拟胃液中的浓度的溶出曲线。
20.图15是布洛芬作为纯结晶材料释放与从由按体积计25%的缩醛交联剂组成的崩解水凝胶释放相比,释放后布洛芬在模拟胃液中的浓度的溶出曲线。
21.图16是尼罗替尼作为纯结晶材料释放与从由按体积计25%的缩醛交联剂组成的崩解水凝胶释放相比,释放后尼罗替尼在模拟胃液中的浓度的溶出曲线。
22.图17是蒽醌作为纯结晶材料释放与从由按体积计25%的缩醛交联剂组成的崩解水凝胶中释放相比,释放后蒽醌在模拟胃液中的浓度的溶出曲线。
23.图18是大麻二酚作为纯结晶材料释放与从由按体积计25%的缩醛交联剂组成的崩解水凝胶释放相比,释放后大麻二酚在模拟胃液中的浓度的溶出曲线。
24.图19是帕唑帕尼作为纯结晶材料释放与从由按体积计25%的缩醛交联剂组成的崩解水凝胶释放相比,释放到模拟胃液后帕唑帕尼在经过转变为禁食状态模拟肠液中的浓度曲线。
具体实施方式
25.本公开涉及交联聚合材料(称为水凝胶)的化学组合物、制备方法和用作向有需要的患者口服递送具有营养、治疗作用和/或兽医学价值的化合物的口服剂型的用途,包括但不限于补充剂、基于细胞的治疗剂和活性药物成分。水凝胶包含两个主要成分:主链和连接或交联它们的可水解降解的键。这种设计独特地促进了(1)负载材料(例如食品级或药物级材料)在主链之间的水凝胶孔隙空间内机械稳定地且化学稳定地封装,以及(2)通过可降解的键在酸性和/或中性流体(包括但不限于胃和胃肠道的胃肠液)中的降解(通过酸催化水解或酶催化裂解)实现水凝胶的快速崩解。水凝胶是通过聚合可水解降解的交联剂产生的,该交联剂含有共价结合到可聚合基团的可降解键,在聚合反应完成时,该可聚合基团转化为主链。为了本公开的目的,可水解降解的交联剂(有时仅称为交联剂)被定义为一种含有
可水解降解的键(有时仅称为键)的多功能化学品,其是一种含有一个或多个可水解降解的官能团的化学成分,其中该官能团与两个或多个可聚合的官能团共价结合。在键降解后,将其连接到交联剂的可聚合官能团的共价键得以保持。因此,主链由交联剂的可聚合官能团以及在聚合反应过程中存在于溶液中的任何其他可聚合单体(也简称为单体)形成。交联剂的键组分及其水解降解产物的亲水性质使得具有接枝/梳状结构的水溶性聚合物与水凝胶孔的负载材料一起释放。重要的是,交联剂化学成分包括生物相容性化学成分,例如但不限于聚乙二醇(也称为peg),以确保低毒性。如果主链还包含疏水性烷基链,例如丙烯酸十八烷基酯,则释放的梳状聚合物将具有表面活性剂的特性,这将有助于提高水凝胶的负载物的溶解度,特别是药物和/或食品级物质。
26.在更详细地描述本发明的组合物和方法之前,应理解本发明不限于所描述的特定过程、组合物或方法,因为它们可以变化。还应理解,描述中使用的术语仅用于描述特定版本或实施例的目的,并不旨在限制本发明的范围,本发明的范围将仅由所附权利要求限制。除非另有定义,否则本文使用的所有技术和科学术语具有与本领域普通技术人员通常理解的相同含义。尽管与本文所述的那些相似或等效的任何方法和材料可以用于本发明的实施例的实践或测试,但是现在描述优选的方法、装置和材料。本文提及的所有出版物均通过引用整体并入。本文中的任何内容均不应被解释为承认本发明无权因在先发明而早于此类公开。
27.还必须注意,如本文和所附权利要求中使用的,单数形式“一”、“一个”和“该”包括复数,除非上下文另有明确规定。因此,例如,“燃烧室”是指“一个或多个燃烧室”及其本领域技术人员已知的等同物,等等。
28.如本文所用,术语“约”是指与其一起使用的数字的数值的正负10%。因此,“约50”的意思是“在45-55的范围内”。
29.本公开涉及交联聚合材料(称为水凝胶)的化学组合物、制备方法和用作向有需要的患者口服递送具有营养、治疗作用和/或兽医学价值的化合物的口服剂型的用途,包括但不限于补充剂、益生菌、基于细胞的治疗剂和活性药物成分。水凝胶包含两个主要成分:主链和连接或交联它们的可水解降解的键。这种设计独特地促进了(1)负载材料(例如食品级或药物级材料)在主链之间的水凝胶孔隙空间内机械稳定地且化学稳定地封装,以及(2)通过可降解的键在酸性和/或中性流体(包括但不限于胃和胃肠道的胃肠液)中的降解(通过酸催化水解或酶催化裂解)实现水凝胶的快速崩解。在键降解后,将其连接到交联剂的可聚合官能团的共价键得以保持。因此,主链由交联剂的可聚合官能团以及在聚合反应过程中存在于溶液中的任何其他单体形成。交联剂的亲水性质确保它们在水溶液中的水合和随后的降解,使得具有接枝/梳状结构的水溶性聚合物与水凝胶孔的负载材料一起释放。以这种方式,可将较少水溶性或不溶性负载物递送至水性环境。如果主链还含有疏水性烷基链,如甲基丙烯酸甲酯、甲基丙烯酸乙酯、甲基丙烯酸丁酯、甲基丙烯酸十二烷基酯或甲基丙烯酸十八烷基酯或其丙烯酸酯衍生物,则释放的支化聚合物将具有两亲特性(类似于表面活性剂),这将有助于提高水凝胶的负载物的溶解度。一些实施例包括:
30.一种水凝胶基质,其含有能够在酸性至中性缓冲液中分解成水溶性降解产物的可水解降解的交联剂。对于立即释放,降解应在2小时内发生,而在特定胃肠道位置的释放可以通过调节降解速率和对ph的敏感性来调整。
31.一种可水解降解的足够疏水的水凝胶基质,用于封装负载物(例如基质中的有机液体溶液)并用于随后释放以获得营养和/或治疗效果。
32.水凝胶降解后释放的两亲聚合物化学物质产生类似于表面活性剂分子的特性,其可以提高与水凝胶降解产物伴随的从水凝胶中释放的负载物的溶解度。两亲聚合物结构的实例包括但不限于接枝有亲水链(例如聚乙二醇)的疏水聚合物主链(例如聚甲基丙烯酸酯)或接枝有疏水链(例如丙烯酸丁酯)的亲水聚合物主链(例如聚乙烯吡咯烷酮)。
33.合适的水凝胶基质包含单组分或多组分主链聚合物链,这些聚合物链通过与所述聚合物链共价连接的可水解降解的键连接。当水凝胶仅包含交联剂时,单组分聚合物链在水凝胶降解时释放,其中主链由交联剂的可聚合官能团组成。多组分聚合物链从含有交联剂和其他单体的水凝胶降解中释放出来。
34.可用作单体(即,其他聚合物组分)的化学物质的实例包括甲基丙烯酸、甲基丙烯酸甲酯、甲基丙烯酸乙酯、甲基丙烯酸丁酯、甲基丙烯酸二甲氨基乙酯、甲基丙烯酰胺、甲基丙烯酸羟乙酯、2-甲基丙烯酰氧基乙基三甲基氯化铵、聚乙二醇甲基丙烯酸酯、甲基丙烯酸鲸蜡酯、甲基丙烯酸月桂酯(或任何甲基丙烯酸酯组分的丙烯酸酯衍生物)、2-丙烯酰胺-2-甲基丙磺酸、乙烯基膦酸、n-乙烯基己内酰胺、n-乙烯基吡咯烷酮、乙酸乙烯酯和乙烯醇本身或作为其任何组合的共聚物。
35.交联剂在键内含有至少一个可水解降解的官能团,该键在ph 0至8、1至7、1至5或1至4范围内的酸性和/或中性条件下降解。
36.包含在交联剂中的示例性可水解降解的官能团包括但不限于缩醛、酸酐、硼酸酯、烯胺、腙、酰亚胺、亚胺、缩酮、肟、烷基甲硅烷基醚和甲硅烷基醚基团。
37.在一些实施方案中,可水解降解的键包含缩酮、缩醛、烷基甲硅烷基醚或甲硅烷基醚基团中的至少一种作为可降解官能团。在多个甲硅烷基醚基团的情况下,它们可以彼此分开,例如通过聚乙二醇,或者在多单元链段中构造为彼此相邻,例如聚二甲基硅氧烷。
38.在一些情况下,可水解降解的键是基于聚乙二醇的。
39.在一些实施方案中,可水解降解的交联剂包含一个或两个甲硅烷基醚、烷基甲硅烷基醚或聚硅氧烷作为可水解官能团。单一使用甲硅烷基醚或聚硅氧烷可以共价结合到两个聚乙二醇甲基丙烯酸酯部分(参见下面的式i)。
40.其中:
41.z是聚二甲基硅氧烷重复单元的数量,其中单个甲硅烷基醚表示为z=1,聚硅氧烷表示为z》2,并且
42.w表示可水解官能团和可聚合官能团之间的聚乙二醇单元数,其中w》2。
43.在一些实施方案中,z为3至7,可以在线性聚二甲基硅氧烷实体的任一侧上的两个烷基甲硅烷基醚基团水解后形成环甲硅油。因此,z值的范围可以为2至1000、2至100、2至20、3至20、3至10、3至7、4至7、4至6,或4至5。
44.包含通过接头彼此分开的两个甲硅烷基醚基团或两个聚硅氧烷链段的实施方案可以由在两侧与二甲基硅氧烷官能团结合的中心聚乙二醇单元组成,该二甲基硅氧烷官能团各自也与聚乙二醇甲基丙烯酸酯官能团结合(参见下面的式ⅱ)。
45.分隔两个可水解基团的中心聚乙二醇接头的重复单元的数量(式ii中所示的实施方案具有z=1的甲硅烷基醚基团或z》2的聚硅氧烷基团或两者的混合)由参数x表示,可以在1至1000、1至100、1至50、3至50、3至25或3至10的范围内变化。分隔可聚合官能团和可水解基团的聚乙二醇链的重复单元数(由下式ii中的甲基丙烯酸酯基团表示)由参数y表示,其中y可以在1至1000、1至100、1至50、2至50、2至25、2至10、3至25或3至10的范围内变化。
46.某些可水解官能团是各向异性的,因为它们仅具有一个可水解的共价键。这种类型的交联剂的一个实施方案,其中单个各向异性可水解基团是烷基甲硅烷基醚,可以由与甲基丙烯酰基丙基二甲基硅烷基团结合的聚乙二醇甲基丙烯酸酯组成(参见下面的式iii)。
47.在式iii中,参数v表示分隔可聚合基团(式iii中的甲基丙烯酸酯官能团)和各向异性可水解基团的聚乙二醇重复单元的数量,其中v可以在1至1000、1至100、1至50、1至25、1至10、2至50、2至25、2至10、3至50、3至25或3至10的范围内变化。
48.包含两个各向异性可水解基团的一个实施方案,其中两者都是烷基甲硅烷基醚基团,可以由两个甲基丙烯酰基丙基二甲基硅烷基团组成,所述两个甲基丙烯酰基丙基二甲基硅烷基团结合到具有任何分子量但优选足够大的聚乙二醇部分(参见下面的式iv)以产生足以实现高载药量的孔径。参数x与前面在式ii中定义的相同,表示在交联剂内分隔两个可水解基团的聚乙二醇重复单元的数量。
49.在一些实施方案中,可水解降解的交联剂包含缩醛和/或缩酮可水解官能团,而不是如前所述的基于硅烷的可水解官能团。一个实施方案包括分子量不小于约150g/mol(相当于参数x等于或大于3)的中心聚乙二醇链段,其中两个末端羟基连接到乙醛基团,乙醛基团是缩醛官能团,其同时结合至分子量不小于约174g/mol的peg甲基丙烯酸酯基团(相当于
参数y等于或大于2)(参见下式v)。
50.在一些实施方案中,酸催化的可水解交联剂的结构包含两个可水解缩酮官能团和两个可聚合甲基丙烯酸酯官能团。
51.在一些实施方案中,交联剂是三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)缩醛],其相当于下式v中参数x=3且参数y=9。当这种交联剂在前体溶液中(可聚合官能团聚合之前)以等于或高于约10%体积的浓度配制时,形成有效的崩解水凝胶,以确保形成机械稳定的聚合物网络,浓度等于或低于约35%体积则确保聚合物网络的水解解体,以大致实现封装在所述网络的孔内的负载物的完全释放。含有高于约35%浓度的组合物是未来实验的主题。
[0052]
其他合适的交联剂包括但不限于:丙酮二[甲基丙烯酰氧基聚(乙二醇)]缩酮(参见下面的式vi)和乙醛丙烯酰氧基乙醇甲基丙烯酰氧基聚(乙二醇)缩醛(参见下面的式vii)
[0053]
参数w与前面描述的含有基于硅烷的可水解官能团的可水解交联剂相同。式vii中所示的实施方案是各向异性可水解交联剂的实例,其中可水解官能团一侧的参数w的值为1,而另一侧的参数w的值可以是前述范围内的任何数字。由乙醛丙烯酰氧基乙醇甲基丙烯酰氧基聚(乙二醇)缩醛制成的水凝胶在合成过程中当交联剂在前体溶液中的体积分数高于约20%时不会完全降解。阻止水解的确切机制(例如,空间位阻、快速逆反应等)尚不确定。
[0054]
其他交联剂包括:丙酮二(丙烯酸羟乙酯)缩酮(参见下式viii)和丙酮二(甲基丙烯酸羟乙酯)缩酮(参见下式ix)。不希望受理论束缚,可水解缩酮官能团与这些交联剂的可聚合官能团的紧密接近阻碍但不阻止酸催化的水解反应,这使得药物释放较慢。此外,交联剂的小分子量降低了有机溶剂存在下的溶胀,因此导致封装在水凝胶孔隙中的负载物减少。
ppg-peg三嵌段共聚物和脂肪酸peg酯,其被改性为包括可聚合官能团,称为可聚合表面活性剂。在一些实施方案中,这些单体包含与非离子表面活性剂和可聚合官能团共价结合的可水解官能团,其被称为可水解表面活性剂单体。在一些实施方案中,表面活性剂是烷基聚乙二醇醚,例如但不限于peg-20硬脂醚。含有可聚合表面活性剂的水凝胶在水解后释放的聚合物中保留表面活性剂的疏水特性,而含有可水解表面活性剂单体的水凝胶在可水解官能团分解时分别释放表面活性剂和梳状聚合物。
[0068]
负载有包含活性药物成分的基于脂质的制剂的疏水改性的可水解水凝胶
[0069]
在一些实施方案中,水凝胶的空隙空间包含负载物,该负载物包含自乳化或自发胶束形成脂质溶液,该脂质溶液单独包含有机溶剂、疏水溶剂(油)、表面活性剂和助表面活性剂,或包含其任何可能的组合。在一些实施方案中,脂质溶液负载物还包含活性药物成分。
[0070]
制备可水解水凝胶并负载活性成分的方法
[0071]
图2是崩解水凝胶内负载物的载药和药物释放的示意图。负载物标记为a,连接主链聚合物链的键标记为b,键内的可水解官能团标记为c,主链聚合物链标记为d。负载后,负载物位于交联聚合物网络的孔内。水解后,两亲梳状聚合物链与负载物结合以提高溶解度。
[0072]
在一些实施方案中,本文所考虑的水凝胶是通过将极性(质子或非质子)溶剂与可水解降解的交联剂和引发剂(例如,光引发剂、热引发剂等)在均匀溶液中混合而产生的,然后添加到给定形状的惰性模具中并暴露于引发源(例如,uv灯、加热元件等)一段时间以诱导交联剂充分聚合成机械稳定的交联水凝胶。
[0073]
在一些实施例中,起始溶液包含按体积计15%至35%的交联剂三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)缩醛]和按体积计约5%的光引发剂2-羟基-2-甲基苯丙酮溶解在二甲基甲酰胺中,然后将其分散到硅胶模具中并暴露在365nm波长的灯下20分钟。
[0074]
该水凝胶的化学组成如下式x所示:
[0075]
含有式x所示结构的崩解水凝胶,在一些实施方案中,按摩尔计100%的交联剂三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)缩醛]的组合物在可水解官能团水解时,转化为具有下式xi所示结构的梳状聚合物,特别是聚(聚甲基丙烯酸乙二醇酯)聚合物。在水凝胶崩解时释放的该组合物或任何其他组合物的所得梳状聚合物的分子量可以从1000g/mol变化至1000000g/mol。含有式x结构的水凝胶分解的副产物包括三乙二醇和乙醛。
[0076]
在一些实施方案中,本文所考虑的水凝胶通过将极性(质子或非质子)溶剂与单官能单体、双官能可水解降解的交联剂和引发剂(例如,光引发剂、热引发剂等)在均匀溶液中结合,然后添加到给定形状的惰性模具中并暴露于引发源(例如,uv灯、加热元件等)一段必要的时间以诱导充分聚合将官能组分转化为机械稳定的交联水凝胶。
[0077]
在一些实施方案中,起始溶液包含按体积计约20%的交联剂三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)缩醛]、按体积计约10%的等摩尔的甲基丙烯酸二甲氨基乙酯和甲基丙烯酸甲酯溶液,以及约5%的光引发剂2-羟基-2-甲基苯丙酮溶解在二甲基甲酰胺中,然后将其分散到硅胶模具中并在365nm波长的灯下暴露20分钟。
[0078]
化学交联水凝胶的一个实施方案的化学结构,其包含优选的酸不稳定交联剂三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)缩醛]和疏水单体(甲基丙烯酸烷基酯)以及在水溶液中促进水合、溶胀和溶解的其他两种单体成分(甲基丙烯酸甲酯和甲基丙烯酸二甲氨基乙酯)。这种水凝胶的这种化学组成如下式xii所示。参数x和y与前面描述的相同,参数u表示在甲基丙烯酸酯基团和末端甲基之间的烷氧基甲基丙烯酸酯单体内的重复甲基单元的数量,可以为0至21,或1至17,或3至17。参数r是指用于引发和终止聚合过程的任何其他单体单元和/或官能团,分别例如光引发剂和溶剂。
[0079]
该组合物产生一种水凝胶,在洗涤以去除未反应的单体和光引发剂后,当添加到ph 1的水性缓冲液中时,该水凝胶将在不超过30分钟的时间内完全水解和溶解,条件是水凝胶的最小尺寸为约10mm以下。
[0080]
具有式xii的组合物的交联水凝胶在暴露于酸性水溶液时,由于键内的缩醛官能团的水解,将转变为具有式xiii所示组成的单独的聚合物链。
[0081]
在一些实施方案中,起始溶液包含按体积计15%至30%的交联剂三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)缩醛],按体积计1%至20%的可水解的表面活性剂单体,以及按体积计约5%的光引发剂2-羟基-2-甲基苯丙酮溶解在二甲基甲酰胺中,然后将其分散到硅胶模具中,并在365nm波长的灯下照射20分钟。该崩解水凝胶的所得化学结构显示在下面的式xiv中。参数x、y、u和r与前面描述的相同,参数q表示表面活性剂分子中包含的重复聚乙二醇单元的数量,可以为2至100或4至20。具有式xiv的组合物的交联水凝胶在暴露于酸性水溶液时,由于键内的缩醛官能团水解,将转变为具有式xi所示组成的单独聚合物链,但可能与具有不同参数值y的单体,因为在水凝胶合成过程中使用的可水解表面活性剂和可水解交联剂组成不同。含有式xiv所示的结构的水凝胶崩解的副产物包括三乙二醇、乙醛和用于合成可水解表面活性剂单体的非离子表面活性剂。
[0082]
一种将膳食成分或活性药物成分负载到通过上述方法合成的崩解水凝胶中的方法,其中将给定的活性成分溶解在极性(质子或非质子)溶剂中并将该溶液添加到含有水凝胶的模具中,溶剂被蒸发以将活性成分浓缩到水凝胶的孔隙空间中并最终去除所有或基本上所有的溶剂。
[0083]
该过程导致负载物,例如具有高于约20℃的熔化温度的膳食成分或活性药物成分(即,在室温下为固体)转化为平均尺寸为10nm至1000nm、10nm至500nm、10nm至300nm、10nm至100nm、20nm至500nm、20nm至300nm、20nm至100nm、小于300nm、小于200nm、小于100nm或小
于50nm的纳米晶体。
[0084]
遵循该过程的结果是形成负载有难溶性药物的可水解水凝胶,该药物随后可以在ph 1的酸性水溶液中在240分钟内、或120分钟内、或90分钟内、或60分钟内、或40分钟内、或30分钟内释放该药物,直至溶解度大于药物本身的饱和浓度。
[0085]
上述载药过程也可以用极性(非质子或质子)溶剂完成,该溶剂包含基于脂质的制剂混合物(包括但不限于甘油酯、表面活性剂和助表面活性剂和/或助溶剂),除活性药物成分外,使得在除去溶剂后,基于脂质的制剂和活性药物成分被包封在崩解水凝胶的孔隙空间中。所得崩解水凝胶药物产品将以乳液形式释放增溶聚合物、脂质制剂成分和活性药物成分,以提高活性药物成分的溶解度(见图1)。
[0086]
通过在聚合反应之前将所需细胞添加到极性溶剂、交联剂和引发剂的前体溶液中来实现基于细胞的治疗剂负载的崩解水凝胶。随后暴露于引发源,使交联剂聚合成水凝胶,其中细胞封装在所述水凝胶的孔隙空间中。
[0087]
通过在负载过程中控制活性药物成分、营养补充剂、兽药成分和/或基于细胞的治疗剂在溶液中的浓度,崩解水凝胶内的负载物的质量分数(即负载物的质量除以负载物和水凝胶的总质量)可以控制在1%至99%、5%至90%、10%至90%、15%至80%、20%至70%、20%至60%、20%至50%、30%至70%、30%至60%,或30%至50%的范围内。
[0088]
可水解水凝胶的化学多功能性使其成为与难溶性活性药物成分最广泛相容的口服剂型。可以修改水凝胶的化学成分,包括交联剂和任何所有单体,以最大限度地提高与任何化学负载物,特别是活性药物成分的化学相容性。用于溶解负载物的溶剂(例如活性药物成分)及其在该溶液中的浓度也可以调整,以最大限度地增加水凝胶的溶胀,从而最大限度地提高能够注入到水凝胶的孔隙中的负载物的量(按质量或体积计)。已经使用几种活性药物成分进行了研究,这些成分具有对口服药物递送过程中的溶解度和吸收而言至关重要的广泛化学性质,包括0.8至10.5范围内的亲脂分配系数(logp),-54℃至301℃范围内的熔化温度(tm),206g/mol至1203g/mol范围内的分子量(mw),0.01μg/ml至120μg/ml范围内的水溶性(c_s)。崩解水凝胶口服剂量也已被证明与广泛的化学类别相容,包括但不限于激酶抑制剂类、他汀类、激素类、抗氧化类、大环内酯类、非甾体抗炎类(nsaid)、抗感染类和血脂调节类。测试的药物及其相应参数总结在表1中。除了表1中列出的药物外,与可水解降解的水凝胶相容的活性药物成分的例子中nsaid类包括乙酰水杨酸、萘普生、非诺洛芬、酮洛芬、氟比洛芬、吲哚美辛、双氯芬酸、醋氯芬酸、甲芬那酸、托芬那酸和吡罗昔康;抗感染类包括万古霉素、克林霉素、红霉素、利奈唑胺、替加环素、强力霉素、利托那韦、洛匹那韦、替诺福韦、利匹韦林、依非韦伦、伊曲康唑、酮康唑、灰黄霉素和咪康唑;抗氧化类包括β-胡萝卜素、泛醌、番茄红素、植物甲萘醌、甲萘醌、钙化醇、胆钙化醇和姜黄素;大麻素类包括四氢大麻酚、大麻酚、大麻二酚、大麻色素、大麻二酚和大麻二环醇;血脂调节类包括二十碳五烯乙酯、二十二碳六烯酸、苯培多酸、氯贝特、辛贝特和吉非贝齐;他汀类包括瑞舒伐他汀、氟伐他汀、洛伐他汀、辛伐他汀和普伐他汀;激酶抑制剂类包括威罗非尼、瑞格非尼、奥希替尼、伊马替尼、索拉非尼、依鲁替尼、厄洛替尼、达沙替尼、奥拉帕尼、乐伐替尼和吉非替尼;大环内酯类包括红霉素、达托霉素、克拉霉素、卡波霉素a、螺旋霉素、他克莫司、西罗莫司、制霉菌素、克伦塔林、游霉素和可内酯;类视黄醇类包括视黄醇、依维a酸、阿维a、贝沙罗汀和阿达帕林;甾体激素类包括雌二醇、炔雌醇、依托孕烯、米非司酮、睾酮、地塞米松、泼尼松、加那松、布
雷克松龙、孕烯醇酮、醋酸阿比特龙、左炔诺孕酮、布地奈德和糠酸氟替卡松。
[0089]
图3-图19是上述负载物的溶出曲线。
[0090]
实施例1——合成二缩醛交联剂三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)缩醛]
[0091]
合成上述交联剂,其中聚乙二醇二乙烯基醚与2摩尔当量的聚乙二醇甲基丙烯酸酯加入到含有甲苯磺酸作为催化剂的二氯甲烷中,并在25℃下反应1小时。通过向甲苯磺酸中加入5摩尔当量的三乙胺来终止反应。反应溶液用等体积的1m氢氧化钠溶液洗涤以提取甲苯磺酸三乙铵盐和过量的三乙胺。将剩余的反应溶液干燥以除去残留的水,然后通过蒸发除去二氯甲烷来纯化产物。
[0092]
实施例2——使用基于二缩醛的交联剂合成崩解水凝胶
[0093]
通过将交联剂三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)缩醛]和光引发剂2-羟基-2-甲基苯丙酮分别按体积25%和5%溶解在二甲基甲酰胺中来制备前体溶液。一旦混合成均匀的溶液,然后将其分配到硅胶模具中并暴露在365nm波长的灯下20分钟。然后将半固态崩解水凝胶从模具中机械取出并在体积为凝胶体积5倍的乙醇中连续浸泡3次,以确保残留单体、光引发剂和二甲基甲酰胺的含量远低于每个组分原始含量的1%。
[0094]
实施例3——崩解水凝胶中的苯芴醇
[0095]
将不同体积的200mg/ml苯芴醇在二甲基甲酰胺中的溶液负载至全部由三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)乙缩醛]交联剂组成的水凝胶,产生一系列含有按重量计10%至59%的苯芴醇的水凝胶。将片剂溶解在模拟胃液中,导致高于苯芴醇天然溶解度的不同程度的过饱和度。所达到的最高过饱和度是载药水平为按重量计29%时饱和浓
度的13倍,如图6所示。
[0096]
实施例4——崩解水凝胶中的生育酚(维生素e)
[0097]
将不同体积的400mg/ml生育酚在乙醇中的溶液负载至全部由三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)乙缩醛]交联剂组成的水凝胶,产生一系列含有按重量计30.7%至63.2%的生育酚的水凝胶。将片剂溶解在模拟胃液中,导致高于生育酚天然溶解度的不同程度的过饱和度。药物释放后达到的相应过饱和水平为饱和浓度的约13倍至约74倍,如图3所示。
[0098]
实施例5——用活性药物成分负载崩解水凝胶并将其释放到生理相关缓冲液中
[0099]
首先由0.125ml含有按体积计25%的交联剂三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)乙缩醛]和按体积计5%的光引发剂2-羟基-2-甲基苯丙酮的二甲基甲酰胺溶液形成崩解水凝胶,然后通过在乙醇中洗涤数次进行纯化。然后将这种崩解水凝胶转移到相同的溶剂中,以最大限度地溶解目标活性药物成分。将水凝胶转移到硅树脂模具中并加热最少的时间以蒸发大部分浸入水凝胶孔中的溶剂。然后将溶解在优选溶剂中的活性药物成分的约0.1ml溶液添加到含有水凝胶的有机硅模具中,使其溶胀以吸收溶液。一旦吸收,在真空烘箱中除去溶剂以诱导活性药物成分在水凝胶孔中结晶。崩解水凝胶中包含的活性药物成分的质量通过实验确定,然后通过两种组分的组合质量进行归一化以量化活性药物成分的重量分数。几种活性药物成分的这些值总结在表1中标记为“药物重量百分比”的列中。
[0100]
分别在玻璃小瓶中,放置在带有设置为以每分钟150转的速度旋转的搅拌棒的搅拌板顶部每分钟填充一定体积(以ml计)的模拟胃液,该模拟胃液的量等于载药崩解水凝胶中所含的活性药物成分(以mg计)的量。将水凝胶添加到小瓶中并使其在2小时内溶解。通过紫外-可见光谱法监测水溶液中活性药物成分的存在,以量化相对于没有水凝胶存在的活性药物成分的固有溶解度的浓度。过饱和度为从崩解水凝胶中释放时达到的溶解度与在没有崩解水凝胶时溶解时达到的溶解度之比。几种活性药物成分的过饱和值汇总在表1中标记为“x_sat”的列中。
[0101]
如图所示,维生素e(生育酚)、非诺贝特、孕酮和苯芴醇,所有难溶性api封装在0.1m hcl溶液(ph=1)中酸催化水解可降解水凝胶的速释形式中,证明在40分钟内释放80%的封装药物。由于水凝胶降解产物的溶解度增强特性,每种药物的最终浓度分别达到了每种物质固有溶解度的74倍、351倍和11倍的过饱和水平。水凝胶标记为缩醛水凝胶[w/10%表面活性剂]{w/15%表面活性剂},是通过聚合含有按体积计25%[20%]{20%}的三乙二醇二[乙基-1-甲基丙烯酰氧基聚(乙二醇)缩醛]交联剂、按体积计0%[3.9%]{3.9%}的甲基丙烯酸甲酯、按体积计0%[6.1%]{6.1%}的甲基丙烯酸二甲氨基乙酯和按体积计0%[10%]{15%}的可水解表面活性剂单体:乙醛-(硬脂基peg-20醚)-(丙烯酸酯乙二醇)缩醛而合成的。首先将每种药物物质溶解在乙醇中并将有机溶液添加到含有预先形成和洗涤的水凝胶的硅树脂模具中,然后蒸发溶剂,从而将每种药物物质负载到水凝胶的孔中。将足够的药物物质溶液添加到模具中以达到一定范围的载药值。
[0102]
实施例6——合成可水解表面活性剂单体乙醛-(硬脂基peg-20醚)-(丙烯酸酯乙二醇)缩醛
[0103]
可水解表面活性剂单体乙醛-(硬脂基peg-20醚)-(丙烯酸酯乙二醇)缩醛的合成是通过首先合成中间体2-丙烯酰氧基-乙醇乙烯基醚来进行。该中间体是通过将丙烯酰氯
与1摩尔当量的乙二醇乙烯基醚(在二氯甲烷中)与3摩尔当量的三乙胺混合而合成的。使该溶液在25℃下反应12小时。从溶液中过滤得到氯化三乙铵盐,通过蒸发除去残余的三甲胺和二氯甲烷,得到粗中间体。
[0104]
在含有甲苯磺酸作为催化剂的溶剂二氯甲烷中,混合2-丙烯酰氧基-乙醇乙烯基醚与1摩尔当量的非离子表面活性剂硬脂基peg-20醚以合成可水解表面活性剂单体产物。使该溶液在25℃下反应1小时。通过向甲苯磺酸中加入5摩尔当量的三乙胺来终止反应。反应溶液用等体积的1m氢氧化钠溶液洗涤以萃取甲苯磺酸三乙铵盐和过量的三乙胺。将剩余的反应溶液干燥以除去残留的水,然后通过蒸发除去二氯甲烷来纯化产物。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1