一种治疗Ⅱ型糖尿病的中药组合物及其制备方法与流程
本发明属于中药技术领域,涉及一种中药组合物及其制备方法,具体涉及一种预防或治疗ⅱ型糖尿病的中药组合物及其制备方法。
背景技术:
糖尿病是一种复合病因的综合病症,是胰岛素绝对或相对不足,或伴有胰岛素抵抗所引起的糖、脂肪、蛋白质、水和电解质等一系列以高血糖为主要特征的代谢紊乱综合症,其高血糖特征的长期存在,会导致各种组织,特别是眼、肾、心脏、血管、神经的慢性损害、功能障碍。近年来,随着我国经济、社会发展水平的迅速提高,人民饮食结构改变、生活节奏加快、老龄化趋势加重、肥胖人群比例增加,促使我国糖尿病出现爆发性增长,成为继肿瘤和心血管疾病之后死亡率最高的疾病,严重威胁着人类的健康,甚至生命。
在我国,糖尿病以ⅱ型糖尿病为多见,至2013年患病率就已达到10.4%,其症状多为多饮、多尿、多食、疲乏无力和肥胖等。然而,目前临床上治疗糖尿病的口服药物磺脉类、双肌类和α-葡萄糖普酶抑制剂类等,长期服用往往会对肝、肾造成不同程度的损害。中药在我国用药历史悠久,尽管较西药而言起效稍慢,但其多成分多靶点的治疗机理决定,其具有标本同治、疗效显著且持久、副作用小、复发率低、不存在药物依赖等优势,显现出很大的研究价值和发展潜力。
中医认为,糖尿病的病机有阴虚火旺、气阴两虚、阴阳俱虚、脾虚湿盛、癖血阻络等,其病变涉及多个脏腑,以脾、肺、胃、肾为多见。中国专利cn200410073959.4公开了参芪降糖方在制备糖尿病药物中的用途。其临床应用显示该方对糖尿病具有显著的治疗作用,副作用低,有广阔的医疗应用前景,现已获得生产批准,产品为“参芪降糖颗粒”。该产品由人参皂苷、山药、天花粉、覆盆子、茯苓、麦冬、五味子、枸杞子、黄芪、地黄、泽泻11种药材组方,作用温和,不会引起血糖骤然下降。该产品用于糖尿病早期治疗时,由于血糖波动幅度小,可以很好地稳定血糖。
此外,组方中天花粉具有清热泻火,生津止渴,排脓消肿的功效,但其有效成分的含量和药效均需要一定的生产周期来保证,生产周期难以缩短,采挖出土、去皮晾晒费时费力,价格较不稳定,药农种植积极性低,产量供应不足;覆盆子能有效保护肾阳虚,延缓体内血糖上升值,但其有效成分的含量需要在夏初果实由绿变绿黄时采收才能得到保证,而农户间对颜色的判断存在主观差异,实际操作过程中采收时间往往较随意,导致药材质量参差不齐,不合格率高,影响临床疗效。因此,临床上亟需提供一种药材价格低廉,供应充足、药效发挥稳定的中药组合物来制备ⅱ型糖尿病。
技术实现要素:
本发明是针对参芪降糖方临床用药受限,以及组方中天花粉产量低、价格高和覆盆子质量不均一、合格率低的问题,本着科学审慎的态度,本发明在专利cn1245198c的基础上,提供一种治疗ⅱ型糖尿病的中药组合物及其制备方法,使之既具有更好的参芪降糖主治功能和临床疗效,又可用其它药味替代天花粉及覆盆子,从而避免可能存在的原料药材供应和质量问题。
本发明的第一方面在于提供一种预防或治疗ⅱ型糖尿病的中药组合物,所述中药组合物由人参皂苷、白术、地黄、黄芪、山药、芦根、麦冬、五味子、枸杞子、泽泻、茯苓、葛根、知母和山茱萸制备而成,具有益气养阴、补脾益肾、清热生津、活血化瘀之功效,可用于治疗ⅱ型糖尿病。以供给充足且药效稳定的知母、葛根和芦根对原组方中天花粉进行针对性有效替代,并结合糖尿病阴阳俱虚、癖血阻络特点,以山茱萸替代处方中的覆盆子补益肝肾,同时增加白术养气、燥湿、化浊功效,使之既能保留参芪降糖颗粒功能主治与确切的临床疗效,又能较大增加降糖效果,作为临床独立降糖用药,同时克服原料药材供应和质量问题,提高药物品质和性价比,增强患者依从性。
本发明的技术目的是通过以下技术方案实现的:
一种治疗ⅱ型糖尿病的中药组合物,由下列中药组分制成:
优选地,上述中药组合物由下列中药组分制成:
在一个优选的实施方式中所述的中药组合物包括如下组分:
优选地,所述的地黄为生地黄。
中医认为糖尿病属“消渴病”范畴,消渴之疾,病在三焦。气血以脾胃为生化之源,以三焦为通道,布达全身,“三焦燥热怫郁而气衰也”,气郁化热,耗伤阴津,阴伤及气,渐致气阴两虚,气行则血行,气滞则血瘀,气虚帅血无力,燥热煎熬阴液,则瘀血内阻,经络不通。可见,糖尿病证候分布为血瘀证、气阴两虚证、阴虚燥热证等。故本发明以清热润燥、补脾益肾、益气养阴、活血化瘀为治则。
“消渴病”的发生发展与脾胃功能密切相关,脾虚可导致痰浊瘀血,脉络痹阻等,为发病关键。处方中,人参皂苷为人参的活性成分,人参性甘、微苦,平,有大补元气、补脾益肺之功,起到扶正固本的作用,《本草汇言》谓之“补气生血,助精养神之药也”,用于主治因虚致瘀。地黄,性味甘、苦,性寒,有清热凉血、养阴生津之功效,用其主治阴虚火旺。两者合用,能使气旺而阴津得以化生,津液生则渴可止。再者,现代研究表明,人参和地黄均具有降低血糖的作用,故选上二味药为君。
黄芪,甘温,善入脾胃,长于补中益气、利水退肿;白术,甘苦性温,有健脾益气的作用,两者同用,增强人参补气生血功效。知母,性甘寒质润,有清热泻火,生津润燥之功,《神农本草经》称其“主消渴热中,除邪气,肢体浮肿,下水,补不足,益气”,现代研究证实,其所含知母聚糖a、b、c、d均有降血糖作用;葛根,味甘、辛,性凉,能解肌退热,透疹,生津止渴,《医学中衷参西录》中黄芪同用能补气生津,促进津液生成与输布而止渴;芦根,性味甘寒,有清热泻火,生津止渴之功效,三者性味相合、相辅相成,共行清热润燥之功。麦冬,性甘,微苦寒,有养阴生津之功,可助地黄化生津液,现代医学亦证实口服其水、醇提取物有降血糖作用。泽泻,味甘、淡,性寒,有利水渗湿,泄热,化浊降脂之功,用以主治ⅱ型糖尿病常见的肥胖症状,因此以上六药共为臣药。
山药,性味甘平,既补脾益气,又滋养脾阴,用其与人参、白术相伍,加强治疗气阴两虚的作用,为辅佐之药。枸杞子,性味甘平,具有滋补肝肾,益精明目之功;山茱萸,性酸涩微温,具补益肝肾之效,现代研究证实此两药均具有降血糖的功效,与地黄配伍,补肾摄精,肝肾两益,加强治疗阴虚消渴之力,故为辅佐之药。五味子,性酸、甘,温,甘以益气,酸能生津,与黄芪、山药相伍,加强补虚强阴、益气生津止渴力量,也为佐药。
茯苓,味甘、淡,性平,能入络,有利湿去热,通利关节之功,用其引方中诸药入经,深入百络,以达病灶,故为使药。上述诸药相合,药材之间相须或相佐,依据中医“君臣佐使”理论三焦并理,共奏清热润燥、补脾益肾、益气养阴、活血化瘀之功,相对参芪降糖原处方具有更强药力及更大的适用范围。
本发明另一个技术目的在于提供一种含有上述中药组合物的制备方法,所述制备方法包括以下步骤:
a、取白术、知母、山药和茯苓粉碎成细粉ⅰ备用;
b、麦冬用5~10倍量温水浸渍1-3次,每次0.5-3h,滤过,合并滤液,减压浓缩,并浓缩成相对密度1.30~1.40(55-60℃)的浸膏ⅰ,备用;
c、五味子用8-12倍量40-70%乙醇渗漉,滤过,减压回收乙醇,浓缩成相对密度为1.30~1.40(55-60℃)的浸膏ⅱ备用;
d、山茱萸、知母、芦根、枸杞子、黄芪、地黄、泽泻和葛根用5~10倍量水煎煮1-3次,每次0.5-3h,滤过,合并滤液,滤液减压浓缩至相对密度为相对密度1.15~1.25(55-60℃)的稠膏,放冷,加入乙醇,使醇含量为40%-80%,静置,滤取上清液,回收乙醇,浓缩成相对密度1.30~1.40的浸膏ⅲ,备用;
e、将浸膏ⅰ、ⅱ、ⅲ合并,加入细粉ⅰ及人参皂苷,混匀制备成临床上可接受的口服制剂。
优选地所述的临床上可接受的口服制剂包括但不限于丸剂、颗粒剂、胶囊剂、片剂。
例如将浸膏ⅰ、ⅱ、ⅲ合并,加入细粉ⅰ及人参皂苷,混匀,采用泛制法制丸,干燥,打光,即得丸剂;
或将浸膏ⅰ、ⅱ、ⅲ合并,混匀,干燥,粉碎成细粉后,再与细粉ⅰ及人参皂苷混匀,按照常规制剂工艺加入适量糊精和适量羧甲基淀粉钠,混匀,制粒,干燥,即得颗粒剂;
或将浸膏ⅰ、ⅱ、ⅲ合并,混匀,干燥,粉碎成细粉,再与细粉ⅰ及人参皂苷混匀,按照常规制剂工艺加入适量糊精和羧甲基淀粉钠混匀后,制粒,干燥,再加入氢氧化铝、硬脂酸镁适量,混匀,压片,包薄膜衣,即得片剂;
或将浸膏ⅰ、ⅱ、ⅲ合并,混匀,干燥,粉碎成细粉,再与细粉ⅰ及人参皂苷混匀,按照常规制剂工艺加入适量糊精和羧甲基淀粉钠混匀后,制粒,干燥,加入微粉硅胶,灌装,磨光机中抛光,剔除破损胶囊,即得胶囊剂。
优选地,步骤2)麦冬用6倍量温水浸渍二次,每次2小时;减压浓缩成的浸膏ⅰ相对密度为1.40。
优选地,步骤3)五味子用10倍量50%乙醇渗漉;浓缩成相对密度为1.40的浸膏ⅱ。
优选地,步骤4)山茱萸、知母、芦根、枸杞子、黄芪、地黄、泽泻、葛根加8倍量水煎煮二次,每次2h,滤过,合并煎液,减压浓缩至相对密度1.20(55-60℃)的稠膏,加入95%的乙醇使含醇量达60%,冷藏24h,滤过,滤液回收乙醇,浓缩成相对密度1.40(55-60℃)的浸膏ⅲ。
本发明第三目的在于提供所述中药组合物在制备治疗ⅱ型糖尿病药物中的用途。
本发明的中药组合物有效避免可能存在的原料药材供应和质量问题,原料供应充足,价格低廉,药效发挥稳定。为验证本发明中中药组合物治疗ⅱ型糖尿病的功效,发明人开展了药效学试验研究。需要说明的是,本发明药品药效学试验所选取的药品为本发明具有代表性的配方及其制备方法所得的药品,本发明所包含的其它配方及制备方法所得药品涉及的试验及其结果,由于篇幅限制,在此不穷举。
实验例1参芪降糖改方对小鼠血糖、饮水量、摄食量和糖耐量的影响实验
1实验材料
1.1实验动物
40只12周龄的雄性db/db小鼠均购买自南京君科生物工程有限公司(符合国家动物标准,实验动物许可证号:scxk(鲁)2014007),按照spf级饲养标准适应性喂养1周,期间自由摄食、饮水。1周后将动物禁食8h后于spf室内称重,并将db/db小鼠和野生型小鼠随机各分为4组,即安慰剂组、改进方组、原处方组和二甲双胍组。
1.2材料和仪器
改进方为实施例2参芪降糖颗粒,原处方为鲁南厚普制药有限公司中成药产品参芪降糖颗粒(国药准字z10950075),20%葡萄糖溶液(上海联硕生物科技有限公司),盐酸二甲双胍片(中美上海施贵宝制药有限公司,国药准字h20023370);强生稳豪倍优型血糖试纸和强生稳豪倍优型血糖仪(美国强生公司)。
2实验方法
2.1给药
每日8时,按照0.4ml/只,分别给安慰剂组、改进方组、原处方组和二甲双胍组灌胃生理盐水、实施例2参芪降糖颗粒(0.45g/kg)、鲁南厚普制药有限公司参芪降糖颗粒(0.45g/kg)和盐酸二甲双胍片(0.13g/kg),持续4周。记录给药前一周和给药后4周的摄食量和饮水量。
2.2空腹血糖的测定
分组后,禁食8h,期间不限饮水,用剪尾法剪掉小鼠尾部约1mm,使尾静脉血自然流出,并用强生稳豪倍优型血糖仪测量各组动物的基础血糖值(第0天)。之后,每周结束(第7、14、27、28天)以同样的方法测定血糖并记录。
2.3葡萄糖耐量的测定
4周治疗结束,所有小鼠禁食不禁水16h后,按照2μl/kg体重的标准,给每只小鼠腹腔注射浓度为400mg/ml的葡萄糖溶液,注射葡萄糖后0min,30min,60min,120min采用尾静脉取血的方式测定小鼠的血糖值并计算血糖应答曲线下面积(areaundercurve,auc)。
2.4统计学分析
全部实验数据均采用graphpadprism软件版本5(graphpadsoftware,美国)进行统计学处理,结果均以平均数±标准差表示。p<0.05被认为有显著性差异。
3结果
3.1参芪降糖改进方干预前后血糖变化
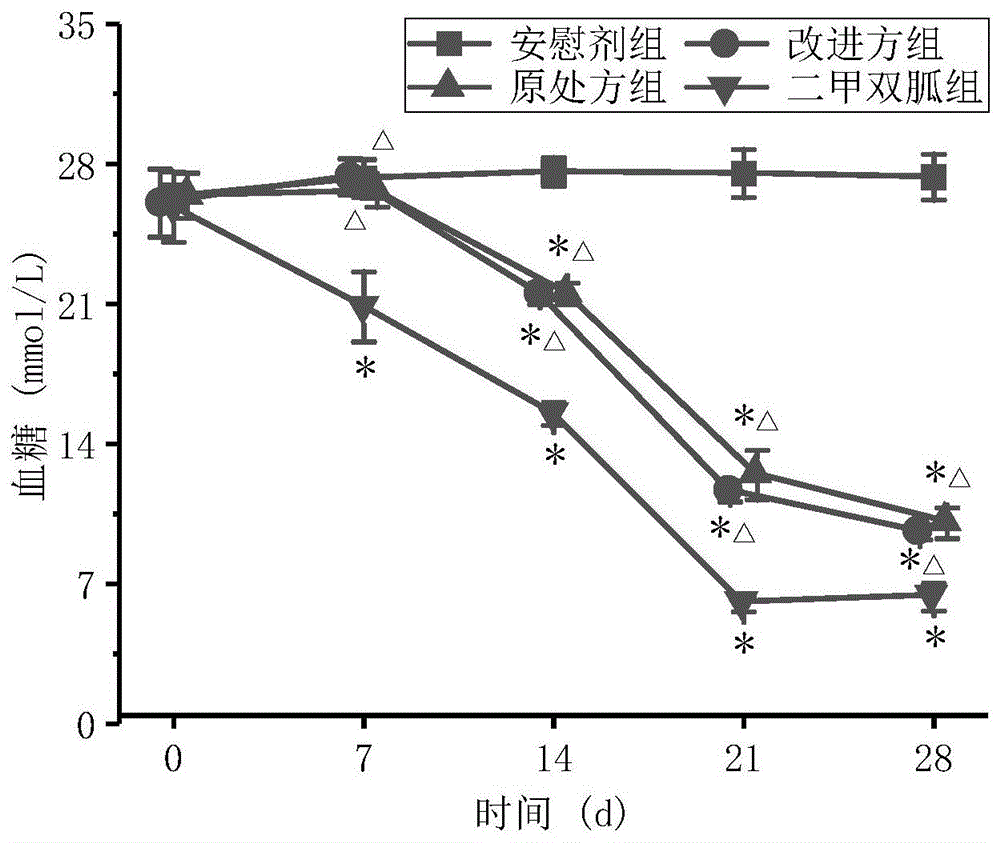
如表1、图1血糖检测结果所示,参芪降糖改进方干预前(第0天),各组动物基础血糖值均在11.1mmol/l以上,满足高血糖的要求,为患糖尿病小鼠。随着药物干预时间的延长,改进方组、原处方组和二甲双胍组小鼠的血糖均呈逐渐下降的趋势。对药物干预后各组小鼠血糖值进行统计学分析显示,相比安慰剂组,药物干预后第7天起,二甲双胍组小鼠的血糖开始显著降低(p<0.05),第14天起,改进方组和原处方组小鼠的血糖开始显著降低(均p<0.05);药物干预开始7天后,二甲双胍的降血糖效果均明显优于原处方和改进方(均p<0.05);药物干预后第21天起,改进方组血糖的平均值比原处方组略低,但无统计学意义(均p>0.05)。
表1参芪降糖改进方干预前后空腹血糖变化(n=10,
注:“*”表示与安慰剂组比较p<0.05,“△”表示与二甲双胍组比较p<0.05。
3.2参芪降糖改进方干预前后摄食量变化
摄食量变化情况(表2、图2)显示,与同期安慰剂组比较,原参芪降糖方、改进方和二甲双胍均可明显抑制db/db小鼠的摄食量(均p<0.05),但同期原参芪降糖方和改进方抑制db/db小鼠摄食的效果均明显比二甲双胍更弱(均p<0.05),且参芪降糖方改进方抑制db/db小鼠摄食的效果与同期原参芪降糖方无显著差异(均p>0.05)。
表2参芪降糖改进方干预前后摄食量变化(n=10,
注:“*”表示与安慰剂组比较p<0.05,“△”表示与二甲双胍组比较p<0.05。
3.3参芪降糖改进方干预前后饮水量变化
对各组小鼠每周的饮水量进行统计学分析,结果如表3、图3所示,与同期安慰剂组比较,原参芪降糖方、改进方和二甲双胍在第1、2、3、4周均使db/db小鼠饮水明显减少(均p<0.05),且原参芪降糖方和改进方减少小鼠饮水的效果与二甲双胍无显著差异(均p>0.05)。
表3参芪降糖改进方干预前后饮水量变化(n=10,
注:“*”表示与安慰剂组比较p<0.05。
3.4参芪降糖改进方干预后葡萄糖耐量变化
统计学分析不同药物干预后各组小鼠的葡萄糖耐量(表4、图4)差异,结果显示,药物干预后,相比同期安慰剂组,原处方组、改进方组和二甲双胍组小鼠的葡萄糖耐量auc均显著性下降(均p<0.05),原处方和改进方干预后葡萄糖耐量auc比二甲双胍组药物明显更大(p<0.05),但改进方和原处方干预后葡萄糖耐量auc无明显差异(均p>0.05)。
表4参芪降糖改进方干预后糖耐量变化及auc(n=10,
注:“*”表示安慰剂组比较p<0.05,“△”表示与二甲双胍组比较p<0.05。
实验例2参芪降糖改进方对小鼠糖代谢生化指标的影响
1实验材料
1.1实验动物
上述糖耐量实验后的各组小鼠。
1.2材料和仪器
dmso(sigma,美国),小鼠胰岛素elisa试剂盒(mercodia,瑞士),小鼠糖化血红蛋白试剂盒(r&d,美国),总胆固醇含量检测试剂盒(r&d,美国),spectramaxm5微孔板分光光度计(moleculardevices,美国)。
2实验方法
2.1标本留取
铁盘铺满冰块后,将动物解剖台及装有pbs缓冲液的培养皿放置其上预冷;将动物按照不同体质量予以注射1%戊巴比妥钠麻醉剂,待其失去肌张力完全麻醉后固定于动物解剖台上;剪去胡须,摘眼球法取眼眶血,置于1.5ml离心管中,血样置4℃冰箱3~4h,待血液凝结后,将血样置于离心机中,以2000r/min离心15min分离血清,分装后置-20℃储存,以备酶联免疫吸附法检测之用。整个过程于冰上进行,保证蛋白活性。
2.2酶联免疫吸附法检测基础胰岛素
①准备:将试剂盒于室温下平衡约5min,防抗体降解。准备1×酶联结合物及样品复温。并按需准备足够的酶标板、标准品及样品。
②加样:分别设空白孔(空白对照孔不加样品及酶标试剂,其余各步操作相同)、标准品孔及待测样品孔。在酶标包被板上标准品孔中分别加入试剂盒中标示的由高至低浓度的标准品1-5号,每孔各25μl,待测样品孔中每孔加血清25μl。再向每孔中加入100μl的酶联结合物。
③温育:室温下,置于水平摇床上以700-900rpm孵育2h,不需要封板膜。
④配液:将21倍浓缩洗涤液用蒸馏水稀释成1×洗涤液后备用。
⑤洗涤:弃去液体,甩干,每孔加满洗涤液,静置30s后弃去,如此重复5次,拍干。
⑥加酶:每孔加入tmb底物200μl,空白孔除外,室温下孵育15min。
⑦终止:每孔加终止液500μl,终止反应(此时蓝色立转黄色),置水平摇床上混匀约5s。
⑧测定:以空白空调零,在加终止液后30min以内,于450nm波长测量各孔的吸光度(od值)。
2.3酶联免疫吸附法检测糖化血红蛋白
①标准品的稀释与加样:
a在酶标包被板上设标准孔,共5孔,在第一孔中加入100μl标准品,再在第一孔加50μl标准品稀释液,反复吹打混匀操作轻柔,勿触及孔底;
b取第一孔100μl加到第二孔,再加标准品稀释液50μl至第二孔,混匀;
c取第二孔50μl,弃掉,再取50μl到第三孔,向第三孔加标准品稀释液50μl,混匀;
d取第四孔50μl加至第五孔中,再加标准品稀释液50μl至第四孔,混匀后再取第四孔50μl至第五孔,加标准品稀释液50μl至第五孔,混匀,弃第五孔50μl。稀释后各孔加样量都为50μl,浓度分别为2400nmol/l、1600nmol/l、800nmol/l、400nmol/l、200nmol/l,标准曲线以同法做复孔。
②加样:分别设空白孔(空白对照孔不加样品及酶标试剂,其余各步操作相同)、待测样品孔。在酶标包被板上待测样品孔中先加样品稀释液40μl,然后再加待测样品10μl(样品最终稀释度为5倍)。将样品加于酶标板孔底部,尽量不触及孔壁,轻轻晃动混匀。
③温育:用封板膜封板后置37℃温育30min。
④配液:将30倍浓缩洗涤液用蒸馏水30倍稀释后备用。
⑤洗涤:小心揭掉封如此重复5次,拍干。
⑥加酶:每孔加入酶标试剂50μl,空白孔除外。
⑦温育:操作同上述步骤③。
⑧洗涤:操作同上述步骤⑤。
⑨显色:每孔先加入显色剂a50μl,再加入显色剂b50μl,轻轻震荡混匀,37℃避光显色15min。
⑩终止:每孔加终止液50μl,终止反应(此时蓝色立转黄色)。
2.4酶联免疫吸附法检测总胆固醇
同2.3。
2.5统计学分析
同实验例1。
3结果
3.1参芪降糖改进方治疗后基础胰岛素的变化水平
用酶联免疫吸附法测定基础胰岛素变化情况,结果显示,相比安慰剂组,参芪降糖改进方、原参芪降糖方和二甲双胍干预后均显著下调了db/db小鼠的基础胰岛素水平,由5.11±0.09μg/l分别下降至3.29±0.22μg/l、3.25±0.06μg/l和1.21±0.01μg/l(均p<0.05),且改进方组和原处方组基础胰岛素水平的下调无明显差异(p>0.05),但改进方组和原处方组小鼠的基础胰岛素水平明显比二甲双胍组更高(p<0.05),且见表5、图5。
表5药物干预后基础胰岛素的变化水平(n=10,
注:“*”表示与安慰剂组比较p<0.05,“△”表示与二甲双胍组比较p<0.05。
3.2参芪降糖改进方治疗后糖化血红蛋白的变化水平
用酶联免疫吸附法测定糖化血红蛋白变化情况,结果显示,相比安慰剂组,原参芪降糖方、参芪降糖改进方和二甲双胍干预后db/db小鼠糖化血红蛋白水平均明显下调(均p<0.05),由322.99±9.39nmol/l分别下降至259.70±28.83nmol/l、223.49±8.79nmol/l和226.513±7.58nmol/l,且改进方组和二甲双胍组无明显差异(p>0.05),但原处方组比二甲双胍基础胰岛素水平明显更高(p<0.05),见表6、图6。
表6药物干预后糖化血红蛋白的变化水平(n=10,
注:“*”表示与安慰剂组比较p<0.05,“△”表示与二甲双胍组比较p<0.05。
3.3参芪降糖改进方治疗后总胆固醇的变化水平
用酶联免疫吸附法测定总胆固醇变化情况,结果显示,相比安慰剂组,参芪降糖改进方、原参芪降糖方和二甲双胍干预后db/db小鼠总胆固醇水平均显著下调(均p<0.01),由4.64±0.40mmol/l分别下降至3.83±0.22mmol/l、3.91±0.32mmol/l和2.20±0.29mmol/l,改进方组和原处方组总胆固醇水平均明显高于二甲双胍组(p<0.01),但改进方组和原处方组小鼠总胆固醇水平无明显差异(p>0.05),见表7、图7。
表7药物干预后总胆固醇的变化水平(n=10,
注:“*”表示与安慰剂组比较p<0.05,“△”表示与二甲双胍组比较p<0.05。
以上结果表明,参芪降糖改进方在降血糖,改善ⅱ型糖尿病小鼠多饮、多食现象,提高糖耐量等方面与原参芪降糖方具有相似的治疗效果,能够用于ⅱ型糖尿病的治疗。
附图说明
图1为参芪降糖改进方干预前后血糖变化(n=10,
图2为参芪降糖改进方干预前后摄食量变化(n=10,
图3为参芪降糖改进方干预前后饮水量变化(n=10,
图4(a)为参芪降糖改进方干预后糖耐量变化,(b)为0-120min血糖应答曲线下面积(auc)比较示意图(n=10,
图5为药物干预后基础胰岛素的变化水平(n=10,
图6为药物干预后糖化血红蛋白的变化水平(n=10,
图7为药物干预后总胆固醇的变化水平(n=10,
具体实施方式
以下通过具体实施例进一步说明本发明,但本领域相关技术人员理应知晓,此所述实施例并不以任何方式限制本发明。
实施例1颗粒剂的制备
a、山药、茯苓、白术,知母粉碎成细粉ⅰ,备用;
b、麦冬用6倍量温水浸渍二次,每次2h,滤过,合并滤液,减压浓缩成相对密度为1.40的浸膏ⅰ,备用;
c、五味子用10倍量50%乙醇渗漉,滤过,减压回收乙醇,浓缩成相对密度为1.40的浸膏ⅱ备用;
d、山茱萸、芦根、枸杞子、黄芪、地黄、泽泻、葛根七味,用10倍量水煎煮两次,每次2h,滤过,合并滤液,滤液减压浓缩至相对密度1.20的稠膏,放冷,加入95%的乙醇使含醇量达60%,冷藏24h,滤过,滤液回收乙醇,浓缩成相对密度1.40的浸膏ⅲ,备用;
e、将浸膏ⅰ、ⅱ、ⅲ合并,混匀,干燥,粉碎成细粉后,再与细粉ⅰ及人参皂苷混匀,按照常规制剂工艺加入适量糊精和羧甲基淀粉钠(重量比2:1),混匀,制粒,干燥,即得颗粒剂。
实施例2丸剂的制备
a、山药、茯苓、白术,知母粉碎成细粉ⅰ,备用;
b、麦冬用5倍量温水浸渍3次,每次0.5h,滤过,合并滤液,减压浓缩成相对密度为1.30的浸膏ⅰ,备用;
c、五味子用8倍量40%乙醇渗漉,滤过,减压回收乙醇,浓缩成相对密度为1.30的浸膏ⅱ备用;
d、山茱萸、芦根、枸杞子、黄芪、地黄、泽泻、葛根七味,用10倍量水煎煮2次,每次1h,滤过,合并滤液,滤液减压浓缩至相对密度1.25的浸膏,放冷,加入95%的乙醇使含醇量达80%,冷藏24h,滤过,滤液回收乙醇,浓缩成相对密度1.35的浸膏ⅲ,备用;
e、将浸膏ⅰ、ⅱ、ⅲ合并,加入细粉ⅰ及人参皂苷,混匀,采用泛制法制丸,干燥,打光,即得丸剂。
实施例3片剂的制备
a、山药、茯苓、白术,知母粉碎成细粉ⅰ,备用;
b、麦冬用10倍量温水浸渍3h,滤过,合并滤液,减压浓缩成相对密度为1.35的浸膏ⅰ,备用;
c、五味子用12倍量70%乙醇渗漉,滤过,减压回收乙醇,浓缩成相对密度为1.35的浸膏ⅱ备用;
d、山茱萸、芦根、枸杞子、黄芪、地黄、泽泻、葛根七味,用9倍量水煎煮3次,每次0.5h,滤过,合并滤液,滤液减压浓缩至相对密度1.15的浸膏,放冷,加入95%的乙醇使含醇量达40%,冷藏24h,滤过,滤液回收乙醇,浓缩成相对密度1.30的浸膏ⅲ,备用;
e、将浸膏ⅰ、ⅱ、ⅲ合并,混匀,干燥,粉碎成细粉,再与细粉ⅰ及人参皂苷混匀,按照常规制剂工艺加入加入配方量的微晶纤维、羟丙基纤维(重量比4:3)混匀后,制粒,干燥,加入0.2%硬脂酸镁和0.1%的滑石粉,混匀,压片,包薄膜衣,即得片剂。
实施例4胶囊剂的制备
a、山药、茯苓、白术,知母粉碎成细粉ⅰ,备用;
b、麦冬用8倍量温水浸渍二次,每次2.5h,滤过,合并滤液,减压浓缩成相对密度为1.30的浸膏ⅰ,备用;
c、五味子用9倍量60%乙醇渗漉,滤过,减压回收乙醇,浓缩成相对密度为1.30的浸膏ⅱ备用;
d、山茱萸、芦根、枸杞子、黄芪、地黄、泽泻、葛根七味,用10倍量水煎煮2次,每次2.5h,滤过,合并滤液,滤液减压浓缩至相对密度1.20的浸膏,放冷,加入95%的乙醇使含醇量达60%,冷藏24h,滤过,滤液回收乙醇,浓缩成相对密度1.35的浸膏ⅲ,备用;
e、将浸膏ⅰ、ⅱ、ⅲ合并,混匀,干燥,粉碎成细粉,再与细粉ⅰ及人参皂苷混匀,按照常规制剂工艺加入加入配方量的淀粉、微粉硅胶、低取代羟丙基纤维素(重量比3:2:1),混匀后,制粒,干燥,整粒,灌装,磨光机中抛光,剔除破损胶囊,即得胶囊剂。
实施例5颗粒剂的制备
a、山药、茯苓、白术,知母粉碎成细粉ⅰ,备用;
b、麦冬用7倍量温水浸渍二次,每次1.5h,滤过,合并滤液,减压浓缩成相对密度为1.30的浸膏ⅰ,备用;
c、五味子用11倍量55%乙醇渗漉,滤过,减压回收乙醇,浓缩成相对密度为1.30的浸膏ⅱ备用;
d、山茱萸、芦根、枸杞子、黄芪、地黄、泽泻、葛根七味,用10倍量水煎煮2次,每次1.5h,滤过,合并滤液,滤液减压浓缩至相对密度1.15的浸膏,放冷,加入95%的乙醇使含醇量达50%,冷藏24h,滤过,滤液回收乙醇,浓缩成相对密度1.30的浸膏ⅲ,备用;
e、将浸膏ⅰ、ⅱ、ⅲ合并,混匀,干燥,粉碎成细粉后,再与细粉ⅰ及人参皂苷混匀,按照常规制剂工艺加入适量糊精和羧甲基淀粉钠(重量比2:1),混匀,制粒,干燥,即得颗粒剂。
实施例6颗粒剂的制备
a、山药、茯苓、白术,知母粉碎成细粉ⅰ,备用;
b、麦冬用9倍量温水浸渍二次,每次1h,滤过,合并滤液,减压浓缩成相对密度为1.40的浸膏ⅰ,备用;
c、五味子用11倍量45%乙醇渗漉,滤过,减压回收乙醇,浓缩成相对密度为1.40的浸膏ⅱ备用;
d、山茱萸、芦根、枸杞子、黄芪、地黄、泽泻、葛根七味,用9倍量水煎煮2次,每次3h,滤过,合并滤液,滤液减压浓缩至相对密度1.25的浸膏,放冷,加入95%的乙醇使含醇量达70%,冷藏24h,滤过,滤液回收乙醇,浓缩成相对密度1.40的浸膏ⅲ,备用;
e、将浸膏ⅰ、ⅱ、ⅲ合并,混匀,干燥,粉碎成细粉后,再与细粉ⅰ及人参皂苷混匀,按照常规制剂工艺加入适量糊精和羧甲基淀粉钠(重量比2:1),混匀,制粒,干燥,即得颗粒剂。
实施例7颗粒剂的制备
a、山药、茯苓、白术,知母粉碎成细粉ⅰ,备用;
b、麦冬用10倍量温水浸渍二次,每次2h,滤过,合并滤液,减压浓缩成相对密度为1.30的浸膏ⅰ,备用;
c、五味子用8倍量70%乙醇渗漉,滤过,减压回收乙醇,浓缩成相对密度为1.30的浸膏ⅱ备用;
d、山茱萸、芦根、枸杞子、黄芪、地黄、泽泻、葛根七味,用10倍量水煎煮两次,每次2h,滤过,合并滤液,滤液减压浓缩至相对密度1.25的稠膏,放冷,加入95%的乙醇使含醇量达40%,冷藏24h,滤过,滤液回收乙醇,浓缩成相对密度1.30的浸膏ⅲ,备用;
e、将浸膏ⅰ、ⅱ、ⅲ合并,混匀,干燥,粉碎成细粉后,再与细粉ⅰ及人参皂苷混匀,按照常规制剂工艺加入适量糊精和羧甲基淀粉钠(重量比2:1),混匀,制粒,干燥,即得颗粒剂。
实施例8颗粒剂的制备
a、山药、茯苓、白术,知母粉碎成细粉ⅰ,备用;
b、麦冬用6倍量温水浸渍二次,每次2h,滤过,合并滤液,减压浓缩成相对密度为1.40的浸膏ⅰ,备用;
c、五味子用12倍量40%乙醇渗漉,滤过,减压回收乙醇,浓缩成相对密度为1.40的浸膏ⅱ备用;
d、山茱萸、芦根、枸杞子、黄芪、地黄、泽泻、葛根七味,用10倍量水煎煮两次,每次2h,滤过,合并滤液,滤液减压浓缩至相对密度1.15的稠膏,放冷,加入95%的乙醇使含醇量达80%,冷藏24h,滤过,滤液回收乙醇,浓缩成相对密度1.40的浸膏ⅲ,备用;
e、将浸膏ⅰ、ⅱ、ⅲ合并,混匀,干燥,粉碎成细粉后,再与细粉ⅰ及人参皂苷混匀,按照常规制剂工艺加入适量糊精和羧甲基淀粉钠(重量比2:1),混匀,制粒,干燥,即得颗粒剂。
- 还没有人留言评论。精彩留言会获得点赞!