血府逐瘀制剂在制备卒中后脑损伤痛觉异常药物中的应用的制作方法
1.本发明涉及制药技术领域,特别是涉及一种血府逐瘀制剂在制备卒中后脑损伤痛觉异常药物中的应用。
背景技术:
2.有研究报道卒中后大约有25%的患者存在躯体感觉异常,其中约2%的患者不仅存在感觉缺损,还存在自发性中枢性卒中后疼痛(丘脑综合征),伴随针刺感、疼痛等痛觉异常敏感的表现,严重影响了卒中患者的生活质量。有研究报道,疼痛等痛觉异常可被具有单胺活性的第一代抗抑郁剂阿米替林、脱甲丙咪嗪所缓解。此外还有研究报道丘脑血管收缩引起的出血性中风或缺血可引起疼痛敏感性的增加。鉴于血府逐瘀制剂对血管活性的调节作用,其缓解卒中后感觉功能异常作用可能是其临床潜在药效作用之一。
技术实现要素:
3.本发明要解决的技术问题是:卒中后患者因脑出血或者缺血脑损伤导致的痛觉异常。
4.为了解决上述技术问题,本发明提供了一种血府逐瘀制剂在制备卒中后脑损伤痛觉异常药物中的应用。
5.优选的,本发明的上述应用,按重量份数计,所述血府逐瘀制剂包括以下组分:柴胡24~30份、当归75~85份、地黄72~88份、赤芍50~56份、红花75~86份、炒桃仁100~110份、麸炒枳壳50~56份、甘草24~30份、川芎32~45份、牛膝75~83份、桔梗45~55份。
6.优选的,本发明的上述应用,所述血府逐瘀制剂的用量或者用药浓度为0.43~2.16g/kg/d,即血府逐瘀药物制剂的用量为0.43~2.16g克/kg/天,相当于临床1~5倍的等效剂量。有关血府逐瘀制剂的制备方法可参考天津宏仁堂药业有限公司专利号为cn100422737c、cn100560103c、cn101647895b、cn103356796b、cn1320904c中公开的制备方法。
7.优选的,本发明的上述应用,所述血府逐瘀制剂包括药学上可接受的载体。
8.优选的,本发明的上述应用,所述载体优选自常用的药用辅料或者生理盐水或者蒸馏水。
9.进一步地,所述药学上可接受的辅料为:填充剂、崩解剂、润滑剂、助悬剂、粘合剂、甜味剂、矫味剂、防腐剂、基质等。填充剂包括:淀粉、预胶化淀粉、乳糖、甘露醇、甲壳素、微晶纤维素、蔗糖等;崩解剂包括:淀粉、预胶化淀粉、微晶纤维素、羧甲基淀粉钠、交联聚乙烯吡咯烷酮、低取代枪兵纤维素、交联羧甲基纤维素钠等;润滑剂包括:硬脂酸镁、十二烷基硫酸钠、滑石粉、二氧化硅等;助悬剂包括:聚乙烯吡咯烷酮、味精纤维素、蔗糖、琼脂、羟丙基甲基纤维素等;粘合剂包括:淀粉浆、聚乙烯吡咯烷酮、羟丙基甲基纤维素等;甜味剂包括:糖精钠、阿斯帕坦、蔗糖、甜蜜素、甘草次酸等;矫味剂包括:甜味剂及各种香精;防腐剂包括:尼泊金甲酯或乙酯苯甲酸、苯甲酸钠、山梨酸及其眼泪、苯扎溴铵、醋酸氯已定、桉叶油
等;基质包括:peg6000、peg4000、虫蜡等。
10.进一步地,本发明的上述应用,所述药物为血府逐瘀制剂按照常规工艺加入常规辅料制成临床上可接受的片剂、胶囊剂、散剂、合剂、汤剂、丸剂、颗粒剂、糖浆剂。
11.与现有技术相比,本发明具有以下优点:
12.本发明通过研究发现,血府逐瘀制剂干预对卒中后脑损伤导致的痛觉异常的热痛阈值降低现象具有一定的改善作用,可以作为制备卒中后脑损伤导致的痛觉异常的药物。
附图说明
13.图1为本发明实验例复制大鼠mcao模型前各试验组的痛阈值测试结果图。
14.图2为本发明实验例的mcao模型大鼠痛觉异常敏感的筛选结果图。
15.图3为本发明实验例血府逐瘀制剂对脑卒中后痛觉异常大鼠约1周后热痛阈值测试的结果图。
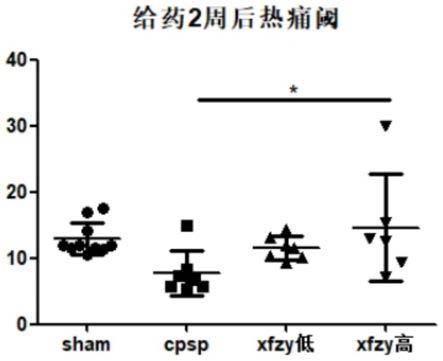
16.图4为本发明实验例血府逐瘀制剂对脑卒中后痛觉异常大鼠约2周后热痛阈值测试的结果图。
17.图5为本发明实验例血府逐瘀制剂对脑卒中后痛觉异常大鼠约3周后热痛阈值测试的结果图。
18.图6为本发明实验例假手术组大鼠在术后3、7、14、21天的热痛阈值测试的结果图。
19.图7为本发明实验例模型组大鼠在术后3、7、14、21天的热痛阈值测试结果图。
20.图8为zfxy低剂量组大鼠在术后3、7、14、21天的热痛阈值测试结果图。
21.图9为zfxy高剂量组大鼠在术后3、7、14、21天的热痛阈值测试结果图。
具体实施方式
22.下面结合附图和实验例,对本发明的技术方案进行清楚、完整的描述,显然,所描述的实施例仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明的保护范围。
23.实验例1:本实验例提供一种血府逐瘀制剂在制备卒中后脑损伤痛觉异常药物中的应用,下面通过具体的实验例来证明本发明的技术方案。
24.1实验材料
25.1.1实验动物
26.270-300g的wistar雄性大鼠多只,购于北京维通利华实验动物技术有限公司,许可证号:scxk(京)2016-0006。饲养于中国医学科学院放射医学研究所spf级屏障室,饲养室温度为21
±
2℃,气压恒定,昼夜12小时交替。
27.1.2药物配制
28.本实验例采用天津宏仁堂药业有限公司生产的血府逐瘀胶囊,该血府逐瘀胶囊每粒含生药0.4g,成人每次服用6粒,每日服两次,每日服药量4.8g,按正常成人体重50kg来计算,参考徐叔云教授主编的《药理实验方法学》,大鼠临床等效剂量是0.43g/kg/d,根据文献1(血府逐瘀胶囊对自发性高血压大鼠心肌肥厚的作用及机制研究[d].中国中医科学院,2012),选用5倍临床等效剂量2.16g/kg/d为给药剂量。精密称取血府逐瘀胶囊内药粉适量,
加少量纯净水调匀后稀释,超声波助溶,4℃保存,供大鼠灌胃给药用,每天现用现配。术后7天开始灌胃给药。
[0029]
2实验方法
[0030]
2.1痛觉异常模型的建立
[0031]
卒中后丘脑痛(cpsp)大鼠模型的建立分为两个部分。
[0032]
2.1.1脑卒中模型的建立
[0033]
采用大脑中动脉闭塞(mcao)的方法,沿右侧颈内动脉插入线栓并向前推进,直至大脑中动脉起始部被阻断,造成脑卒中模型,假手术组仅分离颈总动脉。阻断大脑供血时间为60min,60min后缓慢拔除线栓,恢复供血。
[0034]
2.1.2脑卒中后痛觉异常的筛选
[0035]
术前一天测定大鼠热痛阈值,将大鼠置于热板仪上,以大鼠舔后足为指标,筛选出热痛阈值在5-30s内的大鼠用于后续实验。文献中脑卒中1周后,大鼠会出现对侧后肢的热刺激和机械刺激的敏感上升,但经过前期预实验,术后三天大鼠即可出现对侧后肢热痛阈的降低,故术后3天,对造模大鼠进行热痛阈测试,以术前1天测量值为参考值,在模型组中挑选出发生痛觉异常的大鼠,随机分为模型组与给药组。
[0036]
2.2实验分组及给药种类和用量
[0037]
术后3天通过对mcao大鼠的热痛阈进行测试后,筛选出发生痛觉异常的实验大鼠22只进行分组给药(给药第一天,由于灌胃原因死亡大鼠1只,故每组均为7只大鼠),随机分为3组:模型组,血府逐瘀胶囊低剂量给药组与血府逐瘀胶囊高剂量给药组,每组7只,每天灌胃给药1次,连续给药21天。假手术组10只。实验分组、用药量及方法如下表1所示:
[0038]
表1:实验分组及给药数据表
[0039]
组别n给药种类及用量假手术组(sham)10灌胃等体积蒸馏水模型组(cpsp)7灌胃等体积蒸馏水低剂量给药组(xfzy低)70.43g/kg/d(临床等效剂量)高剂量给药组(xfzy高)72.16g/kg/d(5倍临床等效剂量)
[0040]
2.3热痛阈测定
[0041]
术前1天、术后3天,给药后7天,14天,21天,测定大鼠热痛阈值。
[0042]
热板法:为了避免后足基线温度的差异,先将大鼠置于37℃的热板仪上进行2分钟的适应期。然后将大鼠置于50℃的热板仪上,以60秒为上限值,以舔后足为观察指标,测试完毕,将大鼠放回笼中,间隔至少15分钟后重复测试,重复三次,取其平均值。
[0043]
2.4统计学方法
[0044]
采用graphpad prism 5.0软件进行统计学分析,计量数据以均数
±
标准差表示,大鼠热痛阈的比较选用单因素方差分析,p<0.05表明差异具有显著性。
[0045]
3实验结果
[0046]
3.1模型筛选结果
[0047]
复制大鼠mcao模型,在复制模型前后利用热板法对实验动物进行筛选,筛选结果如附图1所示,复制模型前实验各组痛阈值无显著差异(p>0.05)。复制大鼠mcao后3天利用热板法对痛觉敏感大鼠进行筛选,筛选出其中发生痛觉敏感的大鼠68只。测定68只mcao大
鼠的热痛阈值,结果显示其中22只存在痛觉敏感情况,发病率32.35%。测定结果如附图2所示,从中可以得出:术后三天出现痛觉异常的大鼠与sham组相比,其他各组热痛阈值均下降。相比假手术组10~20s的热痛阈值,模型组的热痛阈值下降为7~10s,血府逐瘀胶囊低剂量组和血府逐瘀胶囊高剂量组的热痛阈值下降为8~11s,热痛阈值显著降低(p<0.05),提示脑缺血导致了实验大鼠痛觉异常,但给药各组之间均无统计学差异(p<0.05)。其中术前热板仪温度为55℃,术后3天由于仪器问题,热板仪温度仅能达到50℃,故术后加假手术组热痛阈较术前升高,且给药后每周测定热板仪温度均为50℃。
[0048]
3.2血府逐瘀胶囊对卒中后脑损伤痛觉异常大鼠热痛阈的影响
[0049]
对痛觉异常大鼠进行筛选后开始灌胃给予血府逐瘀胶囊进行干预,给药1周后,如附图3所示,与假手术组比较,模型组的热痛阈值显著降低(p<0.05),提示脑缺血导致了实验大鼠痛觉异常。
[0050]
但模型组与假手术组之间的差异仍存在(p<0.05),提示mcao引起的痛觉异常现象并不会自愈,除此之外,各组均无统计学差异(p>0.05)。通过对低剂量的自身对照,低剂量给药组在给药1周后,热痛阈值升高(p<0.05),症状改善。
[0051]
给药2周后,如附图4所示,zfxy低剂量组的大鼠的热痛阈值相比术后三天以及给药一周后的热痛阈值逐渐增大,热痛阈值由术后三天的7~10s恢复到用药一周后的8~16s,再到用药两周后的8~15s,证明zfxy低剂量组大鼠的热痛阈值在逐渐恢复,大鼠的疼痛敏感性降低。
[0052]
与假手术组比较,模型组热痛阈值显著降低(p<0.05),提示脑缺血导致的实验大鼠痛觉异常无自行恢复现象;与模型组比较,血府逐瘀胶囊干预组热痛阈值显著升高(p<0.05)。仅zfxy高剂量组与模型组之间存在统计学差异,但zfxy高剂量组数据标准差过大,数据存在差异,证明xfzy高剂量组药效不稳定。
[0053]
给药3周后,如附图5所示,假手术组和血府逐瘀低剂量组均与模型组出现统计学差异(p<0.05),表明通过给药使脑卒中后出现痛觉异常的实验大鼠的热痛阈值逐渐恢复到正常水平,可以作为药物存在药效的证据,提示血府逐瘀胶囊对mcao引起的缺血性脑卒中后热痛阈值降低具有一定改善作用。
[0054]
下面通过对各组大鼠术前以及术后给药热痛阈值的变化进行数据对比:
[0055]
如附图6所示,假手术组大鼠的热痛阈值在术后3-21天内除个别极值外基本没有变化。
[0056]
如附图7所示,模型组大鼠的热痛阈值在术后3-21天热痛阈值相较假手术组降低,但组内整体未发生较大变化,排除极值点外,热痛阈值始终在7~11s范围内。
[0057]
如附图8所示,zfxy低剂量组在给药1周后,热痛阈值升高(p<0.05),说明热痛阈值在恢复,大鼠的疼痛敏感性在降低,在给药2
‑
3周时段内,热痛阈值基本维持在这一范围内。
[0058]
如附图9所示,zfxy高剂量组在给药三周后,热痛阈值未出现明显变化,仍在7~18s范围内。
[0059]
以上实验过程证明:通过mcao的方法制造的缺血性脑卒中模型可以引起实验大鼠痛觉异常,发生率约为30%,血府逐瘀胶囊干预对卒中后脑损伤导致的痛觉异常大鼠的热痛阈降低现象具有改善作用,可以将脑卒中后痛觉异常的大鼠热痛阈将6~10s恢复至10~
20s,说明血府逐瘀制剂能够降低疼痛的敏感性,缓解给患者带来的疼痛感,使痛觉感知恢复正常,即血府逐瘀制剂可以作为制备卒中中后脑损伤痛觉异常的药物,以应用在制备治疗卒中侯脑损伤痛觉异常的药物中。
[0060]
本发明还研究了血府逐瘀制剂干预复制大鼠局灶性脑缺血损伤模型和利用丘脑注射内皮素直接诱导丘脑缺血模型,并分别采用热板法考察实验动物对热刺激疼痛的反应情况,实验结果证明:血府逐瘀制剂对两种模型的热刺激疼痛反应,均能够降低疼痛的敏感性,缓解疼痛感,使患者的痛觉感知恢复正常。
[0061]
本发明的研究发现,血府逐瘀制剂干预对脑卒中后痛觉异常的热痛阈值降低现象具有改善作用,可以作为潜在的制备卒中后脑损伤痛觉异常的药物,以治疗或减缓脑损伤患者的痛觉异常。
[0062]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明技术原理的前提下,还可以做出若干改进和替换,这些改进和替换也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1