一种具有生物活性涂层的多孔钽植入物及其制备方法与流程
1.本发明涉及医用材料技术领域,尤其涉及一种具有生物活性涂层的多孔钽植入物及其制备方法。
背景技术:
2.钽金属植入物应用于骨科植入物已经有10多年历史,由于钽金属密度高,因此大部分钽金属植入物以多孔钽的形式进行设计制备,钽金属植入物具有良好的生物相容性。3d打印技术为个性化多孔钽植入物的制备提供技术保障,多孔骨小梁结构有利于骨组织长入,但根据实际临床过程中研究发现,多孔钽植入物的骨长入效果难以明确,钽-细胞-骨界面整合能力仍然有限。例如:cn105177523a公开的的多孔钽金属材料孔隙率高,且为互相连通的多孔结构,孔隙死腔少,与人体松质骨相似,可促进骨长入,可应用于体内多部位的骨创伤及骨坏死后骨缺损的修复;cn109806032a公开的一种3d打印多孔钽棒,多孔分布均匀且可控,多孔钽棒抗压强度为120~180mpa,弹性模量为10~20gpa,孔隙率为75~85%。
3.现有技术中的多孔钽材料表面生物活性改性不尽理想,制备的多孔钽与骨的成分不同,在植入早期不能与骨形成化学结合,也没有促进新骨形成的能力。例如cn111481738a公开了一种生物活性多孔钽植入物制备方法,在预处理材料表面形成具有生物活性物质的原位生长膜层,对原位生长膜层进行水热处理,得到生物活性多孔钽植入物。
4.因此,有必要研发一种多孔钽植入物及其制备方法,解决现有技术中存在的多孔钽植入物生物学性能低等技术问题。
技术实现要素:
5.根据最新研究发现,通过功能性大分子蛋白等修饰的多孔钽骨整合能力得到提高,修饰过的多孔钽和骨界面的微观结构发生改变,产生“界面机械负荷”的力学作用,这种力学信号可以刺激细胞基质蛋白完成成骨过程,从而进一步提升钽生物学性能,提高钽-细胞-骨界面整合效率,促进钽材料的增值利用。
6.本发明的目的是提供一种具有生物活性涂层的多孔钽植入物及其制备方法,更具体地涉及一种利用骨长入活性物质和多醛基海藻酸钠对多孔钽植入物表面进行改性,获得多醛基海藻酸钠与多肽链的交联作用生成的钽金属活性涂层,从而使得多孔钽植入物生物学性能得到提高,进而提高骨整合能力。
7.基于上述技术目的,本发明采用如下技术方案:
8.一方面,本发明提供一种具有生物活性涂层的多孔钽植入物的制备方法,是指将骨长入活性物质与多醛基氧化海藻酸钠交联反应,进一步与氨基修饰的多孔钽植入物反应得到具有生物活性涂层的多孔钽植入物。
9.进一步地,所述制备方法,具体包括以下步骤:
10.(1)将多孔钽植入体经酸化改性、氨基修饰获得氨基修饰的多孔钽植入体;
11.(2)将海藻酸钠分散于乙醇中配制悬浊液a;高碘酸钠或高碘酸溶于水配制溶液b;
将溶液b加入溶液a中避光反应,制得多醛基氧化海藻酸钠(osa);
12.(3)将骨长入活性物质和多醛基氧化海藻酸钠交联反应制得混合溶液;
13.(4)将氨基修饰的多孔钽植入物加入步骤(3)的混合溶液中反应,制得具有生物活性涂层的多孔钽植入物。
14.进一步地,步骤(1)中所述多孔钽植入体通过含量大于99.99%的高纯球形钽粉采用3d打印技术打印制得。其中所述3d打印技术可以采用选择性激光熔融(slm)技术或电子束熔融(ebm)技术。
15.进一步地,步骤(1)中所述多孔钽植入体包括多孔钽髋臼杯、多孔钽椎间融合器、膝关节假体、髋膝关节垫块等。
16.进一步地,步骤(1)中所述酸化改性过程如下:
17.a将高锰酸钾溶于水中,加入浓硫酸稀释获得高锰酸钾硫酸溶液;
18.b将多孔钽植入物置于高锰酸钾硫酸溶液中酸化改性,即得。
19.进一步地,所述高锰酸钾硫酸溶液中硫酸质量分数在20~50%。
20.进一步地,所述酸化改性的温度为常温,在15~25℃;酸化改性时间为15~30min。
21.进一步地,步骤(1)中所述氨基修饰过程如下:将经酸化改性的多孔钽植入体置入聚乙烯亚胺(pei)水溶液中即得。进一步优选地,所述聚乙烯亚胺水溶液质量浓度为0.3%~1%,反应时间为20~40min,处理温度为15~25℃。
22.进一步地,步骤(2)所述悬浊液a制备过程如下:将10g海藻酸钠分散于50ml无水乙醇中配成悬浊液a。
23.进一步地,步骤(2)中所述溶液b制备过程如下:将高碘酸钠或高碘酸配制水溶液b,。
24.进一步地,步骤(2)所述避光反应过程为:按照高碘酸钠或高碘酸与海藻酸钠单体的摩尔比:60%~80%,将溶液b加入悬浊液a中,避光室温磁力搅拌10-24h后,加入与高碘酸钠等摩尔的乙二醇终止反应;将反应混合物倒入剧烈搅拌的大量乙醇中,析出沉淀,抽滤、40℃真空干燥,所得固体粉末采用蒸馏水透析12h除掉未反应的高碘酸钠及乙二醇等小分子杂质,得到多醛基氧化海藻酸钠。
25.进一步地,步骤(3)中所述骨长入活性物质为蛋白分子、多肽或特异性氨基酸等,具体的可以是:rgd多肽(精氨酸(r)-甘氨酸(g)天冬氨酸(d))、ogp多肽(骨生长激素肽)、髓鞘碱性蛋白(mbp蛋白)中至少一种。
26.进一步地,步骤(3)中所述交联反应过程为:将骨长入活性物质溶于去离子水中,然后加入多醛基氧化海藻酸钠、氯化钠和氰基硼氢化钠,添加去离子水溶解后,用稀盐酸调ph3~6,常温混合反应制得混合溶液。其中,所述骨长入活性物质反应溶液浓度为0.01~0.05mg/ml;osa反应溶液浓度为0.05-2mg/ml,nacl浓度为0.01~0.55mol/l,氰基硼氢化钠浓度为0.01~0.1mg/l;稀盐酸浓度为0.01mmol/l。
27.进一步地,步骤(4)中所述反应的时间为3~5h,温度为30~40℃。
28.骨长入活性物质与多醛基氧化海藻酸钠(osa)交联反应的反应物包括骨形成蛋白、rgd多肽、特异性氨基酸序列等促进骨生长的活性因子;进一步与氨基修饰的多孔钽植入物通过空间物理缠绕、活性基团之间的离子键及重点固定法等得到具有生物活性涂层的多孔钽植入物。
29.另一方面,本发明提供一种具有生物活性涂层的多孔钽植入物,具体通过本发明的方法制备得到。
30.相对于现有技术,本发明提供的技术方案具备有益效果如下:
31.1)本发明基于钽金属稳定的化学性质和生物相容性,对多孔钽植入物进行表面酸化改性引入活性氨基层;其次通过将多肽链或蛋白与多醛基氧化海藻酸钠交联后进一步与氨基修复的多孔钽植入物通过空间物理缠绕、离子键及终点固定法等方式获得具有生物活性涂层的多孔钽植入物。其中,通过高碘酸或高碘酸钠氧化海藻酸钠使其产生具有极高反应活性的醛基(醛基可以和骨形成蛋白、rgd多肽、特异性氨基酸序列等活性因子发生交联反应);在多孔钽植入物表面获得的活性涂层,交联了能够促进骨组织生长的rgd多肽,可以促进成骨细胞对钽表面的粘附,进一步促进种植入物的骨整合长入效果。
32.2)本发明采用的多孔钽3d打印技术已经有成熟的制备工艺,成本较低,成品直接酸化处理,最后制备涂层,工艺流程简单。
33.3)海藻酸钠作为一种天然多糖,采用其制备的多醛基氧化海藻酸钠,是生物医疗领域无毒、水溶、成本低廉的生物高分子交联剂。多醛基氧化海藻酸钠交联剂在多孔钽的内部结构中与活性氨基/rgd多肽实现更加紧密的物理缠绕,大幅提高多孔钽植入物内部的生物活性,促进多孔钽植入手术的患者康复的速度,具有很高的实用价值。
34.4)本发明技术方案能够为增强多孔钽植入物的生物学性能,进一步提高骨整合能力提供一种低成本的可靠方案,工艺流程简单。
附图说明
35.图1为未进行处理前的多孔钽植入体结构示意图;
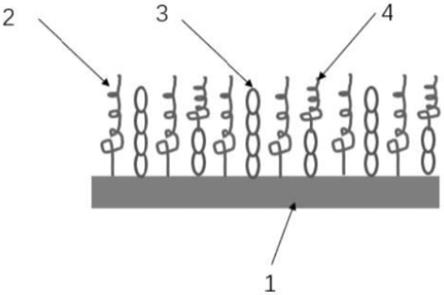
36.图2为本发明实施例制得的具有生物活性涂层的多孔钽植入物的结构示意图。图中,1为多孔钽植入体表面;2为多肽链、蛋白或氨基酸序列;3为多醛基氧化海藻酸钠;4为多醛基氧化海藻酸钠与多肽链交联后的反应物。
具体实施方式
37.以下实施例旨在说明本发明内容,而不是对本发明保护范围的进一步限定。
38.本发明实施例使用的多孔钽植入物:湖南普林特医疗器械有限公司采用slm技术生产的多孔钽假体。
39.实施例1
40.本发明制备一种具有生物活性涂层的多孔钽植入物的步骤如下:
41.第一步,采用含量大于99.99%的高纯球形钽粉利用slm技术3d打印技术打印多孔钽髋臼杯,产品孔隙率为75%;
42.第二步,称取15g高锰酸钾溶于500ml去离子水中,搅拌均匀后继续加入wt95%浓硫酸200ml,使得浓硫酸和高锰酸钾均匀混合;
43.第三步,在常温下将多孔钽髋臼杯置入上述溶液中酸化改性15分钟,取出用去离子水清洗干净;
44.第四步,将清洗干净的多孔钽髋臼杯至于wt0.5%的聚乙烯亚胺溶液中反应30min,得到氨基修饰的多孔钽髋臼杯;
45.第五步,将10g海藻酸钠溶于50ml无水乙醇中配成悬浊液a;配置高碘酸钠水溶液;
46.按照高碘酸钠与海藻酸钠单体单元的摩尔比为6:10,将溶液b加入悬浊液a中,避光室温磁力搅拌12h,加入与高碘酸钠等摩尔的乙二醇终止反应;
47.将反应混合物倒入96wt%的乙醇溶液中沉淀,抽滤在40℃真空干燥,所得固体粉末采用蒸馏水透析12h除掉未反应的高碘酸钠及乙二醇等小分子杂质,得到多醛基氧化海藻酸钠(osa);
48.第六步,取rgd多肽10mg溶于200ml去离子水中搅拌均匀,然后加入20mg多醛基海藻酸钠,加入1.75g的nacl粉末和0.02gnabh3cn,添加去离子水溶解后,在常温下混合反应溶液,以0.1mmol/l的盐酸溶液调节ph至3.0;
49.第七步,将氨基修饰的多孔钽髋臼杯置于步骤六制备的溶液中在35℃下反应3h,得到具有生物活性涂层的多孔钽植入物。
50.实施例2
51.本发明制备一种具有生物活性涂层的多孔钽植入物的步骤如下:
52.第一步,采用含量大于99.99%的高纯球形钽粉利用ebm技术3d打印技术打印多孔钽膝关节假体,产品孔隙率为80%;
53.第二步,称取15g高锰酸钾溶于500ml去离子水中,搅拌均匀后继续加入wt95%浓硫酸200ml,使得浓硫酸和高锰酸钾均匀混合;
54.第三步,在常温下将多孔钽膝关节假体置入上述溶液中酸化改性20分钟,取出用去离子水清洗干净;
55.第四步,将清洗干净的多孔钽膝关节假体至于wt1%的聚乙烯亚胺溶液中反应20min,得到氨基修饰的多孔钽膝关节假体;
56.第五步,将10g海藻酸钠溶于50ml无水乙醇中配成悬浊液a;配置高碘酸钠水溶液;
57.按照高碘酸钠与海藻酸钠单体单元的摩尔比为8:10,将溶液b加入悬浊液a中,避光室温磁力搅拌24h,加入与高碘酸钠等摩尔的乙二醇终止反应;
58.将反应混合物倒入96wt%的乙醇溶液中沉淀,抽滤在40℃真空干燥,所得固体粉末采用蒸馏水透析12h除掉未反应的高碘酸钠及乙二醇等小分子杂质,得到多醛基氧化海藻酸钠(osa);
59.第六步,取bmp蛋白50mg溶于1l去离子水中搅拌均匀,然后加入100mg多醛基海藻酸钠,加入8.76g的nacl粉末和0.1gnabh3cn,添加去离子水溶解后,在常温下混合反应溶液,以0.1mmol/l的盐酸溶液调节ph至3.0;
60.第七步,将氨基修饰的多孔钽膝关节假体置于步骤六制备的溶液中在40℃下反应3h,得到具有生物活性涂层的多孔钽植入物。
61.实施例3
62.第一步,采用含量大于99.99%的高纯球形钽粉利用slm技术3d打印技术打印多孔钽椎间融合器,产品孔隙率为78%;
63.第二步,称取15g高锰酸钾溶于500ml去离子水中,搅拌均匀后继续加入wt95%浓硫酸200ml,使得浓硫酸和高锰酸钾均匀混合;
64.第三步,在常温下将多孔钽椎间融合器置入上述溶液中酸化改性30分钟,取出用去离子水清洗干净;
65.第四步,将清洗干净的多孔钽椎间融合器至于wt0.3%的聚乙烯亚胺溶液中反应40min,得到氨基修饰的多孔钽椎间融合器;
66.第五步,将10g海藻酸钠溶于50ml无水乙醇中配成悬浊液a;配置高碘酸钠水溶液b;
67.按照高碘酸钠与海藻酸钠单体单元的摩尔比为6:10,将溶液b加入悬浊液a中,避光室温磁力搅拌10h,加入与高碘酸钠等摩尔的乙二醇终止反应;
68.将反应混合物倒入96wt%的乙醇溶液中沉淀,抽滤在40℃真空干燥,所得固体粉末采用蒸馏水透析12h除掉未反应的高碘酸钠及乙二醇等小分子杂质,得到多醛基氧化海藻酸钠(osa);
69.第六步,取ogp多肽100mg溶于200ml去离子水中搅拌均匀,然后加入200mg多醛基海藻酸钠,加入1.75g的nacl粉末和0.02gnabh3cn,添加去离子水溶解后,在常温下混合反应溶液,以0.1mmol/l的盐酸溶液调节ph至3.0;
70.第七步,将氨基修饰的多孔钽椎间融合器置于步骤六制备的溶液中在30℃下反应5h,得到具有生物活性涂层的多孔钽植入物。
71.实施例4
72.本发明制备一种具有生物活性涂层的多孔钽植入物的步骤如下:
73.第一步,采用含量大于99.99%的高纯球形钽粉利用ebm技术3d打印技术打印多孔钽膝关节假体,产品孔隙率为80%;
74.第二步,称取15g高锰酸钾溶于500ml去离子水中,搅拌均匀后继续加入wt95%浓硫酸200ml,使得浓硫酸和高锰酸钾均匀混合;
75.第三步,在常温下将多孔钽膝关节假体置入上述溶液中酸化改性20分钟,取出用去离子水清洗干净;
76.第四步,将清洗干净的多孔钽膝关节假体至于wt0.5%的聚乙烯亚胺溶液中反应30min,得到氨基修饰的多孔钽膝关节假体;
77.第五步,将10g海藻酸钠溶于50ml无水乙醇中配成悬浊液a;配置高碘酸钠水溶液b;
78.按照高碘酸钠与海藻酸钠单体单元的摩尔比为7:10,将溶液b加入悬浊液a中,避光室温磁力搅拌12h,加入与高碘酸钠等摩尔的乙二醇终止反应;
79.将反应混合物倒入96wt%的乙醇溶液中沉淀,抽滤在40℃真空干燥,所得固体粉末采用蒸馏水透析12h除掉未反应的高碘酸钠及乙二醇等小分子杂质,得到多醛基氧化海藻酸钠(osa);
80.第六步,取bmp蛋白50mg溶于1l去离子水中搅拌均匀,然后加入100mg多醛基海藻酸钠,加入8.76g的nacl粉末和0.1gnabh3cn,添加去离子水溶解后,在常温下混合反应溶液,以0.1mmol/l的盐酸溶液调节ph至3.0;
81.第七步,将氨基修饰的多孔钽膝关节假体置于步骤六制备的溶液中在35℃下反应3h,得到具有生物活性涂层的多孔钽植入物。
82.实施例5
83.第一步,采用含量大于99.99%的高纯球形钽粉利用slm技术3d打印技术打印多孔钽椎间融合器,产品孔隙率为78%;
84.第二步,称取15g高锰酸钾溶于500ml去离子水中,搅拌均匀后继续加入wt95%浓硫酸200ml,使得浓硫酸和高锰酸钾均匀混合;
85.第三步,在常温下将多孔钽椎间融合器置入上述溶液中酸化改性30分钟,取出用去离子水清洗干净;
86.第四步,将清洗干净的多孔钽椎间融合器至于wt0.5%的聚乙烯亚胺溶液中反应30min,得到氨基修饰的多孔钽椎间融合器;
87.第五步,将10g海藻酸钠溶于50ml无水乙醇中配成悬浊液a;配置高碘酸钠水溶液b;
88.按照高碘酸钠与海藻酸钠单体单元的摩尔比为7:10,将溶液b加入悬浊液a中,避光室温磁力搅拌12h,加入与高碘酸钠等摩尔的乙二醇终止反应;
89.将反应混合物倒入96wt%的乙醇溶液中沉淀,抽滤在40℃真空干燥,所得固体粉末采用蒸馏水透析12h除掉未反应的高碘酸钠及乙二醇等小分子杂质,得到多醛基氧化海藻酸钠(osa);
90.第六步,取bmp蛋白20mg溶于200ml去离子水中搅拌均匀,然后加入40mg多醛基海藻酸钠,加入1.75g的nacl粉末和0.02gnabh3cn,添加去离子水溶解后,在常温下混合反应溶液,以0.1mmol/l的盐酸溶液调节ph至3.0;
91.第七步,将氨基修饰的多孔钽椎间融合器置于步骤六制备的溶液中在35℃下反应3h,得到具有生物活性涂层的多孔钽植入物。
92.采用骨生长因子与多醛基海藻酸钠交联形成活性膜的多孔钽植入假体相比纯钽裸金属植入物的生物活性明显增强,其表面骨组织细胞生长速度要高于裸金属钽植入物。
93.具有生物活性涂层的多孔钽骨植入物能够促进骨增殖,进一步提高骨整合能力。
94.尤其是多醛基海藻酸钠可以与骨生长因子通过空间缠绕的方式大量存在于多孔钽植入物内部,相比单纯将多孔钽在活性因子溶液浸泡的涂层,本技术制备的涂层稳定性大幅度提高。
95.虽然,上文中已经用一般性说明、具体实施方式及试验,对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1