缓解肠道病毒性感染损伤的组合物及其制备方法和应用与流程
1.本发明属于生物医药制备技术领域,具体涉及一种缓解肠道病毒性感染损伤的组合物及其制备方法和应用。
背景技术:
2.轮状病毒感染(rv)是诱发婴幼儿腹泻的重要原因,尤其是3岁以下儿童。rv感染的急性腹泻婴幼儿会伴有明显肠道菌群失衡、血清炎症因子水平升高现象,其发病主要原因是自身免疫功能降低,病原微生物入侵,导致炎症感染,rv感染性肠炎在一定程度上会导致呼吸、心肌及神经系统损害。迄今为止,临床上主要采用补液治疗和接种口服rv减毒活疫苗等手段,但目前为止,尚无抗rv的特效药物。
3.益生菌是一类对宿主有益的活性微生物,具有维持机体微生态平衡、调节免疫反应、减少传染性疾病以及肠道炎症的发生等功能,益生菌补充也是临床上预防、缓解rv感染的一个重要途径。
4.目前常用西药缓解肠道病毒性感染所致的肠道损伤、腹泻,对身体存在一定的副作用,因此如何筛选、提取、利用天然活性成分减轻或避免副作用,缩短rv感染导致的腹泻持续时间、减少腹泻次数、增强rv弱毒苗的免疫效果成为一种新的思路。
技术实现要素:
5.本发明的目的是要提供一种由天然活性成分和益生菌组成,能够缩短病毒感染导致的腹泻持续时间、减少腹泻次数、增强免疫效果,且副作用小、疗效独特的缓解肠道病毒性感染损伤的组合物及其制备方法和应用。
6.为了解决上述技术问题,本发明采取的技术方案如下:
7.一种缓解肠道病毒性感染损伤的组合物,其包括山楂活性多糖、蓝莓多酚类化合物及益生菌,所述山楂活性多糖、蓝莓多酚类化合物及益生菌的质量百分比为1:0.003-0.03:0.05-0.5。
8.上述的一种缓解肠道病毒性感染损伤的组合物,其所述蓝莓多酚类化合物包括结构式为的蓝莓多酚-a、结构式为的蓝莓多酚
ꢀ‑
b、结构式为的蓝莓多酚-c中的任意两种或三种。
9.上述的一种缓解肠道病毒性感染损伤的组合物,其所述的蓝莓多酚类化合物采用如下方法制得:取新鲜蓝莓,粉碎,加入3-5倍重量的纯水混合,离心 15分钟,取上清液,减压浓缩,得到浸膏;将浸膏加适量水混悬,用乙酸乙酯萃取,得乙酸乙酯部位以及水部位的萃取物;将水部位萃取物采用硅胶柱层析分离,以乙酸乙酯-甲醇系统梯度洗脱,获得不同馏分;将具有最佳保护活性的馏分经制备型hplc甲醇-三氟乙酸水系统得到含蓝莓多酚-a、蓝莓多酚-b、蓝莓多酚-c的所述的蓝莓多酚类化合物。
10.上述的一种缓解肠道病毒性感染损伤的组合物,其所述益生菌包括长双歧杆菌、乳双歧杆菌、短双歧杆菌、罗伊氏乳杆菌、副干酪乳杆菌中的一种或几种。
11.上述的一种缓解肠道病毒性感染损伤的组合物,其所述山楂活性多糖采用如下方法制得:取山楂多糖并加入5-10倍重量的纯水溶解,山楂多糖水溶液用孔径小于等于15kd的透析袋透析,收集透析液,冻干即可。
12.一种缓解肠道病毒性感染损伤的组合物的制备方法,其包括以下步骤:
13.称取山楂活性多糖、蓝莓多酚类化合物及益生菌,所述山楂活性多糖、蓝莓多酚类化合物及益生菌的质量百分比为1:0.003-0.03:0.05-0.5;将山楂活性多糖、蓝莓多酚类化合物混合均匀,加去离子水调成固含量为3-30%的浆状液体,所述浆状液体经过冻干制成混合物粉末;将混合物粉末再复配益生菌,混合均匀后再次冻干,即可制得。
14.上述的一种缓解肠道病毒性感染损伤的组合物的制备方法,其所述蓝莓多酚类化合物采用如下方法制得:取新鲜蓝莓,粉碎,加入3-5倍重量的纯水混合,离心15分钟,取上清液,减压浓缩,得到浸膏;将浸膏加适量水混悬,用乙酸乙酯萃取,得乙酸乙酯部位以及水部位的萃取物;将水部位萃取物采用300-400 目的硅胶柱层析分离,以乙酸乙酯-甲醇系统按100:0
→
0:100的梯度洗脱,获得不同馏分;将具有最佳保护活性的馏分经制备型hplc甲醇-三氟乙酸水系统得到含蓝莓多酚-a、蓝莓多酚-b、蓝莓多酚-c的所述的蓝莓多酚类化合物。
15.上述的一种缓解肠道病毒性感染损伤的组合物的制备方法,其所述山楂活性多糖采用如下方法制得:取山楂多糖并加入5-10倍重量的纯水溶解,山楂多糖水溶液用孔径小于等于15kd的透析袋透析,收集透析液,冻干即可。
16.上述的一种缓解肠道病毒性感染损伤的组合物的制备方法,其所述山楂活性多糖的分子量小于等于15kd,优选山楂活性多糖的分子量在1-3kd。
17.一种缓解肠道病毒性感染损伤的组合物的应用,其所述缓解肠道病毒性感染损伤的组合物适用于轮状病毒所致的肠道屏障、功能损伤、腹泻。
18.有益效果:
19.本发明通过简单的、基于活性评价的方法分离获得山楂活性多糖、蓝莓多酚类化合物,然后将山楂活性多糖、蓝莓多酚类化合物优化组合并复配长双歧杆菌、乳双歧杆菌、短双歧杆菌、罗伊氏乳杆菌、副干酪乳杆菌冻干菌粉,将这种活性多糖、活性天然产物成分复配益生菌组合物用于缓解病毒性感染造成的肠道屏障、功能损伤,增强肠道免疫力有非常显著的活性,且无副作用。
附图说明
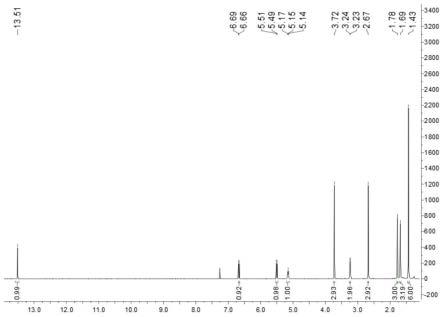
20.21.图1为本发明蓝莓多酚-a的1h nmr图
22.图2为本发明蓝莓多酚-a的
13
c nmr图
23.图3为本发明蓝莓多酚-a的dept-135图
24.图4为本发明蓝莓多酚-a的hmbc图
25.图5为本发明蓝莓多酚-b的1h nmr图
26.图6为本发明蓝莓多酚-b的
13
c nmr图
27.图7为本发明蓝莓多酚-b的dept-135图
28.图8为本发明蓝莓多酚-b的1h-1
h cosy图
29.图9为本发明蓝莓多酚-b的hmbc图
30.图10为本发明蓝莓多酚-c的1h nmr图
31.图11为本发明蓝莓多酚-c的
13
c nmr图
32.图12为本发明蓝莓多酚-c的dept-135图
33.图13为本发明蓝莓多酚-c的hmbc图
34.图14为本发明对感染rv乳鼠血清tnf-α、il-1β、caspase-1含量的影响
35.图15为本发明对感染rv乳鼠p65、nf-κb、claudin-4及tjp-1蛋白表达的影响
具体实施方式
36.以下提供具体实施例以实现本发明所述的技术方案,但不限于这些实施例。应理解,这些具体实施方式及附图仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
37.除非另有定义,否则在公开本发明时使用的所有术语(包括技术和科学术语)具有本发明所属领域的普通技术人员通常理解的含义。借助于进一步引导,包括术语定义以更好地理解本发明的教导。
38.实施例1
39.本实施例的缓解肠道病毒性感染损伤的组合物,包括山楂活性多糖、蓝莓多酚类化合物及益生菌。其中,蓝莓多酚类化合物包括结构式为的蓝莓多酚-a、结构式为的蓝莓多酚-b、结构式为的蓝莓多酚-c中的任意两种或三种。蓝莓多酚类化合物通过新鲜蓝莓制得。所述益生菌包括长双歧杆菌、乳双歧杆菌、短双歧杆菌、罗伊氏乳杆菌、副干酪乳杆菌。所述山楂活性多糖通过山楂多糖制得。山楂
活性多糖、蓝莓多酚-a、蓝莓多酚-b、蓝莓多酚-c、长双歧杆菌、乳双歧杆菌、短双歧杆菌、罗伊氏乳杆菌、副干酪乳杆菌的质量比为
40.1:0.005:0.005:0.005:0.05:0.05:0.05:0.05:0.05。
41.本发明的制备方法如下:
42.(1)山楂活性多糖的制备
43.取山楂多糖100g,加入500-1000g的纯水溶解,山楂多糖水溶液用孔径为 3kd的透析袋透析,分别收集透析液,冻干获得分子量1-3kd之间的山楂活性多糖。基于构建的轮状病毒感染诱发小鼠腹泻模型评价不同分子量山楂多糖的保护活性。实验结果显示,1-3kd之间的山楂多糖对轮状病毒感染诱发的腹泻小鼠保护活性最佳。
44.(2)活性天然产物蓝莓多酚类化合物的制备
45.新鲜蓝莓1kg,粉碎,加纯水3-5l,6000g离心15分钟,取上清液,减压浓缩,得到浸膏124g。将浸膏加适量水混悬,用乙酸乙酯萃取,得乙酸乙酯部位51g以及水部位。基于构建的轮状病毒感染诱发小鼠腹泻模型,筛选不同萃取物的保护活性。
46.将具有最佳保护活性的水部位采用硅胶(300-400目)柱层析分离,以乙酸乙酯-甲醇系统(100:0
→
0:100)梯度洗脱,获得8个馏分(fr.1-8)。基于构建的轮状病毒感染诱发小鼠腹泻模型,筛选不同馏分的保护活性。
47.将具有最佳保护活性的乙酸乙酯-甲醇按30:70的洗脱组分经制备型 hplc(甲醇-三氟乙酸水系统)得到含量最多的组分,并最终鉴定为蓝莓多酚-a、蓝莓多酚-b、蓝莓多酚-c。
48.蓝莓多酚-a:
49.淡黄色油状物,薄层层析后,香草醛-浓硫酸加热反应显红色。hr-esi-ms 显示准分子离子峰m/z 357.1676[m+na]
+
(c
19h26
o5na,理论计算值:357.1672)确定分子式为c
19h26
o5,不饱和度为7。
[0050]
如图1所示,1h nmr(400mhz,cdcl3)谱中共显示24个质子信号。δ
h 13.51 (1h,s)提示有1个苯环上的羟基氢信号;δ
h 5.15(1h,t,j=6.8hz), 3.24(2h,d,j=6.8hz),1.78(3h,s),1.69(3h,s)提示分子中含有一个3-甲基-2-丁烯基团;此外,该化合物还有1组顺式烯烃质子信号[δ
h 5.50(1h,d,j =10.0hz),6.67(1h,d,j=10.0hz)];4个甲基单峰质子信号[δ
h 3.72(3h,s),2.67(3h,s),1.43(6h,s)]。
[0051]
如图2所示,
13
c nmr(100mhz,cdcl3)谱中共出现19个碳信号,如图3 所示,结合dept-135谱可知其分别为9个季碳、3个次甲基、1个亚甲基和6 个甲基。低场区可见δ
c 203.6的1个酮羰基信号;δ
c 131.3,123.3和δ
c 126.8,116.3为2对双键碳信号;δ
c 161.1,159.1,158.7,115.0,109.1,106.1 可推测为苯环的碳信号。根据以上数据,并推测化合物蓝莓多酚-a可能是酰基间苯三酚类化合物。
[0052]
如图4所示,在hmbc谱中,可以观察到h-2
″′
(δ
h 6.67)与c-3
″′
(δ
c 78.0),c-4
″′
/5
″′
(δ
c 28.5)有相关,结合一对顺式烯烃质子信号数据,可证实此结构中存在1个3-甲基-3-羟基-1-丁烯片段。同时可观察到h-1
″′
(δ
h 5.50)与 c-3
′
(δ
c 106.1),c-4
′
(δ
c 158.7)有相关,证明该结构片段在苯环上的连接位置是c-3
′
位。
[0053]
综合以上数据,证实了苯环上的取代基团的结构,从而推断出该化合物结构。结合1d和2d nmr谱信息,对蓝莓多酚-a进行了全归属。综合以上的结构解析,鉴定化合物的结构
并命名为蓝莓多酚-a。
[0054]
表1蓝莓多酚-a 1d and 2d nmr数据(cdcl3,δppm)
[0055][0056][0057]
蓝莓多酚-b:
[0058]
淡黄色油状物,薄层层析后,香草醛-浓硫酸加热反应显红色。hr-esi-ms 显示准分子离子峰m/z 357.1678[m+na]
+
(c
19h26
o5na,理论计算值:357.1672)确定分子式为c
19h26
o5,不饱和度为7。
[0059]
如图5所示,1h nmr(400mhz,cdcl3)谱中共显示24个质子信号。δ
h 14.19(1h,s)提示有1个苯环上的羟基氢信号;该化合物还有2组烯烃质子信号δ
h 6.52(1h,overlapped),6.64(1h,dd,j=16.2,7.0hz)和δ
h 6.51(1h,overlapped),5.62(1h,d,j=10.0hz);6个甲基质子信号[δ
h 3.77(3h,s),2.68(3h,s),1.48(6h,s),1.09(6h,d,j=6.5hz)],其中2个是连氧甲基信号[δ
h 3.77(3h,s),2.68(3h,s)]。
[0060]
如图6所示,
13
c nmr(100mhz,cdcl3)谱中共出现19个碳信号,结合图7 所示的dept-135谱可知其分别为8个季碳、5个次甲基和6个甲基。低场区可见δ
c 203.6的1个酮羰基信号;δ
c 142.6,115.7和δ
c 128,116.9为2对双键碳信号;δ
c 163.9,157.9,157.3,110.7,108.6,107.1可推测为苯环的碳信号。根据以上数据,推测化合物可能是酰基间苯三酚类化合物。
[0061]
将蓝莓多酚-b的nmr数据与蓝莓多酚-a对比,发现二者碳的化学位移非常相似。除了都有2,4-二羟基苯乙酮的骨架之外,二者也都存在一个3-甲基-3
‑ꢀ
羟基-1-丁烯片段[δ
h 6.51(1h,overlapped),5.62(1h,d,j =16.2,7.0hz),1.48(6h,s)]。两者的区别在于与蓝
莓多酚-a比,c-1
″
位上的化学位移由δ
c 22.5变成烯烃碳信号δ
c 115.7,而c-3
″
位上的化学位移由δ
c 131.3 向高场移至δ
c 33.2。因此推测该化合物可能为蓝莓多酚-a上苯环侧链取代位 c-2
″
的双键位置发生改变的产物。
[0062]
如图8所示,在1h-1
h cosy谱中,h-2
″
(δ
h 6.64)
″
与h-1
″
(δ
h 6.52)有相关,同时可见h-3
″
(δ
h 2.46)与h-2
″
(δ
h 6.64),h-4
″
/5
″
(δ
h 1.09)有相关,可证明该化合物中有一个3-甲基-1-丁烯基团。
[0063]
如图9所示,在hmbc谱中,可以观察到h-1
″
(δ
h 6.52)与c-4
′
(δ
c 163.9),c-5
′
(δ
c 110.7),c-6
′
(δ
c 157.9)有相关,可证实此结构中的3-甲基-1
‑ꢀ
丁烯片段连接在c-5
′
位。
[0064]
综合以上数据,证实了苯环上的取代基团的结构,从而推断出该化合物结构。结合1d和2d nmr谱信息,对蓝莓多酚-b进行了全归属。综合以上的结构解析,鉴定化合物的结构,命名为蓝莓多酚-b。
[0065]
表2蓝莓多酚-b 1d and 2d nmr数据(cdcl3,δppm)
[0066][0067]
蓝莓多酚-c:
[0068]
黄色油状物,薄层层析后,香草醛-浓硫酸加热反应显红色。hr-esi-ms显示准分子离子峰m/z 335.1855[m+h]
+
(c
19h27
o5,理论计算值:335.1853)确定分子式为c
19h26
o5,不饱和度为7。
[0069]
如图10所示,1h nmr(400mhz,cdcl3)谱中共显示24个质子信号。δ
h 13.74 (1h,s)提示有1个苯环上的羟基氢信号;δ
h 5.22(1h,m),3.28(2h,d,j =7.3hz),1.79(3h,s),1.67(3h,s)提示分子中含有一个3-甲基-2-丁烯基团。此外,该化合物还有1组顺式烯烃质
子信号[δ
h 5.60(1h,d,j =10.0hz),6.50(1h,d,j=10.0hz)];4个甲基单峰质子信号[δ
h 3.76(3h,s),2.68(3h,s),1.44(6h,s)]。
[0070]
如图11所示,
13
c nmr(100mhz,cdcl3)谱中共出现19个碳信号,如图12 所示,结合dept-135谱可知其分别为9个季碳、3个次甲基、1个亚甲基和6 个甲基。低场区可见δ
c 203.3的1个酮羰基信号;δ
c 128.1,116.9和δ
c 122.3,131.5为2对双键碳信号;根据δ
c 163.6,158.1,157.0,113.3,108.8,107.0可推测为苯环的碳信号。根据以上数据,推测蓝莓多酚-c可能是酰基间苯三酚类化合物。
[0071]
将蓝莓多酚-c的nmr数据与化合物蓝莓多酚-a对比,发现两者碳的化学位移非常相似,并且所有碳的类型都一致。除了都有1个3-甲基-2-丁烯基团外,二者也都存在1个3-甲基-3-羟基-1-丁烯片段[δ
h 5.60(1h,d,j =10.0hz),6.50(1h,d,j=10.0hz),1.44(6h,s)]。与化合物蓝莓多酚-a比,蓝莓多酚-c苯环上碳的化学位移都发生了较大的变化。因此推测该化合物可能为蓝莓多酚-a上苯环c-3
′
与c-5
′
连接的侧链取代基团的连接位置发生改变的产物。
[0072]
如图13所示,在hmbc谱中,可以观察到h-1
″
(δ
h 5.60)与c-5
′
(δ
c 107.0), c-6
′
(δ
c 157.0)有相关,可证实此结构中的3-甲基-3-羟基-1-丁烯片段连接在 c-5
′
位。同时可观察到h-1
″′
(δ
h 3.28)与c-2
′
(δ
c 158.1),c-3
′
(δ
c 113.3),c-4
′
(δ
c 163.6)有相关,证明3-甲基-2-丁烯片段在苯环上的连接位置是c-3
′
位。
[0073]
综合以上数据,证实了苯环上的取代基团的结构,从而推断出该化合物结构。结合1d和2d nmr谱信息,对蓝莓多酚-c进行了全归属。
[0074]
表3蓝莓多酚-c 1d and 2d nmr数据(cdcl3,δppm)
[0075][0076]
综合以上的结构解析,鉴定出化合物的结构,命名为蓝莓多酚-c。
[0077]
(3)活性益生菌筛选方法
[0078]
基于构建的轮状病毒感染诱发的小鼠腹泻模型评价多种益生菌的保护活性。实验结果显示,长双歧杆菌、乳双歧杆菌、短双歧杆菌、罗伊氏乳杆菌、副干酪乳杆菌对轮状病毒感染诱发的腹泻小鼠保护活性最佳。
[0079]
(4)组合物的制备方法
[0080]
山楂活性多糖、活性天然产物蓝莓多酚类化合物及益生菌组合物,具体配方如下:
[0081]
配方:分子大小在1-3kd之间的山楂多糖1g、蓝莓多酚-a 0.005g、蓝莓多酚-b 0.005g、蓝莓多酚-c 0.005g,长双歧杆菌冻干粉0.05g、乳双歧杆菌冻干粉0.05g、短双歧杆菌冻干粉0.05g、罗伊氏乳杆菌冻干粉0.05g、副干酪乳杆菌冻干粉0.05g。
[0082]
将分子大小在1-3kd之间的山楂多糖1g、蓝莓多酚-a 0.005g、蓝莓多酚-b0.005g、蓝莓多酚-c 0.005g混匀,加去离子水调成固含量为3-30%的浆状液体;将获得的浆状液体冻干获得混合冻干粉,将混合冻干粉加入长双歧杆菌冻干粉 0.05g、乳双歧杆菌冻干粉0.05g、短双歧杆菌冻干粉0.05g、罗伊氏乳杆菌冻干粉0.05g、副干酪乳杆菌冻干粉0.05g混匀,再次冻干,即可制得本发明的组合物。
[0083]
本发明对缓解病毒性感染造成的肠道屏障、功能损伤、腹泻,增强肠道免疫力应用实验
[0084]
将4日龄乳鼠按窝分为正常组、模型组、利巴韦林组、活性多糖(分子大小在1-3kd之间的山楂多糖)组、活性天然产物(蓝莓多酚-a、蓝莓多酚-b、蓝莓多酚-c之间质量比为1:
1:1)组、益生菌(长双歧杆菌与乳双歧杆菌、短双歧杆菌、罗伊氏乳杆菌、副干酪乳杆菌之间质量比为1:1:1:1:1)组、本发明组合物组,每组10只。正常组灌服dmem培养液100μl/只;模型组和给药组灌服sa-11株rv液(100tcid
50
,100倍病毒的半数组织培养感染剂量),100μl/ 只,a群轮状病毒检测试剂盒检测结果为阳性时表明造模成功。24h后,利巴韦林组0.1g/kg/d、活性多糖组0.1g/kg/d、活性天然产物组0.1g/kg/d、益生菌组0.05g/kg/d、本发明的组合物组0.1g/kg/d剂量灌服,灌服量均为100l;正常组及模型组灌服双蒸水,每日1次,连续5d。
[0085]
每日记录各组乳鼠临床特征:精神状况、皮肤脱水情况、肛门红肿及腹部膨胀等现象。每日记录每只乳鼠的体重,连续记录6d(造模1d,给药5d,一共 6d)。计算乳鼠体重增长情况。轻按每只乳鼠腹部,观察其排出的粪便,基于乳鼠粪便的颜色、形态对其腹泻程度进行评分并记录腹泻分数,分为0~4分。0 分:没有粪便;1分:正常大便;2分:淡黄色软便;3分:淡黄色稀便;4分:水样便。腹泻分数的判断由同一人完成。
[0086]
给药第1日和第5日,收集各组每只乳鼠大便分别置于1.5ml无菌ep管,按a群轮状病毒检测试剂盒使用说明书进行检测rv抗原,计算rv抗原转阴率, rv抗原转阴率=(给药第1日rv阳性个数-给药第5日rv阳性个数给药)/第 1日rv阳性个数。
[0087]
第5日给药1h后,断颈采血,处死乳鼠,取血液于无菌ep管中,4℃1000
ꢀ×
g离心10min取血清,elisa试剂盒检测ifn-α/β、tnf-α、il-1β、 caspase-1。western blot检测肠组织中p65、nf-κb、肠道细胞紧密连接蛋白-1(tjp-1)、紧密连接蛋白-4(claudin-4)蛋白表达情况。
[0088]
结果如下:
[0089]
正常组乳鼠从实验开始到结束,大便呈黄棕色颗粒状,未见腹泻,皮肤红润饱满。
[0090]
模型组和各给药组乳鼠在感染rv后12~24h,出现腹部膨胀,体毛蓬松,活力下降,皮肤皱缩等现象,并陆续出现腹泻。模型组在造模后到实验结束持续腹泻。
[0091]
利巴韦林组、本发明组合物组给药第2日腹泻程度减轻或没有出现腹泻,精神明显好转,活动能力提升;在给药第3日本发明组合物组乳鼠腹泻程度明显减轻,在给药第5日基本不再出现腹泻;其中,本发明组合物组的临床表现和利巴韦林组差异无统计学意义。
[0092]
表4活性多糖、活性天然产物及益生菌组合物对各组小鼠体重增长情况的影响
[0093][0094]
由表4可看出,与正常组相比,模型组乳鼠在造模后第1日体重增长较正常组缓慢(p<0.05),造模后第2~5日体重增长较正常组更缓慢(p<0.01);与模型组相比,给药第3日,活性多糖、活性天然产物及益生菌组合物组和利巴韦林组乳鼠体重增长较模型组快(p<0.05),其余各给药组体重增长较慢;与利巴韦林组比较,给药第5日,活性多糖组、活性天然产物组及益生菌组体重增长缓慢(p<0.05),在整个给药过程中,活性多糖、活性天然产物及益生菌组合物组乳鼠体重增长与利巴韦林组差异无统计学意义(p>0.05)。相比于活性多糖组、活性天然产物组及益生菌组,活性多糖、活性天然产物及益生菌组合物组的保护
活性比单独使用活性多糖、活性天然产物或益生菌,其治疗效果更佳。
[0095]
表5活性多糖、活性天然产物及益生菌组合物对各组小鼠不同给药天数的粪便指数的影响
[0096][0097]
由表5可看出,与正常组相比,模型组乳鼠粪便指数明显大于正常组(p< 0.01);与模型组相比,给药第2日,各给药组乳鼠粪便指数均有下降,给药第 3~5日,各个给药组乳鼠粪便指数均下降明显(p<0.05)。给药第1~5日活性多糖、活性天然产物及益生菌组合物组乳鼠粪便指数下降情况接近于利巴韦林组(p>0.05)。表明活性多糖、活性天然产物及益生菌组合物具有优异的抗rv 乳鼠腹泻的功效。
[0098]
表6活性多糖、活性天然产物及益生菌组合物对感染rv乳鼠抗原转阴率的影响
[0099][0100]
由表6可看出,经5d给药干预后,与模型组比较,各给药组乳鼠rv抗原转阴率明显高于模型组,其中活性多糖、活性天然产物及益生菌组合物组与利巴韦林组转阴率高达100%。
[0101]
表7活性多糖、活性天然产物及益生菌组合物对感染rv乳鼠血清ifn-α/β含量
[0102][0103]
由表7可看出,感染rv后,与正常组相比,模型组乳鼠血清ifn-α/β含量高于正常组,且差异具有统计学意义(p<0.01);给活性多糖、活性天然产物及益生菌组合物药干预后,给药组乳鼠血清ifn-α/β水平含量均高于模型组(p<0.01),乳鼠血清ifn-α/β含量与利巴韦林组接近。
[0104]
如图14所示,与正常对照组比较,模型组小鼠il-1β、tnf-α、caspase-1 表达明显升高,差异有统计学意义(p《0.01);而与模型组比较,活性多糖、活性天然产物及益生菌组合物组l-1β、tnf-α、caspase-1表达明显下调,差异有统计学意义(p《0.01)。
[0105]
如图15所示,与正常对照组比较,模型组p65、nf-κb、claudin-4蛋白表达显著上调,tjp-1蛋白表达显著下降,差异有统计学意义(p《0.01);与模型组比较,活性多糖、活性天然产物及益生菌组合物组p65、nf-κb、claudin-4 蛋白表达明显下调,tjp-1蛋白表达显著升高,差异有统计学意义(p《0.01)。
[0106]
本发明的急性毒性试验
[0107]
1、试验动物:昆明种小鼠,体重20
±
2g,由广东省实验动物中心提供
[0108]
2、药物:本发明的组合物。
[0109]
3、试验方法:根据国家药品监督管理局颁布修订的“中药新药研究技术要求”,对本发明的含活性多糖、活性天然产物及益生菌组合物进行急性毒性实验。因受药物浓度及体积限制,无法测定ld
50
,故进行最大给药量实验。取昆明种小鼠30只,雌性各半,灌胃给予本发明组合物1g/ml,每只0.8ml,即小鼠的最大灌胃体积用药后观察小鼠活动状态、饮食、粪便、呼吸、体重及死亡情况,连续观察14d。
[0110]
4、试验结果:各组小鼠灌胃给药后生长良好,体重增加,行为正常,均未见死亡及明显反应。将动物处死后,肉眼观察各主要脏器无异常现象。
[0111]
结果表明,本发明的组合物最大剂量口服应用,对动物无明显损害,未发现对机体产生的毒性反应,是一种安全可靠的食物、膳食补充剂、功能性食品或药物。
[0112]
实施例2
[0113]
本实施例与实施例1的不同之处在于,本实施例所述益生菌选用长双歧杆菌、乳双歧杆菌两种,山楂活性多糖、蓝莓多酚-a、蓝莓多酚-b、长双歧杆菌、乳双歧杆菌的质量比为1:0.0075:0.0075:0.125:0.125,长双歧杆菌、乳双歧杆菌各0.125g。
[0114]
进一步地,益生菌可以包括长双歧杆菌、乳双歧杆菌、短双歧杆菌、罗伊氏乳杆菌、副干酪乳杆菌中的一种或几种的组合物。
[0115]
进一步地,益生菌包括长双歧杆菌、乳双歧杆菌、短双歧杆菌、罗伊氏乳杆菌、副干酪乳杆菌,山楂活性多糖、蓝莓多酚-b、蓝莓多酚-c、长双歧杆菌、乳双歧杆菌、短双歧杆菌、罗伊氏乳杆菌、副干酪乳杆菌的质量比为 1:0.0015:0.0015:0.1:0.1:0.1:0.1:0.1。
[0116]
进一步地,益生菌包括长双歧杆菌、乳双歧杆菌、短双歧杆菌、罗伊氏乳杆菌、副干酪乳杆菌,山楂活性多糖、蓝莓多酚-a、蓝莓多酚-c、长双歧杆菌、乳双歧杆菌、短双歧杆菌、罗伊氏乳杆菌、副干酪乳杆菌的质量比为 1:0.015:0.015:0.01:0.01:0.01:0.01:0.01。
[0117]
进一步地,益生菌选用罗伊氏乳杆菌,山楂活性多糖、蓝莓多酚-a、蓝莓多酚-b、蓝莓多酚-c、及罗伊氏乳杆菌的质量百分比为 1:0.007:0.005:0.006:0.4。
[0118]
进一步地,制备山楂活性多糖时,山楂多糖水溶液可以选用孔径为15kd,或10kd、5kd、3kd、1kd的不同透析袋透析,分别收集分子量为10-15kd,或5-10kd、 3-5kd、1-3kd、小于1kd的透析液。
[0119]
前述的实例仅是说明性的,用于解释本发明所述方法的一些特征。所附的权利要求旨在要求可以设想的尽可能广的范围,且本文所呈现的实施例仅是根据所有可能的实施例的组合的选择的实施方式的说明。因此,申请人的用意是所附的权利要求不被说明本发明的特征的示例的选择限制。在权利要求中所用的一些数值范围也包括了在其之内的子范围,这些范围中的变化也应在可能的情况下解释为被所附的权利要求覆盖。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1