一种提高二甲双胍格列本脲稳定性的组合物及其制备方法与流程
:
1.本发明属于药物制剂领域,具体涉及一种提高二甲双胍格列本脲稳定性的组合物及其制备方法。
背景技术:
2.糖尿病是一种以高血糖为特征的代谢性的疾病。高血糖是由于胰岛素分泌缺陷或其生物作用受损,或两者兼有引起。长期存在高血糖,导致各种组织,特别会造成眼睛、肾脏、心脏、血管、神经的慢性损害和功能性的障碍。
3.糖尿病分为1型和2型,1型糖尿病需要用胰岛素治疗。2型糖尿病患者可采用口服降糖类药物,或采用联合治疗方式。
4.目前治疗2型糖尿病的药物根据作用机制不同,包括:减少肝脏中葡萄糖的形成,如二甲双胍;能够刺激胰腺β细胞分泌更多的胰岛素,如格列本脲;激活氧化物酶体增殖物激活受体γ增强胰岛素的生物效应,如吡格列酮;抑制肠道内葡萄糖的生成,如阿卡波糖;促进胰腺的β细胞分泌胰岛素,如利拉鲁肽;抑制体内glp-1的降解,如西格列汀。
5.最初针对2型糖尿病患者,治疗方法包括饮食控制和锻炼,当小疗法不够时,服用口服抗糖尿病药物。如治疗效果不加,合用不同作用机理的药物,进行联合疗法。二甲双胍和格列本脲为不同作用机理药物,两种药物同时服用,避免患者服用单一成分,而导致病情不可控;同时避免过量服用同一组分而引起的低血糖。
6.本发明人在研究二甲双胍格列本脲复方制剂过程中,发现两种原料药相容性较差,为改善本药物的稳定性,发明人经过了大量的试验,将格列本脲进行制粒,避免两个药物直接接触,解决了稳定性的问题。在制备过程中,发现二甲双胍占比较大,可压性较差及对溶出曲线影响较大,发明人通过对粘合剂比例的筛选,选出合适的粘合剂用量,解决了可压性问题及与参比制剂溶出曲线拟合的问题。
技术实现要素:
7.本发明的目的是提供一种提高二甲双胍格列本脲稳定性的组合物及其制备方法。
8.本发明采用的技术方案如下:
9.一种稳定的二甲双胍格列本脲口服药物组合物,其特征在于,采用粘合剂,利用流化床制粒工艺,将格列本脲进行包裹,避免二甲双胍和格列本脲原料药直接接触,提高制剂的稳定性。
10.所述的组合物中的药物赋形剂,包括填充剂、粘合剂、崩解剂、润滑剂,或它们的任意组合物。处方中粘合剂用量15~35mg/片,崩解剂用量8~20mg/片,填充剂用量40~70mg/片,润滑剂用量4~9mg/片。
11.所述的组合物,其特征在于所述的组合物包括格列本脲颗粒层和二甲双胍颗粒层;按重量百分比计,其中格列本脲颗粒层:填充剂为2.0%~3.0%,粘合剂为1.5%~2.5%,崩解剂为0.2%~0.5%;二甲双胍颗粒层,填充剂为3.0%~10.0%,粘合剂为2.0%
~3.0%,崩解剂为1.0~3.0%;润滑剂在组合物中为0.5%~1.5%。
12.所述的组合物中,粘合剂为聚维酮、羟丙基纤维素、羟丙甲纤维素中一种,或两种的组合物,优选聚维酮。
13.粘合剂型号,分别为聚维酮k30、聚维酮k90、羟丙基纤维素-l、羟丙基纤维素-sl、羟丙基纤维素-ssl、羟丙甲纤维素-e5、羟丙甲纤维素-e50,优选聚维酮k30。聚维酮k30最佳用量为25mg/片,其中格列本脲颗粒聚维酮k30最佳用量为10mg/片,二甲双胍颗粒最佳用量为15mg/片。
14.所述组合物中崩解剂为交联羧甲基纤维素钠、交联聚维酮、羧甲基淀粉钠、低取代羟丙基纤维素中一种,或两种组合物,优选交联羧甲基纤维素钠。
15.所述组合物,其特征在于填充剂为微晶纤维素、玉米淀粉、乳糖中一种,或两种组合物,优选微晶纤维素。
16.所述的组合物,其特征在于润滑剂为硬脂酸镁、滑石粉、硬脂酸、胶态二氧化硅中的一种,或两种组合物,优选硬脂酸镁。
17.所述的组合物,制备方法为:
18.①
格列本脲层:将格列本脲进行粉碎,称量并将处方量的格列本脲和处方中填充剂放入流化床中混合。采用粘合剂,喷雾制粒并干燥。
19.②
二甲双胍层:将二甲双胍过40目筛,称量并将处方量的二甲双胍和处方中填充剂放入湿法制粒机中,进行混合。加入粘合剂,进行制粒;将上述颗粒干燥,并过筛。
20.③
将格列本脲和二甲双胍颗粒进行混合和过筛,压片、包衣。
21.创新点:制备过程二甲双胍格列本脲过程中,二甲双胍占比较大,原料药可压性较差,通过对粘合剂比例筛选,找出合适比例的粘合剂,提高二甲双胍颗粒的可压性,且溶出曲线能够与参比制剂溶出拟合。二甲双胍和格列本脲相容性较差,通过将两种颗粒分别制粒,避免两种原料药的接触,提高组合物的稳定性。
22.有益效果:
23.本发明涉及一种提高二甲双胍格列本脲稳定的组合物。二甲双胍和格列本脲两种药物,相容性较差,通过粘合剂将格列本脲包裹,避免两种药物的直接接触,提高制剂的稳定性,保证在患者服用药物期间,不会因杂质产生不可控的不良反应。
24.本发明涉及的制备工艺,将二甲双胍和格列本脲分开制粒,所制备样品,可压性好,工艺重现性良好,溶出行为与参比制剂一致,符合片剂质量和稳定性要求。
附图说明:
25.图1为本发明和参比制剂盐酸二甲双胍溶出曲线对比,
26.图2为本发明和参比制剂格列本脲溶出曲线对比。
具体实施方式:
27.本发明通过以下制备实施例和对比实施例详细阐述本发明,所述实施例不应被认为是局限性的。
28.实施例1
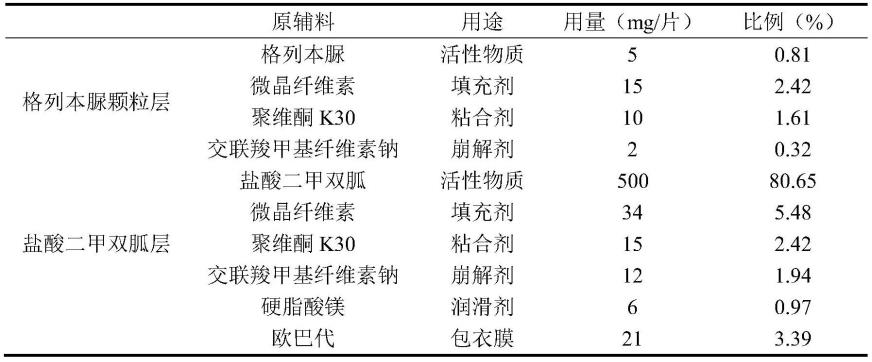
29.表1制备实施例1处方组成
[0030][0031]
制备工艺:
[0032]
格列本脲层:
[0033]
1)原辅料处理:格列本脲机械粉碎,并过80目筛;微晶纤维素、交联羧甲基纤维素钠、硬脂酸镁等辅料,分别过40目筛。
[0034]
2)粘合剂配制:将聚维酮k30配制为8%粘合剂。
[0035]
3)制粒:
[0036]
①
预混:按照处方组成,将格列本脲层中格列本脲、微晶纤维素、交联羧甲基纤维素钠,放入流化中,设置进风温度为45℃~65℃,进风风量为500~800m3/h,开启进风温度和风量,使物料混合均匀。
[0037]
②
流化床制粒:待物料温度达到50℃,将上述2)中的粘合剂,采用顶喷的方式,喷入粘合剂,至粘合剂喷至完全,干燥,获得颗粒。其中设定雾化压力为2000-3000mbar,其中粘合剂溶液喷入速度范围为30~50rpm,进风温度为45℃~65℃,进风风量为500~800m3/h。
[0038]
③
干整粒:将上述流化床中所制的颗粒,过40目筛整粒。
[0039]
盐酸二甲双胍层:
[0040]
1)原辅料处理:二甲双胍、微晶纤维素、交联羧甲基纤维素钠、硬脂酸镁,分别过40目筛。
[0041]
2)粘合剂配制:将聚维酮k30配制为5%粘合剂
[0042]
3)制粒:
[0043]
①
预混:按照处方组成,将二甲双胍、微晶纤维素和交联羧甲基纤维素钠,放入湿法制粒机中,设定搅拌速度5rpm/s,剪切速度1rpm/s,混合5min。
[0044]
②
制粒:将粘合剂喷入湿法制粒机中,设定搅拌速度5rpm/s,剪切速度50rpm/s,制粒时间2-3min,将上述湿颗粒过40目筛。
[0045]
③
干燥:将上述湿颗粒放入烘箱或流化床中,干燥至水分小于2%。
[0046]
④
整粒:将干燥后颗粒40目筛整粒。
[0047]
1)总混:按照处方组成,将格列本脲和二甲双胍颗粒,进行混合。再加入处方量的硬脂酸镁,混合5min。
[0048]
2)压片和包衣:将上述总混颗粒,进行压片和包衣。
[0049]
实施例2
[0050]
表2制备实施例2处方组成
[0051][0052]
制备工艺:
[0053]
格列本脲层:
[0054]
1)原辅料处理:格列本脲机械粉碎,并过80目筛;微晶纤维素、交联羧甲基纤维素钠、硬脂酸镁等辅料,分别过40目筛。
[0055]
2)粘合剂配制:将羟丙基纤维素-l配制为8%粘合剂。
[0056]
3)制粒:
[0057]
①
预混:按照处方组成,将格列本脲层中格列本脲、微晶纤维素、交联羧甲基纤维素钠,放入流化中,设置进风温度为45℃~65℃,进风风量为500~800m3/h,开启进风温度和风量,使物料混合均匀。
[0058]
②
流化床制粒:待物料温度达到50℃,将上述2)中的粘合剂,采用顶喷的方式,喷入粘合剂,至粘合剂喷至完全,干燥,获得颗粒。其中设定雾化压力为2000-3000mbar,其中粘合剂溶液喷入速度范围为30~50rpm,进风温度为45℃~65℃,进风风量为500~800m3/h。
[0059]
③
干整粒:将上述流化床中所制的颗粒,过40目筛整粒。
[0060]
盐酸二甲双胍层:
[0061]
1)原辅料处理:二甲双胍、微晶纤维素、交联羧甲基纤维素钠、硬脂酸镁,分别过40目筛。
[0062]
2)粘合剂配制:将羟丙基纤维素-l配制为5%粘合剂
[0063]
3)制粒:
[0064]
①
预混:按照处方组成,将二甲双胍、微晶纤维素和交联羧甲基纤维素钠,放入湿法制粒机中,设定搅拌速度5rpm/s,剪切速度1rpm/s,混合5min。
[0065]
②
制粒:将粘合剂喷入湿法制粒机中,设定搅拌速度5rpm/s,剪切速度50rpm/s,制粒时间2-3min,将上述湿颗粒过40目筛。
[0066]
③
干燥:将上述湿颗粒放入烘箱或流化床中,干燥至水分小于2%。
[0067]
④
整粒:将干燥后颗粒40目筛整粒。
[0068]
4)总混:按照处方组成,将格列本脲和二甲双胍颗粒,进行混合。再加入处方量的硬脂酸镁,混合5min。
[0069]
5)压片和包衣:将上述总混颗粒,进行压片和包衣。
[0070]
对比例1:(制备工艺为常规湿法制粒)
[0071]
处方组成与实施例1中处方组成相同。
[0072]
制备工艺为:
[0073]
1)原辅料处理:将处方中格列本脲机械粉碎,并过80目筛;其余辅料分别过40目筛。
[0074]
2)粘合剂配制:将处方量中聚维酮k30配制为10%粘合剂。
[0075]
3)制粒:
[0076]
①
预混:按照处方组成,将格列本脲、盐酸二甲双胍、微晶纤维素、交联羧甲基纤维素钠混合,设定搅拌速度5rpm/s,剪切速度1rpm/s。
[0077]
②
制粒:将粘合剂喷入湿法制粒机中,设定搅拌速度5rpm/s,剪切速度50rpm/s,制粒时间2-3min,将上述湿颗粒过40目筛。
[0078]
4)干燥:将上述湿颗粒放入烘箱或流化床中,干燥至水分小于2%。
[0079]
5)整粒:将干燥后颗粒40目筛整粒。
[0080]
6)总混:将上述整粒后的颗粒,再加入处方量的硬脂酸镁,混合5min。
[0081]
7)压片和包衣:将上述总混颗粒,进行压片和包衣。
[0082]
对比例2:(格列本脲颗粒层聚维酮k30用量减少)
[0083]
表3制备对比例2处方组成
[0084][0085][0086]
对比例3:(二甲双胍颗粒层聚维酮k30用量减少)
[0087]
表4制备对比例3处方组成
[0088][0089]
对比例4(二甲双胍颗粒层聚维酮k30用量增加)
[0090]
表5制备对比例4处方组成
[0091][0092]
制备工艺同实施例1。
[0093]
脆碎度和硬度考察:
[0094]
脆碎度测定法:参考2020年版《中国药典》四部通则0923片剂脆碎度检查法,称取片剂6.5g,用吹风机吹去片剂脱落的粉末,精密称重,将片剂置于片剂脆碎度检查仪中,转动100次,取出,网法除去粉末,精密称重。
[0095]
硬度测定法:将上述实施例的片剂,放入硬度检测仪中,检测。
[0096]
崩解时限测定法:测定法:参考2020年版《中国药典》四部通则0921崩解时限检查法,取供试品6片,分别置崩解仪中吊篮的玻璃管中,启动崩解仪,记录片剂完全崩解的时间。
[0097]
表6片剂检测结果
[0098]
[0099]
由表可以看出,对比实施例3中,将二甲双胍颗粒层粘合剂用量降低,颗粒可压性下降,脆碎度不满足药典要求。
[0100]
稳定性试验:
[0101]
参考《化学药物(原料药和制剂)稳定性研究技术指导原则》,对上述实施例(除对比实施例3)样品,放置40℃
±
2℃/rh75%
±
5%条件下,放置6个月,进行加速试验考察,于1月、2月、3月、6月末各取样一次,检测有关物质,结果与0月比较,结果如表所示:
[0102]
表7加速条件格列本脲有关物质(%)检测结果
[0103][0104][0105]
由表1可以看出,实施例1和实施例2格列本脲稳定性较好,对比例1和对比例2稳定性结果较差,尤其杂质n(酸降解杂质)增长较快。
[0106]
对比例1制备工艺为常规湿法制粒,二甲双胍和格列苯脲接触较为充分。对比例2制备工艺中聚维酮k30的用量较少,格列本脲层颗粒,可能会暴露部分原料药,该原料药可能会与二甲双胍颗粒接触。对比例1和对比例2均未有效阻断二甲双胍和格列本脲的相互作用。实施例1和实施例2中无论采用聚维酮k30还是羟丙甲纤维素,均有效的将两种原料药阻断,提高了格列本脲的稳定性。
[0107]
溶出曲线考察:
[0108]
测定法:取本品,照溶出度与释放度测定法(中国药典2020年版四部0931中第三法),以900ml、ph4.5+0.4%sds作为溶出介质,温度设定为37℃、转速为50rpm,依法操作,液相分别检测盐酸二甲双胍和格列本脲的含量。
[0109]
表8实施例1-2、对比例4和参比制剂盐酸二甲双胍溶出曲线对比
[0110][0111]
表9实施例1-2、对比例4和参比制剂格列本脲溶出曲线对比
[0112][0113]
上述实施例1-2检测溶出曲线,对比参比制剂在ph4.5+0.4%sds介质的溶出,结果在该条件下,实施例1和实施例2中二甲双胍和格列本脲与参比制剂溶出曲线拟合较好(f2》50)。
[0114]
对比例4中,在ph4.5+0.4%sds介质中,实施例4中二甲双胍颗粒中含聚维酮k30用量为4.03%,较高的粘合剂比例,致使二甲双胍颗粒偏硬,溶出较参比制剂偏慢(f2《50)。格列本脲与参比制剂在该介质中拟合较好(f2》50)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1