一种利用萤石矿含钙废液制备硫酸钙的方法与流程
本发明涉及一种含钙废液的无害化处理方法,具体涉及到一种利用萤石精矿酸浸提纯产生的含钙废液制备高品质硫酸钙产品的方法。
背景技术:
萤石,又称氟石,是工业上氟元素的主要来源,是世界上20几种重要的非金属矿物原料之一。萤石的用途十分广泛,随着科学技术的进步,应用前景越来越广阔。目前主要应用于冶金、炼铝、玻璃、陶瓷、水泥、化学工业。纯净无色透明的萤石可作为光学材料,色泽艳丽的萤石亦可作为宝玉石和工艺美术雕刻原料。萤石又是氟化学工业的基本原料,其产品广泛应用于航天、航空、制冷、医药、农药、防腐、灭火、电子、电力、机械和原子能等领域。
萤石矿主要成分为caf2,常伴生方解石碳酸钙矿物,两种矿物均为含钙矿物,其表面化学性质相近,矿物可浮性相近,常规的浮选工艺不能完全实现萤石和方解石的有效分离,萤石精矿品位偏低。为了进一步提高萤石精矿品位,大部分的萤石生产企业采用往萤石精矿矿浆中加入盐酸进行溶浸,将萤石精矿残留的少量碳酸钙变为氯化钙溶液而除掉,从而进一步提高萤石精矿的品位,但与此同时,氯化钙溶液中的cacl2不断富集,达到一定浓度(一般cacl2含量达到20%)后就不能再用于萤石精矿盐酸溶浸调浆,变成必须外排的cacl2酸性废液,这些高浓度的cacl2酸性废液成为萤石矿开采企业污染环境的一大污染源,如何将此部分cacl2酸性废液实现低成本的无害处理就成为萤石矿开采企业面临的现实问题。
工业上对于cacl2母液的处理通常采用多效蒸发工艺回收其中的cacl2,该工艺往往适合高浓度cacl2母液(30%以上),当cacl2浓度低于30%时,蒸发量过大,能耗高,处理成本高,经济效益差,并不适用。处理低浓度cacl2废液(低于0.5%)的工艺是通过电渗析、反渗透膜浓缩、纳滤膜过滤、离子交换吸附等富集母液中的cacl2浓度,但这些工艺往往投资大、能耗高、运营成本高,由于经济成本和投资效费比不过关,大大限制了该类工艺在萤石精矿除杂形成的cacl2废液处理中的应用。目前,萤石矿含钙废液的处理大多采用硫酸与cacl2废液反应生成石膏的方法除去ca2+,同时得到稀盐酸,稀盐酸可循环用于萤石精矿除钙,但这种方法的缺点是得到的硫酸钙粒度极细(平均粒度仅为5~20微米),过滤、干燥等脱水效率低、能耗高,且硫酸钙的杂质含量高,无法转化为使用价值更高的硫酸钙产品对外销售,废液处理效益欠佳。
cn111547756a的发明公开了一种含有机物的氯化钙废液的处理方法,包括如下步骤:s1,向含有机物的氯化钙废液中加入硫酸钠进行沉淀反应生成硫酸钙和氯化钠,废液中的氯化钙与硫酸钠的物质的量比为1.05~1.1:1;s2,沉淀反应后向废液中加入过量碳酸钠,静止澄清,固液分离,得到沉降固体和不含固体的水溶液;s3,沉降固体经洗涤,压滤,得到硫酸钙产品;向不含固体的水溶液中加入盐酸,调节ph至6.8~7.2,然后蒸发结晶得到含有机物的固体盐,采用自蔓延热解焚烧工艺去除固体盐中的有机物,得到氯化钠产品。然而,该发明中没有涉及如何控制硫酸钙产品的粒径和纯度等手段,且工艺过程较繁琐,增加了生产制造成本和能耗。
cn102453951b的发明公开了一种利用制碱废液和废硫酸制高品质硫酸钙晶须的方法,采用制碱工业的外排废液cacl2溶液和硫酸工业产生的废硫酸,联合生成硫酸钙,制作高品质硫酸钙晶须。该发明采用制碱工业的废液cacl2溶液和硫酸工业产生的废硫酸为原料进行反应,利用晶体的成核、生长理论,控制晶体生长,得到粒径小于4μm,长径比大于200的高品质硫酸钙晶须。虽然该发明中涉及通过控制硫酸钙结晶生长获得硫酸钙晶须的过程,但该发明需要加热保温,耗能较高,反应容器、管道均要求保温,处理完后获得的硫酸钙晶须需要用去离子水或无水乙醇洗涤,工艺控制比较苛刻,尽管如此,最后获得硫酸钙晶须的粒径仍较小,同时获得难以再次利用的稀hcl,整体经济效益偏低。
cn101367538b的发明公开了一种利用含硫酸盐卤水和含钙盐卤水制取硫酸钙的方法,将两种经过精制的卤水在控制结晶反应器中和循环提升装置的循环液连续均匀混合,形成较大粒径的二水硫酸钙结晶,再经沉降、离心洗涤和干燥制备高纯度的二水硫酸钙产品。该含钙废液的无害化处理虽然工艺新颖,最终获得的二水硫酸钙的平均粒径在0.1~0.3mm,干燥后硫酸钙含量可达到98%以上,符合gb1852-2007食品添加剂硫酸钙的要求,但其需要事前先对含硫酸盐卤水和含钙卤水进行精制,需要使用特殊的控制结晶反应器和循环提升装置等反应设备,维护费用较高,且工艺条件苛刻,so42-和ca2+摩尔比严格控制在1﹕1,实际生产中难以如此精确控制,含硫酸盐卤水中so42-质量浓度较低,实际生产时,需要结晶反应器及配套的沉降器、输送泵、管道较大,投资较高。此外,该发明没有应用数学算法实现自动化控制,不利于规模化生产的工艺控制,故该发明并不能简单用于投资和运营成本要求严格的环保废水处理项目。
综上所述,探寻一种利用萤石精矿酸浸提纯产生的含钙废液制备高品质硫酸钙产品的无害化和资源化处理工艺是亟需解决的问题。
技术实现要素:
针对上述问题,本发明提供一种利用萤石矿含钙废液制备硫酸钙产品的方法。其中,对萤石精矿酸浸提纯后产生的含钙(主要为cacl2)废液,利用机械结晶技术,通过加入含so42-离子的溶液将ca2+转化成结晶硫酸钙的形式析出,从而获得具有一定粒径的高品质结晶硫酸钙产品,整个工艺简单易于实施,是一种有效利用资源,又减少污染的方法。
本发明的具体方案如下:
一种利用萤石矿含钙废液制备硫酸钙的方法,所述方法包括如下步骤:
s1:将萤石矿含钙废液和含so42-离子的溶液依次加入到反应容器中进行结晶沉淀反应;
s2:控制所述结晶沉淀反应中生成的硫酸钙结晶速率,得到硫酸钙晶体料浆;
s3:将步骤s2获得的所述硫酸钙晶体料浆经过过滤、淋滤、干燥后,得到固相产物为硫酸钙针状或晶须状海绵体,滤液为稀盐酸,其中所述硫酸钙的平均粒径≥150um,干基纯度≥95%,白度≥90;
进一步地,所述方法还包括s4:将步骤s3获得的稀盐酸浓缩后返回至萤石精矿酸浸槽循环利用。
进一步地,步骤s1的生产方式为连续生产或间歇生产。
本发明中,连续生产效率高,但往往晶体粒度略小于间歇生产,相反,间歇生产的晶体粒度较好控制,但生产效率低。
进一步地,步骤s1中,所述含so42-离子的溶液可以是硫酸,也可以是硫酸钠、硫酸镁、硫酸钾等各种水溶性硫酸盐。
进一步地,步骤s1中,所述反应容器可以是烧杯、沉淀池、搅拌槽、反应釜或结晶器。
进一步地,步骤s2中,所述萤石矿含钙废液中ca2+离子的质量百分数为2%~25%,所述含so42-离子的溶液中so42-离子的质量百分数为1%~50%;所述ca2+离子与所述so42-离子的摩尔比为1:1.1至1:0.7。
进一步地,步骤s2中,通过控制所述含钙废液和所述含so42-离子的溶液的加料速率,和/或所述硫酸钙的结晶沉淀反应时间来控制所述结晶沉淀反应中硫酸钙的结晶速率,按照所述反应容器的有效容积计算,所述含钙废液的加料速率不高于45kg/(m3·h),所述含so42-离子的溶液的加料速率不高于105kg/(m3·h),所述硫酸钙的结晶沉淀反应时间不小于3h。单位体积单位时间内加料量越大,沉淀反应速率越快,则形成的晶核越多,在硫酸钙溶质量相同情况下,晶核越多,平均分配到每个晶核上供其生长的溶质量越少,故最终晶粒越小,晶体无法长大。
进一步地,步骤s2中,通过调整反应容器的搅拌速率来控制硫酸钙晶核的生成数量,所述搅拌线速度控制在0至2m/s。
本发明中,搅拌速率越快,晶体粒度越小,反之越大。但搅拌速率太小,造成混合不均匀,反应不充分。通常,在其它有利于结晶生长的工艺条件下,在一个没有特殊结构的普通烧杯或反应釜中,如果搅拌线速度达到2m/s以上,则硫酸钙的平均粒径只有30~40um;而同等条件下,如果将搅拌线速度优选控制在0.8~1.2m/s,则硫酸钙晶体的平均粒径可达80~400微米,优选达到150~400um。
进一步地,所述反应容器的搅拌速率依靠检测获得的硫酸钙平均粒度与晶浆循环区固液质量比等工艺参数进行调整。
本发明中,影响所述硫酸钙的结晶速率或硫酸钙晶核的生长数量的因素实际上是反应容器内部流场的分布环境,而所述反应容器的内部流场主要依靠前文阐述的所述含钙废液的加料速率、所述含so42-离子的溶液的加料速率以及所述搅拌速率等手段获得有利于硫酸钙晶体的生长环境。
进一步地,调整所述反应容器的内部流场的目的,是促使反应容器内部形成抑制晶核生成同时促进晶体生长的流场环境,它表现为流场中ca2+浓度梯度和so42-浓度梯度比较平缓,晶浆循环区的固液质量比较高,而结晶生长区的固液质量比很低,且结晶生长区的流体基本不受搅拌器搅拌速率大小的影响,确保硫酸钙过饱和溶液拥有一个适合晶体生长的介稳区,因为流体流动越缓慢,越能保证硫酸钙晶核不被二次碰撞破坏(从而防止生成更多新晶核,促使有限溶质分配生长到数量较少的晶核上),越能促进硫酸钙晶体长大。
进一步地,步骤s1或s2中,加入摩尔百分数为1至10%的硫酸钙晶种,用于加快硫酸钙结晶生长速率,基于理论生成的所述硫酸钙针状或晶须状海绵体的总量计。
进一步地,步骤s2中,控制所述硫酸钙结晶的反应温度为10℃至120℃,所述硫酸钙晶体料浆中硫酸钙晶体的质量百分数为1%~25%。
进一步地,步骤s3中,对所述硫酸钙晶体料浆进行快速过滤和淋滤,在真空负压下控制过滤时间为90~120s,得到含水率低于15%的滤饼,其中,过滤的滤网材质为80至200目孔径的滤纸或滤布,淋滤所用的淋洗水为自来水或去离子水,淋洗用水量为所述硫酸钙晶体体积的10%~100%。
进一步,步骤s3中,所述硫酸钙针状或晶须状海绵为高品质硫酸钙产品,包括但不限于建筑石膏、水泥缓凝剂、模型制作材料、纸张填料、油漆填料、污水处理催化剂、食品添加剂或医用石膏等。
进一步地,步骤s3中,所述滤液中,稀盐酸的质量百分数为1%~16%,残余ca2+的质量百分数为0.2%~5%。
本发明具有以下有益的技术效果:
1、本发明对现有技术中萤石精矿酸浸提纯产生的含钙废液的处理工艺进行了显著改进。由于现有的处理工艺通常得到较小粒径(5~20微米)的硫酸钙固体,因此造成后处理工序如过滤、干燥等操作不顺畅、工序更加繁琐、低效率和高能耗;此外,这种硫酸钙固体易发生结块且杂质含量高,无法转化为使用价值更高的高品质硫酸钙产品,例如医用石膏或食品添加剂等,因此,现有技术中常规的含钙废液处理工艺的附加值不高,经济效益偏低。本发明在此基础上获得的大粒径的硫酸钙晶体是一种硫酸钙针状或晶须状海绵体,其理化性能可达到平均粒径≥150um,干基纯度≥95%,白度≥90,为高品质硫酸钙产品。
2、本发明利用机械结晶技术对萤石矿含钙废液进行无害化工艺处理。在该工艺中,通过一定手段控制硫酸钙结晶速率:(1)通过控制原料加料速率和/或硫酸钙的结晶沉淀反应时间来控制硫酸钙晶体的生长速率;(2)通过调整反应容器的搅拌速率及内部流场来控制硫酸钙晶核的生成数量,任一种或两种结合均能获得高品质硫酸钙晶体。
3、本发明工艺流程简单、操作简便顺畅、投资少、能耗低、运营成本低、项目效益好,实现了cacl2酸性废液的无害化处理和资源化利用,避免大量cacl2酸性废液给厂区周围环境带来巨大的生态环境安全隐患,大幅减少或杜绝萤石矿上对新鲜盐酸的使用,提高了萤石矿浮选生产的安全操作环境。本发明为含钙废液特别是萤石矿选矿产生的cacl2废液的无害化资源化处理提供了新技术和新思路,具有很高的应用推广价值和投资价值。
附图说明
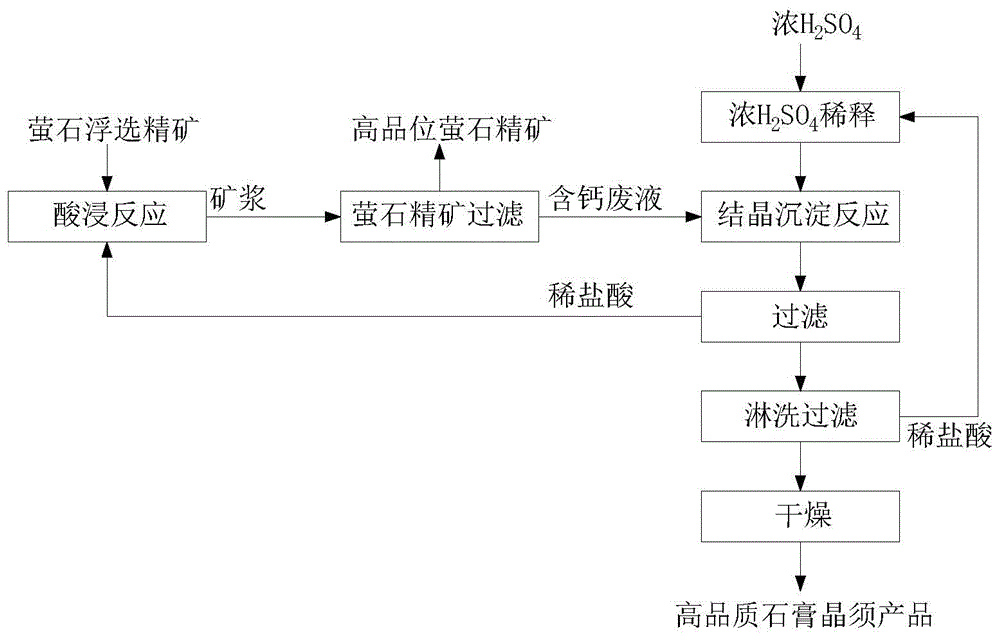
图1为本发明方法的工艺流程图;
图2a-图2b为实施例1的白色针状石膏产品的sem图谱;图2a为200倍se图谱,图2b为500倍se图谱。
实施例
以下结合实施例对发明做详细的说明:
实施例1
具体步骤如下:
s1:将萤石矿含钙废液和稀硫酸依次加入到结晶器中进行结晶沉淀反应,
萤石矿含钙废液中ca2+的质量百分数为12.49%,稀硫酸的质量百分数为10%,其中,ca2+离子与so42-离子的摩尔比为1:0.7;
s2:通过以下手段控制结晶沉淀反应中生成的硫酸钙结晶速率,得到硫酸钙晶体料浆,
其中,室温下,控制含钙废液的加料速率为23.5kg/(m3·h)、稀硫酸的加料速率为56kg/(m3·h)、硫酸钙的结晶沉淀反应时间为5h、结晶器的搅拌线速度为0.8m/s;
s3:将步骤s2获得的硫酸钙晶体料浆经过120目普通滤布快速过滤、自来水淋滤1次,用水量为硫酸钙晶体体积的20%,得到含水率为10.83%的滤饼,滤液为稀盐酸;
将滤饼在80℃下干燥,即得白色针状石膏产品,平均粒径为155um,白度为91.71,其产品β-caso4·1/2h2o质量含量达到95.57%,经简单加工可作各种建筑石膏或模型石膏;
s4:将步骤s3获得的滤液,其中hcl质量百分数为3.5%、残余ca2+的质量百分数为1.89%的稀盐酸浓缩至hcl质量百分数15%后,返回至萤石精矿酸浸槽循环利用。
由图2a-图2b的不同放大倍数的sem图谱可以看出,实施例1的二水石膏产品晶体呈纤维状,由众多细小针状晶体集合而成,长度400微米左右,宽50微米左右,与天然石膏晶体形态一致。
实施例2
具体步骤如下:
s1:将预计生产获得的caso4的5%(摩尔百分数)的晶种、萤石矿含钙废液和稀硫酸依次加入到搅拌槽中进行结晶沉淀反应,生产方式为间歇生产,
萤石矿含钙废液中ca2+的质量百分数为19.81%,稀硫酸的质量百分数为20%,其中,ca2+离子与so42-离子的摩尔比为1:1;
s2:通过以下手段控制结晶沉淀反应中生成的硫酸钙结晶速率,得到硫酸钙晶体料浆,
其中,在45℃下控制硫酸钙的结晶沉淀反应时间为3h、搅拌槽的搅拌线速度控制在0.8m/s;
s3:将步骤s2获得的硫酸钙晶体料浆经过200目普通滤布快速过滤、自来水淋滤2次,用水量为硫酸钙晶体体积的50%,得到含水率为14.70%的滤饼,滤液为稀盐酸;
将滤饼在80℃下干燥,即得白色针状石膏产品,平均粒径为202um,白度为91.83,其产品β-caso4·1/2h2o质量含量达到85.32%,经简单加工可作各种建筑石膏或模型石膏;
s4:将步骤s3获得的滤液,其中hcl质量百分数为9.30%、残余ca2+的质量百分数为0.15%的稀盐酸浓缩至hcl质量百分数15%后,返回至萤石精矿酸浸槽循环利用。
实施例3
具体步骤如下:
s1:将预计生产获得的caso4的2%(摩尔百分数)的晶种、萤石矿含钙废液和稀硫酸依次加入到反应釜中进行结晶沉淀反应,生产方式为间歇生产,
萤石矿含钙废液中ca2+的质量百分数为24.85%,稀硫酸的质量百分数为50%,其中,ca2+离子与so42-离子的摩尔比为1:0.95;
s2:通过以下手段控制结晶沉淀反应中生成的硫酸钙结晶速率,得到硫酸钙晶体料浆,
其中,在115℃下控制硫酸钙的结晶沉淀反应时间为24h、反应釜的搅拌线速度为0.8~1.0m/s;
s3:将步骤s2获得的硫酸钙晶体料浆经过100目普通滤布快速过滤、去离子水淋滤5次,用水量为硫酸钙晶体体积的100%,得到含水率为8.20%的滤饼,滤液为稀盐酸;
将滤饼在80℃下干燥,即得白色针状石膏产品,平均粒径为190um,白度为92.77,其产品β-caso4·1/2h2o质量含量达到99.7%,可用作模型石膏、填料石膏或医用石膏的制备原料;
s4:将步骤s3获得的滤液,其中hcl质量百分数为15.67%、残余ca2+的质量百分数为0.62%的稀盐酸直接返回至萤石精矿酸浸槽循环利用。
实施例4
具体步骤如下:
s1:将预计生产获得的caso4的8%(摩尔百分数)的晶种、萤石矿含钙废液和稀硫酸依次加入到烧杯中进行结晶沉淀反应,生产方式为一次性反应,
萤石矿含钙废液中ca2+的质量百分数为9.41%,稀硫酸的质量百分数为10%,其中,ca2+离子与so42-离子的摩尔比为1:0.9,加料方式为稀硫酸缓慢地滴入含钙废液中;
s2:通过以下手段控制结晶沉淀反应中生成的硫酸钙结晶速率,得到硫酸钙晶体料浆,
其中,在95℃下控制硫酸钙的结晶沉淀反应时间为12h、结晶器的搅拌线速度为0.5~0.8m/s;
s3:将步骤s2获得的硫酸钙晶体料浆经过80~120目普通滤布快速过滤、去离子水淋滤3次,用水量为硫酸钙晶体体积的60%,在真空负压下控制过滤时间为120s,得到含水率为8.20%的滤饼,滤液为稀盐酸;
将滤饼在80℃下干燥,即得白色针状石膏海绵体产品,平均粒径为390um,白度为93.29,其产品β-caso4·1/2h2o质量含量达到99.9%,可用作模型石膏、填料石膏或医用石膏的制备原料;
s4:将步骤s3获得的滤液,其中hcl质量百分数为2.67%、残余ca2+的质量百分数为0.20%的稀盐酸浓缩至hcl质量分数为15%后返回至萤石精矿酸浸槽循环利用。
实施例5
s1:将预计生产获得的caso4的10%(摩尔百分数)的晶种、萤石矿含钙废液和稀硫酸依次加入到带搅拌的沉淀池中进行结晶沉淀反应,生产方式为一次性反应,
萤石矿含钙废液中ca2+的质量百分数为12.49%,稀硫酸的质量百分数为10%,其中,ca2+离子与so42-离子的摩尔比为1:1.05,加料方式为稀硫酸缓慢地滴入含钙废液中;
s2:通过以下手段控制结晶沉淀反应中生成的硫酸钙结晶速率,得到硫酸钙晶体料浆,
其中,在常温下控制硫酸钙的结晶沉淀反应时间为5h、结晶器的搅拌线速度为0.5~0.8m/s;
s3:将步骤s2获得的硫酸钙晶体料浆经过80~120目普通滤布快速过滤、去离子水淋滤3次,用水量为硫酸钙晶体体积的60%,在真空负压下控制过滤时间为120s,得到含水率为8.15%的滤饼,滤液为稀盐酸;
将滤饼在80℃下干燥,即得白色针状石膏海绵体产品,平均粒径为185um,白度为93.10,其产品β-caso4·1/2h2o质量含量达到99.5%,可用作模型石膏、填料石膏或医用石膏的制备原料;
s4:将步骤s3获得的滤液,其中hcl质量百分数为2.80%、残余ca2+的质量百分数为0.20%的稀盐酸浓缩至hcl质量分数为15%后返回至萤石精矿酸浸槽循环利用。
对比实施例1
s1:将质量百分数为9.41%的萤石矿含钙废液和浓度为10%的稀硫酸按摩尔比cacl2:h2so4=1:0.9先后加入烧杯中,反应方式为一次性反应,加料方式为稀硫酸一次性快速加入含钙废液中;
s2:在反应温度为95℃下,控制搅拌线速度为5m/s,反应时间约30min,获得硫酸钙晶体料浆;
s3:将步骤s2所得硫酸钙晶体料浆进行过滤、淋滤,滤网材质为80~120目普通滤纸,淋洗1次,淋洗水为去离子水,用水量为硫酸钙晶体体积的10%,过滤时真空负压值达到0.09mpa,过滤13min后得到过滤后滤饼及滤液,滤饼游离水含水率为26.80%;
将滤饼在80℃下干燥,即得白色晶须状石膏海绵体产品,产品白度82.56,产品平均粒径18um,其产品β-caso4·1/2h2o质量含量达到79.17%;
s4:步骤s3所得滤液即为稀盐酸,其中hcl的质量百分数为3.05%、残余ca2的质量百分数为0.29%,经浓缩至hcl的质量百分数为15%的稀盐酸后返回至萤石精矿溶浸槽用于萤石精矿除钙提纯。
对比实施例2
s1:将质量百分数为12.49%的萤石矿含钙废液和浓度为10%的稀硫酸按摩尔比cacl2:h2so4=1:1.05先后加入烧杯中,反应方式为一次性反应,加料方式为稀硫酸一次性快速加入cacl2废液中;
s2:在常温下,控制搅拌线速度为3m/s,反应时间约30min,获得硫酸钙晶体料浆;
s3:将步骤s2所得硫酸钙晶体料浆进行过滤、淋滤,滤网材质为80~120目普通滤纸,淋洗1次,淋洗水为自来水,用水量为硫酸钙晶体体积的10%,过滤时真空负压值达到0.09mpa,过滤20min后得过滤后滤饼及滤液,滤饼游离水含水率为31.70%。
将滤饼在80℃下干燥,即得白色晶须状石膏海绵体产品,产品白度80.39,产品平均粒径12um,其产品β-caso4·1/2h2o质量含量达到77.98%。
s4:步骤s3所得滤液即为稀盐酸,其中hcl的质量百分数为3.23%、、残余ca2的质量百分数为0.18%,经浓缩至hcl的质量百分数为15%的稀盐酸后返回至萤石精矿溶浸槽用于萤石精矿除钙提纯。
本发明的实施例1至5与对比实施例1至2的实验数据对比见表1。
表1本发明实施例1至5与对比实施例1至2的实验数据对比
由表1数据可见,本发明通过对现有的萤石矿含钙废液工艺参数的改进,特别是利用控制原料加料速率和/或硫酸钙结晶沉淀反应时间,以及调整反应容器的搅拌速率及内部流场等手段,获得了比现有硫酸钙石膏晶体的大数倍至数十倍的粒径数值,且硫酸钙产品的白度和纯度也显著提高,这些都赋予了硫酸钙石膏产品更高的品质和使用价值;同时,本发明改进后的处理工艺流程简单、操作简便、高效率、低能耗,具有应用推广价值和投资价值。
以上所述,仅是本发明的较佳实施例而已,并非是对本发明作任何其他形式的限制,而依据本发明的技术实质所作的任何修改或等同变化,仍属于本发明所要求保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!