海芋中具抗肿瘤作用的一个木脂素酰胺新化合物、制备方法和药物用途与流程
本发明涉及中药化学及医药技术领域,具体涉及从海芋(Alocasia macrorrhiza(L.)SCHOTT)中得到的一个新化合物、制备方法和药物用途。
背景技术:
海芋(Alocasia macrorrhiza(L.)SCHOTT)为天南星科海芋属植物,主要分布于我国广东、四川等地,喜生于溪谷湿地或田边,是著名的壮药,最早记载于《广西实用中草药新选》,其味微苦,大寒,有毒,有解毒退热,消肿镇痛之功效。临床多用于治疗钩端螺旋体病、毒蛇咬伤等,也可配伍甘草等治疗哮喘[3]。值得关注的是,其根茎在中医临床被用于治疗乳腺癌,效果良好,且四川等地民间常用其水煎液口服治疗各种癌症,亦有良好效果。迄今,海芋的化学研究只有2篇文献见诸报道:Kaur等从卜芥中分离得到一种对人宫颈癌细胞有一点细胞毒活性(IC50=100μg/mL)的外源凝集素N-acetyl-D-lactosamine。我们利用气质联用的方法对其50%乙醇提取物的石油醚部位进行化学研究,鉴定了其中43个化学成分的结构,主要成分为长链不饱和脂肪。
技术实现要素:
本发明涉及一个新化合物的结构及其在制备抗肿瘤药物中的运用,属于医药领域。
本发明目的在于提供一个从海芋中得到的新化合物。
本发明的另一目的在于提供提取、分离本发明新化合物的方法。
本发明的另一目的是上述新化合物在制备抗肿瘤的药物方面的用途。
本发明的目的通过下列技术措施实现。
发明人从尖尾芋中分离得到一个新化合物,其结构如附图1所示。
该新化合物从尖尾芋中分离得到,其方法包括以下步骤:
(1)取海芋根茎,用溶剂提取,回收提取液,得到稠浸膏。
(2)将稠浸膏经过大孔树脂、正相和反相以及凝胶色谱层析分离,得到目标化合物。
提取溶剂可以是水、乙醇、甲醇、丙醇、丁醇、丙酮、石油醚、氯仿、乙酸乙酯等溶剂以及任意比例混合的醇水溶剂,优选5%-100%的含水甲醇或乙醇。提取方法可以是煎煮、回流、冷浸、渗漉、微波提取或超声提取,优选是回流和超声提取。
提取液浓缩后可通过极性或非极性大孔吸附树脂,用水洗去杂质,用含水低于95%的甲醇或乙醇进行洗脱,将含有目标化合物1和2的洗脱液进行浓缩,得 到精制液。也可以用正相和反相硅胶,优选反相硅胶,用洗脱液洗脱,收集含有目标化合物1和2的浓缩,分别得到精制液。
浓缩后的精制液分别可在硅胶、氧化铝等正相吸附材料中进行色谱分离,也可在硅烷键合硅胶、含有氰基或氨基的硅烷键合硅胶等反相材料中进行色谱分离,收集含有目标化合物的洗脱液,洗脱液重结晶或蒸干溶剂后分别得到该新化合物。
发明人发现该化合物对肿瘤细胞具有显著的抑制生长作用。
附图说明
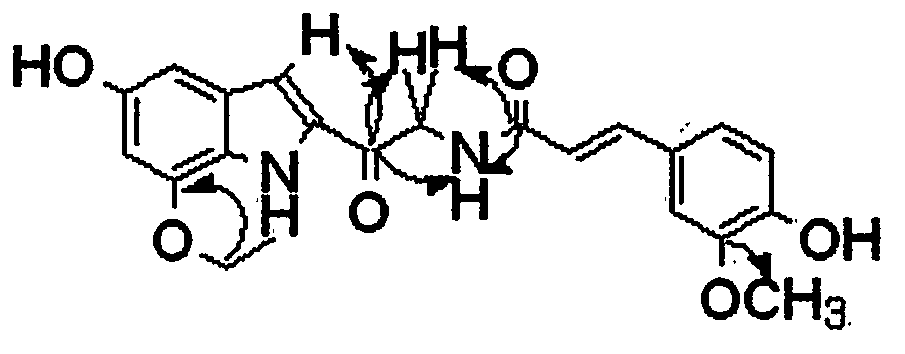
附图1.化合物1的结构式
附图2.化合物1的HMBC谱
具体实施例
实施例1.新化合物(E)-N-(2-(6-hydroxy-1H-indol-2-yl)-2-oxoethyl)-3-(4-hydroxy-3-metho-xyphenyl)acry-lamide的制备。
干燥海芋根茎粉末4kg,用50%的含水乙醇提取三次,每次10升,合并提取液,提取液过滤,滤液减压回收溶剂,得稠浸膏200g。稠浸膏用D101柱层析进行分离,分别用水、20%和40%含水乙醇进行洗脱,40%含水乙醇洗脱液减压回收溶剂,得稠浸膏35g。该稠浸膏用正相硅胶柱层析分离、梯度洗脱,洗脱剂为氯仿-甲醇-水,根据薄层层析情况分成5个部分(fr.A-fr.E)。fr.B(2.6g)进行反复硅胶和凝胶柱层析分离得到化合物(E)-N-(2-(6-hydroxy-1H-indol-2-yl)-2-oxoethyl)-3-(4-hydroxy-3-metho-xyphenyl)acry-lamide。
实施例2.新化合物(E)-N-(2-(6-hydroxy-1H-indol-2-yl)-2-oxoethyl)-3-(4-hydroxy-3-metho-xyphenyl)acry-lamide结构鉴定。
化合物1为白色无定型粉末,茴香醛-硫酸显色显绿色,以及Ehrlich反应呈阳性提示该化合物含有吲哚基团。
UV光谱在223、280、270和299nm的特征强吸收揭示该化合物含有吲哚基团。
IR光谱在1619、1489、1480cm-1处有强烈吸收提示该化合物有吲哚苯环存在,3486cm-1、1646cm-1处有强吸收提示有酰胺羰基官能团存在。
由负离子高分辨HR-ESI-MS(m/z 365.1138)推定分子式为C21H20O5N2,不饱和度为12。
1H NMR给出2个芳环ABX系统,1对反式双键,1个杂环质子,4个活泼氢质子,1个亚甲基双氢质子,分别为(δ ppm):[6.92(d,J=8.0),7.15(d d, J=1.6,8.0),7.29(d,J=1.6)],[7.38(d,J=8.8),6.82(d d,J=2.4,8.8),7.68(d,J=2.4)],[7.48(d,J=15.6),6.80(d,J=15.6)],8.45(d,J=3.2),11.7(s),9.57(s),9.31(s),8.34(t,J=5.6),4.68(2H,d,J=5.6),提示该化合物含双取代吲哚和邻位双取代苯反式乙稀结构片段。13C NMR和DEPT谱给出21个碳,其中有16个芳香碳和烯碳,2个羰基碳,1个甲氧基碳,1个甲乙基碳,1个亚甲基碳;据HMQC把其碳谱和氢谱化学位移对应起来和文献数据比对,结合上述显色反应,紫外和红外光谱,推断化合物1含(反式)N-阿魏酸酰基基团[12],6′-羟基吲哚基团;如前所述,化合物1还含有1个羰基(δ(C)190.4)和1个亚甲基((δ(C)46.3,δ(2H)4.68),HMBC谱(表1,图2)显示δ 190.4和δ 166.1两个羰基均和亚甲基氢相关,所以该亚甲基4.68(2H,d,J=5.6)连接δ 190.4羰基和(反式)N-阿魏酸酰基基团中的酰胺基,又δ 190.4羰基和6′-羟基吲哚基团中的2′位质子(δ 8.45)相关,并且其中的4′位C(δ 113.1)也和它相关,所以羰基δ 190.4连接于6′-羟基吲哚基团的2′位和亚甲基之间,即乙酮基连接了(反式)N-阿魏酸酰基和6′-羟基吲哚2个化合物1主要结构片段。并如HMBC谱(图2)所示δ 131.1和A′B′X′自旋系统中的B′质子6.82(d d,J=2.4,8.8)相关,而126.96不和该质子相关,δ153.6和A′B′X′自旋系统中3个质子7.38(d,J=8.8),6.82(d d,J=2.4,8.8),7.68(d,J=2.4)均相关,所以δ 131.05,126.96,153.6分别定位于4′a,7′a,6′位,即证实了该结构片段是6′-羟基吲哚基团。δ 148.3碳和甲氧基质子(δ 3.94)相关,但它和ABX自旋系统中的B质子(δ 7.15)不相关,所以甲氧基连于6位,δ 148.8碳和ABX自 旋系统中的三个质子6.92(d,J=8.0),7.15(d d,J=1.6,8.0),7.29(d,J=1.6)均相关,所以该碳定位于7位并连接羟基,即证实了该结构片段是(反式)N-阿魏酸酰基基团。综上所述化合物1结构推断为(E)-N-(2-(6-hydroxy-1H-indol-2-yl)-2-oxoethyl)-3--(4-hydroxy-3-methoxyphenyl)acry-lamide。该化合物氢谱、碳谱及HMBC谱全归属如表1所示。
表1、化合物(E)-N-(2-(6-hydroxy-1H-indol-2-yl)-2-oxoethyl)-3-(4-hydroxy-3-methoxyphenyl)acry-lamide氢谱、碳谱及HMBC谱全归属(DMSO-d6,δ,ppm.O-TMS).
实施例5.新化合物1对肿瘤细胞生长抑制作用
1.材料和方法
1.1实验材料
1.1.1仪器
SF-160 B型高速粉碎机(上海中联制药装备有限公司);R200型旋转蒸发仪(上海申生科技有限公司);TGL-16B型离心机(上海安亭科学仪器厂);QL-9010旋涡混合器(江苏海门市麒麟医用仪器厂);FA 2104 N型电子天平(上海精密科学仪器有限公司)
1.1.2试药
二甲亚砜(Sigma公司);MTT(Sigma公司);胰蛋白酶(Thermo公司);DMEM高糖培养液(Thermo公司);胎牛血清(GIBCO公司);超纯水(自制);尖尾芋药材(2010年4月采自四川);其余试剂均为分析纯(国药集团化学试剂厂)
1.1.3实验材料
P-388、HT-29。
1.2实验方法
1.2.1 MTT法检测:
1.2.1.2.肿瘤细胞培养和检测方法:
接板:收集对数生长期的待筛选细胞(除K-562人骨髓性的白血病细胞外), 胰蛋白酶消化,吸取适量含细胞的培养液至加样槽中,加适量空白培养液,用排枪接取加入96孔板中,每孔100μL,5%CO2,37℃孵育。
加样:待细胞贴壁后后,加入梯度浓度(孔浓度100μg/mL、10μg/mL、1μg/mL、0.1μg/mL、0.01μg/mL)供试品,设置5个梯度,每个浓度设4个平行孔,每孔100μL。
检测:分别培养24h、48h、72h后,每孔加入MTT 10uL(0.5g/L),孵育4-6h,弃去上清,每孔加入DMSO溶液150uL,振荡15min,待结晶充分溶解后,在450nm波长处读取吸光光度(OD)值,计算样品抑制率(inhibitory rate,IR),以及肿瘤细胞存活率(survival rate,SR)。
IR=(空白组OD值-加药组OD值)/空白组OD值×100%
SR=(1-IR)×100%
检测结果表明新化合物对P-388和HT-29有显著的抑制作用,IC50分别为2.9±0.3、1.6±0.8(ug/mL)。
以上药理实验结果表明:上述来自中药海芋得到的新化合物具有显著的细胞毒活性,因为常规抗肿瘤化合物的体外活性筛选是以化合物的细胞毒活性来体现的,所以本发明化合物具有抗肿瘤活性,可以与药用载体混合,制备抗肿瘤药物。
- 还没有人留言评论。精彩留言会获得点赞!