区分clade2.3.4和clade2.3.4.4H5AIV的实时荧光定量PCR引物的制作方法
本发明属于动物传染病学领域,具体涉及一组区分clade 2.3.4和clade 2.3.4.4 H5 AIV的实时荧光定量PCR引物。
背景技术:
禽流感(Avian influneza,AI)是由A型流感病毒引起的、主要侵害家禽及野鸟的一种急性、高度接触性传染病。高致病性H5亚型禽流感病毒(H5 subtype avian influenza virus, H5 AIV)引起的感染目前已被世界动物卫生组织(OIE)列为必须报告的动物传染病,在我国被列为一类动物疫病。
关于流感的最早记录可追溯到1878年来自意大利的一次报道,随后世界各地陆续发生流感的暴发和流行。1996年,在我国分离到的第一株H5N1亚型HPAIV [A/Goose/Guangdong/1/96(H5N1),GS/GD/96],紧接着香港于1997年发生H5N1亚型禽流感病毒直接感染人事件,这是第一个禽源流感病毒未经中间宿主而直接感染人的证据。由于从祖源病毒GS/GD/96进化出多个谱系且命名不统一,为此WHO、FAO和OIE联合制定了H5N1 HPAIV统一分类准则将H5N1 HPAIV分为0~9共计10个不同clade,其中clade 2.3.4最早于2003~2006年间流行于中国、越南、泰国、老挝和马来西亚等地的病毒株,2006~2009年clade 2.3.4分支在我国很多地区是优势流行株。近年来,出现了处于clade 2.3.4.4的H5亚型病毒。针对clade 2.3.4 H5 AIV的疫苗(Re-5株)和clade 2.3.4.4 H5 AIV的疫苗(Re-8株)已研制成功,对clade 2.3.4和clade 2.3.4.4 H5 AIV进行鉴别诊断有助于指导H5 AIV相应疫苗的科学使用。
然而,clade 2.3.4和clade 2.3.4.4二者之间的HA基因序列同源率高达94.4%(以经典参考毒株比较为例),很难通过常规的分子生物学方法进行鉴别。
本发明的一组区分clade 2.3.4和clade 2.3.4.4 H5 AIV的实时荧光定量PCR引物仅需1组引物对(2条引物)即可有效对clade 2.3.4和clade 2.3.4.4 H5 AIV进行有效区分。该引物根据clade 2.3.4和clade 2.3.4.4 H5 AIV血凝素基因(HA)所存在的特征性核苷酸序列差异来设计,利用实时荧光定量PCR反应后生成的熔解曲线的Tm值和其GC含量正相关的特点,通过观察clade 2.3.4和clade 2.3.4.4 H5 AIV经该组引物进行实时荧光定量PCR扩增反应后的熔解曲线Tm值差异,即可精确对clade 2.3.4和clade 2.3.4.4 H5 AIV感染情况进行准确鉴别诊断,相关研究尚未见国内外文献报道,本发明可填补相关领域空白。
技术实现要素:
本发明的目的在于提供一组区分clade 2.3.4和clade 2.3.4.4 H5 AIV的实时荧光定量PCR引物及其应用,该引物能有效区分clade 2.3.4和clade 2.3.4.4 H5 AIV感染(或共感染),为科学防控 H5AIV提供技术保证。
本发明根据clade 2.3.4和clade 2.3.4.4 H5 AIV血凝素基因(HA)存在特征性的核苷酸序列差异来设计一组实时荧光定量PCR引物。利用该扩增区域clade 2.3.4和clade 2.3.4.4 H5 AIV血凝素基因(HA)存在的核苷酸GC含量差异,通过建立基于Eva Green的实时荧光定量PCR方法对clade 2.3.4和clade 2.3.4.4 H5 AIV血凝素基因(HA)实时荧光定量PCR扩增反应,获得的熔解曲线存在不同的特异峰值(Tm值)差异,根据熔解曲线Tm值差异可直接对clade 2.3.4和clade 2.3.4.4 H5 AIV感染情况进行鉴别诊断。
为实现上述目的,本发明采用以下技术方案:
一组区分clade 2.3.4和clade 2.3.4.4 H5 AIV的实时荧光定量PCR引物,其核苷酸序列为:
上游引物F1:5’- CAAATGTGATAATGAATGTATGGA -3’;
下游引物R1:5’- TTGGTAAGTTCCTATTGATTCC -3’。
通过所述引物建立基于Eva Green实时荧光定量PCR方法,根据利用该引物扩增的clade 2.3.4和clade 2.3.4.4 H5 AIV血凝素基因(HA)存在核苷酸特征性差异,该差异存在GC含量差异,可导致实时荧光定量PCR反应扩增反应后的生成的熔解曲线存在不同的特异峰值(Tm值),可直接对clade 2.3.4和clade 2.3.4.4 H5 AIV感染进行鉴别。
具体包括以下步骤:
(1)设计并合成上述特异性引物对F1/R1;
(2)病毒RNA提取:从检测样品中分别提取clade 2.3.4和clade 2.3.4.4 H5 AIV的病毒RNA;
(3)RT-PCR扩增:设计并合成H5 AIV血凝素基因HA特异性引物对H5-HAF/H5-HAR对提取的病毒RNA进行RT-PCR扩增,获得其HA基因序列;将RT-PCR扩增的目的片段进行胶回收并纯化后,克隆到T载体上,获得含有clade 2.3.4和clade 2.3.4.4 H5 AIV的血凝素基因HA的阳性重组质粒(T-clade2.3.4-1和T-clade 2.3.4.4-1),测定其OD值计算出拷贝数后,连续倍比稀释,作为实时荧光定量PCR反应的标准品。
所用H5 AIV血凝素基因HA特异性引物对H5-HAF/H5-HAR的核苷酸序列为:
H5-HAF: 5’- TGGTTACCATGCAAACAAC -3’;
H5-HAR: 5’- TTACACTTTCCATACATTCATTATC -3’。
(4)实时荧光定量PCR:用所述实时荧光定量引物F1和R1对含有clade 2.3.4和clade 2.3.4.4 H5 AIV的血凝素基因HA的阳性重组质粒(T-clade2.3.4-1和T-clade 2.3.4.4-1)进行Eva Green实时荧光定量PCR扩增,反应完成后获得相应的扩增曲线,并生成Eva Green实时荧光定量PCR扩增的熔解曲线。
(5)病毒感染情况判断:实时荧光定量PCR反应结束后,通过观察扩增曲线判断是否存在clade 2.3.4和clade 2.3.4.4 H5 AIV感染;通过观察熔解曲线其Tm值差异可对clade 2.3.4和clade 2.3.4.4 H5 AIV进行鉴别。
其中,本发明所设计的实时荧光定量PCR引物对F1/R1需满足如下要求:
(1)特异性强:该实时荧光定量PCR引物在针对clade 2.3.4和clade 2.3.4.4 H5 AIV血凝素基因HA核苷酸序列进行分析后保守的区域设计,对二者均具有高特异性,达到仅需一组引物能对clade 2.3.4和clade 2.3.4.4 H5 AIV进行扩增。即观察实时荧光定量PCR反应后的扩增曲线即可判断是否感染clade 2.3.4或clade 2.3.4.4 H5 AIV。
(2)两种病毒的扩增区域GC含量不同:该组引物对扩增的血凝素基因HA在clade 2.3.4和clade 2.3.4.4 H5 AIV中存在核苷酸序列GC含量差异。基于实时荧光定量PCR反应生成的熔解曲线的Tm峰值差异(该差异和核苷酸序列的GC含量差异正相关),即可通过观察实时荧光定量PCR反应后的熔解曲线对clade 2.3.4和clade 2.3.4.4 H5 AIV感染进行判断(可有效区分是clade 2.3.4 H5 AIV还是clade 2.3.4.4 H5 AIV)。
其中,所述的步骤(5)的病毒感染情况判断方法如下:
若在Tm=(78.7±0.14)℃出现单一的特异性Tm峰判为clade2.3.4 H5 AIV阳性;
若在Tm=(79.5±0.09)℃出现单一的特异性Tm峰判为clade 2.3.4.4 H5 AIV阳性;
若在Tm=(78.7±0.14)℃以及Tm=(79.5±0.09)℃出现双峰,则判断为clade 2.3.4和clade 2.3.4.4 H5 AIV双重感染;
其他情况均判为阴性。
本发明所设计的实时荧光定量PCR引物对F1/R1可用于制备区分clade 2.3.4和clade 2.3.4.4 H5 AIV感染的试剂盒。
本发明的有益效果:鉴定方法简单,效率和准确率较高。使用本研究提供的一组实时荧光定量PCR引物对前期分离的2株clade 2.3.4 H5AIV和2株clade 2.3.4.4 H5 AIV进行实时荧光定量PCR检测,均和预期相符。且仅需1组引物对(2条引物)即可有效对clade 2.3.4和clade 2.3.4.4 H5 AIV进行有效区分。
附图说明
图1 为clade 2.3.4和clade 2.3.4.4 H5 AIV血凝素基因HA引物设计区及核苷酸序列特征性差异图
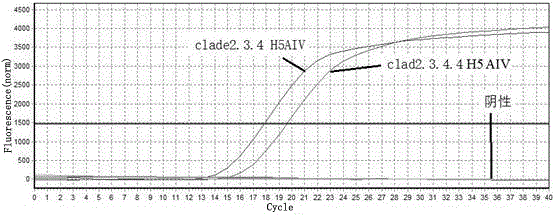
图2 引物对F1/R1对clade 2.3.4和clade 2.3.4.4 H5 AIV进行实时荧光定量PCR反应的扩增曲线:F1/R1对clade 2.3.4和clade 2.3.4.4 H5 AIV病毒感染结果的判断须在扩增成功的前提下做出,若扩增失败,则不可依据熔解曲线做出感染类型判断;若拷贝数相同,则clade 2.3.4和clade 2.3.4.4 H5 AIV扩增曲线一致。
图3 引物对F1/R1对clade 2.3.4和clade 2.3.4.4H5 AIV进行实时荧光定量PCR反应的熔解曲线。
具体实施方式
下面结合实施例对本发明做进一步的描述。
实施例1
1、毒株:
H5亚型流感病毒clade 2.3.4分支(CX1株)和clade 2.3.4.4分支(DK10株)均由福建省农业科学院畜牧兽医研究所保存。
2、引物设计与合成
根据clade 2.3.4和clade 2.3.4.4 H5 AIV的血凝素基因HA核苷酸特征性差异区设计实时荧光定量PCR反应的引物F1和R1,其中F1和R1引物序列为:
上游引物F1:5’- CAAATGTGATAATGAATGTATGGA -3’;
下游引物R1:5’- TTGGTAAGTTCCTATTGATTCC -3’。
3、病毒RNA提取以及RT-PCR扩增:
以常规方法提取clade 2.3.4分支(CX1株)和clade 2.3.4.4分支(DK10株)H5 AIV的核酸RNA。利用针对H5 AIV血凝素基因HA基因,设计特异性引物( H5-HAF: 5’- TGGTTACCATGCAAACAAC -3’和H5-HAR: 5’- TTACACTTTCCATACATTCATTATC -3’)对提取的病毒RNA进行RT-PCR扩增,获得其HA基因序列;将RT-PCR扩增的目的片段进行胶回收后纯化后,克隆到T载体上,获得含有clade 2.3.4和clade 2.3.4.4 H5 AIV的血凝素基因HA的阳性重组质粒(T-clade 2.3.4-1和T-clade 2.3.4.4-1),测定其OD值计算出拷贝数后,连续倍比稀释,作为实时荧光定量PCR反应的标准品。
4、实时荧光定量PCR反应:
优化出的20 μL 最佳反应体系为体系:Eva Green 10 μL,浓度为10 μmol/L的F1、R1各0.2 μL、模板2 μL、水补足至20 μL。最佳反应条件为:95 ℃,2 min预变性;95 ℃ 10 s,58 ℃ 15 s,共40个循环,循环结束后,根据条件做出对应的熔解曲线。
5、病毒感染情况判断:
实时荧光定量PCR反应结束后,观察扩增曲线,判断建立的方法有无特异性扩增(没有扩增曲线,熔解曲线的检测结果没有意义)。实时荧光定量PCR反应结束后做出的熔解曲线,直接在和实时荧光定量PCR仪器连接的电脑上,利用实时荧光定量PCR对应的软件进行分析(可直接肉眼观察),对clade 2.3.4和clade 2.3.4.4 H5 AIV感染情况进行判断,判断方法为:
若在Tm=(78.7±0.14)℃出现单一的特异性Tm峰判为clade 2.3.4 H5AIV阳性;
若在Tm=(79.5±0.09)℃出现单一的特异性Tm峰判为clade 2.3.4.4 H5 AIV阳性;
若在Tm=(78.7±0.14)℃以及Tm=(79.5±0.09)℃出现双峰,则判断为clade 2.3.4和clade 2.3.4.4 H5 AIV双重感染;
其他情况均判为阴性。
从图3可以看出,引物对F1/R1对两株病毒血凝集素基因(HA)片段扩增特异性强,且二者的Tm值存在差异,可有效区分两株病毒。试验结果表明,使用本研究提供的一组实时荧光定量PCR引物对前期分离的2株clade 2.3.4 H5 AIV和2株clade 2.3.4.4 H5 AIV进行实时荧光定量PCR检测,均和预期相符。且仅需1组引物对(2条引物)即可有效对clade 2.3.4和clade 2.3.4.4 H5 AIV进行有效区分。
实施例2
对临床送检的72份死亡鸭病料经处理后进行实时荧光定量PCR检测后发现,clade 2.3.4 H5AIV感染阳性有2株,阳性率为2.77%(2/72);clade 2.3.4.4 H5AIV感染阳性有5株,阳性率为6.94%(5/72);,未检测到临床送检的72份死亡鸭存在clade 2.3.4和clade 2.3.4.4 H5 AIV共感染现象。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
SEQUENCE LISTING
<110> 福建省农业科学院畜牧兽医研究所
<120> 区分clade 2.3.4和clade 2.3.4.4 H5 AIV的实时荧光定量PCR引物
<130> 4
<160> 4
<170> PatentIn version 3.3
<210> 1
<211> 24
<212> DNA
<213> F1
<400> 1
caaatgtgat aatgaatgta tgga 24
<210> 2
<211> 22
<212> DNA
<213> R1
<400> 2
ttggtaagtt cctattgatt cc 22
<210> 3
<211> 19
<212> DNA
<213> H5-HAF
<400> 3
tggttaccat gcaaacaac 19
<210> 4
<211> 25
<212> DNA
<213> H5-HAR
<400> 4
ttacactttc catacattca ttatc 25
- 还没有人留言评论。精彩留言会获得点赞!