用于测序反应的聚合酶的制作方法
本申请根据35 U.S.C.§119(e)要求2016年12月19日提交的美国临时专利申请62/436,410的优先权,其通过引用整体并入本文。
技术领域
本申请总体而言涉及用于生物和/或化学样品的测序分析的方法及组合物。
背景技术:
DNA聚合酶是所有活生物体的基因组复制所必需的核苷酸聚合酶。除其在复制及修复期间保持基因组完整性方面的作用外,DNA聚合酶亦广泛用于体外DNA操控,包括DNA克隆、诱变及测序。DNA聚合酶根据模板DNA合成互补链的基本能力是保守的,尽管包括持续合成能力、保真性及底物核苷酸选择性的具体性质在不同酶中有所不同。
发明简述
本文中所公开的技术的方面涉及可用于进行体外聚合反应的经修饰聚合酶(polymerizing enzymes)(例如聚合酶(polymerases))。在一些方面中,本文中所描述的聚合酶适合用于测序反应(例如核酸测序)。在一些方面中,本公开提供具有一或多个修饰的重组聚合酶。在一些实施例中,本公开的重组聚合酶包含氨基酸突变或结构域取代中的至少一者。
在一些方面中,本公开提供具有基于天然存在的聚合酶(例如选自表1)且包括一或多个氨基酸突变和/或片段取代的氨基酸序列的经修饰聚合酶(例如核酸聚合酶(nucleic acid polymerizing enzyme/nucleic acid polymerase))。在一些实施例中,经修饰聚合酶包含一或多个片段取代(例如其中聚合酶的一或多个片段经一或多个来自不同聚合酶的对应的片段置换)、一或多个氨基酸添加、删除和/或取代或其组合。在一些实施例中,片段包含聚合酶的所定义的区域(例如结构性或功能性结构域或子结构域)或其部分,且任选地包括一或多个侧接氨基酸(例如,在表1的天然产生的聚合酶中,例如,在域或其部分的任一侧上的1至50、1至40、1至30、1至20、5至10、5至25或此等范围内的任何整数个氨基酸)。在一些实施例中,一或多个氨基酸插入、删除或取代对应于两种天然产生的聚合酶间在一或多个位置上的天然产生的差异。在一些实施例中,一或多个氨基酸插入、删除或取代是新的非天然产生的变化。在一些实施例中,氨基酸取代是保守氨基酸取代(例如用一种具有相似性质,例如具有相似带电、极性、疏水性、亲水性和/或其它相似性质(诸如相似大小)的氨基酸置换另一种氨基酸)。在一些实施例中,氨基酸取代是非保守氨基酸取代。在一些实施例中,一或多个氨基酸插入、删除或取代可以在经修饰聚合酶中的任何位置,包括在来自不同聚合酶的一或多个所交换的片段中和/或在原始聚合酶的片段中。
相应地,在一些实施例中,本发明提供具有选自表1的氨基酸序列(或具有与选自表1的氨基酸序列具有至少50%、至少60%、至少70%、至少80%、80%至90%、90%至95%、95%至99%或更高的氨基酸序列同一性的氨基酸序列)且包含来自表2、表3、表4或表5的一或多个氨基酸修饰的重组聚合酶。在一些实施例中,一或多个氨基酸修饰包括至少一个氨基酸突变(例如1、2、3、4、5、6、7、8、9、10、15、20、25或更多个氨基酸突变)。在一些实施例中,一或多个氨基酸修饰包括至少1个且至多5个氨基酸突变、至少1个且至多10个氨基酸突变、至少1个且至多15个氨基酸突变、至少1个且至多25个氨基酸突变、至少1个且至多50个氨基酸突变、或至少1个且至多100个氨基酸突变。在一些实施例中,一或多个氨基酸修饰包括至少一个结构域取代(例如全部结构域的取代或包涵结构域或结构域一部分的片段的取代)。在一些实施例中,至少一个结构域取代包含核酸外切酶结构域取代及聚合酶结构域取代中的至少一者。在一些实施例中,核酸外切酶结构域取代包含核酸外切酶环取代。在一些实施例中,聚合酶结构域取代包含掌型子结构域取代、TPR1子结构域取代、手指型子结构域取代、TPR2子结构域取代或拇指型子结构域取代中的任一者(例如整个聚合酶、掌型、TPR1、手指型、TPR2或拇指型结构域或子结构域或其中任一者的部分,任选地包括一或多个侧接氨基酸的取代)。在一些实施例中,一或多个氨基酸修饰包括至少一个结构域取代及至少一个氨基酸突变。在一些实施例中,氨基酸突变可以是氨基酸嵌入、删除或取代。
在一些实施例中,本公开的重组聚合酶具有选自表2的序列。在一些实施例中,本公开提供具有选自表3的序列的重组聚合酶。
在一些实施例中,重组聚合酶另外包含纯化标签。在一些实施例中,纯化标签共价键结至聚合酶序列中的区域。在一些实施例中,纯化标签共价键结在聚合酶序列的末端。在一些实施例中,纯化卷标是C端标签。在一些实施例中,纯化标签是N端标签。在一些实施例中,纯化标签是His标签(例如重复组氨酸残基的序列,诸如六组氨酸序列)。
在一些实施例中,重组聚合酶另外包含偶联基团。在一些实施例中,偶联基团连接在聚合酶序列中的区域上。在一些实施例中,偶联基团连接在聚合酶的末端。在一些实施例中,偶联基团连接在重组聚合酶的C末端。在一些实施例中,偶联基团连接在重组聚合酶的N末端。在一些实施例中,偶联基团是生物素化序列。在一些实施例中,重组聚合酶包含(例如在其C端)直接连接或由肽连接子(例如5至15个氨基酸长或较长的)分开的纯化标签(例如His标签)及偶联基团(例如生物素化序列)。
在一些实施例中,重组聚合酶固定在表面上。在一些实施例中,表面包含经配置以结合重组聚合酶的偶联基团。在一些实施例中,表面包含奈米孔口。在一些实施例中,表面包含样品槽的底表面。在一些实施例中,样品槽安置于表面(例如芯片或积成装置的表面)上的复数个样品槽中。在一些实施例中,复数个样品槽中的每一者经配置以收纳重组聚合酶。在一些实施例中,复数个样品槽中的每一者包含能够进行单分子测序反应的重组聚合酶。
在一些方面中,本公开提供编码本文中所描述的重组聚合酶的经分离的核酸分子。在一些实施例中,经分离的核酸分子包含RNA。在一些实施例中,经分离的核酸分子包含DNA。在一些实施例中,经分离的核酸分子包含病毒载体。在一些实施例中,经分离的核酸分子包含表达载体。在一些实施例中,经分离的核酸分子包含质体。在一些实施例中,经分离核酸包括启动子(例如诱导型启动子)。在一些实施例中,经分离核酸是在能够表达重组聚合酶的宿主细胞中。在一些实施例中,重组聚合酶自宿主细胞分离(例如来自宿主细胞制备物,例如在生物反应器中生长且经诱导型启动子诱导后)。
在一些方面,本公开提供一种包含本申请案中所描述的重组聚合酶的组合物。在一些实施例中,组合物用于测序核酸的方法中。在一些实施例中,组合物另外包含测序反应混合物。在一些实施例中,测序反应混合物可包括:一或多个多磷酸核苷(例如包含多于一个磷酸根基团的核苷,诸如六磷酸核苷酸或核苷)、待测序的模板核酸、充当互补链合成的起始点的核酸引物、二价金属离子、缓冲组分及盐。在一些实施例中,多磷酸核苷包含可检测部分(例如发光标记)。
在一些方面,本公开提供一种藉由将本申请案中所描述的重组聚合酶与测序反应混合物接触来测序核酸的方法。在一些实施例中,测序反应混合物可包括:一或多个多磷酸核苷(例如包含多于一个磷酸根基团的核苷,诸如六磷酸核苷酸或核苷)、待测序的模板核酸、充当互补链合成的起始点的核酸引物、二价金属离子、缓冲组分及盐。在一些实施例中,多磷酸核苷包含发光标记。在一些实施例中,方法另外包含检测在与模板核酸互补的生长链中的一或多个多磷酸核苷的并入。在一些实施例中,检测包含量测参与并入事件中的经发光标记的多磷酸核苷的一或多个发光性质(例如寿命、强度、光子到达时间、量子产率)。
在一些方面,本公开提供包含包括表1中的重组聚合酶中的任一者的核酸外切酶区域或其部分(及任选地,位于一侧或两侧上的侧接氨基酸)的片段的重组聚合酶。在一些方面,本公开提供包含包括表1中的重组聚合酶中的任一者的掌型区域或其部分(及任选地,位于一侧或两侧上的侧接氨基酸)的片段的重组聚合酶。在一些方面,本公开提供包含包括表1中的重组聚合酶中的任一者的TPR1区域或其部分(及任选地,位于一侧或两侧上的侧接氨基酸)的片段的重组聚合酶。在一些方面,本公开提供包含包括表1中的重组聚合酶中的任一者的手指型区域或其部分(及任选地,位于一侧或两侧上的侧接氨基酸)的片段的重组聚合酶。在一些方面,本公开提供包含包括表1中的重组聚合酶中的任一者的TPR2区域或其部分(及任选地,位于一侧或两侧上的侧接氨基酸)的片段的重组聚合酶。在一些方面,本公开提供包含包括表1中的重组聚合酶中的任一者的拇指型区域或其部分(及任选地,位于一侧或两侧上的侧接氨基酸)的片段的重组聚合酶。在一些方面,本公开提供包含两个或更多个如本文中所描述的片段的重组聚合酶。
相应地,在一些实施例中,重组聚合酶是包含一或多个来自不同聚合酶(例如来自不同物种)的氨基酸片段的嵌合酶。在一些实施例中,嵌合聚合酶包含来自第一聚合酶的氨基酸序列,其中的一或多个片段已经被来自不同聚合酶的片段置换。在一些实施例中,一或多个来自不同聚合酶的片段可以是:包含来自M2Y聚合酶的氨基酸1-51的片段、包含来自粪肠球菌(E.faecium)聚合酶的氨基酸271-375的片段、包含来自粪肠球菌聚合酶的氨基酸72-89的片段和/或包含来自粪肠球菌聚合酶的氨基酸445-449的片段。在一些实施例中,来自M2Y聚合酶的1-51片段置换对应的天然产生的聚合酶片段(例如Φ29聚合酶的氨基酸1-54)。在一些实施例中,来自粪肠球菌聚合酶的271-375片段置换对应的天然产生的聚合酶片段(例如Φ29聚合酶的氨基酸260-359)。在一些实施例中,来自粪肠球菌聚合酶的72-89片段置换对应的天然产生的聚合酶片段(例如Φ29聚合酶的氨基酸75-91)。在一些实施例中,来自粪肠球菌聚合酶的445-449片段置换对应的天然产生的聚合酶片段(例如Φ29聚合酶的氨基酸429-433)。
在一些实施例中,重组聚合酶包含对应于以下Φ2929中的取代的一或多个取代:M8R、V51A、N62D、I71V、L107I、K131E、K135Q、L142K、G197D、Y224K、E239G、V250A/I、L253A/H、Y281H、I288L、T301C、R306Q、R308L、D325E、D341E、K354R、T368F、E375Y、A437G、A444T、E466K、D476H、A484E、E508R、D510K/R、K512Y、E515Q、K539E、D570S及T571V。
在一些实施例中,经修饰聚合酶包含一或多个本文中所描述的片段取代和/或氨基酸插入、删除和/或取代,且亦包含一或多个(例如1至5、5至10、10至25、25至50、50至75、75至100、100至125、125至150个)其他氨基酸插入、删除和/或取代(例如保守或非保守氨基酸取代)。相应地,在一些实施例中,表2或表3的经修饰聚合酶可包括一或多个(例如1至5、5至10、10至25、25至50、50至75、75至100、100至125、125至150个)其他氨基酸插入、删除和/或取代(例如保守或非保守氨基酸取代)。
这些及其他方面在以下详细描述中更详细地描述且藉由非限制性附图及实例说明。
附图说明
熟习此项技术者应理解本文所描述的图仅用于说明性目的。应理解,在一些情况下,为辅助理解本发明,本发明的各种方面可能经放大或扩大显示。在图中,在通篇各图中,相同参考标号一般是指相同特征、功能上相似和/或结构上相似的元件。图式未必为按比例的,而是重点在于说明教导内容的原理。图式不意欲以任何方式限制本教导内容的范围。
根据下文结合附图所阐述的详细描述,本发明的特征及优势将变得更显而易见。
当参照附图描述实施例时,可使用方向参考(“上”、“下”、“顶部”、“底部”、“左”、“右”、“水平”、“竖直”等)。此类参考仅意欲作为读者在正常方向上观看图式的辅助。这些方向参考不意欲描述实施装置的优选或唯一方向。装置可以其他方向实施。
如根据详细描述显而易知,图(例如图1至图7)中描绘且出于说明目的进一步在本申请通篇描述的实例描述非限制性实施例,且在一些情况下出于更清楚说明的目的可以简化某些方法或省略特征或步骤。
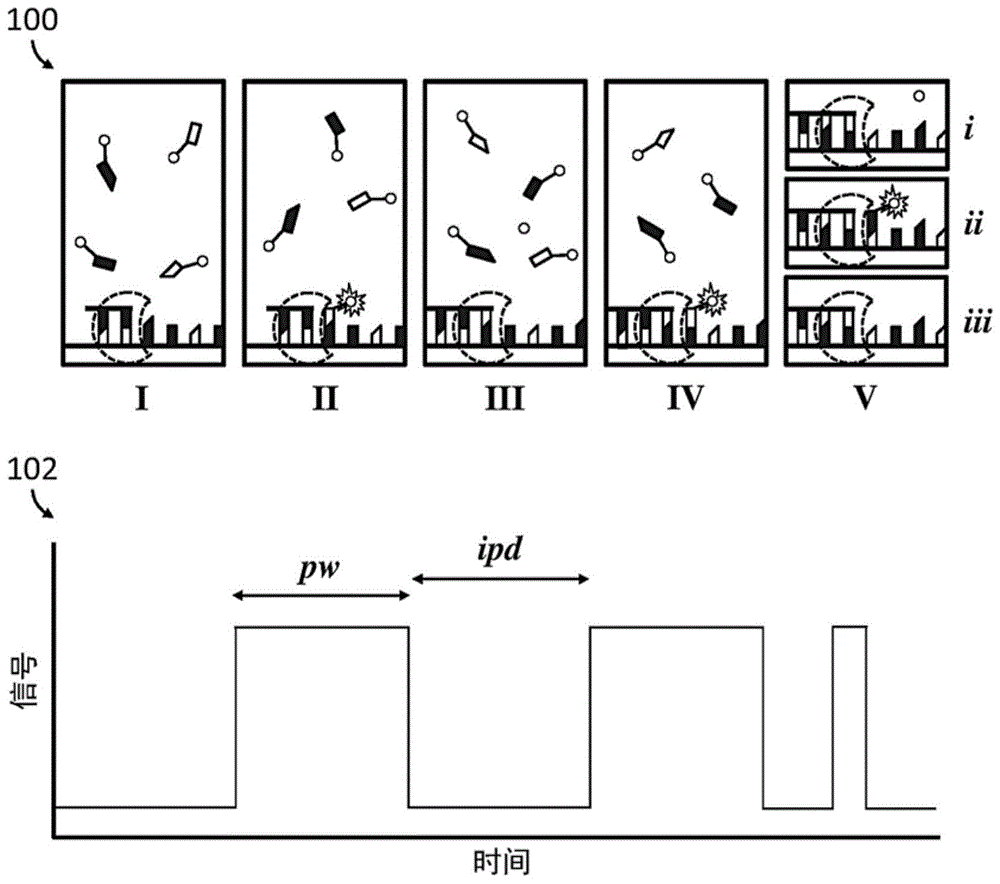
图1是说明监测单分子方法的非限制性方法中与信号读取相关的聚合反应进程的示意图。
图2是描绘Φ29聚合酶及该聚合酶的结构域及子结构域的结构的非限制性图标。
图3描绘所选择的具有在多肽链的结构域及子结构域中的突变位点的突变变异体的非限制性实例。
图4描绘所选择的具有经取代至多肽链中的不同结构域及子结构域的嵌合聚合酶变异体的非限制性实例。
图5A是描绘Φ29聚合酶的核酸外切酶结构域中的环区域的非限制性图标。
图5B描绘Φ29聚合酶与非限制性的一组其他聚合酶的核酸外切酶区域间的序列同源性比对。
图6描绘包含一或多个位点特异性突变的嵌合聚合酶变异体的非限制性通用实例。
图7是所实施的用于评估在大肠杆菌(E.coli)中表达的聚合酶的纯度的SDS-PAGE的图片。
发明详述
本发明的方面涉及经修饰聚合酶及其组合物。在一些方面,本公开提供使用经修饰重组聚合酶及包含所述酶的组合物的方法。在一些实施例中,本公开提供可用于进行体外聚合反应的经修饰重组聚合酶及其组合物。在一些方面,本文中所描述的聚合酶是经修饰重组核酸聚合酶,例如经修饰重组DNA聚合酶。在一些实施例中,由本公开提供的经修饰重组DNA聚合酶可用于与DNA操控(例如DNA测序)相关的体外反应。
在其他方面,本公开提供可用于进行体外聚合反应的经修饰聚合酶(polymerizing enzymes)(例如聚合酶(polymerases))。在一些实施例中,本文中所描述的聚合酶包含单独或组合可用于进行测序反应的一或多个修饰。在一些实施例中,可利用一或多个本文中所描述的修饰来产生具有一或多个适用于进行测序反应的性质,例如,诸如聚合酶持续合成能力、保真性(例如精确性)、底物(例如多磷酸核苷)结合亲和力、底物利用率(例如多磷酸核苷并入至与模板链互补的生长链中的比率)、聚合酶与经修饰底物(例如经标记多磷酸核苷)的相互作用或其某种组合的性质的聚合酶。在一些实施例中,一或多个修饰最小化或消除聚合酶的校读能力。举例而言,在一些实施例中,可对聚合酶的核酸外切酶结构域作出一或多个修饰,其结果为聚合酶的核酸外切酶活性减小。
在一些方面,本申请案涉及具有有利于单分子核酸测序技术的经改变生化性质的经修饰聚合酶。在一些实施例中,本文中所描述的变异体聚合酶已经修饰以在单分子测序反应中提供改善的信号读取。图1提供与实时信号读取相关的测序反应进程的实例图。不希望受理论所束缚,认为一些单分子核酸测序反应根据流程100进行。
在反应开始时(第I组),聚合酶(虚线)被限制于观测区域中且结合于模板链及引物链。如所示,各自具有不同类型的可检测标记的不同类型的核苷酸(例如A、G、T、C、U)存在于相同反应混合物中。当聚合酶与经发光标记的核苷酸结合时(第II组),标记变为被限制在观测区域中一段时间。在并入事件期间,例如,此段时间足够接受标记和/或发出足以在观测区域中检测且鉴别其存在的量的能量。如与信号读取102相关的流程100的第I组及第II组所说明,并入事件可以与对应于脉冲宽度pw的时间段的信号脉冲相关联。
应了解,在一些实施例中,与并入事件相关联的单独信号脉冲可能受各种条件影响,诸如在特定时间点上并入的核苷酸的类型或聚合酶的活性。在一些实施例中,单独信号脉冲可具有约10毫秒与约10秒之间的单独脉冲宽度。相应地,在一些实施例中,可以将单独脉冲宽度平均化以提供用于比较目的的参数。如本文中所使用,在一些实施例中,“脉冲宽度”是指对应于复数个单独信号脉冲的平均值的值,其中各单独信号脉冲具有单独脉冲宽度。
在一些实施例中,本申请案之经修饰聚合酶产生约10毫秒与约10秒之间的脉冲宽度。在一些实施例中,脉冲宽度为至少10毫秒且至多10秒、至少10毫秒且至多5秒、至少10毫秒且至多1秒或在约10毫秒与约1秒之间。在一些实施例中,脉冲宽度在约10与约500毫秒之间、约10与约200毫秒之间、约10与约100毫秒之间、约10与约50毫秒之间、约50毫秒与约1秒之间、约50与约500毫秒之间、约50与约200毫秒之间、约50与约100毫秒之间、约100毫秒与约1秒之间、约100与约500毫秒之间、约100与约200毫秒之间、约200毫秒与约1秒之间、约200与约500毫秒之间或约500毫秒与约1秒之间。
在核苷酸并入至生长链中且发光标记分裂之后,标记扩散至发光体积之外且在观测区域中不再可检测(第III组)。亦如第III组中所说明,在并入事件之后,聚合酶沿模板链进展,使得能够与后续经发光标记的核苷酸结合。类似于自第I组至第II组的进程,在信号迹线102中对应于自第III组至第IV组的进程的信号的强度自相对低强度水平增大至指示结合事件的信号脉冲。关于信号迹线102,并入事件与后续结合事件之间的时间段可以与脉冲间距离ipd相关联。
如在前文中关于脉冲宽度所详述,在一些实施例中,与第一与第二信号脉冲之间的时间段相关联的单独脉冲间距离可以受各种条件影响,诸如在特定时间点上聚合酶的活性或持续合成能力。在一些实施例中,单独脉冲间距离对应于约10毫秒与约1分钟之间或更长的时段(例如约1秒与约60秒之间、约1秒与约30秒之间、约1秒与约20秒之间、约1秒与约10秒之间或小于约1秒)。因此,在一些实施例中,可以将单独脉冲间距离平均化以提供用于比较目的的参数。如本文中所使用,在一些实施例中,“脉冲间距离”是指对应于复数个单独脉冲间距离的平均值的值。
在一些实施例中,本申请案的经修饰聚合酶产生约10毫秒与约10秒之间的脉冲间距离。在一些实施例中,脉冲间距离为至少10毫秒且至多10秒、至少10毫秒且至多5秒、至少10毫秒且至多1秒或在约10毫秒与约1秒之间。在一些实施例中,脉冲间距离在约10与约500毫秒之间、约10与约200毫秒之间、约10与约100毫秒之间、约10与约50毫秒之间、约50毫秒与约1秒之间、约50与约500毫秒之间、约50与约200毫秒之间、约50与约100毫秒之间、约100毫秒与约1秒之间、约100与约500毫秒之间、约100与约200毫秒之间、约200毫秒与约1秒之间、约200与约500毫秒之间或约500毫秒与约1秒之间。
在一些实施例中,可使用脉冲宽度和/或脉冲间距离的特征来鉴别特定发光标记。在一些实施例中,可在测序反应中使用本发明的经修饰聚合酶藉由观测一系列指示经发光标记的核苷酸的缔结的脉波宽度来测定模板链的核苷酸序列。在一些实施例中,在此过程中的假影会引起不正确的测序信息。举例而言,第V组说明结合及释放事件,其中经发光标记的核苷酸被限制在观测区域中一段足以引起信号脉冲的时间但无并入事件。
如第V组中所示,在所检测的第IV组中的并入之后,分裂的发光标记扩散至可观测区域(i)之外。在可观测区域中进一步的经发光标记的核苷酸与聚合酶缔结,发出可检测信号(ii)。该经发光标记的核苷酸并不并入至生长链中而是从聚合酶分裂且扩散回反应混合物(iii)中。由此,在随后成功并入相同类型的核苷酸之后(未图示),对应于第V组的信号脉冲将引起在测序信息读取中的明显插入。因此,在一些实施例中,本申请案的经修饰聚合酶具有长度足以自此等及其他此类假影事件中辨别真正并入事件的脉波宽度。在一些实施例中,本申请案的经修饰聚合酶具有一或多个减小底物自聚合酶活性位点过早释放的概率的修饰。在一些实施例中,本申请案的经修饰聚合酶具有一或多个增加在底物与聚合酶活性位点缔结后并入底物的概率的修饰。
在一些实施例中,由本公开提供的经修饰聚合酶包含根据表1中所阐述的野生型聚合酶序列(SEQ ID NO:1至19)具有一或多个修饰(例如,如在表2至5中例示,或其中两个或更多个的组合)的聚合酶序列。
表1.野生型聚合酶氨基酸序列
在一些实施例中,野生型聚合酶序列(例如如表1中所阐述的)提供大多数聚合酶序列,其中可作出一或多个修饰以产生重组变异体聚合酶。如本文中所使用,经修饰聚合酶的“大多数聚合酶序列”或“大多数序列”是指在该经修饰聚合酶序列中占优势的野生型聚合酶序列(例如,其中经修饰聚合酶序列中的至少50%的氨基酸对应于大多数序列中的氨基酸)。在一些实施例中,经修饰聚合酶序列包含另外包含一或多个氨基酸突变的大多数序列。在一些实施例中,一或多个氨基酸突变包含对应于同源蛋白质中的位置的位置上的氨基酸。举例而言,在一些实施例中,经修饰聚合酶包含对应于Φ29聚合酶(SEQ ID NO:1)中的A484的位置上的突变。在其他聚合酶中对应于A484的氨基酸可藉由包括同源性比对在内的本领域中已知的任何方法来测定。作为此分析的非限制性实例,同源性比对使用多个表1中所报告的聚合酶进行,且确定Φ29聚合酶中的A484对应于M2Y中的A481、芽孢杆菌噬菌体VMY22中的A492、屎肠球菌中的K500及铜绿蝇中的K827。因此,可使用同源性比对及本领域已知的相似方法鉴别对应于本文中所描述的经修饰残基的位置的其他聚合酶中的氨基酸。因此,应了解本公开的修饰不意欲限于本文中所描述的聚合酶(例如在表1中列出的聚合酶)且可扩展至使用已知技术的任何聚合酶。
在一些实施例中,经修饰聚合酶与表1中列出的一或多个聚合酶(例如与SEQ ID NO:1、SEQ ID NO:5或表1中列出的其他序列)具有至少25%氨基酸序列同一性。在一些实施例中,经修饰聚合酶与表1中列出的一或多个聚合酶(例如与SEQ ID NO:1、SEQ ID NO:5或表1中列出的其他序列)具有25%至50%、50%至60%、60%至70%、70%至80%、80%至90%、90%至95%或95%至99%或更高氨基酸序列同一性。在一些实施例中,此类经修饰聚合酶包括一或多个在本申请案中所提供的不同经修饰聚合酶配置和/或实例的内容中所描述的氨基酸突变和/或结构域取代。
在一些实施例中,一或多个来自不同聚合酶的片段或区域被描述为与本申请案中所描述的特定序列具有至少80%氨基酸序列同一性。此类区域可,例如与指定序列(例如与表1的天然产生的聚合酶中的对应的片段或区域)具有80%至90%、90%至95%、95%至99%或100%序列同一性。另外,在替代实施例中,此等片段区域可与指定序列(例如与表1的天然产生的聚合酶中的对应的片段或区域)具有较低序列同一性(例如50%至60%、60%至70%或70%至80%氨基酸序列同一性)。
为了比较两种或更多种氨基酸序列,第一氨基酸序列与第二氨基酸序列之间的“序列同一性”的百分比(在本文中亦称为“氨基酸同一性”)可藉由将[第一氨基酸序列中与第二氨基酸序列中的对应位置上的氨基酸残基相同的氨基酸残基的数目]除以[第一氨基酸序列中的氨基酸残基的总数]且乘以[100%]来计算,其中相比于第一氨基酸序列,第二氨基酸序列中的氨基酸残基的各个删除、插入、取代或添加视为在单个氨基酸残基(位置)的差异,亦即视为如本文中所定义的“氨基酸差异”。替代地,两种氨基酸序列之间的序列同一性程度可使用已知计算机算法(例如藉由Smith及Waterman(1970)Adv.Appl.Math.2:482c的局部同源性算法,藉由Needleman及Wunsch,J.Mol.Biol.(1970)48:443的同源性比对算法,藉由Pearson及Lipman.Proc.Natl.Acad.Sci.USA(1998)85:2444的相似性方法的搜索,或藉由如Blast、Clustal Omega的可利用的算法或其他序列比对算法的计算机化实施方案)且例如使用标准设置来计算。通常,出于根据上文概述的计算方法测定两种氨基酸序列之间的“序列同一性”的百分比的目的,具有最大氨基酸残基数目的氨基酸序列将视为“第一”氨基酸序列且另一氨基酸序列将视为“第二”氨基酸序列。
另外或替代地,可评估两个或更多个序列序列之间的同一性。在两个或更多个核酸或氨基酸序列的情况下,术语“一致”或百分比“同一性”是指相同的两个或更多个序列或子序列。当将两种序列按最大对应在比较窗或指定区域上比较且对齐,如使用以下序列比较算法中的一者或藉由人工比对及目视检查所量测的,若两种序列在指定区域或全部序列上具有指定百分比的相同氨基酸残基或核苷酸(例如至少80%、85%、90%、95%、96%、97%、98%、99%、99.5%、99.6%、99.7%、99.8%或99.9%一致),则两种序列“基本上一致”。任选地,该同一性存在于长度为至少约25、50、75或100个氨基酸的区域上,或更优选长度为100至150、200或更多个氨基酸的区域上。
另外或替代地,可评估两个或更多个序列序列之间的对齐(alignment)。在两个或更多个核酸或氨基酸序列的情况下,术语“对齐”或百分比“对齐”是指相同的两个或更多个序列或子序列。当将两种序列按最大对应在比较窗或指定区域上比较且对齐,如使用以下序列比较算法中的一者或藉由人工比对及目视检查所量测,若两种序列在指定区域或全部序列上具有指定百分比的相同氨基酸残基或核苷酸(例如至少80%、85%、90%、95%、96%、97%、98%、99%、99.5%、99.6%、99.7%、99.8%或99.9%一致),则两种序列“基本上对齐”。任选地,该比对存在于长度为至少约25、50、75或100个氨基酸的区域上,或优选长度为100至150、200或更多个氨基酸的区域上。
在一些实施例中,经修饰聚合酶包含一或多个(例如2个或更多个、5个或更多个、10个或更多个、15个或更多个、20个或更多个,例如所有)在对应于Φ29聚合酶中的K131、K135、L142、Y148、Y224、E239、V250、L253、R306、R308、E375、A437、E466、D476、A484、E508、D510、K512、E515、K539、D570及T571的位置上的氨基酸突变。举例而言,在一些实施例中,当经修饰聚合酶包含Φ29聚合酶大多数序列时,经修饰聚合酶包含一或多个在如前文中列出的位置上的突变。在一些实施例中,当经修饰聚合酶不包含Φ29聚合酶大多数序列时,经修饰聚合酶包含一或多个对应于以上列出的位置的氨基酸,例如,如藉由同源性比对或本领域已知的其他方法测定。
在一些实施例中,经修饰聚合酶包含在一或多个对应于Φ29聚合酶中的Y148、Y226、V250、N251、T368、E375、K379、Q380、A437、P477、K478及A484的位置上的突变。在一些实施例中,本公开的经修饰聚合酶是包含在Y148、Y226、V250、N251、T368、E375、K379、Q380、A437、P477、K478及A484中的一或多者上的突变的经修饰Φ29聚合酶。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484C中的一或多者。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484S中的一或多者。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484T中的一或多者。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484Q中的一或多者。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484N中的一或多者。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484E中的一或多者。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484D中的一或多者。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484K中的一或多者。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484R中的一或多者。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484H中的一或多者。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484Y中的一或多者。在一些实施例中,经修饰聚合酶包含Y148I、Y226F、V250A、N251R、T368F、E375K、K379R、Q380R、A437G、P477D、K478D及A484X中的一或多者,其中X表示非天然氨基酸,如本文中所描述。如本文中所使用,一或多个可以是2个或更多个、4个或更多个、6个或更多个、8个或更多个、10个或更多个、12个或更多个,例如,所有的所列出的氨基酸取代。
在一些实施例中,经修饰聚合酶包含在一或多个对应于Φ29聚合酶中的M8、V51、N62、I71、L107、K131、K135、L142、G197、Y224、E239、V250、L253、Y281、I288、T301、R306、R308、D325、D341、K354、T368、E375、A437、A444、E466、D476、A484、E508、D510、K512、E515、K539、D570及T571的位置(例如在1至35个或其间任何整数个位置,例如2个或更多个、5个或更多个、10个或更多个、15个或更多个、20个或更多个,例如所有)的突变。在一些实施例中,经修饰聚合酶是包含在Φ29聚合酶中的M8、V51、N62、I71、L107、K131、K135、L142、G197、Y224、E239、V250、L253、Y281、I288、T301、R306、R308、D325、D341、K354、T368、E375、A437、A444、E466、D476、A484、E508、D510、K512、E515、K539、D570及T571中的一或多者上的突变的经修饰Φ29聚合酶。在一些实施例中,经修饰聚合酶包含一或多个(例如在1至35个或其间任何整数个,例如2个或更多个、5个或更多个、10个或更多个、15个或更多个、20个或更多个,例如所有)以下突变:M8R、V51A、N62D、I71V、L107I、K131E、K135Q、L142K、G197D、Y224K、E239G、V250A、V250I、L253A、L253H、Y281H、I288L、T301C、R306Q、R308L、D325E、D341E、K354R、T368F、E375Y、A437G、A444T、E466K、D476H、A484E、E508R、D510K、D510R、K512Y、E515Q、K539E、D570S及T571V。
在一些实施例中,经修饰聚合酶包含在一或多个对应于Φ29聚合酶中的K135、L142、Y224、E239、V250、L253、E375、A437、E466、D476、A484、E508、D510、K512、E515、K539、D570及T571的位置(例如在1至18个或其间任何整数个位置,例如2个或更多个、5个或更多个、10个或更多个、15个或更多个,例如所有)上的突变。在一些实施例中,本发明的经修饰聚合酶是包含在K135、L142、Y224、E239、V250、L253、E375、A437、E466、D476、A484、E508、D510、K512、E515、K539、D570及T571中的一或多者上的突变的经修饰Φ29聚合酶。在一些实施例中,经修饰聚合酶包含K135Q、L142K、Y224K、E239G、V250I、L253A、E375Y、A437G、E466K、D476H、A484E、E508R、D510R、K512Y、E515Q、K539E、D570S及T571V中的一或多者(例如1至18个或其间任何整数个,例如2个或更多个、5个或更多个、10个或更多个、15个或更多个,例如所有)。
在一些实施例中,本申请案的经修饰聚合酶包含TPR1区域取代。举例而言,在一些实施例中,经修饰聚合酶包含来自粪肠球菌的TPR1区域(例如SEQ ID NO:5中的V271-M375)替代对应于Φ29聚合酶(SEQ ID NO:1)中的S260-L359的TPR1区域。
在一些实施例中,本申请案的经修饰聚合酶包含一或多个在核酸外切酶区域中的取代。举例而言,在一些实施例中,经修饰聚合酶包含来自M2Y的核酸外切酶区域的部分(例如SEQ ID NO:2中的M1-I51)替代对应于Φ29聚合酶(SEQ ID NO:1)中的M1-V54的氨基酸。在一些实施例中,经修饰聚合酶包含来自粪肠球菌的核酸外切酶区域的部分(例如SEQ ID NO:5中的F72-S89)替代对应于Φ29聚合酶(SEQ ID NO:1)中的E75-N91的氨基酸。在一些实施例中,经修饰聚合酶包含来自M2Y的核酸外切酶区域的部分及来自粪肠球菌的核酸外切酶区域的部分分别替代对应于Φ29聚合酶中的M1-V54及E75-N91的氨基酸。
在一些实施例中,本申请案的经修饰聚合酶包含经修饰掌型区域。举例而言,在一些实施例中,经修饰聚合酶包含来自粪肠球菌的掌型区域的部分(例如SEQ ID NO:5中的L445-V449)替代对应于Φ29聚合酶(SEQ ID NO:1)中的M429-I433的氨基酸。在一些实施例中,经修饰聚合酶包含在对应于Φ29聚合酶中的A444位置上的丙氨酸至胸腺嘧啶突变(例如A444T)。在一些实施例中,经修饰聚合酶包含来自粪肠球菌的掌型区域的部分及对应于Φ29聚合酶中的A444T的氨基酸突变。
在一些实施例中,经修饰聚合酶包含在一或多个(例如1、2或3个)对应于Φ29聚合酶的G197、I71及L107的位置上的突变。在一些实施例中,本公开的经修饰聚合酶是包含在G197、I71及L107中的一或多者(例如1、2或3者)上的突变的经修饰Φ29聚合酶。在一些实施例中,经修饰聚合酶包含G197D、I71V及L107I中的一或多者(例如1、2或3者)。
在一些实施例中,本申请案的经修饰聚合酶包含一或多个在聚合酶的一或多个区域或片段(例如结构域或其部分,任选地包括侧接氨基酸)中的氨基酸突变。在一些实施例中,经修饰聚合酶包含一或多个在核酸外切酶区域、掌型区域、TPR1区域、手指型区域、TPR2区域及拇指型区域中的一或多者中的氨基酸突变。
在一些实施例中,经修饰聚合酶包含在核酸外切酶区域(例如核酸外切酶区域的核酸外切酶环)中的一或多个位置上的突变。在一些实施例中,具有Φ29聚合酶大多数序列的经修饰聚合酶包含在核酸外切酶区域中的一或多个位置上的突变。举例而言,在一些实施例中,本公开的经修饰聚合酶是包含在Φ29聚合酶的核酸外切酶区域中的E75、R76、S82、A83、D84、G85、L86、P87、N88、Y90及N91中的一或多者上的突变的经修饰Φ29聚合酶。在一些实施例中,经修饰聚合酶包含一或多个在对应于Φ29聚合酶中的E75、R76、S82、A83、D84、G85、L86、P87、N88、Y90及N91的位置上的氨基酸突变。因此,在一些实施例中,当经修饰聚合酶不包含Φ29聚合酶大多数序列时,经修饰聚合酶包含一或多个对应于以上所列出的位置的氨基酸,例如,如藉由同源性比对或本领域已知的其他方法所测定。在一些实施例中,经修饰聚合酶包含E75F、R76K、S82C、A83K、D84E、G85A、L86K、P87E、N88R、Y90F及N91S中的一或多者。因此,在一些实施例中,包含核酸外切酶结构域或其部分的片段用于交换来自不同聚合酶的对应的核酸外切酶结构域。举例而言,在一些实施例中,包含一种聚合酶的核酸外切酶结构域的环及侧接氨基酸的片段被来自另一聚合酶的对应的片段置换。举例而言,在一些实施例中,Φ29E75-N91片段被来自粪肠球菌的对应的F72-S89片段置换。在一些实施例中,交换包含核酸外切酶环的片段可以减小聚合酶的脉冲间距离。
在一些实施例中,经修饰聚合酶包含在TPR1区域中的一或多个位置上的突变。举例而言,在一些实施例中,经修饰聚合酶包含在一或多个(例如1、2、3、4、5或6个)对应于Φ29聚合酶中的Y281、I288、T301、D325、D341及K354的位置上的突变。在一些实施例中,本公开的经修饰聚合酶是包含在Y281、I288、T301、D325、D341及K354中的一或多者(例如1、2、3、4、5或6者)上的突变的经修饰Φ29聚合酶。在一些实施例中,在Y281、I288、T301、D325、D341及K354中的一或多者(例如1、2、3、4、5或6者)上的氨基酸改变成在其他聚合酶(例如M2Y、铜绿蝇、芽孢杆菌菌株,例如GA-1)中的对应的位置上的氨基酸。在一些实施例中,经修饰聚合酶包含Y281H、I288L、T301C、D325E、D341E及K354R中的一或多者(例如1、2、3、4、5或6者)。在一些实施例中,在一或多个(例如1、2、3、4、5或6个)对应于Φ29聚合酶中的Y281、I288、T301、D325、D341及K354的位置上的突变增加并入比率(例如在单分子测序反应中)。
在一些实施例中,经修饰聚合酶包含在掌型区域中的一或多个位置上的突变。举例而言,在一些实施例中,经修饰聚合酶包含在一或多个(例如1、2、3、4或5个)对应于Φ29聚合酶中的M429、G430、V431、I433及A444的位置上的突变。在一些实施例中,本公开的经修饰聚合酶是包含在M429、G430、V431、I433及A444中的一或多者(例如1、2、3、4或5者)上的突变的经修饰Φ29聚合酶。在一些实施例中,在M429、G430、V431、I433及A444中的一或多者(例如1、2、3、4或5者)上的氨基酸改变成在其他聚合酶(例如M2Y、铜绿蝇、芽孢杆菌菌株,例如GA-1)中的对应的位置上的氨基酸。在一些实施例中,经修饰聚合酶包含M429L、G430A、V431S、I433V及A444T中的一或多者(例如1、2、3、4或5者)。在一些实施例中,在一或多个(例如1、2、3、4或5个)对应于Φ29聚合酶中的M429、G430、V431、I433及A444的位置上的突变增加准确性(例如在单分子测序反应中)。
在一些实施例中,经修饰聚合酶包含在掌型区域中的一或多个位置及核酸外切酶区域中的一或多个位置上的突变。举例而言,在一些实施例中,经修饰聚合酶包含在一或多个(例如1、2或3个)对应于Φ29聚合酶的G197、M8及V51的位置上的突变。在一些实施例中,本公开的经修饰聚合酶是包含在G197、M8及V51中的一或多者(例如1、2或3者)上的突变的经修饰Φ29聚合酶。在一些实施例中,经修饰聚合酶包含G197D、M8R及V51A中的一或多者(例如1、2或3者)。在一些实施例中,在一或多个(例如1、2或3个)对应于Φ29聚合酶中的G197、M8及V51的位置上的突变可以提高生产产率、热稳定性和/或提高加载效率(例如加载至阵列的样品槽)。
在一些实施例中,经修饰聚合酶包含在掌型区域中的一或多个位置及拇指型区域中的一或多个位置上的突变。举例而言,在一些实施例中,经修饰聚合酶包含在一或多个(例如1、2、3、4或5个)对应于Φ29聚合酶中的E466、D476、K539、D570及T571的位置上的突变。在一些实施例中,本公开的经修饰聚合酶是包含在E466、D476、K539、D570及T571中的一或多者(例如1、2、3、4或5者)上的突变的经修饰Φ29聚合酶。在一些实施例中,经修饰聚合酶包含E466K、D476H、K539E、D570S及T571V中的一或多者(例如1、2、3、4或5者)。
在一些实施例中,经修饰聚合酶包含一或多个(例如1、2、3、4、5、6或7个)在对应于M2Y聚合酶中的N59、Y145、V247、L250、E372、A481及K509的位置上的氨基酸突变。举例而言,在一些实施例中,当经修饰聚合酶包含M2Y聚合酶大多数序列时,经修饰聚合酶包含一或多个在如前文中列出的位置上的突变。在一些实施例中,当经修饰聚合酶不包含M2Y聚合酶大多数序列时,经修饰聚合酶包含一或多个对应于以上列出的位置的氨基酸突变,例如,如藉由同源性比对或本领域已知的其他方法所测定。
在一些实施例中,经修饰聚合酶包含野生型聚合酶(例如如表1中所阐述)的一或多个片段(例如其结构域或部分,任选地包括侧接氨基酸)。在一些实施例中,屎肠球菌聚合酶的一或多个片段(例如其结构域或部分,任选地包括侧接氨基酸)(例如一或多个SEQ ID NO:5的片段)可取代SEQ ID NO:1至4及6至19中的任一者的一或多个片段。在一些实施例中,屎肠球菌聚合酶的一或多个片段(例如其结构域或部分,任选地包括侧接氨基酸)可取代Φ29聚合酶的一或多个片段。在一些实施例中,屎肠球菌聚合酶的一或多个片段(例如其结构域或部分,任选地包括侧接氨基酸)可以取代M2Y聚合酶的一或多个片段。在一些实施例中,屎肠球菌聚合酶的一或多个片段(例如其结构域或部分,任选地包括侧接氨基酸)可以取代一或多个Φ29聚合酶的片段和/或M2Y聚合酶的片段。在一些实施例中,屎肠球菌聚合酶的一或多个片段(例如其结构域或部分,任选地包括侧接氨基酸)(例如,SEQ ID NO:5的结构域或例如含有一或多个氨基酸取代的其经修饰形式)可以取代一或多个本文中所描述的变异体聚合酶(例如表2中所列出的变异体聚合酶或含有一或多个氨基酸取代或表2中所说明的或表3至5中所描述的其他结构域取代的变异体聚合酶)的片段。
在一些实施例中,经修饰聚合酶的大多数序列不包含对应于以上作为实例列出的聚合酶中的位置的一或多个同源氨基酸。在此等情况下,在一些实施例中,经修饰聚合酶不包含一或多个突变。然而,在一些实施例中,当将所需氨基酸序列与本文中所描述的聚合酶序列比较周围同源残基是可识别的时,根据周围同源残基推断,突变氨基酸包括在经修饰聚合酶中作为在聚合酶中的位点上的插入。突变的聚合酶变异体是根据本文中描述的实施例工程改造的且列出于表2(SEQ ID NO:20至96)中。
表2.同源聚合酶变异体
在一些实施例中,根据聚合酶的结构和/或功能选择氨基酸用于修饰。举例而言,图2描绘Φ29聚合酶200的图解说明。折叠的三维结构包含对应于覆盖图202的独特的结构域及子结构域:N端核酸外切酶结构域(1)及含有掌型子结构域(2)、末端蛋白质区域1(terminal protein region,TPR1)子结构域(3)、手指型子结构域(4)、TPR2子结构域(5)及拇指型子结构域(6)的C端聚合酶结构域。这些结构域及子结构域绘制于多肽结构204的多肽链的区域,其以N端至C端方式定向。如所示,N端核酸外切酶结构域(1)跨越野生型Φ29聚合酶的残基1-189且C端聚合酶结构域跨越野生型Φ29聚合酶的残基190-575。在C端聚合酶结构域中,掌型子结构域(2)跨越野生型Φ29聚合酶的残基190-260及427-530,TPR1子结构域(3)跨越野生型Φ29聚合酶的残基261-358,手指型子结构域(4)跨越野生型Φ29聚合酶的残基359-394,TPR2子结构域(5)跨越野生型Φ29聚合酶的残基395-426,且拇指型子结构域(6)跨越野生型Φ29聚合酶的残基531-575。本申请案中所描述的不同聚合酶的等同片段(例如其结构域或部分,任选地包括侧接氨基酸)可以取代彼此以产生嵌合聚合酶。举例而言,来自一种聚合酶(例如具有表1中显示的野生型序列或具有表2中例示或表3至5中所描述的一或多个突变)的核酸外切酶结构域、掌型子结构域、TPR1子结构域、一或多个手指型子结构域、TPR2子结构域和/或拇指型子结构域中的一或多者可以取代另一聚合酶中的对应的结构域(例如具有表1中显示的野生型序列或具有表2中例示或表3至5中所描述的一或多个突变)。在一些实施例中,包含这些结构域中的一或多者的部分的片段,任选地包括一或多个侧接氨基酸,可以经取代。
在一些实施例中,经修饰聚合酶包含除了Φ29聚合酶的外的大多数聚合酶序列。在这类实施例中,大多数聚合酶序列包含一或多个可以类推至Φ29聚合酶200的区域(例如根据同源性比对、计算模建、结构分析或任何适合方法)。如本文中所使用,聚合酶的“区域”是指聚合酶的独特的结构域或子结构域。举例而言,在一些实施例中,聚合酶的区域是指N端核酸外切酶结构域或C端聚合酶结构域。在一些实施例中,聚合酶的区域是指掌型子结构域、TPR1子结构域、手指型子结构域、TPR2子结构域或拇指型子结构域。因此,在一些实施例中,聚合酶的区域是指包含给定结构域或子结构域的所有氨基酸。在一些实施例中,经修饰聚合酶包含对大多数聚合酶序列的一或多个区域的修饰。在一些实施例中,经修饰聚合酶包含对大多数聚合酶序列的一或多个部分的修饰。如本文中所使用,聚合酶的“部分”是指聚合酶序列中的一段两个或更多个连续残基。在一些实施例中,聚合酶序列的部分是指单个聚合酶结构域或单个聚合酶子结构域中的两个或更多个连续氨基酸。在一些实施例中,聚合酶序列的部分是指跨越多于一个聚合酶结构域和/或聚合酶子结构域的两个或更多个连续氨基酸。因此,在一些实施例中,聚合酶序列的部分是聚合酶序列中的任何段的连续氨基酸。在一些实施例中,部分是指构成,例如聚合酶区域或结构域的部分的5-10个连续氨基酸、10-25个连续氨基酸、25-50个连续氨基酸、50-75个连续氨基酸、75-100个连续氨基酸或其他数目的连续氨基酸。
在一些实施例中,经修饰聚合酶包含一或多个如图2中大体描绘的结构域和/或子结构域中的一或多者中的单点突变。举例而言,图3描绘表2的所选择的突变变异体,所述突变变异体具有在各多肽链中的突变的位点(用箭头在附近显示)。多肽链针对以下显示:M2Y及M2Y突变变异体H016(开放填充)、铜绿蝇及铜绿蝇突变变异体H018(点画填充)、屎肠球菌及屎肠球菌突变变异体H020(虚线填充)及芽孢杆菌噬菌体VMY22及芽孢杆菌噬菌体VMY22突变变异体H022(对角线填充)。然而,亦可使用包含如本文中所描述的其他片段交换和/或氨基酸突变的嵌合体。
在一些实施例中,除本文中所描述的一或多个单点突变修饰外或作为替代,大多数聚合酶序列的一段氨基酸(例如两个或更多个连续氨基酸)经修饰。在一些实施例中,该段氨基酸是对应于不同聚合酶序列的部分的一段氨基酸。举例而言,在一些实施例中,大多数聚合酶序列的结构域/子结构域(或其中部分)与不同聚合酶序列的对应的结构域/子结构域(或其中部分)交换。在这类实施例中,聚合酶称为嵌合聚合酶、嵌合聚合酶变异体或嵌合体。嵌合聚合酶是根据本文中描述的实施例工程改造的且列出于表3(SEQ ID NO:97至516)中。
表3.嵌合聚合酶变异体
在一些实施例中,本公开的经修饰重组聚合酶选自表3。在一些实施例中,嵌合聚合酶变异体(例如如表3中所列出)包含具有用不同聚合酶序列的对应的区域或部分取代的大多数序列的区域或部分的大多数聚合酶序列。在一些实施例中,包含大多数聚合酶序列中的区域(例如结构域和/或子结构域)的所有残基用包含不同聚合酶序列中的对应区域的所有残基取代。在一些实施例中,包含大多数聚合酶序列中的区域的残基的至少一部分用包含不同聚合酶序列中的对应区域的残基的至少一部分取代。
在一些实施例中,仅大多数序列中的单个子结构域用不同序列的对应子结构域取代。举例而言,图4描绘选自表3的嵌合聚合酶变异体。六个所选择的变异体显示为具有如其一般在多肽中出现的以氨基端至羧基端定向的子结构域的多肽链。图4的多肽链中的每一者包含Q001的聚合酶大多数序列(黑色填充),其中一或多个结构域和/或子结构域用M2Y聚合酶(SEQ ID NO:2,开放填充)的一或多个对应的结构域和/或子结构域或铜绿蝇(SEQ ID NO:3,点画填充)的一或多个对应的结构域和/或子结构域及或一或多个侧接氨基酸取代。
在一些实施例中,嵌合聚合酶变异体包含具有经取代自不同聚合酶序列的核酸外切酶结构域的大多数聚合酶序列。如图4中所示,C017是包含经取代自M2Y聚合酶序列(例如如SEQ ID NO:2中所阐述)的核酸外切酶结构域的嵌合聚合酶变异体。类似地,C020包含经取代自铜绿蝇聚合酶序列(例如如SEQ ID NO:3中所阐述)的核酸外切酶结构域。在一些实施例中,在聚合酶的校读能力不理想的情况下(例如在测序反应中),在经修饰聚合酶变异体中核酸外切酶结构域的修饰或替换可能很有用。然而,应了解,本公开的经修饰重组聚合酶涵盖其他及替代结构域和/或子结构域取代。
在一些实施例中,嵌合聚合酶变异体包含具有经取代自不同聚合酶序列的核酸外切酶环的大多数聚合酶序列。如本文中所使用,在一些实施例中,“核酸外切酶环”是指形成核酸外切酶结构域中的环区域的一段连续氨基酸。举例而言,图5A描绘全透视图500及放大透视图502中的Φ29聚合酶的图解说明。放大透视图502是于全透视图500中显示的方形区域的特写视图,其显示Φ29聚合酶的核酸外切酶结构域中的环区域。所选择的环残基在放大透视图502中以杆形式显示,具有形成跨越残基N77至N88的核酸外切酶环的该段连续氨基酸。核酸外切酶结构域的此区域的演化保守分析表明,该环及若干侧接残基的保守相对不佳。图5B描绘Φ29聚合酶与选自表1的一组非限制性其他聚合酶的核酸外切酶区域之间的同源性比对504。亦描绘了显示Φ29聚合酶的核酸外切酶环N77-N88与其他聚合酶中对应的核酸外切酶环的环同源性比对506。
根据显示对应于Φ29聚合酶的核酸外切酶环N77-N88的区域中的相对低保守的同源性分析,这提供了在聚合酶变异体中搜索所期望的生化性质时的变化源(例如适合用于测序反应中的)。相应地,在一些实施例中,嵌合聚合酶变异体包含具有经取代自不同聚合酶序列的核酸外切酶环的大多数聚合酶序列,其中“核酸外切酶环”与Φ29聚合酶的核酸外切酶环N77-N88同源(例如如藉由图5B中的环同源性比对506所示)。
如藉由图5B中的实例比对所示,序列同源性分析可用于鉴别与Φ29聚合酶的N77-N88同源的核酸外切酶环序列。借助于实例而非限制,环同源性比对506显示M2Y(H74-N85)、铜绿蝇(N64-G76)、粪肠球菌(N74-R86)、芽孢杆菌GA-1(N74-K88)、芽孢杆菌VMY22(K80-K91)、放线菌AV-1(H93-K105)、马铃薯包囊线虫(L86-K99)、伊比利亚猞猁肠(D73-R87)、候选种(N85-N98)及埃格特菌属(V73-K88)的同源核酸外切酶环序列。因此,在一些实施例中,经取代核酸外切酶环在与Φ29聚合酶的N77-N88同源的区域中可包括约12个与约16个之间的氨基酸。在一些实施例中,经取代核酸外切酶环在与Φ29聚合酶的N77-N88同源的区域中包含约10个氨基酸至至多20个氨基酸、约5个氨基酸至至多15个氨基酸、约5个氨基酸至至多20个氨基酸、或约5个氨基酸至25个氨基酸或更多。
在一些实施例中,本申请案的经修饰聚合酶在包括与Φ29聚合酶的N77-N88同源的核酸外切酶环的核酸外切酶结构域的区域中包含一或多个氨基酸突变。举例而言,在一些实施例中,本公开的经修饰聚合酶是在Φ29聚合酶中的E75、R76、S82、A83、D84、G85、L86、P87、N88、Y90及N91中的一或多者上包含突变的经修饰Φ29聚合酶。在一些实施例中,经修饰聚合酶包含E75F、R76K、S82C、A83K、D84E、G85A、L86K、P87E、N88R、Y90F及N91S中的一或多者。在一些实施例中,经修饰聚合酶在对应于Φ29聚合酶中的E75、R76、S82、A83、D84、G85、L86、P87、N88、Y90及N91的位置上包含一或多个氨基酸突变。举例而言,在一些实施例中,当经修饰聚合酶不包含Φ29聚合酶大多数序列时,经修饰聚合酶包含一或多个对应于以上列出的位置的氨基酸,例如,如藉由同源性比对或本领域已知的其他方法所测定。
在一些实施例中,嵌合聚合酶变异体包含具有经取代自不同聚合酶序列的TPR1子结构域的大多数聚合酶序列。举例而言,C018是包含经取代自M2Y聚合酶序列的TPR1子结构域的嵌合聚合酶。类似地,C021包含经取代自铜绿蝇聚合酶的TPR1子结构域。在一些实施例中,嵌合聚合酶变异体包含具有经取代自不同聚合酶序列的掌型子结构域的大多数聚合酶序列。在一些实施例中,嵌合聚合酶变异体包含具有经取代自不同聚合酶序列的手指型子结构域的大多数聚合酶序列。在一些实施例中,嵌合聚合酶变异体包含具有经取代自不同聚合酶序列的TPR2子结构域的大多数聚合酶序列。在一些实施例中,嵌合聚合酶变异体包含具有经取代自不同聚合酶序列的拇指型子结构域的大多数聚合酶序列。如本文中所描述的,经修饰重组聚合酶包括包含多于一个结构域和/或子结构域取代的嵌合聚合酶变异体。
在一些实施例中,大多数序列中的两个区域(例如结构域/子结构域)用不同序列的两个对应的区域(例如对应的结构域/子结构域)取代。举例而言,如图4中所示,C019是包含用M2Y聚合酶序列的对应核酸外切酶结构域及TPR1子结构域取代的核酸外切酶结构域及TPR1子结构域的嵌合聚合酶。类似地,C022包含用铜绿蝇聚合酶的对应核酸外切酶结构域及TPR1子结构域取代的核酸外切酶结构域及TPR1子结构域。在一些实施例中,涵盖具有本文中所描述的经修饰聚合酶的其他结构域和/或子结构域取代。举例而言,在一些实施例中,大多数序列中的多于两个(例如三、四、五或六个)区域(例如结构域/子结构域)用不同序列的多于两个(例如三、四、五或六个)对应区域取代。
在一些实施例中,嵌合聚合酶变异体的大多数聚合酶序列选自表1至3中的序列。在一些实施例中,大多数聚合酶序列包含一或多个经取代自选自表1至3的不同聚合酶序列的区域和/或部分。举例而言,表4提供自表3中选择的嵌合聚合酶变异体的概述,且针对各者列举大多数聚合酶序列以及经取代区域/部分及该取代所基于的序列的描述。
表4.嵌合聚合酶-经取代部分
然而,可使用和/或进一步的修饰,例如,如本文中的表中的一或多者中所描述且说明的其他嵌合体。
在一些实施例中,嵌合聚合酶变异体可以另外包含一或多个位点特异性突变。因此,在一些实施例中,任何一或多个本文中所描述的突变(例如任何一或多个包括在表2中的各序列中的突变)可应用于本公开中所涵盖的任何嵌合聚合酶(例如如上文中所描述和列出于表3中)。图6大体描绘包含一或多个突变的嵌合聚合酶变异体。举例而言,突变嵌合聚合酶602包含具有经取代M2Y核酸外切酶结构域和该经取代结构域中的突变的Φ29聚合酶大多数序列。在一些实施例中,突变嵌合聚合酶包含具有用对应于两个或更多个不同聚合酶序列的区域取代的两个或更多个区域的大多数序列。举例而言,突变嵌合聚合酶604包含具有经取代屎肠球菌聚合酶TPR1子结构域及经取代M2Y聚合酶TPR2子结构域的Φ29聚合酶大多数序列,其具有在聚合酶序列中的各种位置进行的位点特异性突变。在一些实施例中,突变嵌合聚合酶包含具有经对应于不同聚合酶的区域取代的两个或更多个区域的大多数序列。举例而言,突变嵌合聚合酶606包含具有经取代屎肠球菌聚合酶TPR1、TPR2及拇指型子结构域的Φ29聚合酶大多数序列,其具有在聚合酶序列中的各种位置进行的位点特异性突变。
表5提供自表3中选择的嵌合聚合酶变异体的概述,其针对各者提供大多数聚合酶序列以及对特定变异体所作出的氨基酸突变的描述。
表5.嵌合聚合酶-定点突变体
然而,其他氨基酸突变可以并入至一或多个本文中所描述的嵌合聚合酶中。举例而言,一或多个氨基酸变化可以在位置M8、V51、N62、I71、L107和/或K131中的一或多者上,和/或在参照Φ29聚合酶序列的位置K135、L142、G197、Y224、E239、V250、L253、Y281、I288、T301、R306、R308、D325、D341、K354、T368、E375、A437、A444、E466、D476、A484、E508、D510、K512、E515、K539、D570及T571中的一或多者上并入。举例而言,在一些实施例中,嵌合聚合酶亦可包括以下氨基酸取代中的一或多者:M8R、V51A、N62D、I71V、L107I和/或K131E,和/或以下氨基酸取代中的一或多者:K135Q、L142K、G197D、Y224K、E239G、V250A、V250I、L253A、L253H、Y281H、I288L、T301C、R306Q、R308L、D325E、D341E、K354R、T368F、E375Y、A437G、A444T、E466K、D476H、A484E、E508R、D510K、D510R、K512Y、E515Q、K539E、D570S和/或T571V。
如本文中所使用,术语“聚合酶”(polymerase或polymerizing enzyme)一般是指能够催化聚合反应的任何酶。聚合酶的实例包括但不限于:DNA聚合酶、RNA聚合酶、热稳定聚合酶、野生型聚合酶、经修饰聚合酶、大肠杆菌DNA聚合酶I、T7 DNA聚合酶、噬菌体T4 DNA聚合酶φ29(phi29)DNA聚合酶、Taq聚合酶、Tth聚合酶、Tli聚合酶、Pfu聚合酶、Pwo聚合酶、聚合酶、Deep VENTTM聚合酶、Ex TAQTM聚合酶、LA TAQTM聚合酶、Sso聚合酶、Poc聚合酶、Pab聚合酶、Mth聚合酶、ES4聚合酶、Tru聚合酶、Tac聚合酶、Tne聚合酶、Tma聚合酶、Tca聚合酶、Tih聚合酶、Tfi聚合酶、Taq聚合酶、Tbr聚合酶、Tfl聚合酶、Tth聚合酶、聚合酶、PYROBESTTM聚合酶、Pwo聚合酶、KOD聚合酶、Bst聚合酶、Sac聚合酶、克列诺(Klenow)片段、具有3'至5'核酸外切酶活性的聚合酶,及其变体、经修饰产物及衍生物。在一些实施例中,聚合酶为单个亚单元聚合酶。聚合酶的其他实例包括M2Y聚合酶、铜绿蝇聚合酶、屎肠球菌聚合酶、芽孢杆菌噬菌体VMY22聚合酶、芽孢杆菌噬菌体GA-1聚合酶、放线菌噬菌体AV-1聚合酶、候选莫兰菌聚合酶、芽孢杆菌噬菌体MG-B1聚合酶、埃格特菌属聚合酶、链球菌噬菌体CP-7聚合酶、拟杆菌属聚合酶、沙眼披衣菌聚合酶及马铃薯白线虫聚合酶。DNA聚合酶的非限制性实例及其特性详细描述于DNA Replication第2版,Kornberg及Baker,W.H.Freeman,New York,N.Y.(1991)及其他文献中。此类序列的非限制性实例可见于表1(SEQ ID NO:1至19)中。
在靶核酸的核碱基与互补dNTP之间碱基配对后,聚合酶藉由在新合成的链的3'羟基端与dNTP的α磷酸之间形成磷酸二酯键来将dNTP并入至新合成的核酸链中。在一些实施例中,聚合酶是具有较高持续合成能力的聚合酶。然而,在一些实施例中,聚合酶是具有降低的持续合成能力的聚合酶。聚合酶持续合成能力一般是指聚合酶将dNTP连续并入至核酸模板中而不释放核酸模板的能力。
在一些实施例中,聚合酶是具有低的5'-3'核酸外切酶和/或3'-5'核酸外切酶活性的聚合酶。在一些实施例中,聚合酶经修饰(例如藉由氨基酸取代)以具有相对于对应的野生型聚合酶而言降低的5'-3'核酸外切酶活性和/或3'-5'活性。DNA聚合酶的其他非限制性实例包括9°NMTM DNA聚合酶(新英格兰生物实验室(New England Biolabs))及克列诺外聚合酶的P680G突变体(Tuske等人(2000)JBC 275(31):23759-23768)。在一些实施例中,具有降低的持续合成能力的聚合酶为含有一或多段核苷酸重复区(例如相同类型的两个或多于两个依序碱基)的模板的测序提供提高的准确度。
核酸聚合酶对不同类型的核酸的持续合成能力、核酸外切酶活性、相对亲和力或其他特性可以由本领域技术人员藉由相对于对应野生型聚合酶的突变或其他修饰来增加或降低。
在一些实施例中,经修饰聚合酶包含一或多个非天然氨基酸取代。如本文中所使用,“非天然氨基酸”是指除了以下二十种基因编码的α氨基酸之外的任何氨基酸、经修饰氨基酸或氨基酸类似物:丙氨酸、精氨酸、天冬酰胺、天冬氨酸、半胱氨酸、麸酰氨酸、谷氨酸、甘氨酸、组氨酸、异亮氨酸、亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、脯氨酸、丝氨酸、苏氨酸、色氨酸、酪氨酸、缬氨酸。在一些实施例中,非天然氨基酸可包括除了以上二十种α氨基酸之外的天然产生化合物。非天然氨基酸及非天然氨基酸并入至蛋白质序列中的方法是本领域已知的,例如,如美国专利第7,045,337号中所述,其内容以引用的方式并入本文中。
如本文中所述,当聚合酶和/或聚合酶序列天然或人工地衍生自共同祖代蛋白质或蛋白质序列时,其为“同源”。类似地,当核酸和/或核酸序列天然或人工地衍生自共同祖代核酸或核酸序列时,其为同源。举例而言,任何天然产生的核酸可以藉由任何可利用的诱变方法修饰以在多肽中在给定位置上包括至少一种编码不会天然产生的氨基酸的特定密码子。当表达时,此经诱变核酸编码包含一或多个突变氨基酸的多肽。在一些实施例中,同源性一般根据两个或更多个核酸或蛋白质(或其序列)之间的序列相似性推断。用于确立同源性序列之间的相似性的精确百分比随所研究的核酸及蛋白质而变化,但常规使用小至25%序列相似性来确立同源性。亦可使用更高水平的序列相似性,例如30%、40%、50%、60%、70%、80%、90%、95%或99%或更大,来确立同源性。用于测定序列相似性百分比的方法为本领域熟知。在一些实施例中,相似性可以使用诸如上文中所述的算法的算法,包括例如BLASTP及BLASTN算法,例如使用预设参数,来测定。
在一些实施例中,为表达本公开的聚合酶,将编码该聚合酶的DNA插入至一或多个表达载体中使得所编码聚合酶可操作地连接于转录及翻译控制序列(参见,例如美国专利第6,914,128号,其内容以引用的方式并入本文中)。在此背景下,术语“可操作地连接”意指编码聚合酶的序列连接至载体中使得载体中的转录及翻译控制序列发挥其调节聚合酶的转录及翻译的预期功能。选择与所使用的表现宿主细胞兼容的表达载体及表达控制序列。将聚合酶编码序列藉由标准方法(例如,聚合酶编码序列上的互补限制位点与载体的连接或当无限制位点存在时的钝端连接)插入至表达载体中。
为表达经修饰聚合酶,可以将编码该经修饰聚合酶的表达载体藉由标准技术转染至宿主细胞中。术语“转染”的各种形式意欲涵盖常用于将外源DNA引入至原核或真核宿主细胞中的各种技术,例如电穿孔、磷酸钙沉淀、DEAE-聚葡萄糖转染及类似技术。用于表达本公开的聚合酶的适合宿主细胞包括原核生物、酵母或更高等真核生物细胞。
用于此目的的适合原核生物包括真细菌,诸如革兰氏阴性或革兰氏阳性生物体,例如肠杆菌科(Enterobacteriaceae),诸如埃希氏杆菌属(Escherichia),例如大肠杆菌,肠杆菌属(Enterobacter)、欧文菌属(Erwinia)、克雷伯氏菌属(Klebsiella)、变形杆菌属(Proteus)、沙门氏菌属(Salmonella),例如鼠伤寒沙门杆菌(Salmonella typhimurium),沙雷氏菌属(Serratia),例如黏质沙雷氏菌(Serratia marcescans),及志贺杆菌属(Shigella),以及杆菌(Bacilli),诸如枯草芽孢杆菌(B.subtilis)及地衣芽孢杆菌(B.licheniformis),假单胞菌属(Pseudomonas),诸如绿脓杆菌(P.aeruginosa),及链霉菌(Streptomyces)。除原核生物的外,诸如丝状真菌或酵母的真核微生物是用于编码载体的多肽的适合克隆或表达宿主。在低等真核宿主微生物中,最常用的是酿酒酵母(Saccharomyces cerevisiae)或普通烘焙酵母。然而,在本文中若干其他属、种及菌株通常是可获得的且有用的,诸如粟酒裂殖酵母(Schizosaccharomyces pombe);克鲁维酵母(Kluyveromyces)宿主诸如,例如,乳酸克鲁维酵母(K.lactis)、脆壁克鲁维酵母(K.fragilis)、保加利亚克鲁维酵母(K.bulgaricus)、魏氏克鲁维酵母(K.wickeramii)、沃特克鲁维酵母(K.waltii)、果蝇克鲁维酵母(K.drosophilarum)、耐热克鲁维酵母(K.thermotolerans)及马克斯克鲁维酵母(K.marxianus);巴斯德毕赤酵母(Pichia pastoris);假丝酵母(Candida);瑞氏木霉菌(Trichoderma reesia);粗厚神经胞子菌(Neurospora crassa);许旺酵母(Schwanniomyces)诸如西方许旺酵母(Schwanniomyces occidentalis);及丝状真菌,诸如红霉菌属(Neurospora)、青霉菌属(Penicillium)、弯颈霉属(Tolypocladium)及曲菌属(Aspergillus)宿主诸如,构巢曲菌(A.nidulans)及黑曲菌(A.niger)。
在一些实施例中,宿主细胞经用于产生聚合酶的上述表达或克隆载体转化,且在经修改成适于诱导启动子、选择转化子或扩增编码所需序列的基因的常规营养物培养基中培养。用于产生聚合酶的宿主细胞可以在各种培养基中培养。可商购的培养基,诸如哈姆氏F10TM(Ham's F10TM)(Sigma)、最低基础培养基(Minimal Essential MediumTM)(MEM)(Sigma)、RPMI-1640(Sigma)及达尔伯克改良伊格尔培养基(Dulbecco's Modified Eagle's MediumTM)(DMEM)(Sigma)适用于培养宿主细胞。培养条件(诸如温度、pH及类似条件)为先前用于经选择用于表达的宿主细胞的培养条件,且对于本领域技术人员而言将显而易见。
在一些实施例中,聚合酶变异体可以在周质空间中胞内产生或直接分泌至细胞培养基中。在聚合酶变异体胞内产生的实施例中,宿主细胞或裂解细胞颗粒碎片(例如由均质化产生)可以藉由各种手段移除,包括但不限于藉由离心或超过滤。在聚合酶分泌至培养基中的情况下,来自此类表达系统的上清液可以首先使用可商购的蛋白质浓缩过滤器来浓缩,随后可将其进行一或多个其他纯化技术,包括但不限于:亲和层析,包括蛋白质亲和层析;离子交换层析,诸如阴离子或阳离子交换层析;及疏水相互作用层析。
在一些实施例中,本申请案的方面可用于与生物样品分析相关方法中。在例示性实施例中,本文中所提供的方法适用于测定样品中的一或多个核酸或多肽的序列和/或测定样品中是否存在一或多个核酸或多肽变异体(例如所关注基因中的一或多个突变)的技术中。在一些实施例中,出于诊断、预测和/或治疗目的,可以对患者样品(例如人类患者样品)进行测试来提供核酸序列信息或测定是否存在所关注的一或多个核酸。在一些实例中,诊断测试可包括测序个体的生物样品中的核酸分子,例如藉由测序个体的生物样品中的不含细胞的DNA分子和/或表达产物(例如RNA)。举例而言,本公开提供可有利地利用在共同待决的美国专利申请案第14/543,865号;第14/543,867号;第14/543,888号;第14/821,656号;第14/821,686号;第14/821,688号;第15/161,067号;第15/161,088号;第15/161,125号;第15/255,245号;第15/255,303号;第15/255,624号;第15/261,697号;第15/261,724号;第62/289,019号;第62/296,546号;第62/310,398号;第62/339,790号;第62/343,997号;第62/344,123号及第62/426,144号中所描述的技术中的方法及组合物,各申请案的内容均以引用的方式并入本文中。
本申请案的一些方面适用于能够测序生物聚合物诸如核酸及蛋白质的技术。在一些实施例中,本申请案中所描述的方法及组合物可用于鉴别并入至核酸或蛋白质中的一系列核苷酸或氨基酸单体的技术(例如藉由检测并入一系列经标记核苷酸或氨基酸单体的时程)中。在一些实施例中,本申请案中所描述的方法及组合物可以并入至鉴别并入至藉由聚合酶合成的模板依赖性核酸测序反应产物中的一系列核苷酸的技术中。
在测序期间,聚合酶可以偶联(例如连接)于目标核酸分子的引发位置(例如测序模板的核酸分子)。引发位置可包含与目标核酸分子的部分互补的引物。作为替代方案,引发位置是设置于目标核酸分子的双链片段内的间隔或缺口。间隙或缺口的长度可以为0至至少1、2、3、4、5、6、7、8、9、10、20、30或40个核苷酸。缺口可在双链序列的一个链中提供中断,其可为聚合酶,诸如链置换聚合酶,提供引发位置。
在一些情况下,测序引物可以退火于可能固定或可能不固定于固体撑体的目标核酸分子。固体撑体可包含,例如,用于核酸测序的集成装置上的样品槽。在一些实施例中,测序引物可固定于固体撑体且目标核酸分子的杂交亦使目标核酸分子固定于固体撑体。在一些实施例中,聚合酶固定于固体撑体且使可溶性引物及目标核酸与聚合酶接触。然而,在一些实施例中,在溶液中形成包含聚合酶、目标核酸及引物的复合物且使该复合物固定于固体撑体(例如经由聚合酶、引物和/或目标核酸的固定)。在一些实施例中,样品槽中没有组分固定于固体撑体。举例而言,在一些实施例中,在溶液中形成包含聚合酶、目标核酸及引物的复合物且该复合物不固定于固体撑体。
在适当的条件下,接触退火引物/目标核酸的聚合酶可以将一或多个核苷酸添加或并入引物中,且核苷酸可以5'至3'模板依赖性方式添加至引物中。核苷酸在引物上的此类并入(例如经由聚合酶的作用)一般可称作引物延长反应。各核苷酸可与可检测标签结合,该可检测标签在核酸延长反应期间可被检测及鉴别(例如根据其发光寿命和/或其他特性)且用于测定并入至延长的引物中的各核苷酸且由此测定新合成的核酸分子的序列。经由新合成的核酸分子的序列互补性,亦可测定目标核酸分子的序列。在一些情况下,测序引物退火至目标核酸分子以及核苷酸向测序引物的并入可在相似反应条件(例如相同或相似反应温度)下或在不同反应条件(例如不同反应温度)下发生。在一些实施例中,藉由合成方法测序可包括存在目标核酸分子(例如目标核酸的拷贝)的群和/或为获得目标核酸的群的目标核酸的扩增步骤。然而,在一些实施例中,藉由合成的测序用于测定受评估的各反应中的单个分子的序列(且不需要核酸扩增制备用于测序的目标模板)。在一些实施例中,根据本申请案的方面平行进行(例如在单个集成装置上)复数个单分子测序反应。举例而言,在一些实施例中,复数个单分子测序反应在集成装置上的单独反应室中各自进行。
在一些实施例中,本公开的聚合酶适用于在显著小体积的样品槽中进行的单分子测序反应。举例而言,在一些实施中,样品槽的体积可在约10-21升与约10-15升之间。因为样品槽体积小,可达成单个样品事件检测(例如单分子事件)。在一些实施例中,表面(例如样品槽的表面)经配置以收纳本文中所描述的聚合酶。在一些实施例中,样品槽收纳可置于样品槽的表面(诸如底表面)上的聚合酶。在一些实施例中,样品槽在集成装置内形成,其中样品槽的底表面位于形成其的集成装置的表面的远端。
在某些实施例中,本文所描述的技术是关于可添加至样品槽中的聚合酶及其复合物。在一些实施例中,本文中所描述的聚合酶可被限制在样品槽的目标体积(例如反应体积)内。在一些实施例中,目标体积是样品槽中的区域。在一或多个聚合酶待固定于底表面上的实施例中,可能需要将底表面官能化以使得能连接一或多个聚合酶(例如聚合酶及其复合物)。在一些实施例中,底表面使用包含偶联基团的物质官能化。举例而言,偶联基团可包含化学部分,诸如胺基、羧基、羟基、巯基、金属、螯合剂及类似物。替代地,其可包括特定结合单元,诸如生物素、抗生物素蛋白、抗生蛋白链菌素、中性抗生物素蛋白、凝集蛋白、SNAP-标签TM(SNAP-tagsTM),或其底物,缔合或结合肽或蛋白质、抗体或抗体片段、核酸或核酸类似物或类似物。另外或替代地,偶联基团可用于偶联用于与所关注的分子(例如聚合酶或其复合物)偶联或结合的其他基团,在一些情况下其可以包括化学官能基及特定结合单元。藉助于实例,偶联基团,例如生物素,可在底物表面上沉积且选择性地在给定区域中活化。中间体结合剂,例如抗生蛋白链菌素,可随后偶联于第一偶联基团。所关注的分子(例如聚合酶或其复合物),其在此特定实例中是经生物素标记的,随后偶联于抗生蛋白链菌素。在一些实施例中,本文中所描述的聚合酶可另外包含能够与将聚合酶固定于表面(例如样品槽的表面)的偶联基团形成相互作用的偶联部分。举例而言,在一些实施例中,聚合酶包含能够结合于抗生物素蛋白的N端或C端生物素化序列。在一些实施例中,生物素化序列另外包含连接子序列。举例而言,在一些实施例中,C端连接子/生物素化序列包含氨基酸序列GGGSGGGSGGGSGLNDFFEAQKIEWHE(SEQ ID NO:517)。
实例
实例1.经修饰聚合酶的表达及评估
在大肠杆菌中表达重组聚合酶变异体且使用His-旋转管柱自150mL规模培养物中纯化。藉由SDS-PAGE和随后进行的库马斯蓝(Coomassie Blue)染色分析蛋白质纯度(图7)。在缓冲交换及蛋白质浓缩之后,在dNTP存在下在30℃下追踪捕集器30分钟的条件下,针对活性及持续合成能力评估重组变异体。在捕集器存在下,嵌合聚合酶变异体C017及C020显示出活性、持续合成能力及合成长度。量测变异体聚合酶对dNTP类似物的利用以评估聚合酶在测序反应中的适用性。同源突变变异体及嵌合聚合酶变异体皆展现对dN6P的利用。来自单分子测序的结果如下显示于表6中。
表6.使用经修饰聚合酶的测序结果
等同及范围
在本文中已经描述及说明数种本发明实施例的同时,本领域技术人员将容易地设想用于执行该功能和/或获得所述结果和/或获得本文所述的所述优势中的一或多者的多种其他方法和/或构造,且将此类变化和/或修改的各者视为在本文所述的本发明实施例的范围内。更一般而言,技术人员将容易地理解本文所述的所有参数、尺寸、物质及配置意欲为例示性且实际参数、尺寸、物质和/或配置将视特定应用或使用本发明教导的应用而定。本领域技术人员将认识到或使用不多于常规实验便能够确定本文中所描述的特定本发明实施例的许多等同物。因此应了解,前述实施例仅藉由实例呈现且在随附权利要求书及其等效物的范围内,本发明可以不同于特定描述及主张的其他方式来实施。本公开的实施例是关于本文中所描述的各单独特征、系统、物品、物质、套组和/或方法。另外,若此类特征、系统、物品、物质、套组和/或方法不为彼此不兼容时,则两种或多于两种此类特征、系统、物品、物质、套组和/或方法的任何组合包括在本发明的范围内。
本文中所定义及使用的所有定义应理解为控制在辞典定义、以引用的方式并入的文献中的定义和/或所定义术语的普通含义内。
本文中所公开的所有参考、专利及专利申请案以引用的方式相关于各自经引用的主题并入,其在一些情况下可涵盖文件的全部内容。
除非明确相反指示,否则如在本文说明书及申请专利范围中使用的不定冠词“一(a/an)”应理解为意谓“至少一个”。
如在本文说明书及权利要求书中使用的词组“和/或”应理解为意指如此结合的要素的“任一者或两者”,亦即,在一些情况下结合地存在且在其他情况下未结合地存在的要素。使用“和/或”列出的多个要素应以相同方式解释,亦即,如此结合的要素的“一或多者”。可任选地存在除了藉由“和/或”语句所确切地鉴别的要素以外的其他要素,而无论与确切地鉴别的所述要素相关抑或不相关。因此,作为非限制性实例,指代“A和/或B”在结合诸如“包含”等开放式措辞使用时,在一个实施例中,可仅指A(任选地包括除了B以外的要素);在另一实施例中,可仅指B(任选地包括除了A以外的要素);在另一实施例中,可指A及B两者(任选地包括其他要素);等。
如在本说明书及权利要求书中所用,“或”应理解为具有与上文所定义的“和/或”相同的含义。举例而言,当分隔列表中的项目时,“或”或“和/或”应被解释为包括性的,亦即,包括一些或一系列要素中的至少一个而且包括多于一个,及(任选地)其他未列出的项目。只有指示截然相反的术语,诸如“中的仅一者”或“中的恰好一者”或当用于权利要求书中时“由……组成”将指包括一些或一列要素中的恰好一个要素。一般而言,当置于排他性术语,诸如“任一者”、“中的一者”、“中的仅一者”或“中的恰好一者”的前时,如本文中所使用的术语“或”应仅解释为表明排他性替代方式(亦即“一者或另一者但非二者皆”)。当用于权利要求书中时,“主要由……组成”应具有如其在专利法律领域中所使用的普通含义。
如本说明书及权利要求书中所用,关于一系列一或多个要素的词组“至少一个”应被理解为意指由该系列要素中的要素的任何一或多个中选出的至少一个要素,但未必包括该系列要素内具体列出的各个及每个要素中的至少一者,且未必排除该系列要素中的要素的任何组合。此定义亦允许可任选地存在除词组“至少一个”所指的该系列要素内具体鉴别的要素以外的要素,而无论与具体鉴别的所述要素相关抑或不相关。由此,作为非限制性实例,“至少一个A及B”或等效地“至少一个A或B”或,等效地“至少一个A和/或B”)可在一个实施例中指至少一个(任选地包括超过一个)A而不存在B(且任选地包括除B以外的要素);在另一实施例中,指至少一个(任选地包括超过一个)B而不存在A(且任选地包括除A以外的要素);在又一实施例中,指至少一个(任选地包括超过一个)A及至少一个(任选地包括超过一个)B(且任选地包括其他要素);等。
亦应理解除非截然相反地指示,否则在本文中所主张的包括超过一个步骤或操作的任何方法中,该方法的步骤或操作的顺序并非必需限制于列举该方法的步骤或操作的顺序。
在权利要求书中以及在上述说明书中,所有过渡词组,诸如“包含”、“包括”、“带有”、“具有”、“含有”、“涉及”、“容纳”及类似词组的应理解为开放的,亦即,意谓包括但不限于。仅过渡词组“由……组成”及“基本上由……组成”应分别为封闭或半封闭过渡词组,如美国专利局手册专利考察程序(United States Patent Office Manual of Patent Examining Procedures)第2111.03节中所阐述。应了解,在替代实施例中,此文件中使用开放式过渡词组(例如“包含”)描述的实施例亦涵盖了如“由……组成”及“基本上由……组成”由开放式过渡词组描述的特性。举例而言,若本发明描述“包含A及B的组合物”,则本发明亦涵盖替代实施例“由A及B组成的组合物”及“基本上由A及B组成的组合物”。
- 还没有人留言评论。精彩留言会获得点赞!