一种n-B18H22与环糊精的包合物的制备方法及应用与流程
本发明涉及包化学材料制备技术领域,具体涉及一种n-b18h22与环糊精的包合物的制备方法及应用。
背景技术:
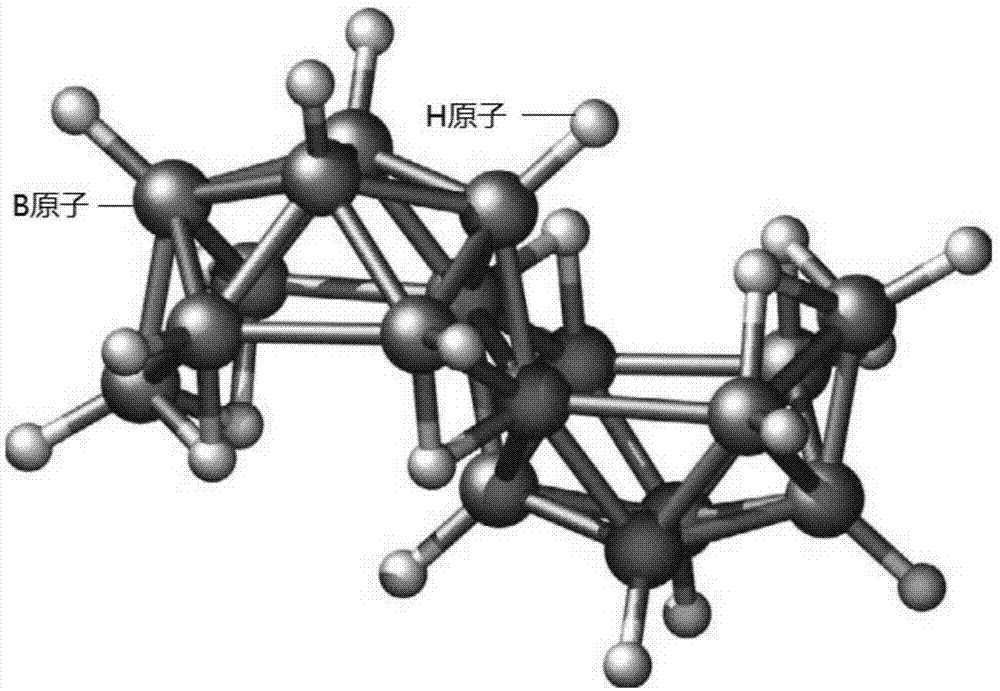
1912年,德国化学家stock在制备过程中运用真空技术合成了丁硼烷,为硼烷化学的发展奠定了基础。由于硼烷材料的特殊物理化学性质,越来越多的科研人员投入到新型功能硼烷材料的制备和性能方面的研究。近年来十八硼烷作为一种新型结构的硼烷材料受到了很多关注。十八硼烷有两种同分异构体,分别是n-b18h22和i-b18h22,因它们独特的对称结构(图1)和高硼含量使得其在医学和新材料方面有很多潜在的应用。2015年2月,捷克科学家与西班牙科学家合作,他们采用λ=337.1nm的氮气激光器激发n-b18h22的环己烷溶液时发现其在λ=406nm处辐射一种高效并抗激光的光源,继而首次开发出基于n-b18h22的硼烷激光,由此奠定了这种新材料成为未来更加环境友好和更加经济的现代激光的基础。此后,有关n-b18h22的研究受到越来越多的重视。
n-b18h22是所有硼烷材料中唯一具有荧光的物质。基于n-b18h22的这一性质,其在光电材料、医学及材料处理等方面有着巨大的应用潜力。但n-b18h22在水溶液里的溶解度较小且较易水解,性质不稳定,严重影响其在水溶液中的性质研究和相关应用。
技术实现要素:
鉴于此,有必要针对上述问题提供一种n-b18h22与环糊精的包合物的制备方法及应用。
本发明是通过以下技术方案实现的:
一种n-b18h22与环糊精的包合物的制备方法,包括:
1)分别称取n-b18h22和环糊精;
2)用溶剂将n-b18h22溶解,获得n-b18h22溶液;
3)配制环糊精的饱和水溶液;饱和溶液提高了环糊精溶解度,提高了n-b18h22包合率;水溶液使n-b18h22和环糊精更充分地混合、作用;
4)将步骤2)制得的n-b18h22的乙腈溶液加入环糊精的饱和溶液里搅拌至均匀,冷藏12h,有浑浊黄色固体出现;将真空中干燥,即得到包合产物。
进一步的,所述步骤1)中,称取的n-b18h22和环糊精的摩尔比为1:1。
进一步的,所述步骤2)中的溶剂为乙晴、无水乙醇等;优选乙晴。
进一步的,所述步骤2),用乙晴将n-b18h22完全溶解即可,优选使用每10ml的乙腈溶解0.0388g的n-b18h22。
进一步的,步骤4)的操作包括:将n-b18h22的乙腈溶液缓慢滴入(混合均匀即可,优选2ml/min)环糊精的饱和溶液里搅拌至均匀,冷藏(4-8℃,优选4℃)12h(结晶完全的最佳时间),有浑浊黄色固体出现;将其在真空中抽滤干燥,最后得到包合产物。
进一步的,所述环糊精包括β-环糊精或γ-环糊精。
一种n-b18h22与环糊精的包合物在水溶液中转移、荧光标记和相关反应(如制备其衍生物)等方面的应用。
本发明有益效果:
发明人采用荧光光谱学方法初步研究了n-b18h22的水解反应动力学及其影响因素,基于这些研究,本发明提出了利用环糊精构建β-cd-n-b18h22包合物以抑制n-b18h22在水中的水解,提高其在水溶液中的稳定性,为进一步开展n-b18h22的性能和应用研究打下良好的基础。
β-环糊精(β-cyclodextrin,简称β-cd)是由7个葡萄糖基本单元在α-1,4-糖苷键的作用下形成的筒状结构(图2),具有内部疏水和外部亲水的性质,与本发明中的n-b18h22形成的包合物中,客体n-b18h22和环糊精之间以氢键或者分子间作用力结合在一起,客体分子在形成包合物前后物理和化学性质都会发生较大的变化。
本发明包合物后续应用中可直接应用,也可解离后再应用,操作方便。
采用饱和水溶液法首次制备了n-b18h22-β-环糊精(β-cd)超分子包合物。运用等摩尔连续变化法证明两者形成了摩尔比为1:1的包合物。通过tg、ftir、xrd和sem多种手段对包合物进行了表征。同时,采用荧光光谱技术研究了形成包合物对n-b18h22在水溶液中稳定性的影响,结果表明和β-cd形成包合物抑制了n-b18h22的水解,其在水溶液中的稳定性大为提高。且β-cd在波长200-500nm处无吸收,β-cd和n-b18h22共存时,不会干扰n-b18h22的吸光。本发明为n-b18h22在水溶液中的研究和应用开辟了一条新的途径。
附图说明
图1为n-b18h22的结构示意图。
图2为β-cd结构示意图。
图3为n-b18h22乙腈溶液中的紫外吸收光谱。
图4为吸光度-浓度曲线。
图5为△a~n-b18h22的摩尔分数曲线。
图6为热重分析曲线:a曲线为n-b18h22,b曲线为β-cd,c曲线为n-b18h22/β-cd包合物,d曲线为物理混合。
图7为红外光谱图(a表示n-b18h22,b表示β-cd,c表示物理混合,d表示包合物)。
图8为xrd分析图(a表示n-b18h22,b表示β-cd,c表示包合物)。
图9为sem图谱:9a表示n-b18h22,9b表示β-cd,9c表示物理混合,9d表示包合物。
图10为n-b18h22水溶液荧光强度随时间的变化,其中,图10a为ph=7.08时n-b18h22包合物水溶液荧光强度随时间变化图,10b为ph=9.63时n-b18h22包合物水溶液荧光强度随时间变化图,10c为ph=11.49时n-b18h22包合物水溶液荧光强度随时间变化图,10d为n-b18h22水溶液荧光强度随时间变化图;10a、10b、10c均为包合后,10d为包合前。
具体实施方式
为了更好的说明本发明技术方案所要解决的问题、采用的技术方案和达到的有益效果,现结合具体实施方式进一步阐述。值得说明的是,本发明技术方案包含但不限于以下实施方式。
本发明实施例中未注明具体技术或条件的,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购等途径获得的常规产品。
实施例1n-b18h22与环糊精包合物的制备方法
1、本发明制备方法包括以下步骤:
1)分别称n-b18h22和环糊精;称取的n-b18h22和环糊精的摩尔比为1:1;
2)用溶剂将n-b18h22溶解,获得n-b18h22溶液;
3)配制环糊精的饱和水溶液;
4)将步骤2)制得的n-b18h22溶液加入环糊精的饱和溶液里搅拌至均匀,冷藏12h,有浑浊黄色固体出现;将真空中干燥,即得到包合产物。
在一些实施例中,步骤1)中,所述环糊精包括β-环糊精或γ-环糊精。
在一些实施例中,步骤2)中,溶剂选用乙晴。
在一些实施例中,步骤2)中,乙晴和n-b18h22的用量为:每10ml的乙腈溶解0.0388g的n-b18h22。
在一些实施例中,步骤4)中,将n-b18h22的乙腈溶液滴入环糊精的饱和溶液中的加入速度优选为2ml/min。
2、实验部分
2.1仪器与试剂
超声波清洗器(昆山市超声仪器有限公司),电子天平(0.1mg,北京赛多利斯仪器系统公司),超纯水仪(英国elga),比色皿(东西仪科技有限公司),集热式恒温加热磁力搅拌器(邦西仪器)。
pl分析:采用f-4600荧光光谱仪(日本hitachi公司),实验条件:激发波长360nm,扫描电压700v,扫描间隔0.5nm,扫描速度1500nm·min-1,激发狭缝10.0nm,发射狭缝10.0nm,采用四通比色皿,
tg分析:采用tga8000热重分析仪(perkinelmer),称取药品2mg放于吊篮坩埚中,采用n2做保护气体,流量100ml/min。温度范围30℃~600℃,升温速率10℃/min。
uv/vis分析:紫外-可见光谱测定采用岛津uv-2400型紫外-可见分光光度计,溶剂及参比为去离子水,溶液浓度为10-4数量级,比色槽光程为1cm。
xrd分析:采用x射线粉末衍射仪(德国brukerd8advance)。测试条件:cu靶,电压40kv,电流为100ma,扫描速率为5o/min。
主要试剂:β-环糊精(上海化学试剂公司出品),n-b18h22(实验室自制,制备方法参考文献:
(1)cerdán,l.,braborec,j.,garciamoreno,i.,costela,a.,londesborough,m.g.:aboranelaser.naturecommunications.2015,6(6):5958
(2)graybillbm,ruffjk,hawthornemf.anovelsynthesisofthetriborohydrideanion,-b3h8[j].journaloftheamericanchemicalsociety,2002,83(12):2669.
(3)liy,sneddonlg.improvedsyntheticrouteton-b18h22[j].cheminform,2006,45(2):470.);
乙腈和其它试剂都是分析纯,实验用水为去离子水。
2.2包合物的制备
经实验后得到如下制备步骤:按摩尔比1:1称取n-b18h22和β-cd;n-b18h22放入圆底烧瓶,并加入乙腈超声(常温下超声30min加速溶解)使得n-b18h22溶解。将准确称量β-cd放入圆底烧瓶,并加入适量的去离子水,之后将圆底烧瓶置于磁力搅拌器上,配置β-cd的饱和水溶液。将n-b18h22的乙腈溶液缓慢滴入β-cd的饱和溶液里搅拌至均匀,置冰箱冷藏12h,烧瓶底部有浑浊黄色固体出现。最后将其在真空中抽滤干燥,最后得到包合产物。
2.3标准曲线的测定
称取适量的n-b18h22溶解在乙腈溶液里,配置一系列浓度(0.004mol/l、0.005mol/l、0.006mol/l、0.007mol/l、0.009mol/l、0.010mol/l)的n-b18h22溶液,进行紫外扫描。结果见图3,吸收曲线在280和363nm处出现两个吸收峰,实验发现n-b18h22形成包合物后,其最大吸收波长并没有发生位移。取363nm处吸光度值与浓度拟合(图4)得出相应的线性回归方程:
c(mol·l-1)=170.43a-0.07r2=0.982
其中,c为浓度(mol/l);a为吸光度;r2为确定系数。
3、结果与分析
3.1包合物产率的测定
称量0.0388g的n-b18h22和0.185g的β-cd按优化后的制备步骤制备得到0.120g包合产物,根据下式计算得到包合物的包和产率:
包合物产率(%)=m(包合物)/[m(环糊精)+m(十八硼烷)]=53%
其中,m表示质量。
3.2等摩尔连续变化法确定最佳包合比
采用等摩尔连续变化法确定最佳包合比,在λmax处测定溶液的吸光度。固定[n-b18h22]+[β-cd]=2.0×10-4mol·l-1,改变n-b18h22与β-cd的浓度比,以加入β-cd前后n-b18h22吸光度的变化值δa对n-b18h22的摩尔分数变化作图。结果如图5所示,δa最大值对应的[n-b18h22]/[n-b18h22]+[β-cd](mol·l-1)为0.5,据此可以确定n-b18h22与β-cd的包合比为1:1。本发明中n-b18h22是一化合物,β-环糊精的空腔直径和n-b18h22的分子直径相近,即一个β-环糊精分子的空腔只可容纳一个n-b18h22分子。
3.3n-b18h22包合率的测定
在优化条件下,精确称量包合物0.0216g置于烧瓶中,加入10ml的乙腈溶液使其完全溶解,在λmax=363nm波长处测定溶液的吸光度(β-cd在200-500nm处无吸收,对n-b18h22的吸收无干扰),代入回归方程计算n-b18h22的浓度,这样可得到包合物中的n-b18h22含量,进而计算得到n-b18h22的包合率:
包合率(%)=m(包合物中的十八硼烷)/m(十八硼烷)=0.0130/0.0388=33.57%
3.4n-b18h22包合物的形貌和性能表征
3.4.1热重分析
通过热重(tg)分析对n-b18h22包合前后的热力学性质的改变进行了研究。图6为n-b18h22包合前后的tg曲线。包合前,n-b18h22在167℃开始分解(曲线a),包合后的分解温度达到261.6℃,说明包合之后,热力学性质发生了改变,热稳定性得到提高。
3.4.2红外光谱测定
采用kbr压片方法,将kbr提前在红外快速干燥器里干燥6h,去除水分。按质量100:1(kbr:样品)分别称取100mgkbr4份,样品1mg混合后充分研磨,使得药品混合均匀,然后压成圆形薄片进行光谱扫描,扫描波数范围500~4000cm-1。
理论分析结果表明,如果n-b18h22与β-cd发生超分子作用并形成包结物时,则包结物的红外光谱图不再是两种物质的简单叠加。各物质的红外光谱见图7。其中图(a)、(b)分别是n-b18h22和β-cd的红外光谱;图(c)为二者机械混合物的红外光谱,图(d)为n-b18h22-β-cd包合物的红外谱图。n-b18h22(1105、1410和826cm-1)的吸收谱带在机械混合物中全部都明显存在,只是叠加了β-cd的某些吸收峰。但包合物谱图(d)中,这些峰的峰强度明显减弱了,这是由于n-b18h22和β-cd产生了超分子作用,n-b18h22进入了β-cd的疏水空腔,微环境的改变使n-b18h22的峰形变宽,峰强度减弱,β-cd的吸收峰就将其部分包含。所以实验结果与理论预测一致,充分证明了n-b18h22-β-cd包合物的形成。
3.4.3xrd测定
采用x射线粉末衍射仪(德国brukerd8advance)对n-b18h22、β-cd以及它们的包合物进行扫描分析。结果见图8,从图中可以看出n-b18h22呈现典型的晶体结构,包合物谱图不是n-b18h22和β-cd二者谱图的简单叠加,它有自己的晶体特征衍射峰。当n-b18h22与β-cd作用形成包合物后,其原来的晶体特征峰消失,出现新的属于n-b18h22-β-cd包合物的衍射峰,说明n-b18h22形成包合物后形成新的晶相,通过弱相互作用结合起来的超分子包合物有着与单一的客体不同的晶体结构。xrd实验结果进一步证明了包合物的形成。
3.4.4sem分析
通过扫面电子显微镜对样品的表面形貌进行分析,结果见图9。从图9可以看出所有样品都呈现出晶体结构。n-b18h22(9a)是有孔状结构的块状晶体,并且表现为较不规则。β-cd(9b)为规则结构,并且表面比较光滑。(9c)图明显是由两种晶体物理堆积,物理混合中β-cd粒子并未改变,只是被n-b18h22晶体覆盖。而n-b18h22-β-cd(9d)包合物中粒子形状发生了明显变化,结构更加紧密,形状更加有规则,起始物质的晶体形态基本消失,已经辨认不出n-b18h22和β-cd粒子。n-b18h22包合前后表面形态的变化进一步证明了包合物的形成。
3.4.5包合物的稳定性研究
考察了n-b18h22包和前后在水溶液中的稳定性。分别配制ph=3.27、ph=5.37、ph=7.08、ph=9.63、ph=11.49的包合物水溶液,每隔一段时间测其荧光强度的变化。采用f-4600荧光光谱仪,实验条件:激发波长360nm,扫描电压700v,扫描间隔0.5nm,扫描速度1500nm·min-1,激发狭缝10.0nm,发射狭缝10.0nm,采用四通比色皿,进行发射光谱的测量。由于酸性条件对包合物有影响,故酸性条件(ph=3.27、ph=5.37)不做考虑,图10a为ph=7.08时n-b18h22包合物水溶液荧光强度随时间变化图,10b为ph=9.63时n-b18h22包合物水溶液荧光强度随时间变化图,10c为ph=11.49时n-b18h22包合物水溶液荧光强度随时间变化图,10d为n-b18h22水溶液荧光强度随时间变化图。从图中可以看出,形成包合物后,n-b18h22在酸碱水溶液的荧光强度几乎没有发生变化,峰位也没有发生移动(λem=415nm)。而由(d)图形成包合物前的n-b18h22在水中容易发生分解,在水溶液中9h后荧光强度很弱,相反的,n-b18h22的包合物在水溶液里很稳定,9h内几乎不发生分解。这是由于形成包合物后n-b18h22与β-cd之间存在着分子间作用力,提高了n-b18h22在水溶液中的稳定性;另一方面,形成包合物后,β-cd的腔体屏蔽了外围环境对n-b18h22分子的影响,使得包合物中的n-b18h22稳定性增大。从图6中的热重分析也可看出,包合物分解温度升高,同样证明了包合物的稳定性增强。
在初步实验的基础上,运用饱和水溶液法成功制备了化学计量比为1:1的n-b18h22-β-cd超分子包合物,优化了制备工艺。应用紫外-可见分光光度计得到包合物的吸光度值,进而计算出n-b18h22-β-cd包合物的包合比和包合率。tg、ftir、xrd和sem等表征手段证明了包合物的形成。对比研究表明,客体n-b18h22分子形成包合物后,其在水溶液中的稳定性明显增强,这为扩展n-b18h22在水溶液中的应用研究开辟了一条重要途径。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!