A′-π-A-π-A′型有机小分子及其制备方法与应用与流程
本发明涉及太阳能电池技术领域,特别涉及基于噻吩并[2′,3′:5.6]吡啶并[3,4-g]噻吩并[3,2-c]-异喹啉-5,11(4h,10h)-二酮(简称tpti)结构单元的a′-π-a-π-a′型有机小分子及其制备方法与应用。
背景技术:
有机小分子太阳能电池是一种基于有机小分子的利用光生伏特效应直接实现把太阳能转换为电能的装置。其具有质量轻、价格便宜、制备工艺简单、材料的化学结构可调控性好等优点,在未来的应用上有明显的优势。自上世纪90年代以来,经过近三十年的不懈努力,有机太阳能电池的能量转换效率(pce)稳步提高,显示出广阔的应用和研发前景。目前,基于引达省单元的受体-给体-受体(a-d-a)型有机小分子叠层太阳能电池的pce已经超过17%(mengl,zhangy,wanx,etal.organicandsolution-processedtandemsolarcellswith17.3%efficiency.science,2018,361,1094-1098)。而基于小分子给体材料的有机太阳能电池的pce也已经超过10%(zhangh,liuy,suny,etal.developinghigh-performancesmallmoleculeorganicsolarcellsviaalargeplanarstructureandanelectron-withdrawingcentralunit.chemicalcommunications,2016,53,451-454)。但是有机小分子太阳能电池目前仍然存在载流子迁移率低、合成步骤复杂和稳定性较差等问题,需要开发新的光电性能优异的有机小分子给体材料。
噻吩并[2′,3′:5.6]吡啶并[3,4-g]噻吩并[3,2-c]-异喹啉-5,11(4h,10h)-二酮(tpti)是一个含有酰胺键的共轭五环稠环体系,具有良好的平面性和弱吸电子性能。以含tpti单元的共轭聚合物为给体,富勒烯衍生物(如pcbm)为受体构筑的本体异质结有机太阳能电池显示出良好的光伏性能,其pce已经超过8%(caoj,chens,qiz,etal.anefficientselenophene-containingconjugatedcopolymerfororganicsolarcells.rscadvances,2014,4,5085-5087),这表明tpti单元在构筑高效有机太阳能电池材料方面有较大的开发潜力。然而,目前基于tpti单元的有机小分子太阳能电池给体材料还少有报道,尤其是以弱吸电子的tpti单元为中心核(a),吸电子单元(如1.3-茚满二酮或3-乙基绕丹宁等)为末端(a′),芳杂环类单元为π共轭桥的a′-π-a-π-a′型有机小分子给体材料及其制备方法与光伏应用还尚未见报道。
技术实现要素:
本发明要解决的技术问题是克服现有技术中针对tpti类有机小分子太阳能电池材料种类少,应用领域窄等不足,提供一种基于tpti的a′-π-a-π-a′型有机小分子,通过改变π桥和不同吸电子末端(a′)能够实现对小分子结构、吸收光谱、带隙、前线分子轨道能级等光电性能的调控,达到制备出优异光电性能的小分子光电功能材料的目的。其制备方法简回收率高,可应用于制备太阳能电池。
为解决上述技术问题,本发明提供了一种a′-π-a-π-a′型有机小分子,所述a′-π-a-π-a′型有机小分子具有以下式i的结构式:
所述式i中:r选自以下基团中的任意一种:
r1选自以下基团中的任意一种:-c6h13、-c8h17、-c12h25、-c16h33、
a′选自以下基团中的任意一种:
做为一个总的技术构思,本发明还提供了一种上述的a′-π-a-π-a′型有机小分子的制备方法,所述的a′-π-a-π-a′型有机小分子由中间体m1和a′在溶剂和催化剂的作用下,进行knoevenagel缩合反应得到,所述中间体m1具有以下式iii的结构式:
所述式iii中:r选自以下基团中的任意一种:
r1选自以下基团中的任意一种:-c6h13、-c8h17、-c12h25、-c16h33、
上述的制备方法,优选的,所述中间体m1和a′的摩尔比1︰3~4。
上述的制备方法,优选的,所述催化剂与所述中间体m1的摩尔比为11~14︰1。
上述的制备方法,优选的,所述催化剂为吡啶、哌啶和三乙胺中的一种。
上述的制备方法,优选的,所述溶剂为三氯甲烷、乙腈中的一种。
上述的制备方法,优选的,所述中间体m1采用以下方法制备得到:
s1-1、将化合物1与化合物2反应得到化合物3;
s1-2、将化合物3、醋酸钯,碳酸铯,三环己基磷氟硼酸盐和n,n-二甲基乙酰胺(dmf)加热反应得到化合物4;
s1-3、将化合物4与溴代琥珀酰亚胺(nbs)进行避光反应得到化合物5;
s1-4、将化合物5、3-烷基噻吩锡试剂和四三苯基磷钯混合,加热反应得到化合物6;
s1-5、将化合物6、n,n-二甲基乙酰胺和pocl3反应得到中间体m1;
所述化合物1为
所述化合物2为
所述化合物3为:
所述化合物4为:
所述化合物5为:
所述化合物6为:
中间体m1的反应路线为:
上述的制备方法,优选的,所述s1-1中,所述化合物1和化合物2的摩尔比为2~3︰1。
上述的制备方法,优选的,所述s1-2中,所述化合物3、醋酸钯、碳酸铯和三环己基磷氟硼酸盐的摩尔比为1︰0.6~0.8︰12~16︰1~2。
上述的制备方法,优选的,所述s1-3中,所述化合物4和nbs的摩尔比为1︰2~3。
上述的制备方法,优选的,所述s1-4中,所述化合物5、3-烷基噻吩锡和四三苯基磷钯的摩尔比为1︰3~4︰0.04~0.06。
上述的制备方法,优选的,所述s1-5中,所述化合物6、dmf和pocl3的摩尔比为1︰2~3︰3~5。
做为一个总的技术构思,本发明还提供了一种a′-π-a-π-a′型有机小分子,所述a′-π-a-π-a′型有机小分子具有以下式ii的结构式:
所述式ii中:r选自以下基团中的任意一种:
r1选自以下基团中的任意一种:-c6h13、-c8h17、-c12h25、-c16h33、
a′选自以下基团中的任意一种:
做为一个总的技术构思,本发明还提供了一种上述的a′-π-a-π-a′型有机小分子的制备方法,所述的a′-π-a-π-a′型有机小分子由中间体m2和中间体m3在溶剂和催化剂的作用下进行stille偶联反应得到;
所述中间体m2具有以下示iv的结构式:
所述中间体m3具有以下式v的结构式:
上述的制备方法,优选的,所述中间体m2采用以下方法制备得到:
s2-1、将化合物4、四氢呋喃(thf)和二异丙基氨基锂(lda)在-78℃进行反应,
s2-2、继续添加三甲基氯化锡(me3sncl)在室温下进行反应得到中间体m2,
所述化合物4为:
中间体m2的反应路线为:
上述的制备方法,优选的,所述中间体m3采用以下方法制备得到:
s3-1、将化合物7和a′在溶剂和催化剂的作用下,加热反应得到化合物m3;
所述化合物7为
中间体m3的反应路线为:
上述的制备方法,优选的,所述催化剂为四三苯基磷钯。
上述的制备方法,优选的,所述溶剂为甲苯或氯苯。
上述的制备方法,优选的,所述中间体m2和中间体m3的摩尔比为1︰2~3。
上述的制备方法,优选的,所述催化剂与中间体m2的摩尔比为0.02~0.05︰1。
上述的制备方法,优选的,所述s2-2中,所述化合物4、lda和me3sncl的摩尔比为1︰2~3︰3~5。
上述的制备方法,优选的,所述s3-1中,所述化合物7和a′的摩尔比为1︰2~4。
做为一个总的技术构思,本发明还提供了一种上述的a′-π-a-π-a′型有机小分子在制备太阳能电池中的应用。
上述的应用,优选的,所述应用方法为:
(1)在阳极上旋涂一层pedot︰pss聚合物导电膜;
(2)再旋涂一层a′-π-a-π-a′型有机小分子和pc71bm共混而成的光活性层;
(3)真空蒸镀金属钙作为阴极修饰层;
(4)蒸镀阴极金属铝,得到太阳能电池。
与现有技术相比,本发明的优点在于:
(1)本发明提供了一种基于tpti的具有a′-π-a-π-a′构型的小分子,通过改变π桥和不同吸电子末端(a′)能够实现对小分子结构、吸收光谱、带隙、前线分子轨道能级等光电性能的调控,达到制备出优异光电性能的小分子光电功能材料的目的。
(2)本发明提供了一种基于tpti的具有a′-π-a-π-a′构型的小分子,具有可调控的吸收光谱(300-900nm)。同时具有良好的热稳定性,还拥有高的开路电压,这有利于获得高效的器件。
(3)本发明提供了一种基于tpti的具有a′-π-a-π-a′构型的小分子的制备方法,合成路线具有原料供应广泛和合成简单高效等优点,另外此方法具有很高的推广性,而且重复性非常好。
(4)本发明提供了一种基于tpti的具有a′-π-a-π-a′构型的小分子在制备太阳能电池中的应用,以具有a′-π-a-π-a′构型的小分子为给体相材料与受体相材料(pc71bm)构筑的本体异质结型有机小分子太阳能电池,通过调节给受体比例、添加剂等手段优化光伏性能,获得的能量转换效率(pce)达到3.82%,相应的开路电压(voc)达到1.04v,短路电流(jsc)达到7.04ma/cm2,填充因子(ff)达到52.17%。该结果是tpti类小分子材料在有机太阳能电池方面的首次尝试,说明该类材料在有机光电功能材料,尤其是有机太阳能电池材料方面具有潜在的研发和应用前景。
附图说明
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整的描述。
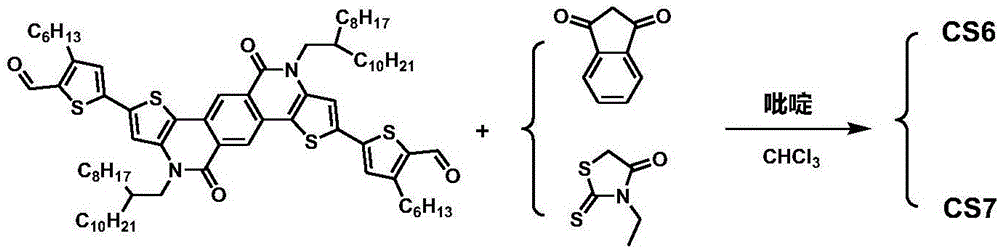
图1为本发明实施例1和实施例2中cs6、cs7的合成路线图。
图2为本发明实施例3和实施例4中cs8、cs9的合成路线图。
图3为本发明实验例中cs6、cs7、cs8和cs9薄膜在石英片上紫外-可见吸收光谱图。
图4为本发明实验例中cs6、cs7、cs8和cs9的循环伏安曲线图。
图5为本发明实验例中太阳能电池的结构图。
图6为本发明实验例中基于cs6、cs7、cs8和cs9四个小分子制备的有机小分子太阳能电池的电流-电压特性(j-v)曲线图。
具体实施方式
以下结合说明书附图和具体优选的实施例对本发明作进一步描述,但并不因此而限制本发明的保护范围。以下所述实施例旨在便于对本发明的理解,而对其不起任何限定作用。所述方法如无特别说明均为常规方法。所述反应物料如无特别说明均能从公开商业途径购买而得。
实施例1:
一种基于tpti单元的a′-π-a-π-a′型小分子cs6,以弱吸电子的tpti单元为中心核a,3-己基噻吩为π共轭桥,1,3-茚满二酮为吸电子末端a′。
cs6具有式ⅰ的结构通式:
其中,r为2-辛基十二烷基,r1为正己基,a′为1,3-茚满二酮。
cs6具体的化学结构式为:
一种本实施例的cs6的制备方法,合成路线参见图1,具体制备方法包括以下步骤:
(1)2,5-二溴-n1,n4-双(2-辛基十二烷基)-n1,n4-二(噻吩-3-基)对苯二甲酰胺(化合物3)的合成。
1.1、氩气氛围下,在250ml的三口瓶中,加入11.6g(30.56mmol)n-(2-辛基十二烷基)噻吩-3-胺(化合物1),5ml三乙胺和40ml干燥的二氯甲烷。
1.2、取5g(13.89mmol)2,5-二溴对苯二甲酰二氯(化合物2)用40ml干燥的二氯甲烷溶解得到混合溶液。
1.3、冰浴下,将步骤1.2的混合溶液缓慢滴加至步骤1.1的三口瓶中,滴加完毕,升至室温反应过夜。
1.4、加水淬灭反应,二氯甲烷萃取获得有机相,将有机相用无水硫酸镁干燥,过滤,旋除溶剂得到粗产品。
1.5、将粗产品用柱层析分离纯化(洗脱剂:二氯甲烷),得到黄色固体8.72g,即为2,5-二溴-n1,n4-双(2-辛基十二烷基)-n1,n4-二(噻吩-3-基)对苯二甲酰胺,产率60%(化合物3)。该化合物的结构表征数据如下:
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):7.13(dd,j=5.1,3.2hz,2h),7.09(s,2h),6.85(br,2h),6.76(dd,j=5.1,1.2hz,2h),3.75(br,4h),1.57-1.52(m,2h),1.29-1.24(m,64h),0.90-0.85(m,12h)。
从核磁共振氢谱可知,该化合物结构正确,为2,5-二溴-n1,n4-双(2-辛基十二烷基)-n1,n4-二(噻吩-3-基)对苯二甲酰胺(化合物3)。
(2)4,10-双(2-辛基十二烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮(化合物4)的合成。
2.1、氩气氛围下,在250ml的三口瓶中,加入8g化合物3(7.64mmol),1.3g醋酸钯(5.85mmol),37g碳酸铯(113.57mmol),3.46g三环己基磷氟硼酸盐(9.42mmol)和150mln,n-二甲基乙酰胺。升温至120℃,反应24小时。
2.2、冷却至室温,加水淬灭反应,用三氯甲烷萃取获得有机相。将有机相用无水硫酸镁干燥,过滤,旋除溶剂得到粗产品。
2.3、将粗产品用柱层析分离纯化(洗脱剂:石油醚︰二氯甲烷=10︰1),得到黄色固体4.25g,即为4,10-双(2-辛基十二烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮(化合物4),产率63%。该化合物的结构表征数据如下:
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):8.88(s,2h),7.49(d,j=5.4hz,2h),7.10(d,j=5.5hz,2h),4.24(s,4h),2.04(s,2h),1.56(s,6h),1.22(s,58h),0.85(m,12h)。
核磁共振碳谱:13cnmr(100mhz,cdcl3,δ/ppm):161.64,139.47,130.04,126.86,126.12,123.67,117.97,117.77,77.32,77.00,76.68,49.74,37.13,31.89,31.85,31.67,29.96,29.60,29.56,29.51,29.31,29.25,26.67,22.66,14.08。
质谱:ms(maldi-tof,m/z)c56h88n2o2s2:理论值885.450;实测值885.776。
由上可知,该化合物结构正确,为化合物4,10-双(2-辛基十二烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮(化合物4)。
(3)2,8-二溴-4,10-二(2-辛基十二烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮(化合物5)的合成
3.1、在250ml三口瓶中,加入4.42g化合物4(5mmol)和120ml三氯甲烷。
3.2、将2.23gnbs(12.5mmol)溶解在30mldmf中得到混合溶液。
3.3、将步骤3.2中的混合溶液缓慢的滴加至步骤3.1的三口瓶中,室温避光反应过夜。
3.4、加水淬灭反应,三氯甲烷萃取有机相。将有机相用无水硫酸镁干燥,过滤,旋出溶剂获得粗产品。
3.5、将粗产品用柱层析分离纯化(洗脱剂:石油醚︰二氯甲烷=15︰1),得到黄色固体4.79g,即为2,8-二溴-4,10-二(2-辛基十二烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮(化合物5),产率92%。该化合物的结构表征数据如下:
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):8.70(s,2h),7.07(s,2h),4.16(s,4h),1.98(s,2h),1.58(s,6h),1.29(d,j=5.5hz,58h),0.86(dd,j=12.1,6.5hz,12h).
核磁共振碳谱:13cnmr(100mhz,cdcl3,δ/ppm):161.15,138.87,129.39,126.88,123.43,120.90,118.84,115.14,77.32,77.20,77.00,76.68,49.78,36.99,31.90,31.86,31.52,29.95,29.61,29.56,29.51,29.32,29.26,26.54,22.67,22.64,14.10,14.08.
质谱:ms(maldi-tof,m/z)c56h86br2n2o2s2:理论值1043.240;实测值1043.737。
由上可知,该化合物结构正确,为化合物2,8-二溴-4,10-二(2-辛基十二烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮(化合物5)。
(4)2,8-双(4-己基噻吩-2-基)-4,10-双(2-辛基十二烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮(化合物6)的合成
4.1、氩气氛围下,在100ml的三口瓶中,加入4.17g化合物5(4mmol),9g3-己基噻吩锡试剂(16mmol),230mg四三苯基磷钯(0.2mmol)和40ml甲苯。升温至120℃,反应24小时。
4.2、冷却至室温,二氯甲烷萃取获得有机相,将有机相用无水硫酸镁干燥,过滤,旋除溶剂得到粗产品。
4.3、将粗产品通过柱层析分离纯化(洗脱剂:石油醚︰二氯甲烷=2︰1),得到3.89g黄色固体,即为2,8-双(4-己基噻吩-2-基)-4,10-双(2-辛基十二烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮(化合物6),产率80%。该化合物的结构表征数据如下:
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):8.74(s,2h),7.14(s,2h),7.07(s,2h),6.92(s,2h),4.21(s,4h),2.63(t,j=7.7hz,4h),2.03(s,2h),1.64(d,j=7.7hz,4h),1.58(s,2h),1.37-1.21(m,72h),0.94-0.84(m,20h)。
核磁共振碳谱:13cnmr(100mhz,cdcl3,δ/ppm):161.46,144.67,139.56,137.99,136.18,129.58,126.80,126.23,123.46,120.49,116.42,113.22,77.32,77.00,76.68,49.47,37.03,31.90,31.88,31.66,30.49,30.37,29.97,29.62,29.56,29.34,29.28,29.00,27.83,26.84,26.69,22.67,22.62,17.51,14.10,13.59。
质谱:ms(maldi-tof,m/z)c76h116n2o2s4:理论值1218.020;实测值1218.325。
由上可知,该化合物结构正确,为2,8-双(4-己基噻吩-2-基)-4,10-双(2-辛基十二烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮(化合物6)。
(5)5,5'-(4,10-双(2-辛基十二烷基)-5,11-二氧代4,5,10,11四氢噻吩[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-2,8-二基)双(3-己基噻吩-2-甲醛)(中间体m1)的合成。
5.1、氩气氛围下,在250ml的三口瓶中,加入4.44g化合物6(3.65mmol)和60ml1.2-二氯乙烷,在0℃温度下将1mldmf(10mmol)缓慢加入反应体系中,反应15min。
5.2、将1.82mlpocl3(13.65mmol)缓慢加入反应体系中,滴加完毕,室温反应1小时。
5.3、升温至80℃,反应24小时。
5.4、降至室温,加水淬灭反应,三氯甲烷萃取有机相,无水硫酸镁将有机相干燥,过滤,得到粗产品。
5.5、粗产品用柱层析分离纯化(洗脱剂:石油醚︰二氯甲烷=1︰1),得到红色固体2.65g,即为化合物5,5'-(4,10-双(2-辛基十二烷基)-5,11-二氧代4,5,10,11四氢噻吩[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-2,8-二基)双(3-己基噻吩-2-甲醛),产率57%。该化合物的结构表征数据如下:
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):10.02(s,2h),8.73(d,j=5.0hz,2h),7.20(s,2h),7.15(s,2h),4.21(s,4h),2.97(t,j=7.0hz,4h),2.01(s,2h),1.81-1.67(m,4h),1.58(s,2h),1.30(dd,j=60.3,15.4hz,72h),0.95-0.80(m,20h)。
核磁共振碳谱:13cnmr(100mhz,cdcl3,δ/ppm):181.39,161.02,153.79,144.40,139.87,136.95,136.11,129.50,127.47,127.04,123.79,118.50,115.32,77.32,77.00,76.68,49.61,37.03,31.88,31.85,31.58,31.54,31.43,29.98,29.63,29.60,29.53,29.32,29.29,29.03,28.60,26.61,22.65,22.64,22.56,14.08,14.05。
质谱:ms(maldi-tof,m/z)c78h116n2o4s4:理论值1274.041;实测值1274.430。
由上可知,该化合物结构正确,为中间体5,5'-(4,10-双(2-辛基十二烷基)-5,11-二氧代4,5,10,11四氢噻吩[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-2,8-二基)双(3-己基噻吩-2-甲醛)(中间体m1)。
(6)小分子cs6的合成
6.1、氩气氛围下,在100ml的三口瓶中,分别加入0.81gm1(0.63mmol),0.37g1.3-茚满二酮(2.51mmol)和60ml的三氯甲烷,搅拌均匀后加入1ml吡啶,搅拌加热至75℃,反应12小时。
6.2、反应完毕,二氯甲烷萃取,水洗,无水硫酸镁干燥,过滤得到粗产品。
6.3、将粗产品用柱层析分离纯化(洗脱剂:石油醚︰二氯甲烷=1︰3),得黑色固体0.67g,即为小分子cs6,产率71%。该小分子的结构表征数据如下:
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):8.48(s,2h),7.84(dd,j=22.5,6.4hz,6h),7.66(dd,j=13.2,6.5hz,4h),7.06(d,j=9.3hz,4h),4.18(s,4h),2.84(t,j=7.4hz,4h),2.00(s,2h),1.78-1.57(m,6h),1.53-1.22(m,74h),0.94(t,j=6.8hz,6h),0.80(m,12h)。
核磁共振碳谱:13cnmr(100mhz,cdcl3,δ/ppm):190.00,189.16,160.65,158.00,145.99,141.91,140.24,140.16,136.30,134.66,134.47,131.87,131.78,129.18,126.77,123.64,122.80,122.67,122.56,118.75,115.03,77.32,77.00,76.68,49.78,36.90,31.89,31.61,31.37,30.04,29.72,29.64,29.62,29.55,29.52,29.36,29.21,26.73,22.66,22.64,14.09,14.07。
质谱:ms(maldi-tof,m/z)c96h124n2o6s4:理论值1530.301;实测值1531.054。
由上可知,该产物结构正确,为结构式(1)所示基于tpti和1,3-茚满二酮的小分子cs6,其中,r为2-辛基十二烷基,r1为正己基,a′为1,3-茚满二酮。
一种本实施例的小分子cs6在制备有机太阳能电池中的应用,上述制备所得的小分子cs6用于有机太阳能电池中作为给体材料,与受体相材料一起构筑本体异质结型有机太阳能电池,该电池的结构如图5所示,为ito/pedot︰pss/光活性层/ca/al,其光活性层由结构式ⅰ所述小分子cs6和pc71bm共混构成。
具体的太阳能电池的制备方法为:
(1)阳极采用氧化铟锡导电玻璃(ito),在上面旋涂一层阳极修饰层pedot︰pss聚合物导电膜,150℃处理15分钟。
(2)旋涂一层由小分子cs6和受体材料pc71bm共混而成的光活性层(cs6︰pc71bm重量比为1︰1,重量比在1︰0.5~2之间均可实施)。
(3)干燥半小时后真空蒸镀金属钙(约20nm)作为阴极修饰层。
(4)最后蒸镀阴极金属铝(约100nm),通过掩膜版控制所镀金属的面积(约4mm2)。
该有机太阳能电池的光伏性能在模拟太阳光下(am1.5g,100mw/cm2)通过keithley2602表源等进行测试。
实施例2:
一种基于tpti单元的a′-π-a-π-a′型小分子cs7,以弱吸电子的tpti单元为中心核a,3-己基噻吩为π共轭桥,3-乙基绕丹宁为吸电子末端a′。
cs7具有式ⅰ的结构通式:
其中,r为2-辛基十二烷基,r1为正己基,a′为3-乙基绕丹宁,具体化学结构式如下所示:
一种本实施例的cs7的制备方法,合成路线参见图1,具体制备方法包括以下步骤:
(1)中间体m1(5,5'-(4,10-双(2-辛基十二烷基)-5,11-二氧代4,5,10,11四氢噻吩[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-2,8-二基)双(3-己基噻吩-2-甲醛))的合成:与实施例1相同。
(2)cs7的合成:以为原料,氩气氛围下,在100ml的三口瓶中,分别加入0.82g中间体m1(0.63mmol),0.40g3-乙基绕丹宁(2.51mmol),搅拌均匀后加入1ml吡啶,搅拌加热至75℃,反应12小时。反应完毕,二氯甲烷萃取,水洗,无水硫酸镁干燥,过滤得到粗产品。将粗产品用柱层析分离纯化(洗脱剂:石油醚︰二氯甲烷=1︰1),得到褐色固体0.63g,产率65%。
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):8.59(s,2h),7.85(s,2h),7.13(s,2h),7.03(s,2h),4.17(m,8h),2.80(t,j=7.8hz,4h),2.00(s,2h),1.73-1.63(m,4h),1.59(s,8h),1.40-1.21(m,70h),0.96-0.79(m,22h)。
核磁共振碳谱:13cnmr(100mhz,cdcl3.δ/ppm):191.44,167.18,160.77,151.10,142.28,139.89,135.96,132.34,129.18,127.23,126.76,123.52,122.40,120.37,117.91,114.20,77.32,77.00,76.68,49.58,39.92,37.05,31.90,31.87,31.62,31.08,29.99,29.69,29.64,29.62,29.58,29.37,29.34,29.19,29.12,26.73,22.67,22.63,14.10,12.30。
质谱:ms(maldi-tof,m/z)c88h126n4o4s8:理论值1560.480;实测值1561.074。
由上可知,该产物结构正确,为结构式i所示基于tpti和3-乙基绕丹宁的小分子cs7,其中r为2-辛基十二烷基,r1为正己基,a′为3-乙基绕丹宁。
一种本实施例的小分子cs7在制备有机太阳能电池中的应用,上述制备所得的小分子cs7用于有机太阳能电池中作为给体材料,与受体相材料一起构筑本体异质结型有机太阳能电池,该电池的结构如图5所示,为ito/pedot︰pss/光活性层/ca/al,其光活性层由结构式ⅰ所述小分子cs6和pc71bm共混构成。
具体的太阳能电池的制备方法为:
(1)阳极采用氧化铟锡导电玻璃(ito),在上面旋涂一层阳极修饰层pedot︰pss聚合物导电膜,150℃处理15分钟。
(2)旋涂一层由小分子cs6和受体材料pc71bm共混而成(cs7:pc71bm重量比为1︰1,重量比在1︰0.5~2之间均可实施)的光活性层。
(3)干燥半小时后真空蒸镀金属钙(约20nm)作为阴极修饰层。
(4)最后蒸镀阴极金属铝(约100nm),通过掩膜版控制所镀金属的面积(约4mm2)。
该有机太阳能电池的光伏性能在模拟太阳光下(am1.5g,100mw/cm2)通过keithley2602表源等进行测试。
实施例3:
一种基于tpti单元的a′-π-a-π-a′型小分子cs8:以弱吸电子的tpti单元为中心核a,3,3″-二辛基-(2,2':5',2″-三噻吩)为π共轭桥,1,3-茚满二酮为吸电子末端a′。
cs8具有式ⅱ的结构通式:
其中,r为2-辛基十二烷基,r1为正辛基,a′为1,3-茚满二酮,小分子cs8的具体化学结构式如下所示:
一种本实施例的cs8的制备方法,合成路线参见图2,具体制备方法包括以下步骤:
(1)化合物4(4,10-双(2-辛基十二烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮)的合成:与实施例1相同。
(2)4,10-双(2-辛基十二烷基)-2,8-双(三甲基锡烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮(中间体m2)的合成:
2.1、氩气氛围下,在250ml三口瓶中,加入0.95g化合物4(1.07mmol)和60ml四氢呋喃,降温至-78℃,将1.16ml二异丙基胺基锂(2.35mmol)缓慢滴加至三口瓶中,保温反应2小时。
2.2、将三甲基氯化锡加入到反应瓶中,升至室温,反应过夜。
2.3、加水淬灭反应,乙醚萃取,有机相用无水硫酸镁干燥,过滤,旋除溶剂得到粗产品。
2.4、粗产品用异丙醇重结晶,得到黄色固体1.17g,即为中间体m2,产率90%。
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):8.88(s,2h),7.10(s,2h),4.26(s,4h),2.05(s,2h),1.57(s,6h),1.30(d,j=64.6hz,58h),0.85(dd,j=11.6,6.7hz,12h),0.59-0.34(m,18h)。
核磁共振碳谱:13cnmr(100mhz,cdcl3,δ/ppm):161.79,140.72,140.20,129.64,126.33,124.67,123.96,123.34,77.32,77.20,77.00,76.68,49.50,37.21,31.89,31.89,31.77,30.00,29.62,29.56,29.33,29.29,26.75,22.66,14.09。
质谱:ms(maldi-tof,m/z)c62h104n2o2s2sn2:理论值1218.019;实测值1217.605。
由上可知,该化合物结构正确,为中间体4,10-双(2-辛基十二烷基)-2,8-双(三甲基锡烷基)-4,10-二氢噻吩并[2',3':5,6]吡啶并[3,4-g]噻吩并[3,2-c]异喹啉-5,11-二酮(中间体m2)。
(3)2-((5″-溴-3,3″-二辛基-[2,2':5',2″-三噻吩]-5-基)亚甲基)-1h-茚-1,3(2h)-二酮(中间体m3)的合成。
3.1、氩气氛围下,在50ml的两口瓶中,加入0.5g化合物7(5″-溴-3,3″-二辛基-[2,2':5',2″-三噻吩]-5-醛,通过商业途径购买所得)(0.86mmol),0.25g1,3-茚满二酮(1.72mmol)和25ml三氯甲烷,室温条件下将1ml哌啶缓慢滴加到反应瓶中,加完后升温至70℃反应过夜。
3.2、降至室温,加水淬灭反应,用二氯甲烷萃取,水洗,无水硫酸镁干燥,过滤得到粗产品。
3.3、将粗产品用柱层析分离纯化(洗脱剂:石油醚︰二氯甲烷=1︰1),得咖啡色固体438mg,产率72%。
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):7.97(dd,j=8.1,3.5hz,2h),7.89(s,1h),7.79(dd,j=13.3,9.3hz,3h),7.37(d,j=3.9hz,1h),7.08(d,j=3.9hz,1h),6.93(s,1h),2.90-2.79(m,2h),2.79-2.67(m,2h),1.66-1.55(m,10h),1.28(s,14h),0.92-0.83(m,6h)。
由上可知,该化合物结构正确,为中间体2-((5″-溴-3,3″-二辛基-[2,2':5',2″-三噻吩]-5-基)亚甲基)-1h-茚-1,3(2h)-二酮(中间体m3)。
(4)小分子cs8的合成
4.1、氩气氛围下,在50ml的双口瓶中,依次加入0.38g中间体m2(0.32mmol),0.5g2-((5″-溴-3,3″-二辛基-[2,2':5',2″-三噻吩]-5-基)亚甲基)-1h-茚-1,3(2h)-二酮(0.70mmol),10mg,pd(pph3)4(0.0087mmol)和20ml干燥的甲苯。用氩气流排气30分钟,在120℃温度下回流反应48小时。
4.2、待反应冷却后,用三氯甲烷萃取,饱和食盐水水洗,无水硫酸镁干燥,过滤得到粗产品。
4.3、粗产品用柱层析分离纯化(洗脱剂:石油醚︰三氯甲烷=1︰3),最终得到青色固体148mg,产率24%。
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):8.80(s,2h),8.00-7.92(m,4h),7.89(s,2h),7.84(s,2h),7.80-7.78(m,2h),7.52(s,2h),7.42(d,j=3.5hz,2h),7.16(s,2h),7.13-7.09(m,2h),7.00(s,2h),4.26-4.23(m,4h),2.87-2.82(m,8h),1.74-1.70(m,6h),1.56-1.52(m,108h),1.32-1.17(m,24h)。
质谱:ms(maldi-tof,m/z)c132h172n2o6s8:理论值2139.320;实测值2138.174。
由上可知,该产物结构正确,为结构式(2)所示基于tpti的小分子cs8,其中r为2-辛基十二烷基,r1为正辛基,a′为1,3-茚满二酮。
一种本实施例的小分子cs8在制备有机太阳能电池中的应用,上述制备所得的小分子cs8用于有机太阳能电池中作为给体材料,与受体相材料一起构筑本体异质结型有机太阳能电池,该电池的结构如图5所示,为ito/pedot︰pss/光活性层/ca/al,其光活性层由结构式ⅰ所述小分子cs8和pc71bm共混构成。
具体的太阳能电池的制备方法为:
(1)阳极采用氧化铟锡导电玻璃(ito),在上面旋涂一层阳极修饰层pedot︰pss聚合物导电膜,150℃处理15分钟。
(2)旋涂一层由小分子cs8和受体材料pc71bm共混而成(cs8:pc71bm重量比为1︰1,重量比在1︰0.5~2之间均可实施)的光活性层。
(3)干燥半小时后真空蒸镀金属钙(约20nm)作为阴极修饰层。
(4)最后蒸镀阴极金属铝(约100nm),通过掩膜版控制所镀金属的面积(约4mm2)。
该有机太阳能电池的光伏性能在模拟太阳光下(am1.5g,100mw/cm2)通过keithley2602表源等进行测试。
实施例4:
基于tpti单元的a′-π-a-π-a′型小分子cs9:以弱吸电子的tpti单元为中心核a,3,3″-二辛基-(2,2':5',2″-三噻吩)为π共轭桥,3-乙基饶丹宁为吸电子末端a′。
cs9具有式ⅱ的结构通式:
其中,r为2-辛基十二烷基,r1为正辛基,a′为3-乙基绕丹宁,小分子cs9的具体化学结构式如下所示:
一种本实施例的cs9的制备方法,合成路线参见图2,具体制备方法包括以下步骤:
(1)(e)-5-((5″-溴-3,3″-二辛基-[2,2':5',2″-三噻吩]-5-基)亚甲基)-3-乙基-2-绕丹宁-4-酮的合成:
1.1、氩气氛围下,在50ml的两口瓶中,加入0.5g化合物7(0.86mmol),0.28g3-乙基绕丹宁(1.72mmol),和25ml三氯甲烷,室温条件下将1ml哌啶缓慢滴加到三口瓶中,加完后升温至70℃反应过夜。
1.2、降至室温,加水淬灭反应,用二氯甲烷萃取,水洗,无水硫酸镁干燥,过滤得到粗产品。
1.3、将粗产品用柱层析分离纯化(洗脱剂:石油醚︰二氯甲烷=2︰1),得到448mg咖啡色固体,产率78%。
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):7.79(s,1h),7.23(s,1h),7.20(d,j=3.8hz,1h),7.05(d,j=3.8hz,1h),6.92(s,1h),4.19(q,j=7.3hz,3h),2.84-2.76(m,3h),2.76-2.69(m,2h),1.71-1.50(m,10h),1.31(dd,j=22.6,15.5hz,14h),0.87(dd,j=7.0,3.4hz,6h)。
由上可知,该化合物结构正确,为中间体(e)-5-((5″-溴-3,3″-二辛基-[2,2':5',2″-三噻吩]-5-基)亚甲基)-3-乙基-2-罗丹宁-4-酮。
(2)制备中间体m2:与实施例1相同。
(3)小分子cs9的合成:
小分子cs9的合成以中间体m2(0.35g,0.29mmol)和(e)-5-((5″-溴-3,3″-二辛基-[2,2':5',2″-三噻吩]-5-基)亚甲基)-3-乙基-2-绕丹宁-4-酮(0.5g,0.69mmol),为主要原料。按照小分子cs8的类似的方法合成,粗产品用柱层析分离纯化(洗脱剂:石油醚/三氯甲烷=1/1),最终得到青褐色固体0.12g,产率19%。
核磁共振氢谱:1hnmr(400mhz,cdcl3,δ/ppm):8.70(s,2h),7.76(s,2h),7.23-7.17(m,4h),7.15-7.08(m,4h),7.10-7.01(m,2h),4.29-4.11(m,8h),2.85-2.82(m,8h),2.03(s,6h),1.69-1.20(m,110h),0.89-0.85(m,30h).
质谱:ms(maldi-tof,m/z)c124h174n4o4s12:理论值2169.501;实测值2168.010。
一种本实施例的小分子cs9在制备有机太阳能电池中的应用,上述制备所得的小分子cs9用于有机太阳能电池中作为给体材料,与受体相材料一起构筑本体异质结型有机太阳能电池,该电池的结构如图5所示,为ito/pedot︰pss/光活性层/ca/al,其光活性层由结构式ⅰ所述小分子cs9和pc71bm共混构成。
具体的太阳能电池的制备方法为:
(1)阳极采用氧化铟锡导电玻璃(ito),在上面旋涂一层阳极修饰层pedot︰pss聚合物导电膜,150℃处理15分钟。
(2)旋涂一层由小分子cs9和受体材料pc71bm共混而成(cs9︰pc71bm重量比为1︰1,重量比在1︰0.5~2之间均可实施)的光活性层。
(3)干燥半小时后真空蒸镀金属钙(约20nm)作为阴极修饰层。
(4)最后蒸镀阴极金属铝(约100nm),通过掩膜版控制所镀金属的面积(约4mm2)。
该有机太阳能电池的光伏性能在模拟太阳光下(am1.5g,100mw/cm2)通过keithley2602表源等进行测试。
实验例:
光谱性质、电化学性质和光伏性质的测定如下:
(1)小分子cs6、cs7、cs8和cs9的光谱性质
附图3是小分子cs6、cs7、cs8和cs9薄膜在石英片上紫外-可见吸收光谱。从紫外-可见吸收光谱可知,小分子cs6、cs7、cs8和cs9在石英片的最大吸收边带峰值(λ)分别为719nm,711nm、860nm和724nm。根据经验公式egopt=1240/λ计算得到聚合物的相应光学带隙分别为1.72、1.74、1.61、1.71ev。
(2)小分子cs6、cs7、cs8和cs9的电化学性质
附图4为小分子cs6、cs7、cs8和cs9的循环伏安曲线。采用三电极体系测试:工作电极是小分子cs6、cs7、cs8和cs9的薄膜刮涂的铂电极,铂丝为对电极,ag/agcl为参比电极,bu4npf6作为支持电解质,二茂铁氧化还原对做内标。测试条件为:扫描范围为-1.6~1.6v(vs.ag/agcl),扫描速率为100mv/s。
根据循环伏安曲线计算得到四个小分子的homo/lumo能级分别为-5.87/-3.57ev、-5.70/-3.57ev、-5.53/-3.56ev、-5.38/-3.65ev。由于此实施例中小分子tpti单元具有吸电子能力,因此实施例中四个小分子homo能级相对来说较低。
(3)小分子cs6、cs7、cs8和cs9的有机小分子太阳能电池的光伏性质
上述制备所得的小分子可用于有机小分子太阳能电池中作为给体材料,与受体相材料一起构筑本体异质结型有机太阳能电池,该电池的结构为ito/pedot:pss/光活性层/ca/al,如附图5所示,其光活性层由实施例1至4中所述小分子中的任一种和pc71bm共混构成。其中附图5附图标记为:a-基地阳极,b-阳极修饰层,c-给体材料与受体材料的混合活性层,d-阴极修饰层,e-阴极。
本发明中所述的有机小分子本体异质结型太阳能电池中,其阳极采用氧化铟锡导电玻璃(ito),在上面旋涂一层阳极修饰层pedot:pss聚合物导电膜,150℃处理15分钟,随后旋涂一层由所制备的小分子和受体材料pc71bm共混而成的光活性层,干燥半小时后真空蒸镀金属钙(约20nm)作为阴极修饰层,最后蒸镀阴极金属铝(约100nm),通过掩膜版控制所镀金属的面积(约4mm2)。该有机小分子太阳能电池器件的光伏性能在模拟太阳光下(am1.5g,100mw/cm2)通过keithley2602表源等进行测试。
附图6为所为基于四个小分子制备的有机小分子太阳能电池的电流-电压特性(j-v)曲线。与该图相应光伏器件最优的光伏性能为:
cs6:能量转换效率(pce)=3.82%,开路电压(voc)=1.04v,短路电流(jsc)=7.04ma/cm2,填充因子(ff)=52.17%。
cs7:能量转换效率(pce)=1.47%,开路电压(voc)=0.92v,短路电流(jsc)=3.23ma/cm2,填充因子(ff)=48.58%。
cs8:能量转换效率(pce)=0.53%,开路电压(voc)=0.63v,短路电流(jsc)=2.67ma/cm2,填充因子(ff)=33.06%。
cs9:能量转换效率(pce)=0.54%,开路电压(voc)=0.86v,短路电流(jsc)=1.89ma/cm2,填充因子(ff)=33.02%。
本发明以合成的基于tpti的含不同π共轭桥和末端单元的小分子为有机半导体活性层做成了多个有机小分子太阳能电池器件。最高的能量转换效率达到3.82%,其开路电压高达为1.04v,填充因子达到52.17%。所有的实验结果表明本发明提供的基于tpti的小分子是优良的小分子半导体材料,在有机太阳能电池方面显示出潜在的应用价值。本发明不仅合成方法简单有效,而且通过制备出一系列的基于tpti的a′-π-a-π-a′型小分子材料。这对于研究该类小分子半导体材料的结构与性能的关系具有非常重要的意义,能够进一步指导开发高光电性能的小分子半导体材料。
以上所述,仅是本发明的较佳实施例而已,并非对本发明作任何形式上的限制。虽然本发明已以较佳实施例揭示如上,然而并非用以限定本发明。任何熟悉本领域的技术人员,在不脱离本发明的精神实质和技术方案的情况下,都可利用上述揭示的方法和技术内容对本发明技术方案做出许多可能的变动和修饰,或修改为等同变化的等效实施例。因此,凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所做的任何简单修改、等同替换、等效变化及修饰,均仍属于本发明技术方案保护的范围内。
- 还没有人留言评论。精彩留言会获得点赞!