4,4’-二硝基苯脲半抗原和人工抗原及其制备方法与应用与流程
本发明属于生物化工技术领域,具体地说,涉及4,4’-二硝基苯脲半抗原和人工抗原及其制备方法与应用。
背景技术:
尼卡巴嗪(nicarbazin,NIC)是由4,4’-二硝基苯脲(4,4-Dinitrocarbanilide,DNC)和2-羟基-4,6-二甲基嘧啶(2-hydroxyl 4,6-dimethylpyrimidine,HDP)组成的一种混合物,广泛用于禽业养殖中球虫病的治疗。虽然尼卡巴嗪的抗球虫效果良好而又不易产生耐药性,但极易在鸡肉组织中残留,对人体健康造成了威胁。国内外均规定尼卡巴嗪在鸡肉组织中的标识残留物(DNC)残留限量为0.2μg/g。因此,加强对鸡肉组织中DNC的监控和检测很有必要。
DNC结构式见式(Ⅰ)。
目前,对DNC在禽畜产品中残留的检测方法主要有高效液相-紫外法、高效液相-串联质谱法和酶联免疫法等。其中,酶联免疫法作为一种免疫分析方法,具有快速,灵敏和适合大批量样本筛查的优点,已成为大批量样本筛查中常用的方法。半抗原的设计与人工抗原的合成是抗体制备及免疫分析方法建立的关键。因此,设计合成可刺激机体产生高灵敏度DNC抗体的新型DNC半抗原及人工抗原显得尤为重要。
技术实现要素:
本发明的目的是提供4,4’-二硝基苯脲(DNC)半抗原和人工抗原及其制备方法与应用。
为了实现本发明目的,第一方面,本发明提供4,4’-二硝基苯脲半抗原(COU-CMO),其结构如式(II)所示:
第二方面,本发明提供所述半抗原的制备方法,以对氨基苯丁酸和对硝基苯异氰酸酯为主料,在DNC的硝基位引入含有4个碳原子的支链羧基间隔臂,合成了DNC半抗原。
进一步地,所述半抗原的制备方法具体如下:将0.1moL(17.9g)对氨基苯丁酸溶于200mL无水DMF中,分3批共加入0.1moL(16.4g)硝基异氰酸酯,之后室温反应1h,反应液倒入1000mL水中,析出固体,抽滤,用乙醇清洗滤饼,烘干即得半抗原。上述方法收率为80%。
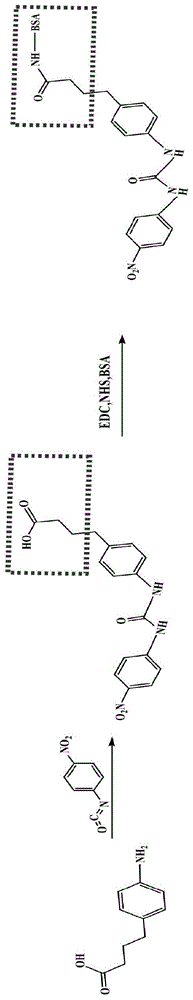
本发明4,4’-二硝基苯脲半抗原合成路线见图1。
第三方面,本发明提供4,4’-二硝基苯脲人工抗原,是由所述4,4’-二硝基苯脲半抗原与载体蛋白偶联后得到。所述4,4’-二硝基苯脲人工抗原可以作为免疫原也可以作为包被原。
其中,所述载体蛋白选自牛血清白蛋白、卵清蛋白、钥孔血蓝蛋白、甲状腺蛋白、人血清白蛋白;优选牛血清白蛋白、卵清蛋白。
第四方面,本发明提供所述人工抗原的制备方法,采用活泼酯法将载体蛋白偶联于所述4,4’-二硝基苯脲半抗原的羧基碳上。
具体方法为:
(1)称取1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC)和N-羟基硫代琥珀酰亚胺(NHS)加入到本发明所述的DNC半抗原中,室温活化3h;
具体地,称取19.2mg 1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC),11.5mg N-羟基硫代琥珀酰亚胺(NHS)和按上述方法制备的DNC半抗原34.3mg,溶于2mL二甲基亚砜溶液中,室温反应过夜,得A液;
(2)称取牛血清蛋白(BSA,或卵清白蛋白,OVA)溶解于硼酸盐缓冲液中。在磁力搅拌下,逐滴将活化后的半抗原加入到装有蛋白溶液的三角烧瓶中,继续搅拌过夜;反应完毕,将反应产物装入透析袋,生理盐水透析3天,每天更换透析液2次,即得到一种DNC人工抗原;
具体地,称取牛血清蛋白66mg(或卵清白蛋白45mg),溶解于10mL硼酸盐缓冲液中,得B液;在磁力搅拌下,将1mL A液逐滴加入到B液中,室温搅拌过夜;然后将反应液装入透析袋,用生理盐水于室温透析三天,每天换水2次,即得到DNC人工抗原。
(3)分装于安培瓶中,-20℃保存。即得到人工抗原:DNC-BSA(供免疫用)和DNC-OVA(供包被用)
第五方面,本发明提供由所述4,4’-二硝基苯脲人工抗原制备的特异性抗体,包括多克隆抗体和单克隆抗体。所述多克隆抗体可通过4,4’-二硝基苯脲人工抗原免疫实验动物(如小鼠),收集血清纯化获得。所单克隆抗体可通过4,4’-二硝基苯脲人工抗原免疫实验动物(如小鼠),采用杂交瘤技术来制备。
第六方面,本发明提供所述4,4’-二硝基苯脲半抗原或所述4,4’-二硝基苯脲人工抗原的以下任一应用:
①在制备抗4,4’-二硝基苯脲特异性抗体中的应用;
②在检测抗4,4’-二硝基苯脲特异性抗体中的应用。
第七方面,本发明提供由所述特异性抗体制备的4,4’-二硝基苯脲检测试剂或试剂盒。
第八方面,本发明提供所述特异性抗体的以下任一应用:
(1)在检测4,4’-二硝基苯脲中的应用;
(2)在制备4,4’-二硝基苯脲的ELISA试剂盒中的应用;
(3)在制备4,4’-二硝基苯脲的免疫层析试纸条中的应用;
(4)在鸡肉食品安全评价中的应用。
本发明所述人工抗原可以用作免疫原和包被原。
在本发明的一个具体实施方式中,以DNC-OVA为免疫原,免疫6周龄Balb/C雌性小鼠。采用一次基础免疫、两次加强免疫的免疫程序免疫小鼠。首次免疫时,将免疫原用PBS缓冲液稀释至1mg/mL,取600μL免疫原与等体积的弗氏完全佐剂混合乳化。采用多点免疫法于小鼠的颈背部皮下进行基础免疫。每次免疫周期为21天。加强免疫时,用弗氏不完全佐剂替代弗氏完全佐剂,用相同的方法制备乳化液,并注射于颈背部皮下进行加强免疫。第3次免疫8天后,尾静脉采血,分离血清。
用间接酶联免疫吸附试验法检测血清抗体效价,间接竞争酶联免疫吸附试验法检测血清灵敏度和特异性。灵敏度高、特异性好的小鼠用于制备单克隆抗体。
基于上述技术方案,本发明具有下列优点及有益效果:
(一)本发明首次公开了一种新型的DNC半抗原、人工抗原及其制备方法,用所述DNC人工抗原免疫动物,可得到效价高,灵敏度高的特异性抗体。本发明提供的DNC半抗原及其制备的抗体,为建立快速、简便、价廉、灵敏、特异的DNC检测方法提供了新手段。
(二)本发明提供的DNC半抗原合成方法尽可能保持4,4’-二硝基苯脲结构不变的情况下,在DNC的硝基位引入含有4个碳原子的支链羧基间隔臂,获得本发明的DNC半抗原。将所获得的纯化后的半抗原偶联载体蛋白用于制备抗体或包被原,继而建立免疫分析方法,具有较大的应用前景。
(三)本发明提供的DNC人工抗原免疫动物后获得的抗血清具有较高的灵敏度(见表1),可特异性地识别检测抗球虫药尼卡巴嗪的残留标识物DNC,在鸡肉食品卫生安全检测中具有良好的应用前景。
附图说明
图1为本发明4,4’-二硝基苯脲半抗原合成路线图。
图2为4-(4-(3-(4-硝基苯基)脲基)苯基)丁酸(DNC半抗原)的子离子扫描质谱图。
图3为4-(4-(3-(4-硝基苯基)脲基)苯基)丁酸的核磁共振氢谱图。
图4为BSA的MALDI-TOF-MS图。
图5为DNC-BSA的MALDI-TOF-MS图。
具体实施方式
以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段,所用原料、试剂均为市售商品。
实施例1 DNC半抗原的合成及鉴定
1、DNC半抗原的合成
将17.9g对氨基苯丁酸溶于200mL无水DMF中,分3批共加入16.4g硝基异氰酸酯,室温反应1h。将反应液倒入100mL水中,析出固体,抽滤,滤饼干燥,得半抗原,产率约为80%。4,4’-二硝基苯脲半抗原合成路线见图1。
2、尼卡巴嗪半抗原的鉴定
用质谱法鉴定DNC半抗原分子量(见图2)。合成产物的离子峰[M+H]+为m/z 344。因此,图2从分子量的角度上说明DNC半抗原合成成功。
用核磁共振鉴定DNC半抗原的结构(见图3):1H NMR(400MHz,DMSO)δ:12.01(s,1H,COOH),9.36(s,1H,NH),8.79(s,1H,NH),8.15(d,2H,j=8.4Hz,ArH),7.65(d,2H,j=8.4Hz,ArH),7.35(d,2H,j=7.6Hz,ArH),7.09(d,2H,j=7.6Hz,ArH),2.51(m,2H,CH2),2.18(m,2H,CH2),1.74(m,2H,CH2).δ:9.36(s,1H,NH),8.79(s,1H,NH)单峰为反应后的特征峰,12.01(s,1H,COOH)为活性基团羧基的特征峰,说明DNC半抗原合成成功。
实施例2尼卡巴嗪人工抗原的合成及鉴定
1、尼卡巴嗪人工抗原的合成
称取19.2mg EDC,11.5mg NHS和34.3mg DNC的半抗原,溶于2mL的二甲基亚砜溶液中,室温过夜反应,得A液;称取BSA 66mg溶解于10mL硼酸盐缓冲液中,得B液;在磁力搅拌下,将1mL A液逐滴加入到B液中,继续搅拌过夜;然后将反应液装入透析袋,室温用生理盐水透析三天,每天换水2次,即得到DNC-BSA人工抗原;分装于安培瓶中,-20℃保存。
将上述BSA更换成OVA 45mg,偶联反应后即获得DNC-OVA包被抗原。
2、尼卡巴嗪人工抗原的鉴定
DNC-BSA人工抗原采用MALDI-TOF-MS法进行鉴定,其中载体BSA MALDI-TOF-MS(结果见图4)分子量为64812.913,人工抗原DNC-BSA的MALDI-TOF-MS(结果见图5)分子量为70552.980,人工抗原的分子量高于载体蛋白BSA的分子量,说明DNC-BSA合成成功。经过计算,半抗原偶联到载体蛋白BSA的偶联比为16.7。
实施例3尼卡巴嗪人工抗原的免疫结果
以DNC-BSA为免疫原,免疫6只6周龄的Balb/C雌性小鼠。采用一次基础免疫、两次加强免疫的免疫程序免疫小鼠。首次免疫时,将免疫原用PBS缓冲液稀释至1mg/mL,取600μL免疫原与等体积的弗氏完全佐剂混合乳化。采用多点免疫法于小鼠的颈背部皮下进行基础免疫。每次免疫周期为21天。加强免疫时,用弗氏不完全佐剂替代弗氏完全佐剂,用相同的方法制备乳化液,并注射于颈背部皮下进行加强免疫。第3次免疫8天后尾静脉采血,分离血清,用间接酶联免疫吸附试验法检测血清抗体效价,间接竞争酶联免疫吸附试验法检测血清对尼卡巴嗪的灵敏度与特异性(见表1)。灵敏度高、特异性好的小鼠可用于制备单克隆抗体。具体步骤如下:
1、试剂配制
碳酸盐缓冲液(pH 9.6):准确称取Na2CO3 1.59g、NaHCO3 2.93g,少量超纯水溶解,定容至1000mL。
洗涤液(pH 7.4):准确称取NaCl 8.00g,KH2PO4 0.20g,Na2HPO4·12H2O2.90g,KCl 0.20g,少量超纯水溶解,加0.5mL Tween 20,定容至1000mL。
磷酸盐缓冲液(pH 7.4):准确称取NaCl 8.00g,KH2PO4 0.20g,Na2HPO4·12H2O 2.90g,KCl 0.20g,少量超纯水溶解,定容至1000mL。
封闭液:准确称取OVA10.00g,加入磷酸盐缓冲液1000mL,搅拌混匀直至蛋白完全溶解。
底物:购自北京维德维康生物技术有限公司。
终止液:准确量取浓硫酸100mL,缓慢滴加到800mL超纯水中。
2、间接竞争酶联免疫吸附试验法测定步骤
(1)包被:用包被缓冲液将实施例2制得的尼卡巴嗪包被原DNC-OVA稀释至1μg/mL,100μL/孔,4℃过夜;
(2)洗涤与封闭:倾去孔内液体,用洗涤液洗涤3次,每次3分钟;每孔加入150μL封闭液,37℃恒温封闭1h,然后洗涤3次,每次3分钟;
(3)加样:将50μL抗血清(20000倍稀释)与50μL DNC标准溶液(0ng/mL,10ng/mL和100ng/mL)依次加到酶标板上,37℃反应1小时,洗涤同步骤2;然后每孔加入100μL HRP-羊抗鼠IgG(5000倍稀释),37℃反应1小时,洗涤同步骤2;
(4)显色测定:每孔加入底物溶液100μL,37℃显色15min,然后每孔加入50μL 2mol/L浓H2SO4终止反应,用酶标仪测定各孔的OD450nm值。
表1第3次免疫后小鼠抗血清检测结果
间接竞争酶联免疫吸附试验法测定结果见表1。由表1可得第3次免疫后,6只小鼠均获得了良好的免疫效果,抗血清稀释倍数高达20000倍,0孔OD450值均大于1.5。当药物浓度为10ng/mL的时候,抑制率均低于50%,说明IC50均低于10ng/mL,也说明采用该半抗原制备的完全抗原免疫小鼠,可以制备出高灵敏度的抗体。此外,在药物浓度为10ng/mL和100ng/mL时,吸光值呈明显的递减梯度。结果说明用新合成的半抗原与载体蛋白偶联物(DNC-BSA)免疫小鼠,获得的抗血清具有较高的灵敏度,可以特异性地识别尼卡巴嗪残留标示物DNC。
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之做一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!