具有光热效应的aza-BODIPY类衍生物和其合成及应用的制作方法
本发明属于生物化学领域,涉及一类aza-bodipy衍生物和其合成及应用,可实现肿瘤的光热治疗,具体地说,涉及氮杂-氟硼吡咯类荧光染料探针的合成方法和生物热疗应用。
背景技术:
光热治疗(ptt)是近年来兴起的肿瘤治疗方法之一,相对于一般药物化疗,ptt具有侵入性小,操作简单,治疗时间短且恢复快等固有优势,使得ptt成为一种潜力无限、前景广阔的抗肿瘤治疗手段。长期以来,研究者致力于开发新型光热材料和制剂,以满足临床应用中对光热诊断治疗的日益增长的需求。但调研文献发现最初的光热材料大部分是以价格昂贵的au、ag、pt为代表的贵金属纳米颗粒或以无近近红外区吸收或近红外区吸收较弱的石墨烯、碳纳米棒为代表的材料,因此构建一种价格低廉,且具有近红外吸收的有机功能小分子光热材料具有一定的挑战性和现实意义。
氟化硼络合二吡咯甲川类(boron-dipyrromethene,简称bodipy)化合物是一类性能优异的新型荧光染料,该类染料具有较高的摩尔消光系数,提高了染料的光敏性能;且具有很好的光热稳定性和化学稳定性,可避免受外界干扰而迅速光降解。当bodipy母体骨架meso位上的c原子被n原子取代后会形成一类新的氮杂-氟硼吡咯(aza-bodipy)类荧光染料。aza-bodipy及其衍生物除具有bodipy类荧光染料的优良性能外,紫外吸收光谱会发生明显红移,使得其具有更小的自发荧光背景干扰及更深的组织穿透性,更有利于其在生物体内的精准定位成像技术。因而近年来aza-bodipy类荧光探针的研究与开发备受科研爱好者的关注。
基于此背景下,本发明设计合成了一系列具有优良光热效应的aza-bodipy衍生物,通过近红外光源照射,材料会在短时间内将光能转化为热能,并成功地将其应用于肿瘤的热疗实验。
技术实现要素:
本发明第一个目的是提供一类aza-bodipy衍生物的合成;
本发明第二个目的是提供一类具有优良光热效应的aza-bodipy衍生物;
本发明第三个目的是提供一类aza-bodipy衍生物在光热治疗中的应用。
本发明通过下述技术方案实现:
具有光热效应的aza-bodipy衍生物,其结构通式如ⅰ所示化合物:
式ⅰ中,r1,r2为芳香醚链或苯并噻二唑中的一种,r3,r4为芳香醚链、4-氨基苯基或其修饰物中的任意一种。
进一步,其中r1,r2,r3,r4中的芳香醚链如式ⅱ所示:
优选,r1和r2均为式ⅱ中的芳香醚链或苯并噻二唑中的一种,r3和r4均为芳香醚链、苯并噻二唑或4-氨基苯基中的一种。
优选,r1,r2和r3为式ⅱ中的芳香醚链,r4为4-氨基苯基。
优选,r1和r3为式ⅱ中的芳香醚链,r2为苯并噻二唑,r4为4-氨基苯基。
优选,r1为式ⅱ中的芳香醚链,r2为苯并噻二唑,r3和r4为4-氨基苯基。
优选,r1为苯并噻二唑,r2和r3为式ⅱ中的芳香醚链,r4为4-氨基苯基。
优选,r1和r2为苯并噻二唑,r3为式ⅱ中的芳香醚链,r4为4-氨基苯基。
优选,r1为苯并噻二唑,r2,r3和r4为式ⅱ中的芳香醚链。
本发明还提供一种上述具有光热效应的aza-bodipy衍生物的制备方法。
具有光热效应的aza-bodipy衍生物的制备,具体制备路线如下:
本发明还提供一种将所述的aza-bodipy类化合物,通过组装作为肿瘤光热治疗的手段(详见实施案例3)。
本发明有益的技术效果:
本发明提供了上述aza-bodipy衍生物吸收在780nm及以上有强的近红外吸收,将其中一种探针用于hct116肿瘤鼠模型上的光热治疗。
本发明提供的aza-bodipy衍生物合成方法简单,成本相对低廉,但光热转换率很高,光热治疗效果成效明显。
附图说明
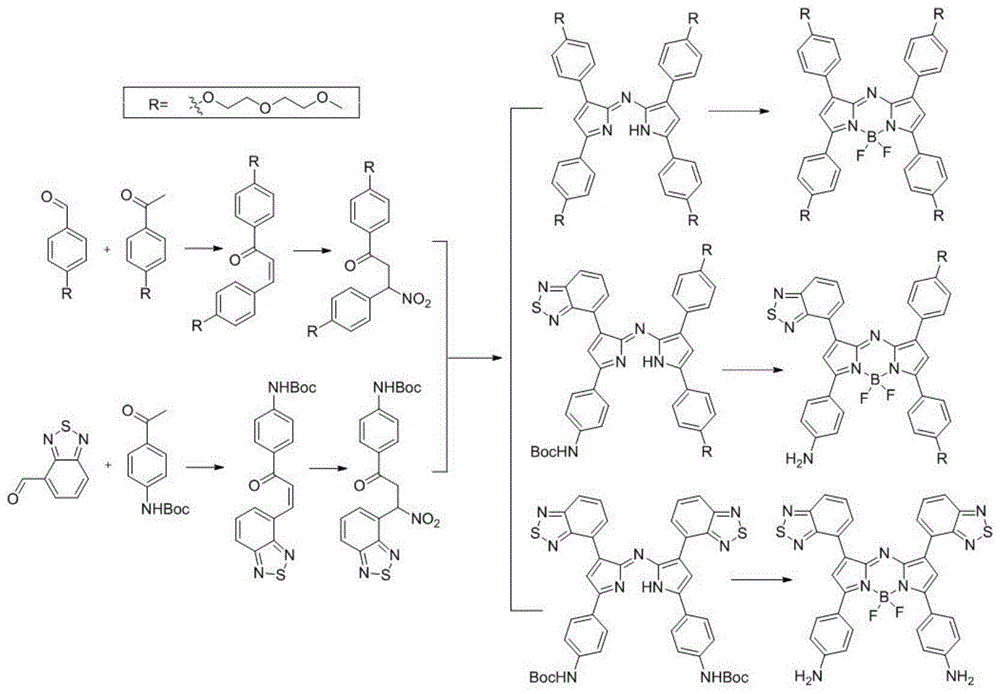
图1为式ⅰ所示aza-bodipy衍生物中几种化合物的合成路线图。
图2为式ⅰ-1所示aza-bodipy(详见实施例1,下同)在cdcl3中的1hnmr图谱。
图3为式ⅰ-1所示aza-bodipy浓度为50μmol/l时在水中的紫外吸收光谱。
图4为式ⅰ-1所示aza-bodipy不同探针浓度下的光热升温曲线(备注:激光波长:785nm,功率密度为3.85wcm-2),说明随着探针浓度的增加,光热效应越来越好。
图5为式ⅰ-1所示aza-bodipy在1小时内3次循环升温曲线(备注:激光波长:785nm,功率密度为3.85wcm-2)说明该探针具有良好的可循环利用的光热效应。
图6为式ⅰ-2所示aza-bodipy(详见实施例2,下同)在动物体内的光热升温效果图(备注:激光波长:785nm,功率密度为1.57wcm-2)
图7为式ⅰ-2所示aza-bodipy在动物治疗一个周期的效果图(备注:探针为100nmol,激光波长:785nm,功率密度为1.57wcm-2)
具体实施方式
下面结合实施例对本发明作进一步阐述,本领域技术人员应当理解,所述实施例仅用于示例,而不对本发明构成任何限制。
实施例1
式ⅰ-1化合物的合成
化合物a的合成
n2气体保护下,称取化合物1(1.0g,4.46mmol)与化合物2(1.5g,6.23mmol),加到200ml圆底烧瓶中,用适量乙醇溶解,加入15ml10%的氢氧化钠溶液,室温搅拌过夜。点半观测,待反应完全,二氯甲烷萃取,合并有机相,无水na2so4干燥,蒸干有机相,柱层析分离,展开剂比例为dcm:ea=20:1,产物a为黄色油状液体,产率为72%。1hnmr(400mhz,cdcl3)δ=8.02(d,j=8hz,2h),7.77(d,j=16hz,1h),7.59(d,j=8hz,2h),7.43(d,j=16hz,1h),6.97(dd,j=8hz,4h),4.23(t,j=4hz,2h),4.19(t,j=4hz,2h),3.89(q,j=4hz,4h),3.75-3.72(m,4h),3.60-3.58(m,4h),3.40(s,6h).
化合物b的合成
n2气体保护下,称取化合物a(1.0g,2.25mmol)与硝基甲烷(1.8ml,33.75mmol),加到200ml圆底烧瓶中,用适量乙醇溶解,加入1ml20%氢氧化钾溶液,将体系升温至90℃回流3h。待反应完成冷却至室温,dcm萃取,合并有机相,无水na2so4干燥,蒸干有机相,柱层析分离,展开剂比例为pe:ea=1:1,产物b为棕色油状液体。产率为93.7%。1hnmr(400mhz,cdcl3)δ=7.88(d,j=8hz,2h),7.17(d,j=8hz,2h),6.93(d,j=8hz,2h),6.86(d,j=8hz,2h),4.82-4.77(m,1h),4.65-4.60(m,1h),4.21(t,j=4hz,2h),4.16-4.13(m,1h),4.10(t,j=4hz,2h),3.88(t,j=4hz,2h),3.84(t,j=4hz,2h),3.73-3.69(m,4h),3.59-3.56(m,4h),3.39(m,6h),3.36-3.33(m,2h).
化合物c的合成
n2气体保护下,称取化合物b(900mg,1.79mmol),正丁醇溶解与200ml圆底烧瓶中,加入醋酸铵(2.07g,26.75mmol),将体系升温至125℃回流3h。待反应完成冷却至室温,ea萃取,合并有机相,无水na2so4干燥,蒸干有机相,柱层析分离,展开剂比例为pe:ea=1:1,产物为蓝黑色固体,产率为88.6%。
式ⅰ-1化合物的合成
称取化合物c(500mg,0.54mmol),适量dcm溶解与200ml圆底烧瓶中,加入dipea(600μl,3.49mmol),三氟化硼乙醚(900μl,7.29mmol),室温搅拌过夜。待反应完成,dcm萃取,合并有机相,无水na2so4干燥,蒸干有机相,用硅胶层析柱分离,展开剂比例为dcm:meoh=300:1,产物ⅰ-1为红棕色固体。产率为78%。1hnmr(400mhz,cdcl3)δ=8.03(t,8h),6.99(d,j=4hz,8h),6.92(s,2h),4.22(m,8h),3.90(m,8h)3.75(m,8h),3.60(m,8h),3.41(s,6h),3.40(s,6h).
实施例2
式ⅰ-2化合物的合成
化合物d的合成
n2气体保护下,称取化合物1(1.0g,4.46mmol)与化合物3(2.5g,10.63mmol),用适量乙醇溶解,加入15ml10%氢氧化钠,室温搅拌过夜。待反应完成,dcm萃取,合并有机相,无水na2so4干燥,蒸干有机相,柱层析分离,展开剂比例为pe:ea=8:1,产物为亮黄色胶状固体,产率为76.2%。1hnmr(400mhz,cdcl3)δ=8.01(d,j=8hz,2h),7.78(d,j=8hz,1h),7.59(d,j=8hz,2h),7.49(d,j=8hz,2h),7.42(d,j=8hz,1h),4.19(t,j=4hz,2h),3.88(q,j=4hz,4h),3.74-3.72(m,4h),3.60-3.58(m,4h),3.40(s,3h),1.54(s,9h).
化合物e的合成
n2气体保护下,称取化合物d(1.55g,3.51mmol)与硝基甲烷(2.8ml,52.3mmol),用适量乙醇溶解,加入1ml20%koh,将体系升温至90℃回流3h。待反应完成冷却至室温,dcm萃取,合并有机相,无水na2so4干燥,蒸干有机相,柱层析分离,展开剂比例为pe:ea=1:1,产物为黄棕色胶状固体。产率为95.5%。1hnmr(400mhz,cdcl3)δ=7.86(d,j=8hz,2h),7.44(d,j=8hz,2h),7.17(d,j=8hz,2h),6.86(d,j=8hz,2h),6.75(s,1h),4.82-4.77(m,1h),4.65-4.60(m,1h),4.16-4.13(m,1h),4.10(t,j=4hz,2h),3.83(t,j=8hz,2h),3.72-3.69(m,2h),3.58-3.56(m,2h),3.39(s,3h),3.35(t,j=8hz,2h),1.53(s,9h).
化合物f的合成
n2气体保护下,称取化合物e(450mg,0.891mmol)与化合物b(450mg,0.897mmol),用少量正丁醇溶解,加入醋酸铵(2.07g,26.73mmol),将体系升温至125℃回流3h。待反应完成冷却至室温,ea萃取,合并有机相,无水na2so4干燥,蒸干有机相,柱层析分离,展开剂比例为pe:ea=1:1,产物为蓝黑色固体。产率为40.6%。
式ⅰ-2化合物的合成
称取化合物f(300mg,0.33mmol),用适量dcm溶解,加入dipea(600μl,3.49mmol),三氟化硼乙醚(900μl,7.29mmol),室温搅拌过夜。待反应完成,dcm萃取,合并有机相,无水na2so4干燥,蒸干有机相,柱层析分离,展开剂比例为dcm:meoh=300:1,产物为红棕色固体。产率为78%。1hnmr(400mhz,d6-dmso)δ=8.18(t,j=8hz,3h),8.09(d,j=4hz,2h),8.0(d,j=4hz,2h),7.74(s,1h),7.16(t,j=8hz,3h),7.10(m,4h),6.81(s,2h),6.71(d,j=4hz,2h),4.21(m,6h),3.78(m,6h),3.62(m,6h),3.48(m,6h),3.26(s,9h).
实施例3
本发明中所有活体实验遵守实验动物饲养和使用的规章制度,实验所用荷瘤鼠购自江苏集萃药康生物科技有限公司,饲养在无菌室中层流通风橱内的无菌鼠笼中,使用高压蒸汽处理过的水和食物进行喂食。
在荷瘤鼠肿瘤部位皮下注射式ⅰ-2的aza-bodipy,一次计量为100nmol,注射后使用激光照射(备注:激光波长:785nm,功率密度为1.57wcm-2),同时使用热成像实时监测温度,照射10min后肿瘤部位体温可升至70℃以上(如图6所示),每天记录小鼠肿瘤大小,发现给药的探针在10天后痊愈且无复发,而不给药的小鼠肿瘤体积在逐渐增长(如图7所示),这说明我们的探针具有很好的光热效应,能成功地应用于肿瘤的光热治疗。
- 还没有人留言评论。精彩留言会获得点赞!