诺如病毒的检测方法与流程
本发明涉及利用逆转录-聚合酶链式反应(reversetranscription-polymerasechainreaction、rt-pcr)检测诺如病毒的方法、以及用于实施该方法的试剂盒。更具体而言,将待检体处理液和rt-pcr反应液的混合液与待检体混合来检测诺如病毒的方法、以及用于实施该方法的试剂盒,所述混合液还包含二甲基亚砜(dimethylsulfoxide、dmso)。
背景技术:
诺如病毒是属于人杯状病毒(humancalicivirus)科的rna病毒,基因组中具有约7000个碱基的单链rna。该病毒是按照用电子显微镜观察到的形态学分类也被称为小圆形结构病毒(smallroundstructuredvirus,srsv)、且以诺沃克样病毒(norwalk-likevirus)这样的属名所称呼的病毒。属于诺如病毒的病毒被分类为基因组(genogroup)(gi)和基因组ii(gii)这2种基因组,进而分别被分类为14和17或更多的基因型(genotype)。
人感染诺如病毒时会引起呕吐、痢疾等急性胃肠炎症状。日本国内每年的食物中毒患者的约半数起因于诺如病毒,其中的约7成发生在11月~2月,诺如病毒作为冬季型的胃肠炎和食物中毒的原因病毒而已知。由诺如病毒导致的食物中毒主要由通过烹饪者的食品污染而产生。诺如病毒的感染性强、容易产生大规模的食物中毒等群体事件。对于人的感染途径主要是经口感染。感染者的粪便或呕吐物以及被它们直接或间接地污染的物品类、或者被诺如病毒污染的牡蛎或者其他的双壳贝类等食品类作为代表性的感染源而被列举。因此,鉴定诺如病毒感染患者、由该病毒导致的污染物对于防止病毒感染的扩大是重要的。
作为用于检测由病毒导致的感染、污染的病毒检查,应用检测病毒抗原的免疫学的测定法、病毒基因扩增法(专利文献1~3、非专利文献1)。作为高灵敏度地检测诺如病毒的手段,可列举出用rt-pcr扩增诺如病毒的rna、测定扩增产物量的方法。例如,根据厚生劳动省药品食品局食品安全部监视安全课的通知(非专利文献2和3),广泛地利用rt-pcr法进行诺如病毒的检测以及利用实时pcr法进行诺如病毒的定量检测。
rna病毒粒子具有由rna基因组与蛋白质形成的核被封入被称为衣壳的蛋白质壳中而成的基本结构。因此,为了利用基因扩增法检测病毒rna,需要从病毒粒子中提取rna。为了检测作为待检体的粪便中的诺如病毒,例如,将粪便待检体以5~10%(w/v)的浓度悬浮于蒸馏水或生理盐水中,由其离心上清,使用市售的病毒rna提取试剂盒(例如,qiaamp(注册商标)viralrnamini、qiagen公司)提取/纯化rna(非专利文献2)。然而,在多阶段的rna提取·纯化操作之后进行rt-pcr的检测过程是复杂的。因此,提出了将粪便悬浮液与待检体处理液混合、进行短时间热处理来去除壳蛋白,使内部的rna游离,将游离的rna直接供于rt-pcr的简易的检测法(非专利文献4)。另一方面,为了对粪便悬浮液与待检体处理液的混合物进行热处理,需要做以下的工作:为了防止该混合物的暴沸、蒸发而用盖子对反应容器进行密闭,热处理之后卸下盖子,添加rt-pcr反应液。为了改善这一点,提出了将待检体与胍盐等离液剂混合,不必进行热处理而利用rt-pcr来检测病毒的方法(专利文献4)。
现有技术文献
专利文献
专利文献1:wo2002/029119
专利文献2:wo2002/029120
专利文献3:日本特开2004-301684
专利文献4:日本特开2017-209036
非专利文献
非专利文献1:kageyamat,etal.broadlyreactiveandhighlysensitiveassayfornorwalk-likevirusesbasedonreal-timequantitativereversetranscription-pcr.jclinmicrobiol.2003apr;41(4):1548-57.
非专利文献2:厚生労働省医薬食品局食品安全部監視安全課食安監発第1105001号(平成15年11月5日)另附「ノロウイルスの検出法について」、最终订正:食安監発0514004号(平成19年5月14日)
非专利文献3:厚生労働省医薬食品局食品安全部監視安全課食安監発第1105001号(平成15年11月5日)另附「ノロウイルスの検出法について」、最终订正:食安監発1022第1号(平成25年10月22日)
非专利文献4:nishimuran,etal.detectionofnorovirusesinfecalspecimensbydirectrt-pcrwithoutrnapurification.jvirolmethods.2010feb;163(2):282-286.
技术实现要素:
发明要解决的问题
本发明的目的在于,提供简便的诺如病毒的检测方法。具体而言,提供简便地检测诺如病毒的方法、以及用于实施该方法的试剂盒,所述方法将待检体处理液和rt-pcr反应液的混合液与待检体混合,从而简便地检测诺如病毒,所述混合液还包含二甲基亚砜(dimethylsulfoxide、dmso)。
用于解决问题的方案
本发明的目的通过以下的发明实现。
〔1〕
一种诺如病毒的检测方法,将待检体处理液和一步法rt-pcr反应液的混合液与待检体混合,通过rt-pcr反应来检测待检体中的诺如病毒,所述混合液还包含二甲基亚砜(dmso)。
〔2〕
根据〔1〕所述的方法,其中,前述诺如病毒基因型为基因组i(gi)或基因组ii(gii)。
〔3〕
根据〔1〕或〔2〕所述的方法,其中,前述待检体源自选自由生物试样、生物来源试样、环境试样和环境来源试样组成的组中的试样。
〔4〕
根据〔1〕或〔2〕所述的方法,其中,前述待检体源自选自由排泄物试样、排泄物来源试样、呕吐物和呕吐物来源试样组成的组中的试样。
〔5〕
根据〔1〕或〔2〕所述的方法,其中,前述待检体为将〔4〕所述的试样悬浮于水、生理盐水或缓冲液而得到的悬浮液。
〔6〕
根据〔1〕或〔2〕所述的方法,其中,前述待检体为对〔5〕所述的悬浮液进行离心分离而得到的离心上清。
〔7〕
根据〔1〕~〔6〕中的任一项所述的方法,其中,前述待检体处理液为诺如病毒检测试剂盒(探针法)(岛津制作所、产品编号241-09325系列)所包含的样品处理试剂(sampletreatmentreagent),前述一步法rt-pcr反应液为前述试剂盒所包含的nov试剂(novreagent)a、b和c的混合物、是包含逆转录酶和dna聚合酶的反应液。
〔8〕
根据〔1〕~〔7〕中的任一项所述的方法,其中,前述待检体处理液与前述一步法rt-pcr反应液的混合比以体积比计为3:4~6。
〔9〕
根据〔1〕~〔8〕中的任一项所述的方法,其中,在前述待检体处理液与前述一步法rt-pcr反应液的混合液中以1~5%(v/v)的浓度包含前述dmso。
〔10〕
根据〔1〕~〔9〕中的任一项所述的方法,其中,前述待检体与还包含dmso的前述混合液的混合比以体积比计为1:20~30。
〔11〕
根据〔7〕所述的方法,其中,前述逆转录酶选自由amv逆转录酶、mmlv逆转录酶、hiv逆转录酶以及它们的突变体组成的组。
〔12〕
根据〔7〕所述的方法,其中,前述dna聚合酶选自由taqdna聚合酶、tthdna聚合酶、koddna聚合酶、pfudna聚合酶以及它们的突变体组成的组。
〔13〕
根据〔1〕~〔12〕中的任一项所述的方法,其中,前述rt-pcr反应通过实时测定而监测。
〔14〕
根据〔1〕~〔13〕中的任一项所述的方法,其中,前述实时测定通过使用荧光滤光片测定rt-pcr产物的扩增曲线,给出判定待检体中的诺如病毒的存在为阳性、或为阴性的结果。
〔15〕
一种诺如病毒的检测试剂盒,其是如下构成的:其包含:待检体处理液、以及含有逆转录酶和dna聚合酶的一步法rt-pcr反应液,前述待检体处理液与前述一步法rt-pcr反应液的混合液中含有1~5%(v/v)的dmso。
〔16〕
根据〔15〕所述的试剂盒,其判定诺如病毒基因型为基因组i(gi)或为基因组ii(gii)。
〔17〕
根据〔15〕或〔16〕所述的试剂盒,其还包含试剂盒的操作步骤说明书。
发明的效果
通过本发明,将包含诺如病毒的粪便等待检体直接添加至待检体处理液与一步法rt-pcr反应液的混合液中,由此能够在同一容器内连续地进行自诺如病毒的rna游离、rt-pcr反应和rt-pcr产物的检测,因此能够简便地进行病毒检测,所述混合液中还包含二甲基亚砜(dmso)。进而,本发明的方法中,为了使rna自诺如病毒粒子游离,不需要一向必要的热处理,简便性得到进一步改善。
附图说明
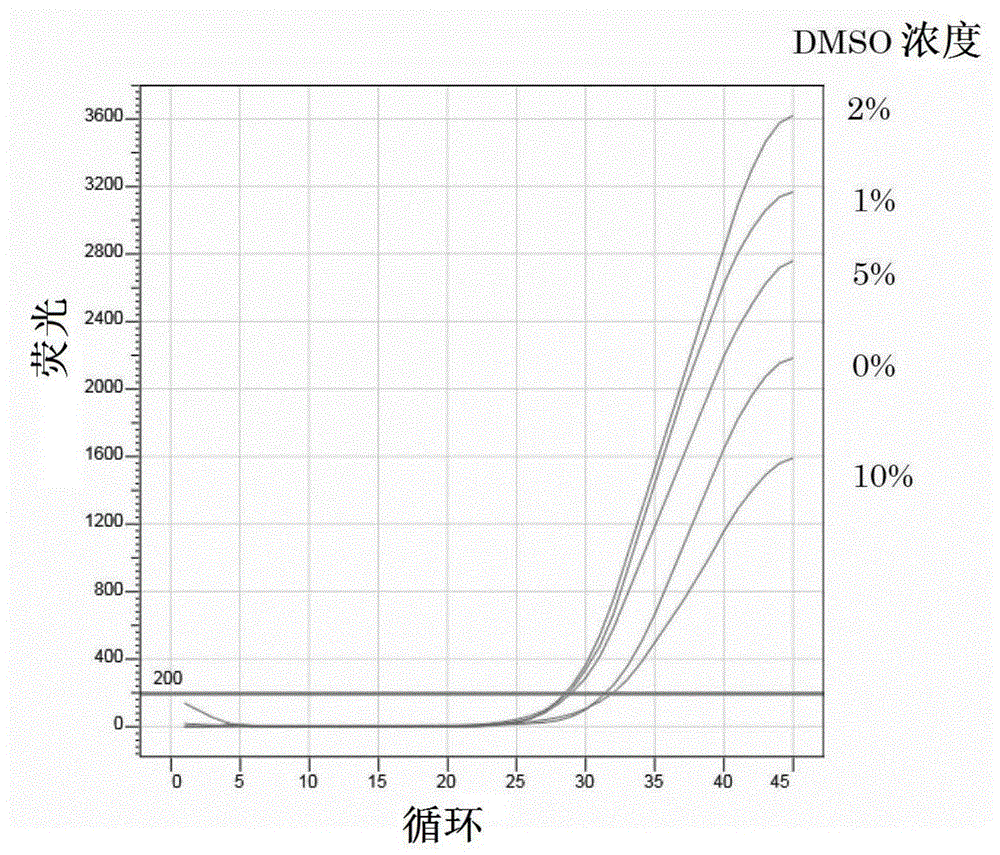
图1是表示将包含诺如病毒的粪便悬浮液的离心上清作为待检体、使用诺如病毒检测试剂盒(探针法)(岛津制作所)、改变反应体系中添加的dmso浓度进行的实时pcr中的扩增曲线的图。
图2是表示对于包含诺如病毒的4种粪便,将粪便悬浮液的离心上清作为待检体,使用诺如病毒检测试剂盒(探针法)(岛津制作所),向反应体系中添加2%dmso或者不添加dmso的条件下进行的实时pcr中的扩增曲线的图。
具体实施方式
本发明提供检测待检体中的诺如病毒的方法。该检测诺如病毒的方法如下:将待检体处理液和一步法rt-pcr反应液的混合液与待检体混合,通过rt-pcr反应来检测待检体中的诺如病毒,所述混合液还包含二甲基亚砜(dmso)。
本发明中,作为待检体中的检测对象的诺如病毒是具有rna作为基因组的rna病毒,是不具有由脂质双层形成的膜即包膜的病毒。包膜的主要成分为脂质,因此容易被醇等有机溶剂、表面活性剂破坏,但不具有这样的包膜的诺如病毒等rna病毒通常对于有机溶剂、表面活性剂表现出抗性。
作为本发明中的待检体,可列举出生物试样、生物来源试样、环境试样和环境来源试样等。作为生物试样,包括包含贝类的中肠腺等的动植物组织以及血液、唾液、鼻涕、组织分泌液等体液。特别是,贝类作为由诺如病毒导致的食物中毒的原因食品最需要被重视。作为生物来源试样,包含对于前述生物试样进行例如超声处理等处理而得到的试样。作为环境试样,可列举出包含空气、土壤、尘埃、水等的所有试样。作为环境来源试样,包含对于前述环境试样进行例如超声处理等处理而得到的试样。
作为本发明的另一实施方式,作为待检体,可列举出排泄物试样、排泄物来源试样、呕吐物试样和呕吐物来源试样等。排泄物试样和呕吐物试样也可以在蒸馏水、生理盐水或缓冲液中以5~10%(w/v)悬浮而制成乳剂,将该乳剂作为待检体。作为前述缓冲液,没有特别的限定,可列举出磷酸盐缓冲液、tris缓冲液、硼酸盐缓冲液、hepes等两性离子(good)缓冲液。前述乳剂也可以以例如10000~12000rpm进行2~20分钟离心分离,将得到的离心上清作为待检体使用。
排泄物来源试样和呕吐物来源试样中包含擦拭试样。擦拭试样是指,以病毒污染的确认作为目的,从手指、食器、菜板、菜刀、烹饪设备、厕所设备、住宅设备等用棉棒、切片棉等擦拭而得到的物质用磷酸盐缓冲液等使之溶出而得到的试样。可以使用对于得到的溶出液进行超离心分离、将离心沉淀悬浮或溶解而得到的物质作为待检体(宗村佳子等、食品衛生学雑誌、2017年58卷4号p.201-204)。
本发明中所使用的待检体处理液和一步法rt-pcr反应液优选组合市售的诺如病毒检测试剂盒(探针法)(岛津制作所、产品编号241-09325系列、241-09325-91或241-09325-92)所包含的试剂。作为待检体处理液,可以使用本试剂盒所包含的样品处理试剂(sampletreatmentreagent)。作为一步法rt-pcr反应液,可以使用本试剂盒所包含的nov试剂a、b和c的混合物。nov试剂a含有镁离子、钾离子和tris。nov试剂b包含逆转录反应引物和pcr引物。nov试剂c包含逆转录酶和dna聚合酶。一步法rt-pcr反应中,通过将逆转录酶与dna聚合酶预先混合,从而能够在同一容器内进行逆转录反应(单链cdna合成)和pcr。前述待检体处理液与前述一步法rt-pcr反应液的混合比以体积比计优选为3:4~6,更优选为3:5~5.2。
前述一步法rt-pcr反应液中所包含的逆转录酶是以病毒rna作为模板、生成单链互补dna(cdna)的酶,只要能催化逆转录反应就没有特别的限定,可以使用禽类成髓细胞性白血病病毒(avianmyeloblastosisvirus、amv)、莫洛尼氏鼠白血病病毒(moloneymurineleukemiavirus、m-mlv)和人类免疫缺陷病毒(humanimmunodeficiencyvirus、hiv)等rna病毒来源的rna依赖性dna聚合酶以及它们的突变体。
前述一步法rt-pcr反应液所包含的dna聚合酶是嗜热细菌来源的耐热性dna聚合酶,可以使用taq、tth、kod、pfu以及它们的突变体,但不限定于这些。为了避免由dna聚合酶所导致的非特异性扩增,也可以使用热启动dna聚合酶。热启动dna聚合酶是例如结合有抗dna聚合酶抗体的dna聚合酶或者对酶活性部位进行了热敏感性化学修饰而得到的dna聚合酶,是在pcr中经过了最初的变性步骤(90℃以上)之后dna聚合酶被活性化的酶。
前述一步法rt-pcr反应液中包含用于使逆转录反应和pcr在适当的条件下进行的所有成分。作为该成分,至少包含前述逆转录酶、逆转录反应引物、前述耐热性dna聚合酶、pcr引物、dntp混合物(包含脱氧核苷5’-三磷酸;datp、dgtp、dctp和dttp的混合物)以及缓冲液。前述反应液中也可以添加rna分解酶抑制剂。作为逆转录反应引物,可以使用对目标rna的序列具有特异性的引物、低聚(dt)引物或随机引物。作为pcr引物,可以使用对于通过逆转录反应生成的cdna的序列具有特异性的引物对(正向和反向)。pcr引物可以与对目标rna序列具有特异性的前述逆转录反应引物相同。另外,可以根据扩增的dna区域、即目标序列的数目向前述一步法rt-pcr反应液中添加2种以上的pcr引物。作为包含前述成分的组合物,可以使用对于市售的诺如病毒检测试剂盒(探针法)(岛津制作所、产品编号241-09325系列、241-09325-91或241-09325-92)所包含的nov试剂a、b和c按照试剂盒处理说明书进行混合而得到的混合物作为一步法rt-pcr反应液。
在检测诺如病毒rna的情况下,通过使用例如专利文献1和2、非专利文献3以及日本特开2018-78806所述的pcr引物,能够检测到诺如病毒基因型中的基因组i(gi)和基因组ii(gii),但不限定于此。前述诺如病毒检测试剂盒(探针法)中包含非专利文献3所述的pcr引物。
本发明中,为了使rna自诺如病毒游离而一向必要的例如进行90℃的热处理的工序并非是必要的。本发明中,可以向前述待检体处理液与前述一步法rt-pcr反应液的混合液中直接添加待检体,通过rt-pcr反应检测诺如病毒。这可以通过向前述混合液中优选以1~5%(v/v)的终浓度添加dmso来实现。dmso只要终浓度成为1~5%(v/v),即可以向前述待检体处理液或前述一步法rt-pcr反应液中添加,或者也可以向前述混合液中添加。前述混合液中的dmso更优选的终浓度为2%(v/v)。
为了效率良好地使rna自诺如病毒游离,或者灵敏度良好地进行基于一步法rt-pcr反应的诺如病毒检测,前述待检体与包含dmso的前述混合液的混合比以体积比计优选为1:20~30,更优选为1:25。
对于rt-pcr中的逆转录反应的反应温度条件、以及pcr条件(温度、时间和循环数)的设定,只要是本领域技术人员就可以容易地进行。
本发明中,在rt-pcr反应中,pcr产物通过实时测定而被监测。进行该实时测定时,rt-pcr以及检测该rt-pcr产物的工序在同一容器内进行。
pcr产物的实时测定也被称为实时pcr。实时pcr中,通常利用荧光检测pcr扩增产物。荧光检测方法有:使用嵌入性荧光色素的方法、以及使用荧光标记探针的方法。作为嵌入性荧光色素,可以使用sybr(注册商标)greeni,但不限定于此。嵌入性荧光色素与通过pcr合成的双链dna结合,通过激发光的照射发出荧光。通过测定该荧光强度,能够测定pcr扩增产物的生成量。
作为荧光标记探针,可列举出taqman探针、分子信标(molecularbeacon)、循环探针等,但不限定于这些。taqman探针是5’末端被荧光色素修饰、且3’末端被猝灭剂物质修饰而得到的低聚核苷酸。taqman探针可以在pcr的退火步骤中与模板dna特异性地杂交,但探针上存在有猝灭剂,因此即便照射激发光也会抑制荧光的发生。在之后的延伸反应步骤中,利用taqdna聚合酶所具有的5’→3’核酸外切酶活性,与模板dna杂交的taqman探针被分解时,荧光色素自探针游离,由猝灭剂导致的荧光发生的抑制被解除,从而发出荧光。通过测定该荧光强度,能够测定扩增产物的生成量。作为前述荧光色素,可列举出fam、rox、cy5,但不限定于这些。作为前述猝灭剂,可列举出tamra(注册商标)和mgb,但不限定于这些。为了将2种以上的dna目标序列区别而进行检测,使用分别结合了不同的荧光色素的2种以上的低聚核苷酸探针(例如taqman探针)进行pcr。
在pcr产物的实时测定中,使用与所使用的荧光色素相对应的荧光滤光片,监测rt-pcr产物的扩增曲线。与pcr循环数相应地荧光强度增加时,判定为待检体中的分析对象的rna病毒的存在为阳性,另一方面,pcr中荧光强度没有增加的情况下,被判定为阴性。
本发明的一实施方式中,提供一种诺如病毒的检测试剂盒,其是如下构成的:其包含:待检体处理液、以及含有逆转录酶和dna聚合酶的一步法rt-pcr反应液,前述待检体处理液与前述一步法rt-pcr反应液的混合液中含有1~5%(v/v)的dmso。
实施例
以下列举出实施例对本发明详细地进行说明,但本发明的范围不限于此。
实施例1
〔诺如病毒检测中的dmso的效果〕
(1)待检体
采集诺如病毒感染患者的粪便100mg,悬浮于1ml的蒸馏水中,制成约10%(w/v)的粪便乳剂。对于该粪便乳剂利用微量离心分离机以10000rpm进行5分钟离心分离,将得到的离心上清作为待检体。
(2)反应混合液的制备
反应混合液通过混合诺如病毒检测试剂盒(探针法)(岛津制作所、产品编号241-09325系列)中所包含的试剂来制备。对于一步法rt-pcr反应液,由本试剂盒的nov试剂a、nov试剂b和nov试剂c分别采集12.5μl、2.5μl和0.25μl,将它们混合来制备。作为待检体处理液由本试剂盒的样品处理试剂采集9μl,添加到该一步法rt-pcr反应液中。得到的待检体处理液与一步法rt-pcr反应液的混合液中,以终浓度成为1%、2%、5%或10%(v/v)的方式添加dmso进行混合,从而制备反应混合液。
(3)待检体与反应液的混合
将(2)中制备的反应混合液25μl加入至pcr反应管中,向其中添加(1)中得到的待检体1μl,使用实时pcr装置(gvp-9600、岛津制作所),直接监测rt-pcr反应。反应混合液中,作为pcr引物包含cog1f/cog1r和cog2f/cog2r,另外作为荧光标记探针包含g1a、g1b和g2。
(4)rt-pcr条件
在45℃/5分钟的逆转录反应之后,进行95℃/3分钟的初期变性,接着进行95℃/1秒-56℃/10秒的pcr45个循环。pcr中的测光在56℃/10秒的步骤中进行。
(5)结果和考察
将测光结果示于图1。表明ct值和荧光强度受到dmso浓度影响。ct值是指在实时pcr中,扩增曲线与阈值(threshold)交叉的循环数。与不添加dmso的情况(0%dmso)相比较,添加了1%、2%和5%(v/v)dmso的情况下,ct值小且得到了强的荧光强度。确认到,该作用在2%dmso的情况下最强。通过向反应混合液中添加1~5%(v/v)dmso,与不添加dmso的情况相比较,表现出初始dna量多、可知检测到了诺如病毒。
实施例2
〔不同的粪便待检体中的dmso的效果〕
(1)待检体
对于诺如病毒感染患者的4种粪便,与实施例1同样地进行,得到各自的离心上清,作为待检体。
(2)反应混合液的制备
将dmso浓度设为2%(v/v)和0%,除此以外,与实施例1同样地进行。
(3)待检体与反应液的混合以及rt-pcr
与实施例1同样地进行。
(4)结果和考察
将测光结果示于图2。在所测定的所有粪便中,向反应混合液中添加2%(v/v)dmso,由此与不添加dmso的情况相比较,表现出ct值小且得到强的荧光强度。因此,可知通过本发明的方法能够简便地检测到诺如病毒,从而能够鉴定诺如病毒感染患者。
- 还没有人留言评论。精彩留言会获得点赞!