用表达TNF的粘液瘤病毒治疗癌症的方法
交叉引用
本申请要求于2018年7月13日提交的美国临时申请号62/697,581的权益,该申请通过引用并入本文。
关于联邦资助研究的声明
本发明是在美国国立卫生研究院授予的p50ca186781的政府支持下完成的。政府拥有本发明的一些权利。
背景技术:
用于治疗各种类型癌症的当前疗法倾向于通过使癌细胞中毒或将其杀死来起作用。遗憾的是,对癌细胞有毒的治疗通常也倾向于对健康细胞有毒。此外,肿瘤的异质性是癌症有效治疗难以实现的主要原因之一。当前主流疗法诸如化学疗法和放射疗法倾向于在狭窄的毒性治疗窗口内使用。这些类型的疗法被认为是由于肿瘤细胞的类型不同而适用性有限以及可以施用这些疗法的窗口有限的钝工具。
技术实现要素:
在某些实施方案中,本文公开了使用被工程化以表达tnf蛋白的粘液瘤病毒(myxv)来抑制或治疗癌症的方法。在一些实施方案中,本文还描述了使用由表达tnf的粘液瘤病毒处理的单核外周血细胞和/或骨髓细胞抑制或治疗癌症的方法。在另外的实施方案中,本文描述包括用于与本文所述的一种或多种方法一起使用的被工程化的粘液瘤病毒和药物组合物。
在某些实施方案中,本文公开了一种被工程化以表达肿瘤坏死因子(tnf)蛋白的粘液瘤病毒(myxv),其中所述myxv包括在一个或多个与兔细胞向性相关的基因处或附近的修饰。在一些实施方案中,所述tnf蛋白是tnfα蛋白。在一些实施方案中,所述tnf蛋白是表面tnf蛋白。在一些实施方案中,所述tnf蛋白是可溶性tnf蛋白。在一些实施方案中,所述tnf是人tnf蛋白。在一些实施方案中,一个或多个与兔细胞向性相关的基因包括m11l、m063、m135r、m136r、m-t2、m-t4、m-t5或m-t7。在一些实施方案中,所述myxv包含m135r基因的部分缺失或全部缺失。在一些实施方案中,所述myxv包含损害m135r基因的功能的m135r基因的修饰。在一些实施方案中,所述tnf蛋白替代myxv基因组内的m135r基因。在一些实施方案中,所述tnf蛋白插入在myxv基因组内的m135r基因与m136r基因之间。在一些实施方案中,所述myxv还包含荧光蛋白。在一些实施方案中,所述myxv是lausanne菌株。在一些实施方案中,所述myxv是vmyx-m135ko-htnf。在一些实施方案中,所述myxv是vmyx-htnf-m135-136。
在某些实施方案中,本文公开了包含本文所述的粘液瘤病毒和药学上可接受的赋形剂的药物组合物。在一些实施方案中,所述药物组合物被配制用于全身施用。在一些实施方案中,所述药物组合物被配制用于局部施用。在一些实施方案中,所述药物组合物被配制用于肠胃外施用。
在某些实施方案中,本文公开了一种组合物,其包含被工程化以表达肿瘤坏死因子(tnf)蛋白的粘液瘤病毒(myxv)离体处理的外周血单核细胞(pbmc)、骨髓(bm)细胞或其组合。在一些实施方案中,本文所述的myxv是粘液瘤病毒。在一些实施方案中,所述myxv是vmyx-sodko-htnf。在一些实施方案中,所述pbmc、bm细胞或其组合包括自体细胞。在一些实施方案中,所述pbmc、bm细胞或其组合获自异源供体。
在某些实施方案中,本文公开了一种在有需要的受试者中抑制或治疗癌症的方法,其包括向所述受试者施用被工程化以表达肿瘤坏死因子(tnf)蛋白的粘液瘤病毒(myxv)。在一些实施方案中,所述myxv是本文所述的粘液瘤病毒。在一些实施方案中,所述myxv是vmyx-sodko-htnf。在一些实施方案中,所述癌症是实体瘤。在一些实施方案中,所述癌症已经转移到所述受试者中的第二位置。在一些实施方案中,所述第二位置包括所述受试者的肺、脑、肝和/或淋巴结。在一些实施方案中,所述癌症包括骨肉瘤、三阴性乳腺癌或黑色素瘤。在一些实施方案中,该方法进一步包括向受试者施用另外的治疗剂。在一些实施方案中,所述另外的治疗剂是免疫检查点调节剂。在一些实施方案中,在施用所述myxv或所述组合物之前向所述受试者施用所述另外的治疗剂。在一些实施方案中,在施用所述myxv或所述组合物之后向所述受试者施用所述另外的治疗剂。在一些实施方案中,所述另外的治疗剂与所述myxv或所述组合物组合施用给所述受试者。在一些实施方案中,所述受试者是人类。在一些实施方案中,所述方法还包括选择患有或疑似患有癌症的受试者。在一些实施方案中,所述粘液瘤病毒能够感染具有先天性抗病毒应答缺陷的细胞。在一些实施方案中,具有先天性抗病毒应答缺陷的细胞包括癌细胞。在一些实施方案中,被所述粘液瘤病毒感染的细胞表达tnf。
在某些实施方案中,本文公开了一种在有需要的受试者中抑制或治疗癌症的方法,其包括向所述受试者施用本文所述的组合物。在一些实施方案中,该方法进一步包括将所述粘液瘤病毒离体吸附到pbmc、bm细胞或其组合的表面上。在一些实施方案中,将所述粘液瘤病毒吸附到所述pbmc、bm细胞或其组合的表面上包括在允许所述粘液瘤与所述pbmc、bm细胞或其组合的表面结合的条件下将所述pbmc、bm细胞或其组合暴露于所述粘液瘤病毒。在一些实施方案中,该条件包括约4℃至约37℃的温度。在一些实施方案中,所述条件包括约20℃至约37℃、约20℃至约28℃、约24℃至约26℃、约30℃至约37℃或约35℃至约37℃的温度。在一些实施方案中,所述条件包括至少5分钟、10分钟、15分钟、20分钟、30分钟、1小时、1.5小时、2小时、3小时、4小时、6小时、8小时、10小时、12小时或更长时间的温育时间。在一些实施方案中,所述pbmc、bm细胞或其组合获自所述受试者或hla相关供体。在一些实施方案中,将吸附所述病毒的pbmc、bm细胞或其组合全身施用给所述受试者。在一些实施方案中,所述癌症是实体瘤。在一些实施方案中,所述癌症已经转移到所述受试者中的第二位置。在一些实施方案中,所述第二位置包括所述受试者的肺、脑、肝和/或淋巴结。在一些实施方案中,所述癌症包括骨肉瘤、三阴性乳腺癌或黑色素瘤。在一些实施方案中,该方法进一步包括向受试者施用另外的治疗剂。在一些实施方案中,所述另外的治疗剂是免疫检查点调节剂。在一些实施方案中,在施用所述myxv或所述组合物之前向所述受试者施用所述另外的治疗剂。在一些实施方案中,在施用所述myxv或所述组合物之后向所述受试者施用所述另外的治疗剂。在一些实施方案中,所述另外的治疗剂与所述myxv或所述组合物组合施用给所述受试者。在一些实施方案中,所述受试者是人类。在一些实施方案中,所述方法还包括选择患有或疑似患有癌症的受试者。在一些实施方案中,所述粘液瘤病毒能够感染具有先天性抗病毒应答缺陷的细胞。在一些实施方案中,所述具有先天性抗病毒应答缺陷的细胞包括癌细胞。在一些实施方案中,被所述粘液瘤病毒感染的细胞表达tnf。
在某些实施方案中,本文公开一种试剂盒,其包含本文所述的粘液瘤病毒、本文所述的药物组合物或本文所述的组合物。
附图说明
本发明的某些实施方案的新颖特征在所附权利要求书中具体阐述。通过参考以下对其中利用到本发明的原理的说明性实施方式加以阐述的详细描述和附图,将会获得对本发明的特征和优点的更好理解,在这些附图中:
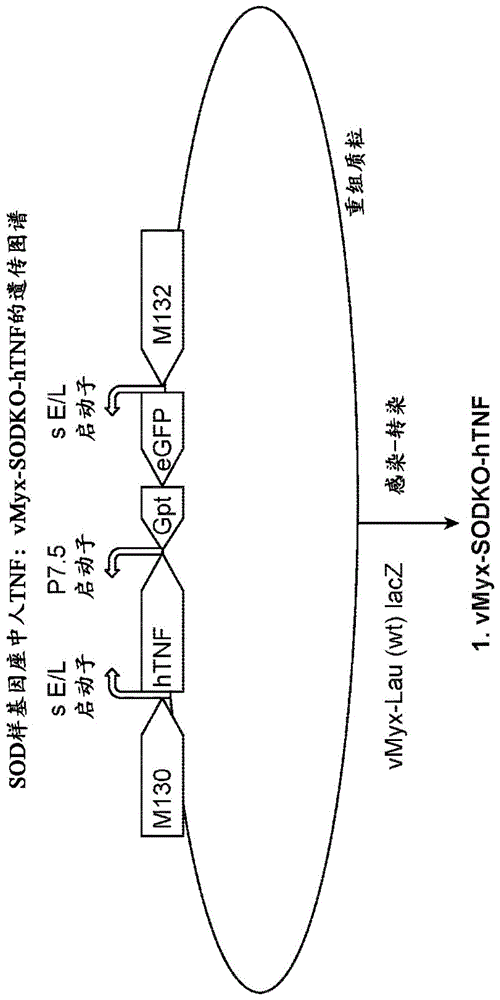
图1示出了vmyx-sodko-htnf插入质粒的遗传图谱和病毒的构建概述。在用vmyx-lacz病毒感染以构建vmyx-sodko-htnf病毒之前,该质粒用于转染rk-13细胞。
图2a和图2b示出了两种示例性的不同工程化myxv的遗传图谱。图2a示出了vmyx-135ko-htnf插入质粒的遗传图谱和重组粘液瘤病毒的遗传图谱概述。注意,该病毒具有敲除病毒m135r基因的功能。图2b示出了vmyx-htnf-(m135-136)插入质粒的遗传图谱和该重组粘液瘤病毒的构建概述。注意,该病毒具有野生型myxv主链,因为tnf转基因插入了病毒m135r和m136r基因之间的基因间基因座,因此没有基因敲除功能。在用亲本野生型vmyx-lau感染以分别构建vmyx-m135ko-htnf(图2a)和vmyx-htnf-(m135-136)(图2b)病毒之前,每种质粒均用于转染rk-13细胞。
图3是k7m2-luc肿瘤接种后2周的balb/c小鼠的一组图像。未经治疗的动物在肺部显示出晚期肿瘤(左),而经vmyx-sodko-htnf治疗的动物显示出明显较小的肿瘤(右)。在第0天用2×106k7m2-luc细胞接种动物,并用4×106离体bm处理,该bm在治疗前已被vmyx-sodko-htnf感染一小时。然后在第2周给动物注射荧光素ip,并使用ivis成像系统成像。计算所有动物的肿瘤发光度并标准化。
图4是显示与其他myxv构建体相比,载有表达htnf的粘液瘤病毒(myxv)的骨髓具有更好的溶瘤能力的图。kaplan-meier生存曲线表明,与对照队列相比,vmyx-sodko-htnf是唯一经测试可显著提高平均生存率的myxv构建体。在第0天用2×106个k7m2-luc细胞接种动物,并用离体骨髓处理,该离体骨髓在治疗前已用各自的myxv构建体感染1小时。然后监测动物的疾病进展,直到达到安乐死标准为止。接种后第8周,所有幸存者均被安乐死。
图5是间隔2周拍摄的两组图像,其示出了未经治疗的对照(左图像)与用vmyx-sodko-htnf病毒治疗的动物(右图像)之间的肿瘤进展差异。在第0天用2×106k7m2-luc细胞接种动物,并用4×106离体pbmc处理,该pbmc在治疗前已被vmyx-sodko-htnf感染一小时。然后在第3周和第5周给动物注射荧光素ip,并使用ivis成像系统成像。计算所有动物的肿瘤发光度并标准化。
图6是显示离体载有vmyx-sodko-htnf的pbmc剂量响应存活的图。用逐步增加剂量的载有vmyx-sodko-htnf的balb/cpbmc处理的balb/c小鼠比未治疗对照存活时间显著更长。在第0天用2×106个k7m2-luc细胞接种动物,并用pbmc处理,该pbmc在治疗前已用各自的myxv构建体感染1小时。然后监测动物的疾病进展,直到达到安乐死标准为止。
图7是一组流式细胞术数据,显示被vmyx-sodko-htnf感染48hpi的细胞在细胞表面表达htnf(灰色和绿色),而对照细胞对htnf为阴性(粉红色和紫色)。用vmyx-sodko-htnf实验感染细胞48小时。在48hpi,使用非酶离解缓冲液提拉细胞并计数。然后使用小鼠抗人htnfpe偶联抗体对细胞染色,并使用流式细胞仪进行分析。
图8是用sytox橙进行的细胞死亡测定的一组图,证实与不表达htnf的对照vmyx-m135ko病毒相比,来自vmyx-sodko-htnf的tnf表达不会在k7m2-luc骨肉瘤细胞系中引起增加的细胞死亡。将细胞用vmyx-m135ko病毒或vmyx-sodko-htnf病毒进行实验感染或用tnf处理。然后将细胞在感染后和治疗后温育24和48小时。然后将细胞用sytox橙染色,并计数荧光细胞的百分比。还针对每个时间点和治疗计数每个孔中的平均细胞数。
图9示出了使用流式细胞术对被感染的人aml(thp1)细胞的细胞死亡的定量。由apc/cy7+细胞群体确定myxv介导的总的杀死的thp1细胞,如通过对用live/dead染色的细胞进行门控所定义。使用holm-sidakt检验进行多次比较确定显著性(*=p<0.05;**=p<0.01;***=p<0.001)。结果显示,在感染后两个时间点(24和48小时)的3个测试的感染复数(moi=10、1或0.1)下,vmyx-sodko-htnf-gfp感染thp-1细胞导致门控的死亡细胞的总数增加。
图10示出了使用流式细胞术对myxv介导的靶点杀死的病毒感染的人aml(thp1)细胞的定量。从apc/cy7+细胞的比例确定myxv介导的thp1细胞“靶点”杀死,该比例来自对gfp阳性的病毒感染的细胞群体进行门控。使用holm-sidakt检验进行多次比较确定显著性(*=p<0.05;**=p<0.01;***=p<0.001)。
图11示出了使用流式细胞术对myxv诱导的脱靶杀死的未感染的人aml(thp1)细胞的定量。从apc/cy7+细胞的比例确定myxv介导的脱靶杀死的thp1细胞,该比例来自对gfp阴性的细胞群体进行门控。使用holm-sidakt检验进行多次比较确定显著性(*=p<0.05;**=p<0.01;***=p<0.001)。
图12示出了使用流式细胞术对被感染的人多发性骨髓瘤(u266)细胞的细胞死亡的定量。从apc/cy7+细胞群体确定myxv介导的总的杀死的u266。使用holm-sidakt检验进行多次比较确定显著性(*=p<0.05;**=p<0.01;***=p<0.001)。
图13示出了在具有免疫能力的小鼠中通过离体负载的同系鼠骨髓白细胞递送的vmyx-sodko-htnf的测试,以消除预先接种的鼠多发性骨髓瘤。图13a示出了使用移植到c57/b1小鼠中的抗硼替佐米的vk*12598骨髓瘤细胞的体内数据,其中它们主要迁移至骨髓和脾。在癌植入后100天产生生存曲线(图13b)。图13c对应于存活百分比。
图14示出了将vmyx-htnf-(m135-m136)离体预负载在具有smac拟态或免疫检查点抑制剂的bm白细胞上的组合疗法。将smac模拟化合物lcl161(50mg/kg)或检查点抑制剂单克隆抗体(mab)α-mupd-1与通过离体预负载的自体小鼠骨髓白细胞递送的vmyx-htnf-(m135-m136)组合,测试组合疗法(图14a)。图14b示出了包括生存曲线的体内数据。图14c描述了存活百分比。
图15示出了人tnf蛋白的表达和被vmyx-htnf-(m135-136)感染的人细胞的部分分泌。
具体实施方式
某些术语
除非另有说明,否则根据常规用法使用技术术语。分子生物学中常见术语的定义可以在benjaminlewin,genesv,oxforduniversitypress出版,1994(isbn0-19-854287-9);kendrew等(编著),theencyclopediaofmolecularbiology,blackwellscienceltd.出版,1994(isbn0-632-02182-9)以及roberta.meyers(编著),molecularbiologyandbiotechnology:acomprehensivedeskreference,vcrpublishers,inc.出版,1995(isbn1-56081-569-8)中找到。
除非另有说明,否则本文使用的所有技术和科学术语均具有与本公开内容所属领域的普通技术人员通常所理解的含义相同的含义。尽管与本文所述的那些类似或等同的方法和材料可以在本公开的实践或测试中使用,但下文描述了合适的方法和材料。另外,材料、方法和实施例仅仅是说明性的,而不是限制性的。
说明书中对“一些实施方案”、“实施方案”、“一个实施方案”或“其他实施方案”的引用是指结合实施方案描述的特定特征、结构或特性包括在本发明的至少一些实施方案中,但不一定包含在所有实施方案中。
本文使用的章节标题仅用于组织的目的,不应当解释为限制所描述的主题。
提供以下术语和方法的解释是为了更好地描述本发明的化合物、组合物和方法,并指导本领域普通技术人员实施本公开内容。还应理解的是,本公开中使用的术语仅用于描述特定实施方案和实施例,而非旨在限定。
如本文所用,除非上下文另外明确指出,否则单数形式“一个(a)”、“一种(an)”和“该(the)”旨在还包括复数形式。
如本文所用,范围和量可表示为“约”特定值或范围。约还包括确切的量。因此,“约5μl”意指“约5μl”,并且还表示“5μl”。通常,术语“约”包括预期在实验误差内的量。
如本文所用,术语“和/或”是指并涵盖一个或多个相关联的所列项目的任何和所有可能的组合,以及当以替代(“或”)解释时缺少的组合。
如本文所用,“一个或多个”或至少一个可表示1、2、3、4、5、6、7、8、9、10或更多,最多为任何数目。
如本文所用,术语“包含”表示“包括”。因此,“包含a或b”表示包括a、b,或a和b。
“有效量”或“治疗有效量”是指足以产生期望效果的本发明化合物或组合物的量,该期望效果可以是治疗效果和/或有益效果。有效量将在本领域技术人员的知识和专业范围内随着年龄、受试者的一般状况、所治疗病况的严重程度、所施用的特定药剂、所治疗的持续时间、任何同时治疗的性质、所使用的药学上可接受的载体以及类似因素而变化。适当地,本领域普通技术人员可以通过参考相关的文本和文献和/或通过使用常规实验来确定在任何单个情况下的有效量或治疗有效量。(例如,参见remington,thescienceandpracticeofpharmacy(最新版))。
如本文所用,术语“受试者”和“患者”在本文可互换使用,并且是指人类和非人类动物。本公开内容的术语“非人类动物”包括所有脊椎动物,例如,哺乳动物和非哺乳动物,诸如非人类灵长类动物、绵羊、狗、猫、马、牛、啮齿动物(例如,小鼠、大鼠等)等。优选地,所述受试者是人类患者。在特定的实施方案中,本公开内容的受试者是人受试者。
本文使用的术语“细胞”包括单个细胞以及多个细胞或细胞群。施用药剂或将药剂暴露于细胞包括体外和体内施用。
“需要其的受试者”或“有需要的受试者”是已知患有或疑似患有癌症诸如实体瘤的受试者。
如本文所用,术语“癌症”是指经历了特征性间变而失去分化、生长速率增加、侵入周围组织并能够转移的恶性肿瘤。
残余癌是在对受试者进行任何形式的治疗以减少或根除癌症后仍保留在受试者中的癌症。转移性癌症是除衍生出转移性癌症的原始(原发性)癌症的起源部位以外的体内一个或多个部位(例如第二部位)的癌症。局部复发是癌症在与原始癌症相同的部位或附近(诸如在相同的组织中)复发。
实体癌(诸如肉瘤和癌)的实例,包括纤维肉瘤、粘液肉瘤、脂肪肉瘤、软骨肉瘤、骨肉瘤、成骨肉瘤和其他肉瘤、滑膜瘤、间皮瘤、尤文肉瘤、平滑肌肉瘤、横纹肌肉瘤、结肠癌、淋巴恶性肿瘤、胰腺癌、乳腺癌、肺癌、非小细胞肺癌、卵巢癌、前列腺癌、肝细胞癌、鳞状细胞癌、基底细胞癌、腺癌、汗腺癌、皮脂腺癌、乳头状癌、乳头状腺癌、髓样癌、支气管癌、肾细胞癌、肝癌、胆管癌、绒毛膜癌、肾母细胞瘤、宫颈癌、睾丸肿瘤、膀胱癌和cns肿瘤(例如,神经胶质瘤、星形细胞瘤、髓母细胞瘤、颅神经胶质瘤(craniopharyogioma)、室管膜瘤、松果体瘤、血管母细胞瘤、听神经瘤、少突神经胶质瘤、血管瘤、黑色素瘤、神经母细胞瘤和视网膜母细胞瘤)。
血液学癌症的实例包括骨髓瘤、淋巴瘤和白血病。在一些情况下,示例性血液学癌症包括b细胞或t细胞血液学癌症。在一些情况下,示例性血液学癌症包括霍奇金淋巴瘤或非霍奇金淋巴瘤。
如本文所用,术语“化学治疗剂”是指在以异常细胞生长为特征的疾病的治疗中具有治疗有效性的任何化学剂。这样的疾病包括肿瘤、赘生物和癌症,以及以增生性生长为特征的疾病,诸如牛皮癣。在一个实施方案中,化学治疗剂是一种用于治疗癌症的药物,诸如抗肿瘤药。在一个实施方案中,化学治疗剂是一种放射性化合物。本领域技术人员可容易地确定所使用的化学治疗剂(例如,参见slapak和kufe,harrison'sprinciplesofinternalmedicine(第14版)中第86章principlesofcancertherapy;perry等人,abeloff,clinicaloncology(第二版)中第17章chemotherapy,2000年churchilllivingstone,inc;baltzer和berkery(编辑):oncologypocketguidetochemotherapy,第二版,st.louis,mosby-yearbook,1995年;fischerknobf和durivage(编辑):thecancerchemotherapyhandbook,第4版,st.louis,mosby-yearbook,1993年。组合化疗是施用一种以上的药剂来治疗癌症。诸如表达tnf的粘液瘤病毒和一种或多种其他化学治疗剂,可同时施用或以任何顺序在时间上分开施用。
如本文所用,术语“抑制或治疗疾病”,诸如癌症,是指抑制疾病或病况的完全发展。“治疗”是指在疾病或病理状况开始发展后改善其体征或症状的治疗性干预。关于疾病或病理状况,术语“改善”是指任何可观察到的治疗的有益作用。可以通过例如在易受感染受试者中疾病的临床症状发作延迟、疾病的一些或全部临床症状的严重程度降低、疾病的进展(诸如转移)较慢、受试者整体健康或生活质量的改善或通过本领域公知的对特定疾病特异的其他参数来证明有益效果。“预防性”治疗是向不表现出疾病体征或仅表现出早期体征的受试者施用的治疗,以降低发展成病理学例如转移性癌症的风险。
如本文所用,与本文所公开的治疗化合物结合使用的“药学上可接受的载体”是常规的。remington’spharmaceuticalsciences,e.w.martin,mackpublishingco.,easton,pa,第19版(1995)描述了适用于药物递送治疗剂的组合物和制剂。
通常,载体的性质取决于所采用的特定施用方式。例如,肠胃外制剂通常包含可注射的流体,其包括药学上和生理学上可接受的流体如水、生理盐水、平衡盐溶液、葡萄糖水溶液、甘油等作为媒介物。对于固体组合物(例如,粉剂、丸剂、片剂或胶囊形式),常规的无毒固体载体可包括例如药物级的甘露醇、乳糖、淀粉或硬脂酸镁。除生物学中性载体外,待施用的药物组合物还可含有少量无毒辅助物质,诸如润湿剂或乳化剂、防腐剂和ph缓冲剂等,例如,乙酸钠或失水山梨糖醇单月桂酸酯。
如本文所用,术语“药物”和“治疗剂”是指当适当地施用于受试者或细胞时能够诱导期望的治疗或预防作用的化合物或组合物。
如本文所用,术语“肿瘤”是指赘生物的产物,其是由过度的细胞分裂导致的组织的异常生长。侵入周围组织和/或可转移的肿瘤被称为“恶性的”。赘生物是增生性疾病的一个实例。
本文所使用的术语“具有复制能力的”是指能够在特定宿主细胞内感染和复制的病毒。
介绍
转移到肺和其他器官的癌症是基础和临床癌症研究的主要挑战。迄今为止,治疗肺转移的能力一直具有挑战性,诸如骨肉瘤、黑色素瘤和乳腺癌的癌症在当前疗法下的5年生存率均低于25%。当前的治疗范例是经典放射疗法、化学疗法和靶向疗法的组合,但是没有一种疗法能对所有肿瘤都有效。曾经被吹捧为癌症治疗的潜在的“灵丹妙药”的一种疗法是肿瘤坏死因子(tnf)。自一个世纪前由williamcoley首次发现tnf和数十年后的分子表征以来,tnf已被证明是一种诱人但神秘的抗癌剂和免疫调节剂。研究其在远端分离的肿瘤中局部治疗以及作为全身治疗的用途已显示出严重的毒性和较低的抗肿瘤应答率。事实上,一些研究还发现,仅全身性施用tnf甚至可能促进某些癌症中的肿瘤生长。
tnf(也称为tnfα、cachexin或恶液质素)是一种细胞因子,是炎症性免疫反应(coley,wb.2015thetreatmentofmalignanttumorsbyrepeatedinoculationsoferysipelas:withareportoftenoriginalcases.am.j.med.sci.105,487–511(1893))的不可或缺的部分。tnf主要作为细胞表面免疫配体表达,但当在表达催化可溶性配体切割和释放的转化酶的细胞(例如,髓系细胞)中表达时,tnf可作为可溶性细胞因子分泌。已被证明的一种tnf效应子途径是通过tnf受体-1(tnfr1)途径诱导细胞死亡,导致凋亡或坏死,这取决于特定靶细胞内的下游作用(moriwakik,bertinj,goughp,orlowskig,chanfk.2016.differentialrolesofripk1andripk3intnf-inducednecroptosisandchemotherapeuticagent-inducedcelldeath.celldeath&disease6:e1636)。tnf也是先天性和适应性免疫反应的激活剂,例如通过激活抗肿瘤cd8+t细胞和nk细胞(kashii,y,giorda,r,herberman,r.b,whiteside,t.l.vujanovic,n.l.constitutiveexpressionandroleofthetnffamilyligandsinapoptotickillingoftumorcellsbyhumannkcells.j.immunol.163,5358–5366;prevost-blondel,a,roth,e.,rosenthal,f.pircher,h.2000crucialroleoftnf-αincd8cell-mediatedeliminationof3ll-a9lewislungcarcinomacellsinvivo.j.immunol.164,3645–3651)。tnf最初被认为是潜在的抗肿瘤特效药。尽管在小鼠中进行tnf全身性注射的初步实验似乎支持了这种乐观论,但从实验室到临床的转变表明,tnf不仅是免疫系统的激活剂,而且在使用可溶性配体进行全身性治疗的患者中引起严重的全身性毒性。研究还表明,这种全身性tnf治疗没有在患者中诱导出与已在小鼠模型中观察到的相当的抗肿瘤效果(balkwill,f.tumornecrosisfactorandcancer.2009naturereviewscancer9,361)。
溶瘤病毒疗法已经重新成为一种可行的治疗策略(russellsj,pengk-w,belljc.2012.oncolyticvirotherapy.naturebiotechnology30:658-670)。尽管利用溶瘤病毒疗法治疗癌症的想法可以追溯到一个世纪以前,但仅在过去的二十年中,它已逐步成为治疗对标准疗法难以治疗的人类肿瘤的更可行的疗法(kellye,russellsj.2007.historyofoncolyticviruses:genesistogeneticengineering.moleculartherapy15:651-659)。
溶瘤病毒是被设计和/或选择其选择性感染和杀死转化的癌细胞的能力,以及其激活不仅针对病毒而且针对肿瘤抗原的宿主免疫系统的能力的哺乳动物病毒(lichtybd,breitbachcj,stojdldf,belljc.2014.goingviralwithcancerimmunotherapy.naturereviewscancer14:559-567)。粘液瘤病毒(myxv)是痘病毒科和兔痘病毒属(leporipoxvirus)的成员(chanwm,rahmanmm,mcfaddeng.2013.oncolyticmyxomavirus:thepathtoclinic.vaccine31:4252-4258;chanwm,mcfaddeng.2014.oncolyticpoxviruses.annualreviewofvirology1:191-214)。实际上,myxv是兔特异性的,不会在人类或小鼠中引起感染或疾病。然而,由于与致癌作用相关的癌症途径突变的性质,来自小鼠和人的大多数(如果不是全部)癌细胞总是失去其抵抗许多病毒(包括myxv)感染的先天能力的要素(chanwm,mcfaddeng.2014.oncolyticpoxviruses。annualreviewofvirology1:191-214;sypulaj,wangf,may,bellj,mcfaddeng,2004,myxomavirustropisminhumantumorcells。genethermolbiol8:103-114)。该系统中生物学的另一个特征是庞大且遗传稳定的痘病毒基因组,可以通过多种治疗性转基因进行基因操作(nayerossadatn,maedeht,alipa,2012,viralandnonviraldeliverysystemsforgenedelivery.advancedbiomedicalresearch1)。如本文所公开的,任选地切除调节不同形式的免疫调节和/或细胞死亡的myxv基因,并引入治疗性抗癌转基因以诱导增加免疫原性和/或诱导优选形式的癌细胞死亡。
工程化的粘液瘤病毒及其使用方法
在某些实施方案中,本文公开的内容包括编码外源性tnf蛋白的工程化的粘液瘤病毒。在一些情况下,粘液瘤病毒包括在一个或多个与兔细胞向性相关的基因处或附近的修饰。在一些情况下,一个或多个与兔细胞向性相关的基因包括m11l、m063、m135r、m136r、m-t2、m-t4、m-t5或m-t7。在一些情况下,一个或多个与兔细胞向性相关的基因包括m135r、m136r或其组合。
在一些情况下,本文公开的内容包括工程化的粘液瘤病毒(myxv),其被工程化以表达tnf蛋白,其中myxv包含m135r基因的修饰。在一些情况下,修饰是一种缺失,其损害了由m135r基因编码的蛋白质的功能。在一些情况下,修饰是m135r基因的部分缺失(例如,10%、20%、30%、40%、50%、60%、70%、80%、90%或95%缺失)。在其他情况下,修饰是m135r基因的完全缺失。在另外的情况下,修饰是用tnf蛋白替代m135r基因。在其他情况下,工程化的myxv是vmyx-m135ko-htnf。在其他情况下,工程化的myxv是如图2a所示的vmyx-m135ko-htnf。
在一些情况下,本文公开的内容包括工程化的粘液瘤病毒(myxv),其被工程化以表达tnf蛋白,其中将tnf蛋白插入myxv基因组内的m135r基因和m136r基因之间。在一些情况下,工程化的myxv是vmyx-htnf-m135-136。在一些情况下,工程化的myxv是如图2b所示的vmyx-htnf-m135-136。
在一些情况下,tnf蛋白包含至少90%、95%、96%、97%、98%或99%,诸如在95%至98%之间、95%和99%之间,包括90%、91%、92%、93%、94%、95%、96%、97%、98%、99%的序列同一性或包含如uniprotkb-p01375中所示的序列,该uniprotkb-p01375公布于2019年7月3日(条目版本247),并通过引用并入本文。在一些情况下,tnf蛋白是可溶性tnf,其包含与uniprotkb-p01375的残基77-233的至少90%、95%、96%、97%、98%或99%,诸如在95%至98%之间、95%和99%之间,包括90%、91%、92%、93%、94%、95%、96%、97%、98%、99%的序列同一性。在一些情况下,可溶性tnf包含uniprotkb-p01375的残基77-233。
在一些情况下,包含tnf蛋白的工程化的myxv还包含荧光蛋白。示例性的荧光蛋白包括蓝色/紫外蛋白,诸如tagbfp、azurite、sirus或sapphire;青色蛋白,诸如ecfp、cerulean或mturquoise;绿色蛋白,诸如绿色荧光蛋白(gfp)、emerald、mukg、mwasabi或clover;黄色蛋白,诸如eyfp、citrine、venus或syfp2;橙色蛋白,诸如单体kusabira-orange、mko2或morange;红色蛋白,诸如mraspberrymmcherry、mstrawberry、mtangerine、tdtomato、mapple或mruby;光活化蛋白,诸如pa-gfp、pamcherry1或patagrfp和可光转换蛋白诸如dropna。
在某些实施方案中,本文还描述了一种癌症治疗方法,其使用与溶瘤性粘液瘤病毒(myxv)结合诱导的tnf表达(例如,跨膜tnf蛋白或可溶性tnf蛋白)。如上所述,已显示分泌的tnf是抗肿瘤分子,但是由于其小的治疗窗口和严重的副作用,因此不适合全身使用。此外,溶瘤性myxv已被证明是一种针对多种肿瘤类型具有广泛向性的肿瘤特异性抗肿瘤药。在一些情况下,本文公开了经修饰以例如在病毒感染的肿瘤细胞表面即感染细胞表面表达htnf;或作为分泌性变体的myxv。为了获得本文公开的效果,可以将溶瘤性myxv工程化为从重组myxv构建体(通常称为vmyx-htnf)表达人tnf,作为在强病毒特异性启动子下在病毒感染的细胞中表达的免疫配体。基于myxv的tnf表达的优点是配体仅在被病毒感染的肿瘤组织中表达,并且其表达量低,从而消除了在可溶性tnf配体的全身递送中观察到的严重副作用。
在一些情况下,使用技术人员已知的、并且在例如sambrook等人((2001)molecularcloning:alaboratorymanual,第3版,(coldspringharbourlaboratorypress)中描述的标准分子生物学技术,粘液瘤病毒基因组容易被修饰以表达一种或多种治疗性转基因。技术人员将能够容易地确定粘液瘤病毒基因组的哪些部分可以被删除,使得该病毒仍然能够进行生产性感染,例如提供具有复制能力的病毒。例如,病毒基因组中可被删除的非必需区域可通过比较已发表的病毒基因组序列与其它特征明确的病毒的基因组来推断(参见例如,c.cameron,s.hota-mitchell,l.chen,j.barrett,j.-x.cao,c.macaulay,d.willer,d.evans和g.mcfadden,virology(1999)264:298-318))。因此,本公开内容的方面涉及用于在有需要的受试者中抑制和/或治疗癌症的方法。在某些实施方案中,所述方法包括向受试者诸如人受试者施用表达肿瘤坏死因子(tnf)(例如,跨膜tnf蛋白或可溶性tnf蛋白)的myxv,从而治疗和/或抑制有需要的受试者的癌症。在某些实施方案中,所述myxv包括vmyx-m135ko-htnf。在某些实施方案中,所述myxv包括vmyx-htnf-m135-136。在某些实施方案中,所述myxv包括vmyx-sodko-htnf。在某些实施方案中,所述受试者是人受试者。在某些实施方案中,该方法还包括选择患有或疑似患有癌症的受试者,诸如人受试者。在某些实施方案中,myxv是全身性施用的。在某些实施方案中,myxv在肿瘤和/或转移部位施用。myxv已被证明感染先天性抗病毒应答缺陷的细胞。如本文所用,具有“先天性抗病毒应答缺陷”是指当暴露于病毒或被病毒侵袭时不诱导抗病毒防御机制的细胞,该机制包括抑制病毒复制、干扰素产生、干扰素反应途径的诱导和凋亡。该术语包括与正常细胞(例如,未感染或非癌细胞)相比,在暴露于病毒或被病毒感染后具有降低的或有缺陷的先天性抗病毒应答的细胞,诸如癌细胞。这包括对干扰素无反应的细胞,以及凋亡反应或诱导的凋亡途径减少或有缺陷的细胞。该缺陷可能由多种原因引起,包括感染、遗传缺陷或环境压力。然而,将理解的是,当缺陷由预先存在的感染引起时,myxv的过度感染可以被排除,并且技术人员可容易地识别出这种情况。技术人员无需过多实验即可容易地确定任何给定的细胞类型是否均具有先天性抗病毒应答缺陷,因此确定是否可被myxv感染。因此,在本方法的某些实施方案中,myxv能够感染具有先天性抗病毒应答缺陷的细胞。在一个实施方案中,细胞对干扰素无反应。在特定的实施方案中,细胞是哺乳动物癌细胞。在一个实施方案中,细胞是包括人类实体瘤细胞的人类癌细胞。
myxv可以是属于具有复制能力的痘病毒的兔痘病毒属种的任何病毒。myxv可以是myxv的野生型菌株,也可以是myxv的基因修饰菌株。在一些情况下,myxv是lausanne菌株。在一些情况下,myxv是在南美森林兔(sylvilagusbrasiliensis)中传播的南美myxv菌株。在一些情况下,myxv是在丛毛棉尾兔(sylvilagusbachmani)中传播的加利福尼亚州myxv菌株。在一些情况下,myxv为6918,是减毒的西班牙野生型菌株,其包含在基因m009l、m036l、m135r和m148r中的修饰(基因库登录号eu552530,在此通过引用并入,由基因库在2019年7月11日提供)。在一些情况下,myxv是6918vp60-t2(基因库登录号eu552531,在此通过引用并入,由基因库在2019年7月11日提供)。在一些情况下,myxv是一种称为标准实验室菌株(sls)的菌株。
在一些情况下,myxv与cameron等人,“thecompletednasequenceofmyxomavirus”,virology264:298-318(1999)(其通过引用整体并入本文)中公开的序列具有至少90%、95%或99%的序列同一性。在一些情况下,myxv包含cameron等人,“thecompletednasequenceofmyxomavirus”,virology264:298-318(1999)中公开的序列。
在某些实施方案中,具有先天性抗病毒应答缺陷的细胞包括癌细胞。在某些实施方案中,用myxv感染的细胞表达tnf。在一些情况下,在表面表达tnf。在一些情况下,tnf是一种可溶性tnf。如本文所公开的,针对肺转移所证明的功效结果通过扩展适用于其他实体癌,包括原发性的和转移性的实体癌。tnf既可以是癌细胞的强大杀伤细胞,又可以是针对肿瘤细胞的先天性和适应性免疫应答的激活剂。根据有关病毒和tnf生物学的已知知识,将该病毒应用于广谱肿瘤类型,为治疗多种癌症类型提供了理想的候选方案。可以使用本领域普遍接受的标准来诊断癌症,包括恶性肿瘤的存在。
可以根据所公开的方法治疗的癌症类型包括但不限于实体瘤,诸如肉瘤和癌,包括但不限于纤维肉瘤、粘液肉瘤、脂肪肉瘤、软骨肉瘤、骨肉瘤、成骨肉瘤和其他肉瘤、滑膜瘤、间皮瘤、尤文肉瘤、平滑肌肉瘤、横纹肌肉瘤、结肠癌、淋巴恶性肿瘤、胰腺癌、乳腺癌、肺癌、非小细胞肺癌、卵巢癌、前列腺癌、肝细胞癌、鳞状细胞癌、基底细胞癌、腺癌、汗腺癌、皮脂腺癌、乳头状癌、乳头状腺癌、髓样癌、支气管癌、肾细胞癌、肝癌、胆管癌、绒毛膜癌、肾母细胞瘤、宫颈癌、睾丸肿瘤、膀胱癌和cns肿瘤(例如,神经胶质瘤、星形细胞瘤、髓母细胞瘤、颅神经胶质瘤、室管膜瘤、松果体瘤、血管母细胞瘤、听神经瘤、少突神经胶质瘤、血管瘤、黑色素瘤、神经母细胞瘤和视网膜母细胞瘤)。在某些实施方案中,所述癌症是实体瘤。在一些实施方案中,所述癌症已经转移到所述受试者中的第二位置。在某些实施方案中,所述第二位置包括所述受试者的肺、脑、肝和/或淋巴结。在某些实施方案中,所述癌症包括骨肉瘤、三阴性乳腺癌或黑色素瘤。
在一些实施方案中,癌的类型还包括血液学癌症,诸如霍奇金淋巴瘤或非霍奇金淋巴瘤。
当施用给受试者时,表达tnf的myxv(诸如细胞表面表达的tnf或可溶形式)的有效量是在所述剂量下和足够的时间段内,病毒减轻、改善、缓和、缓解、稳定、防止疾病的扩散、减缓或延迟疾病的进展或治愈疾病(诸如癌症,例如,已转移至肺、脑、肝或任何其它器官的实体瘤)所需的量。例如,其可以是足以实现减少癌细胞或赘生性细胞的数量或将其破坏,或减少长期感染病毒的细胞的数量或将其破坏,或抑制这种细胞的生长和/或增殖和/或减少转移的数量和/或部位的效果的量。
施用于受试者的有效量可以根据许多因素而变化,诸如myxv的药效学特性、施用方式、受试者的年龄、健康和体重、疾病状态的性质和程度、治疗频率和同时治疗(如果有的化)的类型以及病毒的毒力和效价。
myxv最初可以以合适的量施用,该量可以视需要根据受试者的临床反应进行调整。病毒的有效量可凭经验确定,取决于可以安全施用的myxv的最大量,以及产生期望结果的病毒的最小量。
可以使用标准施用方法将myxv施用给受试者,在一个实施方案中,病毒是全身施用的。在另一个实施方案中,通过在疾病部位注射来施用病毒。在各种实施方案中,病毒可以口服或肠胃外或通过本领域已知的任何标准方法施用。
为了在全身施用病毒时产生与通过在疾病部位注射病毒所获得的相同的临床效果,可能需要施用明显更高量的病毒。然而,适当的剂量水平应为可实现期望结果的最小量。
待施用的病毒浓度将根据待施用的myxv的特定菌株的毒力以及所靶向的细胞的性质而变化。在一个实施方案中,将小于约3x1010个病灶形成单位(“ffu”)的剂量(也称为“感染单位”)施用于人受试者,在各种实施方案中,可以单剂量施用约102至约109pfu、约102至约107pfu、约103至约106pfu或约104至约105pfu。
表达tnf的myxv,诸如细胞表面表达的tnf或可溶形式可作为单独的疗法施用,或者可以与包括化学疗法、免疫疗法和/或放射疗法的其他疗法结合施用。例如,表达tnf的myxv可以在原发性肿瘤手术切除之前或之后施用,或者在治疗诸如施用放射治疗或常规化学治疗药物之前、同时或之后施用。
在一些实施方案中,免疫疗法包含免疫调节剂。示例性的免疫检查点调节剂包括但不限于pd-l1抑制剂,诸如来自astrazeneca的德瓦鲁单抗(durvalumab)(imfinzi)、来自genentech的阿特珠单抗(atezolizumab)(mpdl3280a)、来自emdserono/pfizer的阿维鲁单抗(avelumab)、来自cytomxtherapeutics的cx-072、来自novartispharmaceuticals的faz053、来自3dmedicine/alphamab的kn035、来自elililly的ly3300054或来自emdserono的m7824(抗pd-l1/tgfβtrap);pd-l2抑制剂,诸如glaxosmithkline的amp-224(amplimmune)和rhigm12b7;pd-1抑制剂,诸如来自bristol-myerssquibb的纳武单抗(nivolumab)(opdivo)、来自merck的派姆单抗(pembrolizumab)(keytruda)、来自agenus的agen2034、来自beigene的bgb-a317、来自boehringer-ingelheimpharmaceutical的bl-754091、来自cbtpharmaceuticals的cbt-501(genolimzumab)、来自incyte的incshr1210、来自janssenresearch&development的jnj-63723283、来自medimmune的medi0680、来自macrogenics的mga012、来自novartispharmaceuticals的pdr001、来自pfizer的pf-06801591、来自regeneronpharmaceuticals/sanofi的regn2810(sar439684)或来自tesaro的tsr-042;ctla-4抑制剂,诸如来自bristolmeyerssquibb的伊匹木单抗(也称为
在一些实施方案中,表达tnf的myxv被配制为药物组合物中的成分。因此,在另一个实施方案中,提供了一种药物组合物,其包含表达tnf的粘液瘤病毒和药学上可接受的赋形剂或稀释剂。该组合物可常规地包含药学上可接受浓度的盐、缓冲剂、防腐剂和各种相容性载体。
药物组合物可以另外包含另外的治疗剂,诸如另外的抗癌剂。在一个实施方案中,组合物包括化学治疗剂。例如,化学治疗剂可以是基本上是任何对受试者的癌细胞或赘生性细胞表现出溶瘤作用并且不抑制或减少表达tnf的myxv的肿瘤杀灭作用的药剂。例如,化学治疗剂可以是但不限于蒽环类抗生素、烷基化剂、烷基磺酸盐、氮丙啶、乙烯亚胺、甲基三聚氰胺、氮芥、亚硝基脲、抗生素、抗代谢药、叶酸类似物、嘌呤类似物、嘧啶类似物、酶、鬼臼毒素、含铂试剂或细胞因子。优选地,化学治疗剂是已知对癌的或赘生性特定细胞类型有效的化学治疗剂。
在一些情况下,另外的治疗剂包括免疫检查点调节剂,例如如上所述的免疫检查点调节剂。
药学上可接受的赋形剂或稀释剂的比例和身份取决于所选择的施用途径、与活病毒的相容性和标准药学实践。通常,药物组合物将与不会显著损害表达tnf的myxv的生物学特性的组分一起配制。所述药物组合物可通过已知的制备适于施用于受试者的药学上可接受的组合物的方法来制备,使得有效量的一种或多种活性物质与药学上可接受的媒介物在混合物中结合。合适的媒介物在例如remington'spharmaceuticalsciences(remington'spharmaceuticalsciences,mackpublishingcompany,easton,pa.,usa1995)中记载。在此基础上,该组合物包括但不仅限于表达tnf的myxv结合一种或多种药学上可接受的赋形剂、媒介物或稀释剂的溶液,并包含在具有合适ph值和与生理液等渗的缓冲溶液中。
如本领域技术人员将理解的,取决于所选择的施用途径,可以将药物组合物以多种形式施用于受试者。在一些情况下,该药物组合物是全身施用的。在其他情况下,药物组合物是局部施用的。在一些情况下,药物组合物是口服施用的。在另外的情况下,药物组合物是肠胃外施用的。肠胃外施用包括静脉内、腹膜内、皮下、肌内、经上皮、鼻、肺内、鞘内、直肠和局部施用方式。肠胃外施用可以通过在选定的时间段内连续输注来进行。
药物组合物可以例如与惰性稀释剂或载体一起口服施用,或者可以将其封装在硬壳或软壳明胶胶囊中,或者可以将其压制成片剂。对于口服治疗性施用,可以将表达tnf的myxv与赋形剂结合,并以可摄取的片剂、颊含片、锭剂、胶囊剂、酏剂、混悬剂、糖浆剂、薄片剂等形式使用。
表达tnf的myxv溶液可以在生理上合适的缓冲液中制备。在正常的储存和使用条件下,这些制剂含有防止微生物生长但不会使活病毒灭活的防腐剂。本领域技术人员将知道如何制备合适的制剂。用于选择和制备合适制剂的常规程序和成分记载于例如remington'spharmaceuticalsciences和theunitedstatespharmacopeia:thenationalformulary(usp24nf19),1999年出版。所使用的药物组合物的剂量取决于所治疗的特定病况、病况的严重程度、个体受试者参数(包括年龄、身体情况、大小和体重)、治疗持续时间、同时治疗(如果有的话)的性质、具体的施用途径和健康从业者的知识和专业技能范围内的其它类似因素。在某些实施方案中,可将治疗性病毒冷冻干燥以在室温下储存。
表达tnf的myxv或包含表达tnf的myxv的药物组合物也可以包装成试剂盒,其包含使用表达tnf的粘液瘤病毒治疗癌症的说明书。
除了tnf的表达,还可修饰myxv以携带将增强myxv治疗的抗癌作用的任何其他基因。这样的基因可以是参与引发细胞凋亡的基因,或者参与靶向免疫破坏的感染细胞的基因,诸如修复对干扰素缺乏应答的基因,或导致刺激抗体应答的细胞表面标记物(诸如细菌细胞表面抗原)表达的基因。myxv还可以被修饰以表达参与阻断赘生性或癌细胞的增殖和生长的基因,从而防止细胞分裂。同样,病毒可以被修饰以包括治疗基因,诸如参与化学治疗剂合成的基因,或者它可以被修饰以在特定物种的细胞中具有增加的复制水平,待抑制或杀死的细胞来源于所述特定物种的细胞,例如人细胞。
如上所述,myxv能够选择性地感染具有先天性抗病毒应答缺陷的细胞,并可用作细胞中这种缺陷的指标。因此,可以使用本发明的方法测定从受试者中移除的细胞的先天性抗病毒应答的缺陷。当与其他指标结合时,这种确定可以指示受试者可能正在患有特定的疾病状态,例如癌症。可以使用已知的活检方法从包括人受试者的受试者中移除细胞。活检方法将取决于待测试的细胞的位置和类型。根据已知的培养技术培养细胞,并通过向培养基中添加活的myxv将其暴露于myxv。可以改变感染复数(“moi”),以使用已知暴露于myxv后会被感染的阳性对照细胞培养物来确定给定细胞类型、密度和培养技术的最佳moi。
添加到培养细胞中的myxv的量可以根据细胞类型、培养方法和病毒菌株而变化。可使用常规方法通过最少的测试容易地测试和调整此类参数。
可以通过本领域技术人员已知的各种方法来确定培养细胞对myxv的感染性,包括myxv引起细胞死亡的能力。它还可能涉及向细胞培养物中添加试剂,以完成与病毒表达产物的酶促或化学反应。病毒表达产物可以从已经插入myxv基因组中的报告基因表达。
在一个实施方案中,可以修饰myxv以增强检测感染状态的容易性。例如,myxv可以被遗传修饰以表达可以通过相差显微镜检查、荧光显微镜检查或放射成像容易检测的标志物。标志物可以是可能参与比色反应或放射性标记反应的表达的荧光蛋白或表达的酶。在另一个实施方案中,标志物可以是中断或抑制被测试细胞的特定功能的基因产物。
可以使用本领域已知的标准技术制备myxv。例如,病毒可以通过以下来制备:使用待用的myxv菌株感染培养的兔细胞或永生化的许可的人类或灵长类动物细胞,允许感染进展,使得病毒在培养的细胞中复制,并且可通过本领域已知的破坏细胞表面的标准方法释放,从而释放病毒颗粒用于收集。一旦收集,病毒滴度可通过感染兔细胞的汇合菌坪并进行菌斑试验来确定(参见mossman等人,(1996)virology215:17-30,其通过引用整体并入本文)。
进一步公开了一种递送策略,其中在输注诸如重新输回癌症患者之前,将治疗性myxv病毒首先离体吸附至来自骨髓或外周血单核细胞的混合白细胞。在这种策略中,表达人tnf的myxv通过预先被病毒离体感染的白细胞迁移而递送到转移性癌症部位。这种全身递送方法有时被称为“体外病毒疗法”或evv(又名ev2),因为在将病毒注入患者之前,病毒首先被递送至分离的白细胞中。myxv构建体和这种新颖的递送策略已经显示出在鼠肺转移模型中显著降低肿瘤负荷和增加存活的能力(参见实施例1)。如本文所公开的,表达细胞表面人tnf的粘液瘤病毒(myxv)的构建体的施用通过携带病毒的“载体”细胞有效地将myxv病毒递送至转移性肺疾病的位点。此外,如本文所公开的,发明人已经证明了这种表达tnf的病毒(通常称为vmyx-htnf)的细胞辅助递送具有减轻肿瘤负荷和增加患有肺部转移的小鼠的存活的能力(参见实施例1)。这些结果表明,表达tnf的myxv的细胞介导递送增加了直接杀死靶肺转移性肿瘤细胞的水平,但是(尽管不受理论约束)充当宿主免疫系统的激活剂,这可能导致癌症的长期消退。这提供了一种治疗已经转移至肺、肝、脑、骨和/或淋巴结的实体癌(已被证明用当前的治疗方法治疗有困难)的新方法。因此,在某些实施方案中,该方法包括对受试者施用单核外周血细胞和/或骨髓细胞,其中单核外周血细胞和/或骨髓细胞包括表达细胞表面肿瘤坏死因子(tnf)的myxv,从而治疗和/或抑制有需要的受试者的癌症。结合的“白细胞/vmyx-htnf”疗法导致肿瘤床中的细胞死亡增加,从而增强抗肿瘤免疫原性,但基本上仅在病毒感染的转移性肿瘤组织(如肺肿瘤组织)中原位产生tnf,以限制脱靶全身性毒副作用。下文实施例1中在鼠骨肉瘤肺转移模型中所示的测试结果表明,该策略可有效减轻肿瘤负荷并延长中位生存时间。此外,白细胞/vmyx-htnf策略代表了对于所有实体癌的新的潜在治疗方案,这些实体癌通过以癌组织限制性方式选择性表达细胞表面tnf而转移到例如肺,而与原始肿瘤类型无关。不受理论的束缚,据信这种白细胞/vmyx-htnf策略与其他已建立的针对经常转移至例如肺的实体癌的癌症疗法协同作用。在某些实施方案中,该方法包括将myxv吸附到单核外周血细胞和/或骨髓细胞的表面。可能有一部分单核外周血细胞和/或骨髓细胞被感染;然而,这在本文公开的方法中不太可能是显著的。在某些实施方案中,将粘液瘤病毒吸附到单核外周血细胞和/或骨髓细胞的表面包括在允许粘液瘤病毒结合到单核外周血细胞和/或骨髓细胞表面的条件下将单核外周血细胞和/或骨髓细胞暴露于粘液瘤病毒。
本公开内容的方面涉及用于将任何类型的溶瘤性myxv构建体递送至转移性肺疾病的新方法,即通过将治疗性myxv构建体预负载在源自诸如如上文所述的骨髓(bm)或外周血单核细胞(pbmc)的混合白细胞上。此类方法可用于治疗以存在具有先天性抗病毒应答缺陷的细胞(例如癌细胞)为特征的任何疾病状态。可修饰myxv构建体以包括任何治疗性基因或“治疗性转基因”。如本文所用,术语“治疗性基因”或“治疗性转基因”旨在广泛地描述其表达可实现期望结果例如抗癌作用的任何基因。例如,可以修饰病毒以携带将增强病毒治疗的抗癌作用的基因。这样的基因可以是参与引发细胞凋亡的基因,或者参与靶向免疫破坏的感染细胞的基因,诸如修复对干扰素缺乏应答的基因,或导致刺激抗体应答的细胞表面标志物(诸如细菌细胞表面抗原)表达的基因。该病毒还可以被修饰以表达参与阻断赘生性或癌细胞的增殖和生长的基因,从而防止细胞分裂。同样,该病毒可以被修饰以包括治疗基因,诸如参与化学治疗剂合成的基因,或者它可以被修饰以在特定物种的细胞中具有增加的复制水平,待抑制或杀死的细胞来源于所述特定物种的细胞,例如人细胞。
在某些实施方案中,将bm或pbmc细胞离体吸附myxv构建体一小时,然后将负载myxv的白细胞注回接受者中。在某些实施方案中,单核外周血细胞和/或骨髓细胞从受试者获得,例如作为自体细胞。在其他实施方案中,单核外周血细胞和/或骨髓细胞是从一个或多个异源供体获得的。获得骨髓细胞和单核外周血细胞的方法是本领域已知的。
本公开内容的方面涉及表达肿瘤坏死因子(tnf),例如,表面tnf或可溶性tnf的myxv以及包括该myxv的试剂盒。在某些实施方案中,表达tnf的myxv包括vmyx-m135ko-htnf。在某些实施方案中,表达tnf的myxv包括vmyx-htnf-m135-136。表达tnf的粘液瘤病毒或包含表达tnf的myxv的药物组合物也可以包装成试剂盒,包含使用表达tnf的myxv抑制具有免疫应答缺陷的细胞以治疗癌症的说明书。
实施例
提供这些实施例仅仅是为了说明的目的而非限制本文提供的权利要求的范围。
实施例1
该实施例描述了表达tnf的myxv的构建和测试。
病毒设计
第一个vmyx-htnf病毒版本(这里称为vmyx-sodko-htnf)最初设计和记载于wang等人,2008(wangf,gaox,barrettjw,shaoq,barteee,mohamedmr,rahmanm,werdens,irvinet,caoj.dekaban,ga,mcfadden,g.2008).rig-imediatestheco-inductionoftumornecrosisfactorandtypeiinterferonelicitedbymyxomavirusinprimaryhumanmacrophages.plospathogens4:e1000099,其特别地通过引用并入本文)。简而言之,该病毒是使用myxvlausanne亲本菌株产生的,其目的与溶瘤病毒疗法无关或用于任何癌症治疗。插入载体基于pbluescript噬菌粒,并与egfp一起克隆到131rorf(称为sod)中,由离散的合成牛痘早期晚期启动子控制(参见图1的图谱)。基于m135r基因敲除病毒平台生成了第二种表达htnf的病毒(称为vmyx-m135ko-htnf),该平台是正在开发用于人类临床试验的溶瘤myxv构建体的标准减毒遗传本体。m135r敲除构建的策略完整记载于bartee等,2009(barteee,mohamedmr,lopezmc,bakerhv,mcfaddeng.2009.theadditionoftumornecrosisfactorplusbetainterferoninducesanovelsynergisticantiviralstateagainstpoxvirusesinprimaryhumanfibroblasts.journalofvirology,83:498-511和barrettjw,sypulaj,wangf,alstonlr,shaoz,gaox,irvinets,mcfaddeng,2007m135risanovelcellsurfacevirulencefactorofmyxomavirus.journalofvirology,81(1):106-114,二者均通过引用整体并入本文)。简而言之,使用multisitegateway三片段克隆法生成该vmyx-m135ko-htnf病毒。元件1包含m134orf的3’片段以及由合成的早期/晚期启动子控制的egfp。元件2含有也在合成的早期/晚期启动子的控制下的完整的htnf编码序列。最后,元件3包含5’m136基因的片段。将这三个片段组合成单进入载体质粒(single-entryvehicleplasmid),该质粒用于将egfp-htnf串联盒插入任何myxv基因组主链的m135r基因座中。然后将其用于转染/感染,并使用至少三轮噬斑纯化(图2a所示的用于转染的最终质粒)纯化重组病毒。
动物研究
使用具有免疫能力的balb/c小鼠中的同系鼠骨肉瘤模型确认了vmyx-sodko-htnf病毒(通过已离体预负载病毒的白细胞递送)对肺转移性骨肉瘤的功效。在第0天,通过侧尾静脉用2×106个k7m2-fluc鼠骨肉瘤细胞接种动物。接种后四天,收集对照balb/c小鼠的骨髓(bm)、将其计数,并以每个有核细胞2-10个感染性病毒单位的moi(感染复数)感染病毒。使细胞和病毒在37℃下吸附1小时。然后以每只动物4x106个细胞的剂量眼球后注射离体病毒负载的bm。然后使用ivis体内成像系统对动物在每周肿瘤接种后的荧光素酶发光进行成像,作为肿瘤负荷的实时测量,其中大部分在受体肺中观察到。监测动物直至它们达到进行性疾病的预定临床症状,或直至感染后8周,以先到者为准。结果表明,除vmyx-sodko-htnf构建体的明显例外,用所有测试的病毒构建体治疗的动物均表现出与对照相当的肿瘤负荷。除了可能诱发单个长期存活者的vmyx-m135ko病毒外,其他测试病毒也未显示出与对照在统计学上可区分的平均存活率。相比之下,vmyx-sodko-htnf构建体队列在所有成像时间点,通过肿瘤细胞发光测量,其肿瘤在统计学上均小于对照和其他构建体(图3)。与对照相比,vmyx-sodko-htnf的平均存活时间也几乎增加了一倍(图4),并且仅在该队列中观察到大量的明显没有可证明的肿瘤负荷的动物。
根据这些结果,将作为病毒“载体细胞”的bm白细胞与利用大量pbmc作为载体细胞将治疗性myxv构建体递送至转移性肺肿瘤部位进行了比较。有理由认为,pbmc是大多数实体癌的临床相关性更强的载体白细胞来源。如上所述,用k7m2-fluc细胞接种动物。肿瘤接种后四天,如上所述,收集来自对照balb/c小鼠的pbmc,并用vmyx-sodko-htnf(moi=2)离体吸附一小时。然后将动物分为三个剂量组,分别为1x106、2x106和4x106pbmc(每个均用相同的输入病毒moi预吸附),并注射相应的pbmc/病毒剂量。然后从第7天开始对动物进行成像。荧光素酶成像结果显示,动物对治疗的反应呈剂量依赖性,其中与对照动物相比,1x106剂量的动物反应最小,4x106的动物显示出最显著的肿瘤发光减少(图5和图6)。
确认感染vmyx-sodko-htnf的细胞中的tnf表达
为了确认vmyxv-sodko-htnf构建体对htnf的表达,以moi为10用病毒实验性感染了许可的rk-13细胞。使感染在感染后进行48小时,然后使用非酶细胞解离缓冲液收集细胞,以确保膜结合蛋白的完整性。然后使用与pe荧光团缀合的小鼠抗人tnf抗体在仅染色细胞表面表达的分子的非透化条件下对细胞进行流式细胞术染色。然后将细胞与未感染的染色对照和未感染的未染色对照进行比对。该测定的结果证实,在感染后48小时,在vmyx-sodko-htnf感染的细胞的表面上表达了tnf,而未感染的对照细胞没有tnf表达的迹象(图7)。通过蛋白质印迹法未检测到分泌的tnf(未显示),表明感染的细胞不表达理论上可以产生分泌形式的tnf的必需的转化/切割酶。
体外细胞死亡测定
为了更好地了解在接受白细胞/vmyxv-htnf病毒治疗的荷瘤动物中观察到的引起生存改善和肿瘤负荷减小的机制,进行细胞死亡试验,以测量骨肉瘤细胞对不同试验病毒的应答。这是为了确定减小的肿瘤负荷是否由病毒表达的tnf引起的直接肿瘤细胞死亡增加所驱动。使用流式细胞术测定k7m2-fluc细胞的tnfr1和tnfr2的细胞表面表达。这些细胞对tnfr1和tnfr2均呈阳性表达,这意味着tnf可能直接与其肿瘤细胞上的同源受体相互作用,并导致tnf诱导的细胞死亡。为了确认这些细胞是否可以直接被tnf杀死,将它们实验生长并用vmyx-m135ko、vmyx-sodko-htnf感染或与纯化的鼠tnf温育。然后使用sytoxorange测量细胞的活力,sytoxorange仅在与各种形式的细胞死亡相关的细胞膜完整性丧失后才进入并染色细胞。感染/接种后24或48小时,将细胞与sytoxorange温育10分钟,用胰蛋白酶提拉,并将细胞和上清液合并在一起,将其离心以洗去过量的sytox。然后将细胞重悬于100微升dmem中,并使用细胞计数器读书。该测定的结果表明,与对照相比,在48小时时鼠tnf仅导致细胞死亡增加20%,但tnf后24小时无显著差异。相反,与对照相比,在24小时时,vmyx-sodko-htnf感染降低了20%活力,在48小时时降低了50%。这种细胞活力的降低与感染不表达htnf的对照vmyx-135ko病毒后观察到的基本上相同。这表明这些骨肉瘤细胞对htnf的杀伤没有额外的敏感性,在动物研究中观察到的肿瘤减少的增加很可能是由免疫相关机制引起的,该机制与病毒表达的tnf与骨肉瘤细胞上的tnfr1或tnfr2直接相互作用无关(图8)。
实施例2
该实施例描述了通过已经用离体病毒预载的白细胞递送的vmyx-m135ko-htnf病毒对三阴性乳腺癌的功效的测定。
使用具有免疫能力的balb/c小鼠的同系鼠三阴性乳腺癌。在第0天通过侧尾静脉用三阴性乳腺癌细胞接种动物。接种后,收集、计数来自对照balb/c小鼠的骨髓(bm),并用vmyx-m135ko-htnf和/或对照病毒感染。使细胞和病毒在37℃下吸附1小时。然后将离体病毒负载的bm进行眼球后注射。然后使用ivis体内成像系统对动物在每周肿瘤接种后的荧光素酶发光进行成像,作为肿瘤负荷的实时测量,其中大部分在受体肺中观察到。监视动物直至它们达到进行性疾病的预定临床症状。
实施例3
该实施例描述了通过已经用离体病毒预载的白细胞递送的vmyx-m135ko-htnf病毒对转移性黑色素瘤的功效的测定。
使用具有免疫能力的balb/c小鼠的同系鼠三阴性乳腺癌。在第0天,通过侧尾静脉用转移性黑色素瘤细胞接种动物。接种后,收集、计数来自对照balb/c小鼠的骨髓(bm),并用vmyx-m135ko-htnf和/或对照病毒感染。使细胞和病毒在37℃下吸附1小时。然后将离体病毒负载的bm进行眼球后注射。然后使用ivis体内成像系统对动物在每周肿瘤接种后的荧光素酶发光进行成像,作为肿瘤负荷的实时测量,其中大部分在受体肺中观察到。监视动物直至它们达到进行性疾病的预定临床症状。
实施例4
图9示出了使用流式细胞术对被感染的人aml(thp1)细胞的细胞死亡的定量。由apc/cy7+细胞群体确定myxv介导的总的杀死的thp1细胞,如通过对live/dead染色的细胞进行门控所定义。通过holm-sidakt检验进行多次比较确定显著性(*=p<0.05;**=p<0.01;***=p<0.001)。结果显示,在感染后两个时间点(24和48小时)的3个测试的感染复数(moi=10、1或0.1)下,vmyx-sodko-htnf-gfp感染thp-1细胞导致门控的死亡细胞的总数增加。
图10示出了使用流式细胞术对myxv介导的靶点杀死的病毒感染的人aml(thp1)细胞的定量。从apc/cy7+细胞的比例确定了myxv介导的thp1细胞“靶点”杀死,该比例来自对gfp阳性的病毒感染细胞群体进行门控。通过holm-sidakt检验进行多次比较确定显著性(*=p<0.05;**=p<0.01;***=p<0.001)。结果表明,当thp1细胞感染任何一种测试病毒时,无论是对照病毒还是表达tnf的构建体,被病毒感染的死亡细胞的检测都非常相似。该结果与一般观察结果一致,即myxv杀死感染细胞的能力在很大程度上是病毒平台的结果,并且相对不受包括tnf的大多数转基因的影响。
图11示出了使用流式细胞术对myxv诱导的脱靶杀死的未感染的人aml(thp1)细胞的定量。从apc/cy7+细胞的比例确定myxv介导的脱靶杀死的thp1细胞,该比例来自对gfp阴性细胞群体进行门控。通过holm-sidakt检验进行多次比较确定显著性(*=p<0.05;
**=p<0.01;***=p<0.001)。结果表明,与非武装的(unarmed)
myxv对照感染相比,htnf转基因的表达诱导了未感染thp1细胞的大量杀死。
图12示出了使用流式细胞术对被感染的人多发性骨髓瘤(u266)细胞的细胞死亡的定量。从apc/cy7+细胞群体确定myxv介导的总的杀死的u266。通过holm-sidakt检验进行多次比较确定显著性(*=p<0.05;**=p<0.01;***=p<0.001)。结果显示,在感染后两个时间点(24和48小时)的3个测试的感染复数(moi=10、1或0.1)下,vmyx-sodko-htnf-gfp感染u266细胞导致门控的死亡细胞的总数增加。
图13示出了在具有免疫能力的小鼠中通过离体负载的同系鼠骨髓白细胞递送的vmyx-sodko-htnf的测试,以消除预先接种的鼠多发性骨髓瘤。由于多发性骨髓瘤的转基因鼠vk*myc模型是一种非常具有侵略性和耐药性的模型,因此使用myxv病毒的病毒疗法与使用骨髓白细胞的自体干细胞移植(asct)结合使用以提高无癌存活率。图13a示出了使用移植到c57/b1小鼠中的抗硼替佐米的vk*12598骨髓瘤细胞的体内数据,其中它们主要迁移至骨髓和脾。简而言之,将1×106的vk*12598骨髓瘤细胞通过尾静脉静脉内(i.v.)递送到具有免疫能力的c57bl/6小鼠中。癌递送后四天,对小鼠进行如下治疗:不接受骨髓(bm)移植的对照;仅2x106个bm细胞;用vmyx-m135ko非武装的粘液瘤病毒(moi=10)离体预处理的2x106个bm细胞;通过眼球后(ro)注射用vxx-sodko-htnf(moi=10)离体处理的2x106个bm。在癌植入后100天产生生存曲线(图13b)。图13c对应于存活百分比。
图14示出了将vmyx-htnf-(m135-m136)离体预负载在具有smac拟态或免疫检查点抑制剂的bm白细胞上的组合疗法。将smac模拟化合物lcl161(50mg/kg)或检查点抑制剂单克隆抗体(mab)α-mupd-1与通过离体预负载的自体小鼠骨髓白细胞递送的vmyx-htnf-(m135-m136)组合,测试组合疗法。简而言之,将1×106的vk*12598鼠骨髓瘤细胞通过尾静脉静脉内(i.v.)递送到具有免疫能力的c57bl/6小鼠中。四周后,使用血清蛋白电泳(spep)对血清中骨髓瘤蛋白标志物的水平(例如,m峰(m-spike))进行定量。然后在第1、4、8和11天,以moi=10使用已经用vmyx-htnf-(m135-m136)进行离体预处理的2x106个bm细胞治疗小鼠。每次自体移植后,在第2、5、9、12天通过口服管饲50mg/kglcl161进行化学疗法或通过腹膜内(i.p.)注射10mg/kgmabα-mupd-1进行免疫疗法。图14b示出了包括生存曲线的体内数据。图14c描述了存活百分比。
图15示出了人tnf蛋白的表达和被vmyx-htnf-(m135-136)感染的人细胞的部分分泌。两种人类细胞系:以三种不同的感染复数(moi),用vmyx-htnf-(m135-136)和对照vmyx-gfp感染thp1(人单核细胞)和a549(人肺癌)。感染后48小时后,收集上清液,并通过elisa(biolegend)测定从病毒感染的细胞分泌的可溶性人tnf的水平。
实施例5
vmyx-htnf-m135-m136病毒是使用myxvmultisitegateway亲本菌株产生的。简而言之,使用multisitegateway三片段克隆法生成vmyx-htnf-m135-m136病毒。元件1包含m134r-部分和m135rorf的3’片段,以及由合成的早期/晚期启动子控制的egfp。元件2含有也在合成的早期/晚期启动子的控制下的完整的htnf编码序列。元件3包含5’m136r基因的片段。将这三个片段组合成单进入载体质粒,该质粒用于将egfp-htnf串联盒插入myxv基因组主链中m135r和m136r基因之间的基因间位置。然后将其用于转染/感染,并使用至少三轮噬斑纯化(图2b所示的用于转染的最终质粒)纯化重组病毒。
表1中示出了与本文所述的组合物和方法相对应的示例性序列。
表1
在一些情况下,myxv(lausanne菌株)包含基因库所示的序列:af170726.2(在此通过引用并入,由基因库在2019年7月11日提供)。
在一些情况下,vmyx-htnf-m135-136包含如图2b所示排列的seqidno:1-5。在一些情况下,vmyx-htnf-m135-136包含lausanne菌株主链,任选地包含基因库所示的序列:af170726.2。
在一些情况下,vmyx-m135ko-htnf包含如图2a所示排列的seqidno:6、2、4和5。在一些情况下,vmyx-m135ko-htnf包含lausanne菌株主链,任选地包含基因库所示的序列:af170726.2。
虽然本文已经示出和描述了本发明的优选实施方案,但对于本领域技术人员容易理解的是,这样的实施方案只是以示例的方式提供的。本领域技术人员现将会在不偏离本发明的情况下想到许多更改、改变和替代。应当理解,本文中描述的本发明实施方案的各种替代方案可用于实施本发明。以下权利要求书旨在限定本发明的范围,并因此覆盖这些权利要求书范围内的方法和构造物及其等效项。
- 还没有人留言评论。精彩留言会获得点赞!