一种利用微生物诱导碳酸钙沉淀的方法与流程
本发明涉及一种利用微生物诱导碳酸钙沉淀的方法。
背景技术:
微生物诱导碳酸钙沉淀(micp)是脲酶催化尿素水解改良土壤的一种创新方法,随着微生物学、地球化学、土木工程学等学科间的交叉研究的不断发展,微生物诱导碳酸钙沉积技术已逐步应用于各个领域中,该技术对于软土地基强度与稳定性的改善具有很好的作用。
目前,关于micp的研究主要集中在三个方面,一是着重于通过micp的生物矿化来提高水泥胶凝材料的强度和耐久性。micp通过钙碳沉淀在原位胶凝;一是关注由micp引起的碳酸钙矿物沉淀,它们以三种非水化碳酸钙晶体的形式出现:方解石、霰石和vaterite。有研究者发现方解石产自micp,也有学者考虑了由pumilus芽孢杆菌诱导的vaterite生物沉淀,也有学者考虑了mg/ca在4和6摩尔比下诱导的霰石;一是砂土固结方面,通过碳酸钙沉淀固结土体对于提高土体的力学性能具有明显的作用。
在对micp反应的研究过程中,钙离子的沉淀速率及沉淀量该过程的关键因素之一。该过程中,若钙离子沉降速率慢或沉淀量偏少,则不仅会降低反应速率、也会完成钙资源的浪费。
技术实现要素:
针对现有技术中存在的问题,本发明提供了一种利用微生物诱导碳酸钙沉淀的方法。该方法通过钠蒙脱土(na-mmt)与反应液、细菌悬浮液之间的相互作用,钠蒙脱土能够明显加速ca的沉积,增加沉积碳酸钙的总质量,且增加反应液用量时仍然能够使micp较好的向前进行;还能够吸附细菌、降低固结砂样的水导率。
本发明提供了一种利用微生物诱导碳酸钙沉淀的方法,该方法包括:将产脲酶菌与含钙反应液混合得到总胶凝液,总胶凝液与钠蒙脱土混合后进行微生物诱导碳酸钙沉淀。
任选地,所述产脲酶菌为巴氏芽孢杆菌(如保藏号为atcc11859);所述产脲酶菌可以含水的菌悬浮液的形式提供,优选所述菌悬浮液od600=1.0;所述od的测定可以是在室温下、以水为对照测得的,优选地,光在样本中经过的距离可为1cm;所述含钙反应液为水溶液。
任选地,所述钠蒙脱土占总胶凝液的质量百分比为0.25%~1%,如0.25%、0.5%、0.75%或1%。优选地,所述钠蒙脱土占总胶凝液的质量百分比为0.25%~0.5%,更优选地,所述钠蒙脱土占总胶凝液的质量百分比为0.25%。
任选地,所述产脲酶菌悬浮液的制备具体如下:将15g/l的酪蛋白蛋白胨、5g/l的大豆蛋白胨、5g/l的nacl和20g/l的尿素分别加入到1000ml去离子水中,制成培养基,培养基在121℃条件下灭菌30min;细菌在30℃、转速为120rpm条件下,培养基中进行需氧培养48小时;培养完成后,4℃、离心8min,成球;1000ml去离子水中重悬细菌球,得细菌悬浮液、备用。
任选地,所述含钙反应液含有水溶性钙和尿素;水溶性钙与尿素的浓度可相等。
任选地,所述水溶性钙与尿素的浓度均为0.25mol/l。
任选地,所述的水溶性钙为cacl2。
任选地,所述产脲酶菌菌悬浮液与含钙反应液的质量比为1:4。
本发明还公开了上述方法在砂粒固结或土壤改良中的应用。
本发明具有以下有益效果:
采用微生物沉淀碳酸钙反应中,反应液的增加不利于反应的正向进行,直接降低了待沉淀钙离子的量。本发明则通过钠蒙脱土的加入、在钠蒙脱土与反应液及尿素相互作用的条件下,加速了钙离子的沉淀、且使得钙离子能够达到完全沉淀的效果,并在反应液量较多的条件下仍然能够使反应正向进行、使钙离子完全沉淀,明显提高该反应中碳酸钙的沉淀量。钠蒙脱土的存在能够使尿素完全分解,钙离子完全反应形成碳酸钙沉淀。
在钠蒙脱土的存在下,钙离子完全沉积所需时间与无钠蒙脱土加入相比,能够缩短15小时以上,即在能够使钙离子完全反应形成碳酸钙沉淀的条件下非常明显的提高了该反应的效率,具有更大的实际应用价值。
在钠蒙脱土的存在下,反应液中细菌对于钙离子的吸附能力提高62%以上,在反应液量较多的条件下仍然能够达到较高的吸附量,更有利于钙离子的沉淀,克服了现有技术中反应液量较大时不利于反应正向进行的技术问题,且能够使沉淀均匀,固结均一。
钠蒙脱土可以在micp反应过程中实现晶体的团聚,对于生物胶结具有重要的影响。而且钠蒙脱土存在下沉淀的碳酸钙能够更好的防治溶液的渗入,具有良好的防渗效果,更好的提高了其工业应用价值。
附图说明
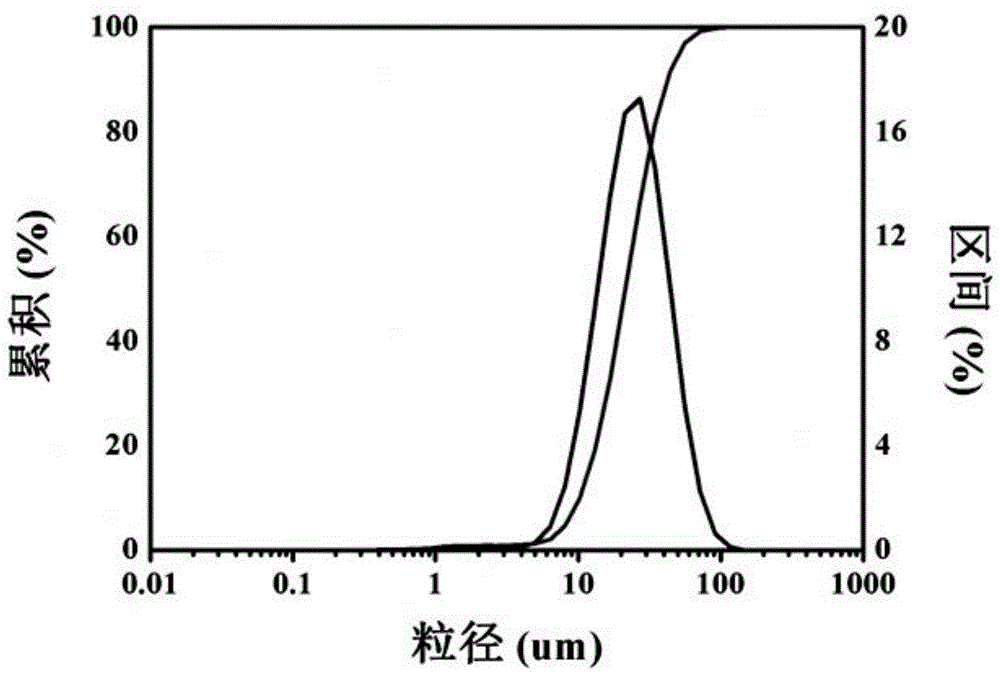
图1表示所用钠蒙脱土的粒径分布图;
图2表示在不同钠蒙脱土加入量条件下、胶凝液中钙离子浓度的变化图;
图3表示不同钠蒙脱土加入量条件下、胶凝液的ph值变化图;
图4表示加入不同量钠蒙脱土的胶凝液中、对细菌的吸附能力;
图5表示加入不同量钠蒙脱土的胶凝液中碳酸钙沉淀总量变化图;
图6表示碳酸钙总质量随钠蒙脱土浓度的变化;
图7表示不同浓度钠蒙脱土对水电导率的影响;
图8(a)表示没有钠蒙脱土存在下碳酸钙沉淀固结沙粒扫描图,图8(b)表示图8(a)的局部放大图,图8(c)表示在钠蒙脱土存在下碳酸钙沉淀固结沙粒扫描图,图8(d)表示图8(c)的局部放大图;
图9为所得碳酸钙沉淀的xrd图;图9(a)为在未加入钠蒙脱土的条件下微生物诱导所得碳酸钙沉淀的xrd图;图9(b)为加入0.25%钠蒙脱土的条件下微生物诱导所得碳酸钙沉淀的xrd图;
图10表示在不同胶凝液条件下对于细菌的吸附量变化图;
图11表示在不同胶凝液存在条件下、碳酸钙沉淀量变化图;
图12表示不同胶凝液条件下不加钠蒙脱土所得碳酸钙的sem图,胶凝液为100g(a)、200g(b)、300g(c)、400g(d);
图13表示不同胶凝液条件下加入0.25%钠蒙脱土所得碳酸钙的sem图,胶凝液为100g(a)、200g(b)、300g(c)、400g(d)。
具体实施方式
下面通过具体实施方式对本发明进行更加详细的解释说明,但并不用于对本发明保护范围的限制。
巴氏芽孢杆菌:atcc11859(保藏号),购买。
尿素、氯化钙(cacl2)、氯化钠(nacl)、酪蛋白蛋白胨、大豆蛋白胨均购自中国上海国药控股化学试剂有限公司;752型紫外可见分光光度计购自上海舜宇恒平科学仪器有限公司。
钠蒙脱土购自浙江丰鸿新材料有限公司,该钠蒙脱土的粒径分布如图1所示;
悬浮培养基的配置:将酪蛋白胨(15g/l)、大豆蛋白胨(5g/l)、nacl(5g/l)和尿素(20g/l)分别加到1000ml去离子水中,调节ph值至7.3,在121℃下灭菌30分钟。
巴氏芽孢杆菌悬液的制备:将巴氏芽孢杆菌atcc11859接种于100l悬浮培养基中,以120转/分的转速在30℃的培养基中培养48小时,获得的菌悬液在4℃离心8分钟、成球,将细菌颗粒悬浮在1000ml去离子水中,以备稀释使用。
取上述巴氏芽孢杆菌atcc11859悬液2l,用去离子水稀释其od600为1.0,以备使用,其中od的检测方法为:将紫外可见分光光度计的波长调至600nm,以水为对照样,在室温下检测菌液的od值,比色皿尺寸为:长1cm,宽1cm,高5cm。
本发明提供的利用微生物诱导碳酸钙沉淀的方法,具体包括以下步骤:
s1、按照上述步骤制备巴氏芽孢杆菌菌悬液;
s2、取cacl2溶液与尿素溶液混合均匀,得到含钙反应液,所得含钙反应液中cacl2及尿素的摩尔浓度均为0.25mol/l;
s3、室温下,将步骤s1的菌悬液与步骤s2的含钙反应液按照1:4的质量比进行混合,得到总胶凝液,混合后向总胶凝液中加入不同质量百分比的钠蒙脱土混合均匀,进行钙离子的沉淀。
对于不同钠蒙脱土加入量的实施例,具体如下:
在该步骤中,具体的,取60g的巴氏芽孢杆菌菌悬液与240g的反应液进行混合。制备5份相同的胶凝液,每份胶凝液中分别加入占胶凝液总质量0%、0.25%、0.5%、0.75%、及1%的钠蒙脱土进行碳酸钙沉淀。对每份加入不同钠蒙脱土的胶凝液的沉淀过程进行以下检测(均采用常规方法进行检测)。
(1),对不同钠蒙脱土加入量的胶凝液中钙离子浓度变化进行检测,结果如图2所示。由图2可得,在钠蒙脱土加入质量占胶凝液质量的百分比为0.25%时,钙离子浓度下降最快,钙离子完全沉淀所用时间与钠蒙脱土加入量为0%相比,缩短了15小时以上。
(2),对分别加入钠蒙脱土的5份胶凝液进行ph值检测,结果如图3所示。由图可得,加入钠蒙脱土量不为0时,胶凝液的ph值在前6小时内迅速增高,然后继续下降,最后在12~27小时之间其ph值在7.6上下波动。其中ph值下降的原因是由于细菌产生的多糖。钠蒙脱土加入量为0.25%时,其ph值高于其他钠蒙脱土含量的ph值,即钠蒙脱土加入量为0.25%时响应速度最快,尿素分解释放更多的nh3,使反应液产生更多的oh-、ph值升高。
(3),测定加入不同量钠蒙脱土的胶凝液中钠蒙脱土对细菌的吸附能力,结果如图4所示。由图可以看出,钠蒙脱土对细菌的吸附能力与模型拟合较好,其测定系数r2=0.986。其中,与不加入钠蒙脱土的相比,钠蒙脱土加入量为0.5%时,对细菌的吸附能力提高了62%。
(4),对加入不同量钠蒙脱土的胶凝液中碳酸钙沉淀总量进行检测,结果如图5所示。由图5可以看出,在钠蒙脱土的作用下,碳酸钙析出相的总质量增加了约118%。从拟合曲线可以看出,在钠蒙脱土的作用下,碳酸钙析出相的生成与钠蒙脱土基本相同,这是因为在钠蒙脱土的存在下,尿素完全分解,ca2+完全反应形成碳酸钙沉淀。
(5),钠蒙脱土的加入对水电导率(碳酸钙沉淀防渗透性能)的影响,结果如图6及图7所示。由图6可以看出,随着钠蒙脱土浓度的增加,碳酸钙质量下降;这说明钠蒙脱土具有良好的封堵能力,能够较好的阻止反应溶液进入沙粒中间,即证明钠蒙脱土的存在具有很好的防渗透效果,这对于其实际工业应用具有很好的价值。由图7可以看出,随着钠蒙脱土浓度的增加,水电导率降低,当注入两次细菌时,水电导率下降更为明显。
然后对得到的沉淀采用扫描电镜进行检测(所述的电子扫描显微镜为本领域技术人员熟知的电子扫描显微镜),结果如图8所示。
由sem图像可以看出,胶结主要发生在砂粒之间的接触点,这是因为细菌在砂粒表面的吸附能力较低。在没有钠蒙脱土存在的条件下,并不是所有的碳酸钙析出物均能在砂粒之间形成,这就会导致砂粒之间有了很大间隙,因此有了很好的导水率、而不能较好的固结。钠蒙脱土固结砂粒的sem图如图8(c)及图8(d)所示,图像表明,钠蒙脱土填充了砂粒之间的空隙,所以钠蒙脱土不仅是碳酸钙沉淀形成的载体,还可以提高砂粒接触点上碳酸钙的沉淀量。所以,钠蒙脱土的加入,更紧密的结构促进了形成砂粒之间桥梁的牢固结合,大大促进了微生物诱导碳酸钙沉淀在砂粒固结、土壤改良中的应用。即在钠蒙脱土的存在下具有更明显的生物堵塞和生物胶结效应,进一步促进了其实际应用。
(6),对于未加钠蒙脱土及加入钠蒙脱土所得碳酸钙沉淀形貌进行xrd检测,结果如图9所示。图9(a)为在未加入钠蒙脱土的条件下,微生物诱导所得碳酸钙沉淀的xrd图;图9(b)为加入0.25%钠蒙脱土的条件下,微生物诱导所得碳酸钙沉淀的xrd图。由图可得,加入0.25%钠蒙脱土的情况下,得到的caco3晶体的主要成分为方解石,为加入钠蒙脱土的情况下,得到的caco3晶体的主要成分也为方解石;即加入钠蒙脱土对于所得碳酸钙沉淀并没有带来影响。
对于采用不同反应液量的实施例,具体如下:
取4份胶凝液,分别为100g(20g菌悬液与80g反应液)、200g(40g菌悬液与160g反应液)、300g(60g菌悬液与240g反应液)、400g(80g菌悬液与320g反应液)。每份胶凝液中均分别加入占胶凝液总质量0.25%的钠蒙脱土进行碳酸钙沉淀。进行以下测试:
1),不同量胶凝液中均加入0.25%钠蒙脱土时,对于细菌的吸附量,如图10所示。由图可得,胶凝液的吸附能力随着胶凝液量的增加而增加,即随着胶凝液量的增加,ca2+离子量增加,同时ca2+离子固定。0.25%钠蒙脱土存在下对细菌具有更好的吸附效果。
2),在不同胶凝液量条件下,对不加入钠蒙脱土及加入0.25%钠蒙脱土时的碳酸钙沉淀量进行检测,结果如图11所示。由图可以看出,碳酸钙沉淀量随着胶凝液量的增加而增加,在0.25%钠蒙脱土存在的条件下,由于ca2+完全沉积,不同量的胶凝液使碳酸钙沉淀总质量达到最大值。
在添加钠蒙脱土时,尿素完全分解,ca2+离子完全反应形成碳酸钙沉淀,钠蒙脱土存在时的拟合曲线斜率大于钠蒙脱土不存在时的拟合曲线斜率,这也进一步表明了在钠蒙脱土存在的条件下,胶凝液质量的增加(反应液质量的增加)对于增加碳酸钙产量更有利。因此,钠蒙脱土能够在反应液量增加的条件下使micp反应向前进行,增加碳酸钙产量,具有很好的应用价值。
3),在不同量胶凝液条件下,对不加钠蒙脱土及加入0.25%钠蒙脱土所得碳酸钙沉淀进行sem检测,结果如图12及图13所示。由图12可得,在不同胶凝液量的条件下,得到了不规则以及规则的菱面体晶体。图13可得,加入0.25%钠蒙脱土所得碳酸钙晶体的形貌与未加入钠蒙脱土的碳酸钙晶体形貌相比,添加有钠蒙脱土的碳酸钙晶体尺寸减小,其中未发现单个的菱面体晶体,而是出现了聚集的菱面体晶体,最大的团聚出现在300g的胶凝液中。所以,在钠蒙脱土存在下,不仅作为对砂土固结最有利的菱面体菱形形态没有变化,而且还可以在micp反应过程中实现菱面体晶体的团聚,这对于生物胶结具有一定的影响,也具有更好的防渗透作用。
- 还没有人留言评论。精彩留言会获得点赞!