检测2019新型冠状病毒突变的组合物、用途及试剂盒的制作方法
本发明属于分子生物学检测领域;具体地,属于2019新型冠状病毒的检测领域;更具体地,能够检测2019新型冠状病毒的两个碱基突变(8782c→t和28144t→c)。
背景技术:
2019新型冠状病毒(sars-cov-2)是引发新型冠状病毒肺炎(新冠肺炎,covid-19)的病原体。该病毒在2019年下半年开始流行并迅速蔓延,世界卫生组织于2020年3月11日宣布全球大流行。截至2020年4月1日,全球累计确诊新冠肺炎病例已超过80万例,且有进一步恶化趋势。
新冠肺炎常见体征有发热、咳嗽、气促和呼吸困难等呼吸道症状。在较严重病例中,感染可导致肺炎、严重急性呼吸综合征、肾衰竭,进一步导致死亡。目前对于2019新型冠状病毒所致疾病没有特异治疗方法,但许多症状可以对症进行辅助护理和支持性治疗。
xiaolutang等人通过病毒全基因分析,发现在第8782位碱基和第28144位碱基存在连锁现象(101/103,98%)。例如,根据这两个碱基的类型,新冠病毒存在两种单倍型:l型(c8782和t28144)和s型(t8782和c28144)。其中l型和s型的命名来自于28144位碱基变化后编码的不同氨基酸,其中l型的t28144所在密码子编码亮氨酸(leucine),s型的c28144所在密码子编码丝氨酸(serine)。
通过数据对比分析,l型和s型在重症率和传染能力上存在差异。这为细化新冠肺炎诊断提供了依据,意味着临床上可通过基因分型检测,确定患者体内病毒的型别,对临床特征和病情发展进行预判,据此制定更具针对性的治疗方案。
因此,检测识别2019新型冠状病毒这两个位点的碱基,对于疫情防控和确诊病患的治疗有积极的意义。但目前尚未有相应检测试剂。
本领域需要一种能够将2019新型冠状病毒8782和28144两个位点的碱基进行检测并识别的相关产品。
技术实现要素:
有鉴于此,本发明提供了一种检测2019新型冠状病毒突变的组合物,所述组合物包括:
第一核酸组合物:
8782c型正向引物:5’-gctgattttgacacatggttcatc-3’(seqidno:1);
28144t型正向引物:5’-atcggtaattatacagtttccagatt-3’(seqidno:2);和
第二核酸组合物:
8782t型正向引物:5’-gctgattttgacacatggtatcgt-3’(seqidno:3);
28144c型正向引物:5’-atcggtaattatacagtttcctttgc-3’(seqidno:4);
其中,所述每个核酸组合物中还包括:
8782反向引物:5’-ccattagttgtgcgtaatatcgt-3’(seqidno:5);
8782探针:5’-cttgcccattgattgctgcagtcataa-3’(seqidno:6);
28144反向引物:5’-caacacgaacgtcatgatactcta-3’(seqidno:7);
28144探针:5’-attgccaggaacctaaattgggtagt-3’(seqidno:8)。
使用该组合物,可以分辨2019新型冠状病毒的8782位为c型或t型,并且可以分辨28144为t或c型)。通过检测两处碱基类型,可以例如区分新冠病毒的s型和l型,为细化新冠肺炎诊断提供了依据,确定患者病毒型别,对临床特征和病情发展进行预判,据此更新并改进治疗方案,对于疫情防控和确诊病患的治疗有积极的意义。
使用本发明的组合物,引物检测扩增特异性靶标的ct值小,扩增效率高;引物检测特异性模板的ct值和非特异性模板的ct值差值大,特异性好。而使用本发明的组合物的对比例,引物检测扩增特异性靶标的ct值大于本发明组合物,其扩增效率较低,同时,特异性模板的ct值和非特异性模板的ct值差值也较本发明组合物小,其特异性也相对较差。
本发明的组合物可用于荧光定量pcr检测。
进一步地,所述组合物中,8782探针与28144探针带有彼此不互相干扰的荧光报告基团。
在本文中,“彼此不互相干扰”是指组合物中每个探针所用的荧光报告基团是不一样的,并且不会影响彼此的检测,即可以利用不同的通道进行检测。例如可以使用fam、hex、rox和cy5,这些基团吸光值不接近,能选择不同的通道,因而不会互相干扰。
进一步地,所述组合物包括:用于监控的内标上游引物、内标下游引物和内标探针。
在本发明中,荧光报告基团可以选自fam、hex、rox、vic、cy5、5-tamra、tet、cy3和joe,但不限于此。
在一个具体的实施方案中,如seqidno:6所示的8782探针的荧光报告基团为hex;如seqidno:8所示的28144探针的荧光报告基团为fam。
进一步地,探针的3’末端还具有淬灭基团,例如bhq1或bhq2。
进一步地,所述组合物中引物的用量为25~800nm;所述组合物中探针的用量为10~500nm。
在一个具体的实施方案中,本发明组合的两种核酸组合物分别存在于单独包装中。
进一步地,本发明的组合物的各成分以混合的形式存在。
第二方面,本发明提供了上述本发明的组合物在制备检测2019新型冠状病毒突变的试剂盒中的用途。
第三方面,本发明提供了一种检测2019新型冠状病毒突变的试剂盒,所述试剂盒包括上述本发明的组合物。
进一步地,所述试剂盒还包括dntp、pcr缓冲液以及mg2+中的至少一种。
常见的pcr缓冲液由tris-hcl、mgcl2、kcl、tritonx-100等缓冲体系构成。一般单个pcr反应管中总体积为20-200µl。
在一个具体的实施方案中,本发明第一核酸组合物的具体成分如下所示:
在一个具体的实施方案中,本发明第二核酸组合物的具体成分如下所示:
更进一步地,所述试剂盒还包括:核酸释放剂、逆转录酶以及dna聚合酶中的至少一种。
进一步地,所述组合物中检测引物的25~800nm;所述组合物中探针的用量为10~500nm。
进一步地,所述逆转录酶的浓度为5u/μl~15u/μl,例如逆转录酶可以是鼠白血病逆转录酶(mmlv)或者tth酶;所述dna聚合酶的浓度为3u/μl~15u/μl,例如dna聚合酶可以是taq酶。
进一步地,所述试剂盒还包括阳性对照。所述阳性对照含有2019新型冠状病毒基因组第8782位附近的序列以及第28144位附近的序列,并且其中,第8782位为c或t,且第28144位为c或t。例如,第8782位为c且第28144位为t,8782位为t且第28144位为c,第8782位为c且第28144位为c,第8782位为t且第28144位为t。
在本文中,术语“第8782位”和“第28144位”是指genebank登录号为:nc_045512.2的新型冠状病毒基因组序列的第8782位和28144位碱基。
在本发明中,术语“第8782位附近的序列”和“第28144位附近的序列”是指包含8782或28144位点,并包括其上下游各100~300bp碱基的序列。
进一步地,将这两个位点附近的序列进行组合,就能得到阳性对照的突变插入序列。例如,所述的2019新型冠状病毒c8782和t28144突变插入序列(seqidno:9)为:
ttaattaaagttacacttgtgttcctttttgttgctgctattttctatttaataacacctgttcatgtcatgtctaaacatactgacttttcaagtgaaatcataggatacaaggctattgatggtggtgtcactcgtgacatagcatctacagatacttgttttgctaacaaacatgctgattttgacacatggtttagccagcgtggtggtagttatactaatgacaaagcttgcccattgattgctgcagtcataacaagagaagtgggttttgtcgtgcctggtttgcctggcacgatattacgcacaactaatggtgactttttgcatttcttacctagagtttttagtgcagttggtaacatctgttacacaccatcaaaacttatagagtacaccaagaatgtagtttacagtcatgtactcaacatcaaccatatgtagttgatgacccgtgtcctattcacttctattctaaatggtatattagagtaggagctagaaaatcagcacctttaattgaattgtgcgtggatgaggctggttctaaatcacccattcagtacatcgatatcggtaattatacagtttcctgtttaccttttacaattaattgccaggaacctaaattgggtagtcttgtagtgcgttgttcgttctatgaagactttttagagtatcatgacgttcgtgttgttttagatttcatctaaacgaacaaactaaaatgtctgataatggaccccaaaatcagcgaaatgcaccccgcattacgtttggtggaccctcagattcaa
所述2019新型冠状病毒t8782和c28144突变插入序列(seqidno:10)为:
ttaattaaagttacacttgtgttcctttttgttgctgctattttctatttaataacacctgttcatgtcatgtctaaacatactgacttttcaagtgaaatcataggatacaaggctattgatggtggtgtcactcgtgacatagcatctacagatacttgttttgctaacaaacatgctgattttgacacatggtttagtcagcgtggtggtagttatactaatgacaaagcttgcccattgattgctgcagtcataacaagagaagtgggttttgtcgtgcctggtttgcctggcacgatattacgcacaactaatggtgactttttgcatttcttacctagagtttttagtgcagttggtaacatctgttacacaccatcaaaacttatagagtacaccaagaatgtagtttacagtcatgtactcaacatcaaccatatgtagttgatgacccgtgtcctattcacttctattctaaatggtatattagagtaggagctagaaaatcagcacctttaattgaattgtgcgtggatgaggctggttctaaatcacccattcagtacatcgatatcggtaattatacagtttcctgttcaccttttacaattaattgccaggaacctaaattgggtagtcttgtagtgcgttgttcgttctatgaagactttttagagtatcatgacgttcgtgttgttttagatttcatctaaacgaacaaactaaaatgtctgataatggaccccaaaatcagcgaaatgcaccccgcattacgtttggtggaccctcagattcaa。
所述阳性对照通过使用慢病毒数字pcr定量检测体系,对两种慢病毒样本进行拷贝数定量。分别将两种定量后的假病毒,使用生理盐水稀释至1.0e+06拷贝/ml而制备。所述假病毒以慢病毒为载体,插入两段新型冠状病毒基因组序列(8582-8982,27944-28344)。两段序列的中间位置分别设计为2019新型冠状病毒t8782和c28144突变和2019新型冠状病毒c8782和t28144突变的对应的碱基。
第四方面,提供了一种用于检测2019新型冠状病毒突变的方法,所述方法包括以下步骤:
1)释放待测样本的核酸;
2)使用如上述本发明的组合物或上述本发明的试剂盒对步骤1)获得的核酸进行荧光定量pcr;
3)获得并分析结果。
在本发明中,用于检测的样本可以是咽拭子、痰液、肺泡灌洗液、血液等,但不限于此。
进一步地,所述荧光定量pcr的反应条件为:
逆转录,温度为50℃,时间25~35分钟,1次循环;cdna预变性,温度为95℃,时间1~10分钟,1次循环;变性,温度为95℃,时间为10~20秒,退火,温度为60℃,时间为20~40秒,40~50次循环。
在一个具体的实施方案中,提供了一种用于以非诊断目的检测2019新型冠状病毒突变的方法,所述方法包括以下步骤:
1)释放待测样本的核酸;
2)使用如上述本发明的组合物或上述本发明的试剂盒对步骤1)获得的核酸进行荧光定量pcr;
3)获得并分析结果。
进一步地,所述荧光定量pcr的反应条件为:
逆转录,温度为50℃,时间25~35分钟,1次循环;cdna预变性,温度为95℃,时间1~10分钟,1次循环;变性,温度为95℃,时间为10~20秒,退火,温度为60℃,时间为20~40秒,40~50次循环。
在本文中,术语“非诊断目的”指并非旨在获得个体是否感染2019新型冠状病毒并罹患肺炎的信息。例如,该方法可以在以科研为目的的实验中检测培养物中是否有2019新型冠状病毒以及病毒的突变类型。
附图说明
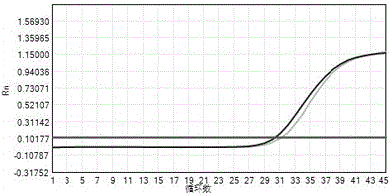
图1:第一组合物检测临床核酸样本扩增结果;
图2:第二组合物检测临床核酸样本扩增结果;
图3:第一组合物检测2019新型冠状病毒c8782和t28144突变模板(1.0e+08拷贝/ml)结果;
图4:第一组合物检测2019新型冠状病毒t8782和c28144突变2019新型冠状病毒t8782和c28144突变模板(1.0e+08拷贝/ml)结果;
图5:第二组合物检测2019新型冠状病毒t8782和c28144突变模板(1.0e+08拷贝/ml)结果;
图6:第二组合物检测2019新型冠状病毒c8782和t28144突变模板(1.0e+08拷贝/ml)结果;
图7:第一组合物检测梯度浓度2019新型冠状病毒c8782和t28144突变,fam通道检测结果;
图8:第一组合物检测梯度浓度2019新型冠状病毒c8782和t28144突变,hex通道检测结果;
图9:第二组合物检测梯度浓度2019新型冠状病毒t8782和c28144突变模板,fam通道检测结果;
图10:第二组合物检测梯度浓度2019新型冠状病毒t8782和c28144突变模板,hex通道检测结果;
图11:不同设计的8782c型引物扩增2019新型冠状病毒c8782和t28144突变模板(实线)和2019新型冠状病毒t8782和c28144突变模板(虚线)的结果,图11a-f分别为本发明引物,和对比例引物8782c1~5的结果;
图12:不同设计的8782t型引物扩增2019新型冠状病毒t8782和c28144突变模板(实线)和2019新型冠状病毒c8782和t28144突变模板(虚线)的结果,图12a-f分别为本发明引物,和对比例引物8782t1~5的结果;
图13:不同设计的28144t型引物扩增2019新型冠状病毒c8782和t28144突变模板(实线)和2019新型冠状病毒t8782和c28144突变模板(虚线)的结果,图13a-f分别为本发明引物,和对比例引物28144t1~5的结果;
图14:不同设计的28144c型引物扩增2019新型冠状病毒t8782和c28144突变模板(实线)和2019新型冠状病毒c8782和t28144突变模板(虚线)的结果,图14a-f分别为本发明引物,和对比例引物28144c1~5的结果。
具体实施方式
下文将结合具体实施方式和实施例,具体阐述本发明,本发明的优点和各种效果将由此更加清楚地呈现。本领域技术人员应理解,这些具体实施方式和实施例是用于说明本发明,而非限制本发明。
实施例1、本发明所使用的引物及探针
本发明所使用的引物及探针如下所示:
8782c型正向引物:5’-gctgattttgacacatggttcatc-3’(seqidno:1);
28144t型正向引物:5’-atcggtaattatacagtttccagatt-3’(seqidno:2);
8782t型正向引物:5’-gctgattttgacacatggtatcgt-3’(seqidno:3);
28144c型正向引物:5’-atcggtaattatacagtttcctttgc-3’(seqidno:4);
8782反向引物:5’-ccattagttgtgcgtaatatcgt-3’(seqidno:5);
8782探针:5’-cttgcccattgattgctgcagtcataa-3’(seqidno:6);
28144反向引物:5’-caacacgaacgtcatgatactcta-3’(seqidno:7);
28144探针:5’-attgccaggaacctaaattgggtagt-3’(seqidno:8)。
其中,8782探针的荧光报告基团为hex,28144探针的荧光报告基团为fam,探针的3’末端还具有bhq1或bhq2淬灭基团。
实施例2、检测2019新型冠状病毒突变的方法
本发明检测样本为咽拭子、痰液、肺泡灌洗液、血液。进行如下操作:
(1)使用圣湘生物核酸释放剂s1014,与阳性对照1:1混合,常温裂解10分钟;
(2)按每种反应液26μl和混合酶4μl的比例,取相应量的反应液和混合酶混匀,以每反应30μl的体积分装至各反应管。分别向各反应管中加入待检测的裂解后样本20μl,然后盖上pcr管盖,瞬时离心后放置于实时荧光pcr仪器中;
(3)按以下循环条件进行反应和检测(荧光采集选取fam通道和hex通道):
结果分析:
1)目的检测信号为fam,hex;
2)baseline的设置:baseline一般设置为3-15个循环,具体可根据实际情况进行调整。其调整原则为:选择指数扩增前荧光信号较稳定的区域,起点(start)避开荧光采集起始阶段的信号波动,终点(end)比最早出现指数扩增的样本ct减少1-2个循环。threshold的设置:设定原则以阈值线刚好超过正常阴性对照品的最高点;
3)如果两个组合物中,各通道均无扩增信号,则为样本浓度低于检测下限;
如果在两个组合物中,有且只有一个组合物存在扩增信号:
其中第一组合物fam和hex均有扩增曲线,且ct<40,表示为2019新型冠状病毒c8782和t28144突变;
其中第二组合物fam和hex均有扩增曲线,且ct<40,表示为2019新型冠状病毒t8782和c28144突变;
如果在两个组合物中,均存在扩增信号,则比较两个组合物中,对应通道的ct值差值:
两种组合物各通道ct值的差值大于10,如第一组合物的ct值较小则为2019新型冠状病毒c8782和t28144突变,第二组合组的ct值较小则为2019新型冠状病毒t8782和c28144突变。
两种组合物各通道ct值的差值小于10,则为两个型别同时存在。
针对第一组合物,当fam和hex均有扩增曲线,且ct<35,表示为2019新型冠状病毒c8782和t28144突变;
针对第二组合组,当fam和hex均有扩增曲线,且ct<35,表示为2019新型冠状病毒t8782和c28144突变;
针对第一组合物以及第二组合物,若fam和hex仅有一条或无扩增曲线,则不能判断该2019新型冠状病毒的类型。判断结果可以参见如下表1所示。
对两管组合物中扩增的结果进行分析,其中“+”指有扩增曲线或ct值小于45,“-”指无扩增曲线或ct值大于45。ct1和ct2分别为第一组合物和第二组合物中对应通道的ct值,δct为这两个ct值差值的绝对值。
表1
实施例3、本发明组合物用于检测2019新型冠状病毒突变
使用本发明实施例1中所述的组合物,按照实施例2所述的方法进行检测。所述样本为临床阳性样本提取核酸。分别用第一组合物和第二组合物进行检测,其结果如图1-2所示。从图中可以判读出,该样本第8782和第28144碱基分别为c和t,其为2019新型冠状病毒c8782和t28144突变。
实施例4、本发明组合物特异性检测
使用本发明实施例1中所述的组合物,按照实施例2所述的方法进行检测。所述样本为两种高浓度(浓度为1.0e+08拷贝/ml)的假病毒样本。使用第一组合物和第二组合物分别检测2019新型冠状病毒c8782和t28144突变,以及2019新型冠状病毒t8782和c28144突变的假病毒模板,结果如图3-图6所示,各检测结果的ct值见下表2。
可见,不同组合物对2019新型冠状病毒c8782和t28144突变假病毒和2019新型冠状病毒t8782和c28144突变假病毒的扩增效率存在显著差异,各δct的最小值(13.00)仍远大于实施案例2所述结果判定方法中对δct的要求(10)。
以各组δct中的最小值13.00计算,两个组合物对特异性模板和非特异性模板的扩增效率差异高达8192倍(2^13),特异性优异。
实施例5、本发明组合物灵敏度检测
使用本发明实施例1中所述的组合物,按照实施例2所述的方法进行检测。所述样本为假病毒样本(2019新型冠状病毒c8782和t28144突变假病毒和2019新型冠状病毒t8782和c28144突变假病毒)经生理盐水稀释梯度,各浓度梯度分别为1.0e+06拷贝/ml、1.0e+05拷贝/ml、1.0e+04拷贝/ml、1.0e+03拷贝/ml、1.0e+02拷贝/ml、1.0e+01拷贝/ml。分别使用第一组合物和第二组合物检测不同浓度的特异性模板,结果如图7-10所示。
第一组合物最低检测浓度为1.0e+03拷贝/ml(10拷贝/反应)。
第二组合物最低检测浓度为1.0e+03拷贝/ml(10拷贝/反应)。
对比例1、本发明另外的探针和引物组合物检测2019新型冠状病毒突变
在本发明创造过程中,针对每一个位点碱基,各设计数十条不同的特异性识别引物。这些引物均遵循arms引物设计原理,在3’端增加1-2个突变,使其能够有选择性地扩增特异靶标,部分对比引物的序列见下:
8782c型正向对比引物:
8782c-1:5’-gctgattttgacacatggtttagc-3’(seqidno:11);
8782c-2:5’-gctgattttgacacatggtttatc-3’(seqidno:12);
8782c-3:5’-gctgattttgacacatggtttcgc-3’(seqidno:13);
8782c-4:5’-gctgattttgacacatggtttctc-3’(seqidno:14);
8782c-5:5’-gctgattttgacacatggtctcgt-3’(seqidno:15);
8782t型正向对比引物:
8782t-1:5’-gctgattttgacacatggtttagt-3’(seqidno:16);
8782t-2:5’-gctgattttgacacatggtttcgt-3’(seqidno:17);
8782t-3:5’-gctgattttgacacatggtttatt-3’(seqidno:18);
8782t-4:5’-gctgattttgacacatggtttcat-3’(seqidno:19);
8782t-5:5’-gctgattttgacacatggttgatt-3’(seqidno:20);
28144t型正向对比引物:
28144t-1:5’-atcggtaattatacagtttcctgttt-3’(seqidno:21);
28144t-2:5’-atcggtaattatacagtttcctcttt-3’(seqidno:22);
28144t-3:5’-atcggtaattatacagtttcctggtt-3’(seqidno:23);
28144t-4:5’-atcggtaattatacagtttcctgggt-3’(seqidno:24);
28144t-5:5’-atcggtaattatacagtttcctctct-3’(seqidno:25);
28144c型正向对比引物:
28144c-1:5’-atcggtaattatacagtttcctgttc-3’(seqidno:26);
28144c-2:5’-atcggtaattatacagtttcctcttc-3’(seqidno:27);
28144c-3:5’-atcggtaattatacagtttcctggtc-3’(seqidno:28);
28144c-4:5’-atcggtaattatacagtttcctgagc-3’(seqidno:29);
28144c-5:5’-atcggtaattatacagtttccaggtc-3’(seqidno:30)。
使用这些引物,与实施例1中的其余引物、探针组合成组合物,按照实施例2所述的方法进行检测。所述样本为两种浓度为1.0e+08拷贝/ml的假病毒样本。检测结果见图11-14所示。各结果图中,实线为各引物扩增其特异性模板的结果(如8782c引物检测2019新型冠状病毒c8782和t28144突变模板——该模板中8782位点为c),虚线为该引物扩增非特异性模板的结果(如8782c引物检测2019新型冠状病毒t8782和c28144突变模板——该模板中8782位点为t)。
评价引物优劣的主要指标为引物的扩增效率和特异性。其中引物检测扩增特异性靶标的ct值越小,其扩增效率越高;引物检测同浓度下特异性模板的ct值和非特异性模板,二者ct值的差值的绝对值约大越好,其特异性越好。
从各个结果中可以看出,各对比引物的扩增效率和特异性的综合性能均劣于本发明组合物。
序列表
<110>圣湘生物科技股份有限公司
<120>检测2019新型冠状病毒突变的组合物、用途及试剂盒
<160>30
<170>patentinversion3.5
<210>1
<211>24
<212>dna
<213>人工序列
<400>1
gctgattttgacacatggttcatc24
<210>2
<211>26
<212>dna
<213>人工序列
<400>2
atcggtaattatacagtttccagatt26
<210>3
<211>24
<212>dna
<213>人工序列
<400>3
gctgattttgacacatggtatcgt24
<210>4
<211>26
<212>dna
<213>人工序列
<400>4
atcggtaattatacagtttcctttgc26
<210>5
<211>23
<212>dna
<213>人工序列
<400>5
ccattagttgtgcgtaatatcgt23
<210>6
<211>27
<212>dna
<213>人工序列
<400>6
cttgcccattgattgctgcagtcataa27
<210>7
<211>24
<212>dna
<213>人工序列
<400>7
caacacgaacgtcatgatactcta24
<210>8
<211>26
<212>dna
<213>人工序列
<400>8
attgccaggaacctaaattgggtagt26
<210>9
<211>800
<212>dna
<213>人工序列
<400>9
ttaattaaagttacacttgtgttcctttttgttgctgctattttctatttaataacacct60
gttcatgtcatgtctaaacatactgacttttcaagtgaaatcataggatacaaggctatt120
gatggtggtgtcactcgtgacatagcatctacagatacttgttttgctaacaaacatgct180
gattttgacacatggtttagccagcgtggtggtagttatactaatgacaaagcttgccca240
ttgattgctgcagtcataacaagagaagtgggttttgtcgtgcctggtttgcctggcacg300
atattacgcacaactaatggtgactttttgcatttcttacctagagtttttagtgcagtt360
ggtaacatctgttacacaccatcaaaacttatagagtacaccaagaatgtagtttacagt420
catgtactcaacatcaaccatatgtagttgatgacccgtgtcctattcacttctattcta480
aatggtatattagagtaggagctagaaaatcagcacctttaattgaattgtgcgtggatg540
aggctggttctaaatcacccattcagtacatcgatatcggtaattatacagtttcctgtt600
taccttttacaattaattgccaggaacctaaattgggtagtcttgtagtgcgttgttcgt660
tctatgaagactttttagagtatcatgacgttcgtgttgttttagatttcatctaaacga720
acaaactaaaatgtctgataatggaccccaaaatcagcgaaatgcaccccgcattacgtt780
tggtggaccctcagattcaa800
<210>10
<211>800
<212>dna
<213>人工序列
<400>10
ttaattaaagttacacttgtgttcctttttgttgctgctattttctatttaataacacct60
gttcatgtcatgtctaaacatactgacttttcaagtgaaatcataggatacaaggctatt120
gatggtggtgtcactcgtgacatagcatctacagatacttgttttgctaacaaacatgct180
gattttgacacatggtttagtcagcgtggtggtagttatactaatgacaaagcttgccca240
ttgattgctgcagtcataacaagagaagtgggttttgtcgtgcctggtttgcctggcacg300
atattacgcacaactaatggtgactttttgcatttcttacctagagtttttagtgcagtt360
ggtaacatctgttacacaccatcaaaacttatagagtacaccaagaatgtagtttacagt420
catgtactcaacatcaaccatatgtagttgatgacccgtgtcctattcacttctattcta480
aatggtatattagagtaggagctagaaaatcagcacctttaattgaattgtgcgtggatg540
aggctggttctaaatcacccattcagtacatcgatatcggtaattatacagtttcctgtt600
caccttttacaattaattgccaggaacctaaattgggtagtcttgtagtgcgttgttcgt660
tctatgaagactttttagagtatcatgacgttcgtgttgttttagatttcatctaaacga720
acaaactaaaatgtctgataatggaccccaaaatcagcgaaatgcaccccgcattacgtt780
tggtggaccctcagattcaa800
<210>11
<211>24
<212>dna
<213>人工序列
<400>11
gctgattttgacacatggtttagc24
<210>12
<211>24
<212>dna
<213>人工序列
<400>12
gctgattttgacacatggtttatc24
<210>13
<211>24
<212>dna
<213>人工序列
<400>13
gctgattttgacacatggtttcgc24
<210>14
<211>24
<212>dna
<213>人工序列
<400>14
gctgattttgacacatggtttctc24
<210>15
<211>24
<212>dna
<213>人工序列
<400>15
gctgattttgacacatggtctcgt24
<210>16
<211>24
<212>dna
<213>人工序列
<400>16
gctgattttgacacatggtttagt24
<210>17
<211>24
<212>dna
<213>人工序列
<400>17
gctgattttgacacatggtttcgt24
<210>18
<211>24
<212>dna
<213>人工序列
<400>18
gctgattttgacacatggtttatt24
<210>19
<211>24
<212>dna
<213>人工序列
<400>19
gctgattttgacacatggtttcat24
<210>20
<211>24
<212>dna
<213>人工序列
<400>20
gctgattttgacacatggttgatt24
<210>21
<211>26
<212>dna
<213>人工序列
<400>21
atcggtaattatacagtttcctgttt26
<210>22
<211>26
<212>dna
<213>人工序列
<400>22
atcggtaattatacagtttcctcttt26
<210>23
<211>26
<212>dna
<213>人工序列
<400>23
atcggtaattatacagtttcctggtt26
<210>24
<211>26
<212>dna
<213>人工序列
<400>24
atcggtaattatacagtttcctgggt26
<210>25
<211>26
<212>dna
<213>人工序列
<400>25
atcggtaattatacagtttcctctct26
<210>26
<211>26
<212>dna
<213>人工序列
<400>26
atcggtaattatacagtttcctgttc26
<210>27
<211>26
<212>dna
<213>人工序列
<400>27
atcggtaattatacagtttcctcttc26
<210>28
<211>26
<212>dna
<213>人工序列
<400>28
atcggtaattatacagtttcctggtc26
<210>29
<211>26
<212>dna
<213>人工序列
<400>29
atcggtaattatacagtttcctgagc26
<210>30
<211>26
<212>dna
<213>人工序列
<400>30
atcggtaattatacagtttccaggtc26
- 还没有人留言评论。精彩留言会获得点赞!