一种制备类泛素探针的多肽荧光底物方法与流程
1.本发明涉及生物技术领域,具体地,本发明涉及制备类泛素探针的多肽荧光底物方法。
背景技术:
2.cbz-rlrgg-amc一种多肽片段的荧光底物。它的主体由蛋白翻译后修饰-泛素c末端5个氨基酸残基arg-leu-arg-gly-gly构成的序列。该序列的n端裸露氨基由cbz(苄氧羰基)保护基进行选择性保护,而c端连接amc(7-氨基-4-甲基香豆素)荧光分子。该底物在遇到去泛素化水解酶,如异肽酶(ipaset)以及其他泛素c末端水解酶(uchs)时,能够模拟野生型泛素链在末端甘氨酸处发生酰胺键水解断裂,从而释放amc分子显著增强其发出的荧光,这样通过荧光就能够精确测定水解效率,确定酶活。泛素cbz-rlrgg-amc作为去泛素化酶的荧光检测试剂,实测去泛素化水解酶的催化水解效率(kcat/km)能够达到95m-1s-1。基于cbz-rlrgg-amc的荧光特性,该多肽荧光底物被作为高通量筛选工具,被广泛用于去泛素化酶抑制剂的开发和靶向去泛素化酶的小分子和多肽药物的筛选。
技术实现要素:
3.本发明提出了一种多肽的合成方法。根据本发明的实施例,所述方法包括:将粗肽的碳端氨基酸与gly-amc进行缩合反应,以便获得所述多肽,所述缩合反应是在缩合剂的活化下进行的,所述缩合剂包括选自hctu(6-氯苯并三氮唑-1,1,3,3-四甲基脲六氟磷酸酯)、hobt(1-羟基苯并三唑)、pyaop(3h-1,2,3-三唑并[4,5-b]吡啶-3-氧基)三-1-吡咯烷基鏻六氟磷酸盐)、pybop(六氟磷酸苯并三唑-1-基-氧基三吡咯烷基磷)、hbtu(苯并三氮唑-n,n,n',n'-四甲基脲六氟磷酸盐)、hatu(2-(7-偶氮苯并三氮唑)-n,n,n',n'-四甲基脲六氟磷酸酯)和hoat(1-羟基-7-偶氮苯并三氮唑)的至少之一。根据本发明实施例的方法,操作简便,所制备的多肽荧光底物产量大,纯度高,成本低,利于荧光试剂的商业化。
[0004]
根据本发明的实施例,上述方法还可以进一步包括如下附加技术特征至少之一:
[0005]
根据本发明的实施例,所述缩合剂为hctu、pyaop或hatu和hoat。发明人发现,所述缩合剂为hctu、pyaop或hatu和hoat,多肽的产率进一步提高。
[0006]
根据本发明的实施例,所述缩合剂为hatu和hoat,所述hatu和hoat的物质的量比为1:1。发明人发现,当缩合剂为hatu和hoat的组合,且二者的物质的量比为1:1时,多肽的产率提高显著。
[0007]
根据本发明的实施例,所述缩合剂为pybop、pyaop、hctu、hatu和hoat或hbtu和hobt,所述缩合反应进一步在加有diea(n,n-二异丙基乙胺)的条件下进行的。
[0008]
根据本发明的实施例,所述缩合剂为hobt,所述缩合反应进一步在加有dic(n,n'-二异丙基碳二亚胺)的条件下进行的。
[0009]
根据本发明的实施例,所述粗肽是通过fmoc固相合成法合成的。
[0010]
根据本发明的实施例,所述粗肽具有rlrgg的氨基酸序列,所述粗肽是通过如下方
式获得的:以氯树脂作为固相载体,经缩合剂活化,将待合成粗肽按照氨基酸由c端向n端的顺序逐个偶联到氯树脂上,最后一个氨基酸用cbz保护,经全保护切割后,获得所述粗肽。
[0011]
根据本发明的实施例,将待合成粗肽按照氨基酸由c端向n端的顺序逐个偶联到氯树脂上是在温度为30~32℃下、hctu活化下进行的。
[0012]
根据本发明的实施例,利用含有20%哌啶的dmf溶液进行脱fmoc反应。
[0013]
根据本发明的实施例,最后一个氨基酸用cbz保护是通过将连接有rlrgg的氯树脂在diea、cbzcl和dmf的混合溶液中进行的,所述混合溶液中的diea、cbzcl和dmf的体积比为1:1:8。
[0014]
根据本发明的实施例,所述全保护切割是通过将连接有rlrgg的氯树脂在1,1,1,3,3,3-六氟-2-丙醇和dcm的混合溶液中进行的,所述混合溶液中的1,1,1,3,3,3-六氟-2-丙醇和dcm体积比为1:4。
[0015]
根据本发明的实施例,将待合成粗肽按照氨基酸由c端向n端的顺序逐个偶联到氯树脂上包括:
[0016]
(1)将用dmf溶解的fmoc-gly-oh与diea在30~32℃下在多肽合成管中进行第一接触,以便将gly偶联到所述氯树脂上;
[0017]
(2)将偶联有gly的氯树脂与含有20%哌啶的dmf溶液进行接触,以便脱除fmoc;
[0018]
(3)将用dmf溶解的fmoc-arg-oh与diea在30~32℃下在多肽合成管中进行第二接触,所述第二接触是在hctu活化下进行的,以便将arg偶联到gly的n端;
[0019]
(4)将偶联有arg-gly的氯树脂与含有20%哌啶的dmf溶液进行接触,以便脱除fmoc;
[0020]
(5)将用dmf溶解的fmoc-leu-oh与diea在30~32℃下在多肽合成管中进行第三接触,所述第三接触是在hctu活化下进行的,以便将leu偶联到arg的n端;
[0021]
(6)将偶联有leu-arg-gly的氯树脂与含有20%哌啶的dmf溶液进行接触,以便脱除fmoc;
[0022]
(5)将用dmf溶解的fmoc-arg-oh与diea在30~32℃下在多肽合成管中进行第四接触,所述第四接触是在hctu活化下进行的,以便将arg偶联到leu的n端;
[0023]
(6)将偶联有arg-leu-arg-gly的氯树脂与含有20%哌啶的dmf溶液进行接触,以便脱除fmoc。
[0024]
本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
[0025]
本发明的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得明显和容易理解,其中:
[0026]
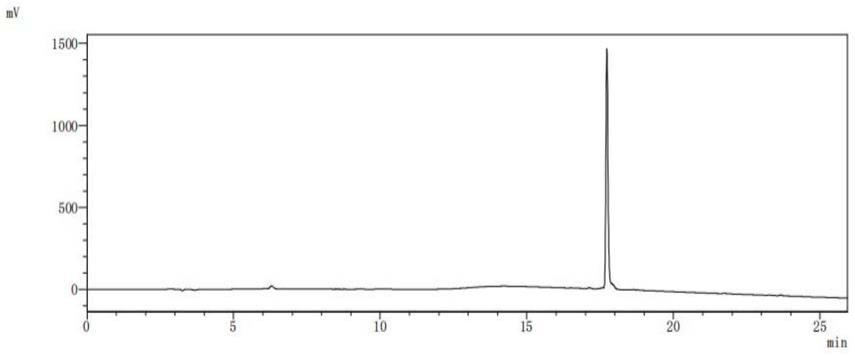
图1是根据本发明实施例的合成多肽的色谱图;
[0027]
图2是根据本发明实施例的合成多肽的质谱图。
具体实施方式
[0028]
下面详细描述本发明的实施例,所述实施例的示例在附图中示出。下面通过参考
附图描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
[0029]
此外,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括至少一个该特征。在本发明的描述中,“多个”的含义是至少两个,例如两个,三个等,除非另有明确具体的限定。
[0030]
本发明所要解决的技术问题是提供一种稳定性好,纯度高的多肽。
[0031]
为了解决上述技术问题,本发明采用如下技术方案:所述多肽的氨基酸序列如cbz-rlrgg-amc所示,本发明还提供上述多肽的合成方法,包括以下步骤:
[0032]
采用fmoc固相合成法,以氯树脂作为固相载体,经缩合剂活化,按照所示的序列将氨基酸由c端向n端逐个偶联到树脂上,最后一个氨基酸需要用cbz保护,经全保护切割后,粗肽与gly-amc反应,经切割液处理后,获得所述多肽。
[0033]
进一步地,所述树脂为氯树脂,这种树脂成本低。
[0034]
进一步地,所述缩合剂选自dic、hatu、hbtu、pyaop、pybop、hctu中一种或任意几种。这里的几种是指两种以上。
[0035]
进一步地,合成温度为31.5℃。在实施本发明的过程中,发明人发现在这个温度下,可以适用于所有氨基酸的反应条件。
[0036]
进一步地,cbz的反应条件为diea:cbzcl:dmf=1:1:8;
[0037]
进一步地,fmoc保护基团的脱除试剂为含有20%哌啶的dmf溶液。
[0038]
进一步地,所述切割液为三氟乙酸、苯酚、水、tips(三异丙基硅烷);
[0039]
进一步地,gly-amc是在缩合剂hctu、hobt、pyaop、pybop、hbtu、hatu和hoat的至少之一存在的条件下进行的,当缩合剂为pybop、pyaop、hctu、hatu和hoat或hbtu和hobt时,所述缩合反应进一步加有diea,当缩合剂为hobt,所述缩合反应进一步加有dic;
[0040]
本发明有益效果为:
[0041]
本发明多肽具合成方法具有稳定性高、纯度高的优点,另外本发明方法操作简便,收率高。
[0042]
下面参考具体实施例,对本发明进行描述,需要说明的是,这些实施例仅仅是描述性的,而不以任何方式限制本发明。
[0043]
实施例1多肽的制备
[0044]
(1)树脂溶涨:称取222mg氯树脂(0.45g/mmol),放入固相合成管中,加入等体积dcm、dmf,静置30min;
[0045]
(2)清洗:依次用dmf、dcm、dmf各洗涤3次,抽干溶剂;
[0046]
(3)第一个氨基酸缩合:将相对于树脂的4倍摩尔量的fmoc-gly-oh氨基酸用3ml dmf溶解,再加入相对于树脂15倍当量的diea,混合均匀后转移至多肽合成管中。将多肽合成管转移至恒温摇床室温振荡过夜(31.5℃)。
[0047]
(2)脱fmoc保护基:向多肽合成管中加入20%(20%哌啶溶液:用量筒量取100ml哌啶,加dmf至量筒刻度500ml)哌啶的dmf溶液淹没树脂,转移至摇床振荡5min,抽干溶剂,依次用dmf、dcm、dmf各洗涤3次。再次向合成管中加入20%哌啶的dmf溶液淹没树脂,振荡时间延长至10min。抽干溶剂,依次用dmf/dcm/dmf各洗涤3次。
[0048]
(3)下一个氨基酸缩合:将相对于树脂的4倍当量的fmoc-arg(pbf,2,2,4,6,7-五
甲基二氢苯并呋喃-5-磺酰基)-oh氨基酸和4倍当量的缩合剂(hctu)用dmf溶解,再加入8倍当量的diea,混合均匀后转移至多肽合成管中。将多肽合成管转移至恒温摇床室温振荡50min。
[0049]
(4)脱fmoc保护:重复步骤(2)操作。
[0050]
(5)第三个氨基酸偶联:将4倍当量的fmoc-leu-oh氨基酸和4倍当量的缩合剂(hctu)用dmf溶解,再加入8倍当量的diea,混合均匀后转移至多肽合成管中。将多肽合成管转移至恒温摇床室温振荡50min。
[0051]
(6)重复步骤(4)、步骤(5),直到完成最后一个氨基酸的合成。
[0052]
(7)多肽末端cbz的保护:
[0053]
7-1)根据步骤2)脱去最后精氨酸的fmoc保护基;
[0054]
7-2)根据比例diea:cbzcl:dmf=1:1:8,配置10ml溶液,取5ml加入合成管,将多肽合成管转移至恒温摇床室温振荡20min后,重复上一步操作;
[0055]
(8)片段的全保护切割
[0056]
1,1,1,3,3,3-六氟-2-丙醇:dcm=1:4,配置5ml溶液,倒入合成管中,将多肽合成管转移至恒温摇床室温振荡60min,将切割液收集到50ml ep管中,用冰乙醚沉淀粗肽并离心,收集再用冰乙醚洗涤粗肽2次,晾干。
[0057]
(9)片段gly-amc的反应
[0058]
取上述反应获得的粗肽平均放入50ml离心管,加入磁子,称取29mg gly-amc,pybop 104mg溶于3ml dmf,加入66.5μl diea,充分混合后加入离心管中,将离心管放入油浴锅中(温度37℃,转速200)反应过夜。
[0059]
(10)片段大切
[0060]
10-1)使用旋转蒸发仪将上述反应溶液旋干,使用乙醚清洗三次,晾干;
[0061]
10-2)苯酚500mg;tips:250μl;h2o:500μl;用三氟乙酸定容到10ml;
[0062]
10-3)将10-2)的切割试剂转移至多肽合成管中反应3h。
[0063]
(11)吹干洗涤:将切割液收集到50ml ep管中,用氮气鼓泡浓缩切割液后,用冰乙醚沉淀多肽并离心收集,再用冰乙醚洗涤多肽2次,晾干。
[0064]
(12)多肽色谱分析及分离:利用hplc和质谱对多肽进行正确性分析。验证正确后,如图1和图2所示,将正确产物分离并冻干。
[0065]
实施例2片段gly-amc的反应条件筛选
[0066]
取上述反应(8)获得的粗肽平均放入6个50ml离心管中(标号1-6,分别对应以下缩合剂的顺序),加入磁子,称取6份29mg gly-amc加入离心管中,分别称取pybop 57mg,pyaop 57mg,hctu 78.5mg,hatu 72mg/hoat 25mg,hbtu 78mg/hobt 25mg,hobt 25mg对应加入离心管中,用3ml dmf溶解,1-5号离心管分别加入66.5μl diea,6号离心管加入31μl dic,充分混合后加入离心管中,将离心管放入油浴锅中(温度37℃,转速200)反应过夜。
[0067]
后经过反应(10)片段大切、(11)吹干洗涤和(12)多肽色谱分析及分离后,1号管获得3.6mg荧光多肽(产率8.6%)、2号管获得7mg荧光多肽(产率16.6%)、3号管获得7.2mg荧光多肽(产率17.1%)、4号管获得9.3mg荧光多肽(产率22.1%)、5号管获得5.6mg荧光多肽(产率13.3%)、6号管获得5.8mg荧光多肽(产率8.6%),其中产率是由下列公式计算获得:实际获得的荧光多肽的质量/理论获得的荧光多肽的质量。
[0068]
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
[0069]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1