一种特布他林的合成方法及其在制备硫酸特布他林中的应用与流程
本发明属于化学制药领域,具体涉及一种特布他林的合成方法及其在制备硫酸特布他林中的应用。
背景技术:
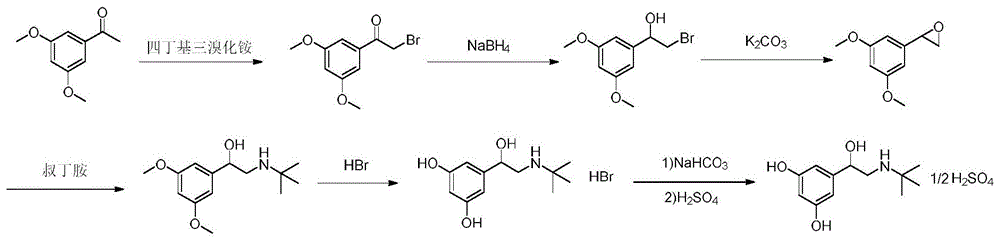
:硫酸特布他林又名间羟舒喘灵,叔丁喘宁,是由阿斯利康公司研发的具有较高选择性的短效β2-受体激动剂型,有舒张支气管作用,临床用于治疗支气管哮喘、慢性和喘息性支气管炎、肺气肿等疾患,为轻、中度慢性阻塞性肺疾病(copd)患者的临床推荐用药。较其他已上市的短效β2-受体激动剂,硫酸特布他林吸入剂具有更低的剂量依赖性副作用。目前,硫酸特布他林的合成路线主要有以下几种。美国专利us3937838合成路线是以3,5-羟基苯甲酸为起始物料,以3,5-二羟基苯乙酸为起始物料,经浓硫酸催化与乙醇酯化反应得到3,5-二羟基苯甲酸乙酯,再用氯苄保护生成3,5-二苄氧基苯甲酸乙酯;用二氯亚砜氯化为酰氯,和偶氮甲烷反应生成偶氮乙酰基,再与氢溴酸反应得到2-溴-3',5'-二苄氧基苯乙酮,2-溴-3',5'-二苄氧基苯乙酮与n-叔丁苄胺亲核取代反应得到1-(3,5-二苄氧基苯基)-2-叔丁氨基-乙酮硫酸盐,1-(3,5-二苄氧基苯基)-2-叔丁氨基-乙酮硫酸盐用pd/c加氢脱苄后,直接用硼氢化钠还原羰基,得到特布他林。与硫酸成盐,得到硫酸特布他林。此工艺合成路线较长,用到氯化亚砜及偶氮甲烷等剧毒、危险试剂,脱苄基过程需用到pd/c加氢,属于高危反应,且终产品中钯残留较难去除,由于该合成路线较长,总摩尔收率仅约12%。中国专利cn106831452a合成路线以3,5-二羟基苯乙酮为起始原料,不保护羟基,直接用溴化铜进行溴化,得到2-溴-3',5'-二羟基苯乙酮;然后经硼氢化钠还原羰基得到2-溴-1-(3,5-二羟基苯基)乙醇,2-溴-1-(3,5-二羟基苯基)乙醇与叔丁胺亲核取代反应生成特布他林,与硫酸成盐得硫酸特布他林。此路线中没有保护羟基,羟基容易被氧化,产生杂质;使用溴化酮做为溴化试剂,后处理难,带来大量副产物及污染,此路线总摩尔收率约30%。另外,中国专利cn103664654a,以市售的硫酸特布他林类似物盐酸班布特罗为原料,经碱性条件下水解得到硫酸特布他林粗品,再在甲醇中重结晶,得到硫酸特布他林。盐酸班布特罗价格相对较高,不适合作为制备硫酸特布他林的起始物料,同时反应路线较短,不适合作为申报工艺,总摩尔收率约50%。目前国内外报道的合成路线均大同小异,合成过程中大多用到剧毒试剂、pd/c加氢高危反应或采用的起始物料价格昂贵等缺点。同时硫酸特布他林终产品制备过程大多采用反应结束浓缩溶剂,加入甲醇析晶的方式,增加了操作难度。技术实现要素:发明目的:本发明所要解决的技术问题是针对现有技术的不足,提供一种特布他林的合成方法,以避免使用pd/c加氢。本发明还要解决的技术问题为提供上述特布他林在制备硫酸特布他林中的应用,在终产品制备过程中采用直接析晶的方式,避免了浓缩溶剂的步骤。为了解决上述第一个技术问题,本发明公开了一种特布他林的合成方法,包括如下步骤:(1)溴代反应:将如式i所示的3,5-二甲氧基苯乙酮与四丁基三溴化铵反应,得到如式ⅱ所示的2-溴-1-(3,5-二甲氧基苯基)乙酮;(2)还原反应:将如式ⅱ所示的2-溴-1-(3,5-二甲氧基苯基)乙酮与还原剂在甲醇中反应,得到如式ⅲ所示的2-溴-1-(3,5-二甲氧基苯基)乙醇;(3)成环反应:将如式ⅲ所示的2-溴-1-(3,5-二甲氧基苯基)乙醇在碱性条件下进行成环反应,生成如式ⅳ所示的2-(3,5-二甲基氧基)环氧乙烷;(4)缩合反应:将如式ⅳ所示的2-(3,5-二甲基氧基)环氧乙烷与叔丁胺反应,生成如式ⅴ所示的1-(3,5-二甲氧基苯基)-2-叔丁氨基-乙醇;(5)水解反应:将如式ⅴ所示的1-(3,5-二甲氧基苯基)-2-叔丁氨基-乙醇在酸性条件水解,得到如式ⅵ所示的1-(3,5-二羟基苯基)-2-叔丁氨基-乙醇的盐;步骤(1)中,所述的溴代反应的溶剂为四氢呋喃、乙酸乙酯、乙腈和甲基叔丁基醚中的任意一种溶剂与甲醇的混合溶剂;优选为四氢呋喃与甲醇的混合溶剂。优选地,四氢呋喃、乙酸乙酯、乙腈和甲基叔丁基醚中的任意一种溶剂与甲醇的体积比为2:1~4:1;进一步优选为3:1。步骤(1)中,所述的3,5-二甲氧基苯乙酮与四丁基三溴化铵的摩尔比为1:1.1~1:1.5;优选为1:1.1。步骤(1)中,控制溶剂的用量,使3,5-二甲氧基苯乙酮的浓度为1~1.5mmol/ml;优选为1.375mmol/ml。步骤(1)中,所述的溴代反应为在室温下搅拌反应1~3h;优选为在室温下搅拌反应2h。步骤(1)中,在反应结束后,向反应液中加入异丙醇和水,冰浴下搅拌析晶,抽滤,将滤饼干燥,即得。步骤(2)中,所述的还原剂为硼氢化钠、硼氢化钾和三乙酰氧基硼氢化钠中的任意一种或几种组合;优选为硼氢化钠。步骤(2)中,所述的还原剂与2-溴-1-(3,5-二甲氧基苯基)乙酮的摩尔比为0.5~1.5;优选为0.5。步骤(2)中,控制甲醇的用量,使得2-溴-1-(3,5-二甲氧基苯基)乙酮的浓度为0.1~0.3g/ml;优选为0.2g/ml。步骤(2)中,所述的还原反应为在室温下搅拌反应1~3h;优选为在室温下搅拌反应2h。步骤(2)中,反应结束后,向反应液中加入水和乙酸乙酯,分液,收集第一有机相;依次用稀盐酸、水洗涤第一有机相,再次分液,收集第二有机相;向第二有机相中加入正庚烷,搅拌析晶,抽滤,所得滤饼干燥,即得。步骤(3)中,所述的成环反应的溶剂为四氢呋喃、甲醇、甲基叔丁基醚和丁酮中的任意一种或几种组合;优选为丁酮。步骤(3)中,所述的碱性条件为无机碱所提供的;其中,所述的无机碱为碳酸钾、碳酸钠和醋酸钠中的任意一种或几种组合;优选为碳酸钾。步骤(3)中,所述的2-溴-1-(3,5-二甲氧基苯基)乙醇与无机碱的摩尔比为1:1.5~1:2.5;优选为1:2。步骤(3)中,控制溶剂用量,使2-溴-1-(3,5-二甲氧基苯基)乙醇的浓度为0.1~0.2g/ml;优选为0.17g/ml。步骤(3)中,所述的成环反应为在室温下搅拌反应2~10h;优选为在室温下搅拌反应6h。步骤(3)中,在反应结束后,直接抽滤,所得滤液不需进一步处理,在下一反应中直接使用。步骤(4)中,2-(3,5-二甲基氧基)环氧乙烷与叔丁胺的摩尔比为1:2~1:3;优选为1:2。步骤(4)中,所述的缩合反应为在50~70℃下搅拌反应3~8h;优选为60℃下搅拌反应6h。步骤(4)中,在反应结束后,直接减压浓缩,即得。步骤(5)中,所述的水解反应的溶剂为甲醇、乙醇和四氢呋喃中的任意一种或几种组合;优选为乙醇。步骤(5)中,控制溶剂用量,使1-(3,5-二甲氧基苯基)-2-叔丁氨基-乙醇的浓度为0.5~1mol/ml;优选为0.72mol/ml。步骤(5)中,所述的酸性条件为无机酸所提供;其中,所述的无机酸为盐酸、氢溴酸和30%稀硫酸中的任意一种或几种组合;优选为氢溴酸。步骤(5)中,控制有机酸的加入量,使其与1-(3,5-二甲氧基苯基)-2-叔丁氨基-乙醇的摩尔质量比为0.2~0.5mol/96g;优选为0.36mol/96g。步骤(5)中,所述的水解反应为60~80℃搅拌反应3~8h;优选为70℃搅拌反应6h。为了解决上述第二个技术问题,本发明公开了上述特布他林在制备如式vii所示的硫酸特布他林中的应用,将1-(3,5-二羟基苯基)-2-叔丁氨基-乙醇的盐用碳酸氢钠水溶液调节ph后(即用碳酸氢钠水溶液游离后),用乙酸乙酯和水搅拌分液,萃取,分出第一有机相;用水洗涤第一有机相,分液,得到第二有机相;向第二有机相中加入乙醇,搅拌下,再向其中滴加稀硫酸溶液,滴毕,搅拌析晶,得到硫酸特布他林;其中,用碳酸氢钠水溶液调节ph为7-8。其中,乙酸乙酯与水的体积比为2~4:1;优选为3:1。其中,乙醇与乙酸乙酯的体积比为1:3~1:5;优选为1:4。其中,所述的稀硫酸溶液为70g浓硫酸(98%)与300ml纯化水混合配制所得。其中,本发明中对搅拌速率没有具体的要求。有益效果:与现有技术相比,本发明具有如下优势:(1)本发明采用甲基作为羟基保护基,避免了pd/c加氢脱苄基过程,具有反应条件更加温和安全,生产成本更加低廉,对环境污染更小等优点。(2)本发明中在1-(3,5-二羟基苯基)-2-叔丁氨基-乙醇(特布他林)溶解在乙酸乙酯和乙醇的混合溶剂时,向其中滴加稀硫酸溶液,常温搅拌下可以直接析晶得到硫酸特布他林成品,操作更加方便,且总摩尔收率约60%,远高于目前文献报道中的收率,适合工业化生产。附图说明下面结合附图和具体实施方式对本发明做更进一步的具体说明,本发明的上述和/或其他方面的优点将会变得更加清楚。图1为实施例1的合成路线图。具体实施方式下面结合具体实施方式对本发明做更进一步的具体说明,本发明的上述和/或其他方面的优点将会变得更加清楚。实施例1:一种硫酸特布他林的制备方法,参照图1所示的合成路线,具体步骤如下:(1)将3,5-二甲氧基苯乙酮100g(mw:180.20,0.55mol)加入三口瓶中,加入300ml四氢呋喃和100ml甲醇,加入294g(mw:482.18,0.61mol)四丁基三溴化铵,室温下搅拌反应2h。反应完毕后,向体系中加入1l异丙醇和1l纯化水,冰水浴下搅拌析晶2h,减压抽滤,将滤饼50℃鼓风干燥8h,得到淡黄色固体129g(摩尔收率90%)。(2)将2-溴-1-(3,5-二甲氧基苯基)乙酮120g(mw:259.10,0.46mol)加入三口瓶中,加入600ml甲醇,冰水浴下分批次加入硼氢化钠8.76g(mw:37.83,0.23mol),加入完毕后,室温搅拌2h。反应完毕后,向体系中加入600ml纯化水,600ml乙酸乙酯,分液,有机相分别用稀盐酸600ml洗涤一次,600ml纯化水洗涤一次,分液,收集有机相,向有机相中加入3.6l正庚烷,搅拌析晶2h,减压抽滤,滤饼50℃鼓风干燥8h,得到类白色固体115g(摩尔收率95%)。(3)将2-溴-1-(3,5-二甲氧基苯基)乙醇110g(mw:261.12,0.42mol)加入三口瓶中,加入660ml丁酮,加入碳酸钾116g(mw:138.21,0.84mol),加入完毕后,室温搅拌6h。反应完毕后,将体系减压抽滤,收集滤液,不经处理直接进行下步投料。(4)向步骤(3)中2-(3,5-二甲基氧基)环氧乙烷(mw:180.20,0.42mol)的反应液中,加入62g叔丁胺(mw:73.14,0.85mol),60℃搅拌反应6h。反应完毕后,将体系减压浓缩,得到90.71g淡黄色油状物1-(3,5-二甲氧基苯基)-2-叔丁氨基-乙醇(步骤3与步骤4合并摩尔收率85%)。(5)向90g淡黄色油状物1-(3,5-二甲氧基苯基)-2-叔丁氨基-乙醇(mw:253.34,0.36mol)中加入500ml乙醇,加入氢溴酸水溶液(4mol/l)300ml,70℃搅拌反应6h。反应完毕后,用碳酸氢钠水溶液调节体系ph至7-8,加入3l乙酸乙酯、1l纯化水,搅拌分液,有机相继续用1l纯化水洗涤一次,分液,收集有机相。向有机相中加入乙醇750ml,搅拌下,向体系中滴加稀硫酸溶液(70g浓硫酸与300ml纯化水混合配制所得),滴毕后,室温搅拌析晶6h,减压抽滤,将滤饼60℃鼓风干燥8h,得到白色固体硫酸特布他林86.8g(摩尔收率89%)。实施例2:对本发明中的硫酸特布他林合成路线做了充分的参数优化,参数优化结果如下:1、溴代反应(1)溴代反应溶剂种类优化结果如下(表1),其他参数同实施例1中步骤(1):表1以上结果可知:当用四氢呋喃/甲醇作为溴代反应溶剂时,后处理过程析晶较好,而另外三种溶剂析晶皆不理想。(2)溴代反应溶剂比列优化结果如下(表2),其他参数同实施例1中步骤(1):表2以上结果可知:当用四氢呋喃/甲醇体积比为3/1时,2h可以反应完全,2/1和4/1时不能反应彻底或反应时间较长,故优选四氢呋喃/甲醇体积比为3/1。(3)溴代反应溴化试剂当量优化结果如下(表3),其他参数同实施例1中步骤(1):表3以上结果可知:四丁基三溴化铵当量(摩尔当量)为1.0时,反应不彻底,而1.1~1.5当量时,反应均较为彻底,且反应时间差别不大,故优选1.1当量。2、还原反应(1)还原反应中还原剂的选择优化如下(表4),其他参数同实施例1中步骤(2):表4以上结果可知:三种还原剂均能使反应较为彻底,优选分子量小的物料,故优选硼氢化钠作为还原剂。(2)还原反应中还原剂当量的优化如下(表5),其他参数同实施例1中步骤(2):表5以上结果可知:硼氢化钠摩尔当量为0.5时2h反应完全,当量超过1.2时产物杂质开始变多变大,故优选0.5当量。3、成环反应(1)成环反应中溶剂种类优化如下(表6),其他参数同实施例1中步骤(3):表6以上结果可知:成环反应中四氢呋喃、甲醇、甲基叔丁基醚、丁酮作为溶剂时,反应均较为彻底,但是由于成环反应结束后,不分离得到产物,直接以反应液进行下步投料,分别以这四种溶剂在缩合反应中制备1-(3,5-二甲氧基苯基)-2-叔丁氨基-乙醇时,发现只有丁酮作为溶剂时反应较好,其余三种溶剂均不能使缩合反应进行的比较彻底或者反应时间超过12h,故优选丁酮作为反应溶剂。(2)成环反应中无机碱种类优化如下(表7),其他参数同实施例1中步骤(3):表7以上结果可知:成环反应中碳酸钾作为无机碱时,反应时间最短,故优选碳酸钾作为反应溶剂。(3)成环反应中无机碱当量优化如下(表8),其他参数同实施例1中步骤(3):表8以上结果可知:成环反应中碳酸钾摩尔当量为2.0时,反应较为彻底,故优选碳酸钾摩尔当量为2.0。4、缩合反应(1)缩合反应中叔丁胺当量优化如下(表9),其他参数同实施例1中步骤(4):表9以上结果可知:缩合反应中叔丁胺当量为2.0时,反应已较为彻底,故优选叔丁胺摩尔当量为2.0。5、水解反应(1)水解反应中溶剂种类优化如下(表10),其他参数同实施例1中步骤(5):表10以上结果可知:水解反应中,乙醇作为溶剂6h反应已较为彻底,故优选乙醇作为水解反应的有机溶剂。(2)水解反应中酸种类优化如下(表11),其他参数同实施例1中步骤(5):表11以上结果可知:水解反应中,氢溴酸作为水解试剂时,6h反应已较为彻底,故优选氢溴酸作为水解试剂。6、硫酸特布他林制备硫酸特布他林制备析晶过程乙醇与乙酸乙酯体积比优化如下(表12),其他参数同实施例1中步骤(5):表12乙醇与乙酸乙酯体积比析晶结果1:3白色固体,产率75%1:4白色固体,产率90%1:5灰白色固体,产率90%以上结果可知:硫酸特布他林制备析晶过程乙醇与乙酸乙酯体积比1:4,析晶产物的状态以及收率均较好,故乙醇与乙酸乙酯体积比优选1:4。硫酸他布他林析晶过程加入乙醇主要目的是促进了水和乙酸乙酯的互溶性,因此析晶过程的溶剂除了乙酸乙酯和水,加入的第三种溶剂必须能与水和乙酸乙酯均互溶。发明人同时考察了甲醇、乙醇、四氢呋喃、n,n-二甲基甲酰胺及二甲基亚砜作为第三种溶剂时的析晶情况,结果显示当加入的第三种溶剂为甲醇、四氢呋喃、n,n-二甲基甲酰胺及二甲基亚砜,得到的产物纯度均低于加入乙醇时析晶得到的产物,故第三种溶剂优选乙醇。具体结果见表13。表13本发明提供了一种特布他林的合成方法及其在制备硫酸特布他林中的应用的思路及方法,具体实现该技术方案的方法和途径很多,以上所述仅是本发明的优选实施方式,应当指出,对于本
技术领域:
的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。本实施例中未明确的各组成部分均可用现有技术加以实现。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1