一种含硼羟基有机化合物及其制备方法和应用与流程
[0001]
本发明属于新材料技术领域,具体涉及一种含硼羟基有机化合物及其制备方法和应用。
背景技术:
[0002]
由于有机半导体材料在合成上具有多样性、制造成本相对较低和优良的光学与电学性能,有机发光二极管(oled)在光电器件(例如平板显示器和照明)的应用方面具有很大的潜力。
[0003]
为了提高纯有机发光材料在有机发光二极管中的发光效率,2012年,日本九州大学的adachi教授设计合成了一些列有机化合物发光材料,其特征在于引入了一系列电子供体单元和电子受体单元,在一定程度减小了化合物单线态能级(s1)与三线态能级(t1)间的能隙,这样可以让三线态激子(t1)从环境中获取热能通过反系间穿越过程实现单线态激子(s1)辐射发光,也叫热激活延迟荧光,该发光过程可以大大提高纯有机材料的发光效率。这引起人们对纯有机热激活延迟荧光材料的浓厚兴趣。至今,纯有机热激活延迟荧光材料的内部量子效率已接近100%。
[0004]
然而,该类材料的发光性能和种类还需进一步改善,特别是目前所选用的电子受体单元种类较少,如含硼羟基的有机电子受体单元的发光材料还未被开发,为了进一步提高该类纯有机发光材料性能和拓宽这类材料选择范围,含新型电子受体单元的纯有机化合物材料急需被开发出来。
技术实现要素:
[0005]
发明目的:鉴于上述现有技术的不足,本发明的目的在于提供一类含硼羟基的新型有机化合物,具体将含硼羟基的氧或硫杂蒽作为电子受体单元,以强给电子能力的三芳香胺、咔唑及其衍生物作为电子供体单元,制备了一系列的新型热激活延迟荧光材料。由于这类化合物具有新型、优良的电子受体单元,且具有良好的刚性、化学及热稳定性,因此可以有效的提高化合物的稳定性、发光效率及相应器件的性能。
[0006]
技术方案:本发明提供一种如通式(i)结构所示的含硼羟基的有机化合物:
[0007][0008]
其中,式i中所述ar1为具有强供电子能力的芳香胺、咔唑或其衍生物的芳香环烃,式i中所述x为氧或硫原子,虚线代表x(氧或硫原子)与羟基(oh)中氢原子所形成的氢键。
[0009]
具体的,所述的含硼羟基有机化合物,优先选自如下通式:
[0010][0011][0012]
其中,x为氧或硫原子。
[0013]
本发明内容还包括含硼羟基有机化合物的制备方法,该制备方法包括以下步骤:
[0014]
1)首先以2-溴-1,3-二氟-5碘苯(1-a)为原料在碱性环境下与苯酚或者苯硫酚高温反应得到相应的二苯氧醚衍生物或二苯硫醚衍生物;
[0015]
2)然后将步骤1)制备的二苯氧醚衍生物(1-b)或二苯硫醚衍生物(2-b)分别与含硼酸或硼脂的芳香胺、咔唑或其衍生物通过suzuki偶联反应合成相应的偶联产物中间体(1-c,2-c,3-c,4-c,9-c,10-c,11-c和12-c);或将二苯氧醚衍生物(1-b)或二苯硫醚衍生物(2-b)分别与二芳胺、咔唑及其衍生物通过buchwald-hartwig偶联反应合成相应的偶联产物中间体(5-c,6-c,7-c,8-c,13-c,14-c,15-c和16-c);
[0016]
3)最后将步骤2)制备的偶联中间体(1-c~16-c)在无水、无氧和低温的条件下,利用正丁基锂n-buli拔去溴原子,然后加入三溴化硼搅拌反应,最后在n,n-二异丙基乙胺的碱性环境下,通过控制反应温度和时间,最终得到本发明的含硼羟基有机化合物,本发明通过控制反应原料、反应条件等使得含硼羟基有机化合物是半边成环产物,具体参见b-1~b16,其结构中含有氢键,属于半边成环产物,主要结构如下:
[0017]
现有技术中合成的化合物均为全成环结构,类似这样:
[0018]
本发明内容还包括一种按照本发明的含硼羟基的有机化合物在有机电子器件中的应用。
[0019]
其中,所述的有机电子器件为有机发光二极管(oled)、有机光伏电池(opv)、有机发光电池(oleec)、有机场效应管(ofet)、有机发光场效应管、有机激光器,有机自旋电子器件,有机传感器及有机等离激元发射二极管(organic plasmon emitting diode)。
[0020]
本发明内容还包括一种有机电子器件,所述有机电子器件包含所述的含硼羟基有机化合物。
[0021]
其中,所述含硼羟基有机化合物质量浓度为5-15wt%。
[0022]
下面给出合适的按照本发明的含硼羟基有机化合物的具体例子,但是不限于:
[0023]
[0024]
[0025][0026]
有益效果:与现有技术相比,本发明具备以下优点:本发明制备的化合物具有新型、优良的电子受体单元,且具有良好的刚性、化学及热稳定性,因此可以有效的提高化合物的稳定性、发光效率及相应器件的性能。本发明还涉及包含有按照本发明含硼羟基有机化合物的有机电子器件,特别是有机发光二极管,及其在显示及照明技术中的应用。通过器件结构优化,改变该含硼羟基有机化合物在基质中的浓度,可达到最佳的器件性能,便于实现高效高亮度高稳定的oled器件,对全彩显示和照明应用提供了较好的材料选项。
附图说明
[0027]
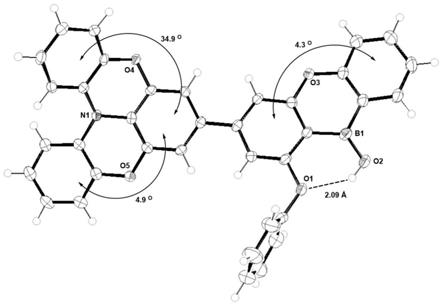
图1含硼羟基有机物b-3的x射线单晶结构;
[0028]
图2含硼羟基有机物b-4的单晶结构。
具体实施方式
[0029]
实施例1含硼羟基有机物的合成
[0030]
含硼羟基有机物b-1的合成路线如下:
[0031][0032]
1、合成中间体1-b:
[0033]
在一个干燥的双口瓶里放置1-a(0.63g,2mmol),碳酸钾(1.10g,8mmol),苯酚(0.75g,8mmol),抽真空充氮气循环三次,然后加入10ml n-甲基吡咯烷酮,150℃搅拌反应24小时,冷却到室温,加水析出沉淀,抽滤,用正己烷洗,干燥,得到白色固体0.79g,产率85%。
[0034]
2、合成中间体1-c:
[0035]
在一个干燥的双口瓶里放置1-b(3.72g,8mmol),4-硼酸三苯胺(2.54g,8.8mmol),pd[(pph)3]4(0.28g,0.24mmol),抽真空充氮气循环三次,然后加入32ml 1,4-二氧六环和
16ml k2co3(2m)水溶液,105℃搅拌反应12小时,冷却到室温,用二氯甲烷萃取,浓缩除去二氧六环,加入大量二氯甲烷过硅胶,滤液浓缩,然后用二氯甲烷和石油醚的混合溶剂重结晶,最后得到白色固体3.73g,产率80%。
[0036]
3、合成硼羟基有机物b-1:
[0037]
在一个干燥的schlenck瓶中加入1-c(0.29g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),(含n-buli正己烷溶液,浓度是2.5mol/l,体积是0.26ml,溶质物质的量为0.65mmol)-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.04g,产率15%。
[0038]
实施例2含硼羟基有机物b-2的合成
[0039]
含硼羟基有机物b-2的合成路线:
[0040][0041]
1、合成中间体2-b:
[0042]
在一个干燥的双口瓶里放置1-a(0.63g,2mmol),碳酸钾(1.10g,8mmol),苯硫醇(0.88g,8mmol),抽真空充氮气循环三次,然后加入10ml n-甲基吡咯烷酮,150℃搅拌反应24小时,冷却到室温,加水析出沉淀,抽滤,用正己烷洗,干燥,得到白色固体0.74g,产率75%。
[0043]
2、合成中间体2-c:
[0044]
在一个干燥的双口瓶里放置2-b(3.98g,8mmol),4-硼酸三苯胺(2.54g,8.8mmol),pd[(pph)3]4(0.28g,0.24mmol),抽真空充氮气循环三次,然后加入32ml 1,4-二氧六环和16ml k2co3(2m)水溶液,105℃搅拌反应12小时,冷却到室温,用二氯甲烷萃取,浓缩除去二氧六环,加入大量二氯甲烷过硅胶,滤液浓缩,然后用二氯甲烷和石油醚的混合溶剂重结晶,最后得到白色固体4.03g,产率82%。
[0045]
3、合成硼羟基有机物b-2:
[0046]
在一个干燥的schlenck瓶中加入2-c(0.31g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应
30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.03g,产率10%。
[0047]
实施例3含硼羟基有机物b-3的合成
[0048]
含硼羟基有机物b-3的合成路线:
[0049][0050]
1、合成中间体3-c:
[0051]
在一个干燥的双口瓶里放置1-b(3.72g,8mmol),4-硼酸酯-二氧桥三苯胺(文献dalton trans.2019,48,4596-4601中的1-b)(3.51g,8.8mmol),pd[(pph)3]4(0.28g,0.24mmol),抽真空充氮气循环三次,然后加入32ml 1,4-二氧六环和16ml k2co3(2m)水溶液,105℃搅拌反应12小时,冷却到室温,用二氯甲烷萃取,浓缩除去二氧六环,加入大量二氯甲烷过硅胶,滤液浓缩,然后用二氯甲烷和石油醚的混合溶剂重结晶,最后得到白色固体3.91g,产率80%。
[0052]
2、合成硼羟基有机物b-3:
[0053]
在一个干燥的schlenck瓶中加入3-c(0.31g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.03g,产率10%。
[0054]
实施例4:含硼羟基有机物b-4的合成
[0055]
含硼羟基有机物b-4的合成路线:
[0056][0057]
1、合成中间体4-c:
[0058]
在一个干燥的双口瓶里放置2-b(3.98g,8mmol),4-硼酸酯-二氧桥三苯胺(3.51g,8.8mmol),pd[(pph)3]4(0.28g,0.24mmol),抽真空充氮气循环三次,然后加入32ml 1,4-二氧气六环和16ml k2co3(2m)水溶液,105℃搅拌反应12小时,冷却到室温,用二氯甲烷萃取,浓缩除去二氧六环,加入大量二氯甲烷过硅胶,滤液浓缩,然后用二氯甲烷和石油醚的混合溶剂重结晶,最后得到白色固体3.86g,产率75%。
[0059]
2、合成硼羟基有机物b-4:
[0060]
在一个干燥的schlenck瓶中加入4-c(0.32g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.02g,产率8%。
[0061]
实施例5含硼羟基有机物b-5的合成
[0062]
含硼羟基有机物b-5的合成路线:
[0063][0064]
1、合成中间体5-c:
[0065]
在一个干燥的双口瓶里放置1-b(5.11g,11mmol),二苯胺(1.69g,10mmol),pd2(dba)3(280mg,0.3mmol),叔丁醇钠(2g,20mmol),三叔丁基磷(1.8ml,0.9mmol),然后加入200ml甲苯,100℃搅拌反应12小时,浓缩除去甲苯,然后加水,用二氯甲烷萃取,滤液浓缩,然后用二氯甲烷∶石油醚=1∶2过柱纯化,最后得到白色固体4.05g,产率80%。
[0066]
2、合成硼羟基有机物b-5:
[0067]
在一个干燥的schlenck瓶中加入5-c(0.25g,0.5mmol),在氮气流下加入5ml干燥
的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.02g,产率10%。
[0068]
实施例6含硼羟基有机物b-6的合成
[0069]
含硼羟基有机物b-6的合成路线:
[0070][0071]
1、合成中间体6-c:
[0072]
在一个干燥的双口瓶里放置2-b(5.47g,11mmol),二苯胺(1.69g,10mmol),pd2(dba)3(280mg,0.3mmol),叔丁醇钠(2g,20mmol),三叔丁基磷(1.8ml,0.9mmol),然后加入200ml甲苯,100℃搅拌反应12小时,浓缩除去甲苯,然后加水,用二氯甲烷萃取,滤液浓缩,然后用二氯甲烷∶石油醚=1∶2过柱纯化,最后得到白色固体4.31g,产率80%。
[0073]
2、合成硼羟基有机物b-6:
[0074]
在一个干燥的schlenck瓶中加入6-c(0.27g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.02g,产率10%。
[0075]
实施例7含硼羟基有机物b-7的合成
[0076]
含硼羟基有机物b-7的合成路线:
[0077]
[0078]
1、合成中间体7-c:
[0079]
在一个干燥的双口瓶里放置1-b(5.11g,11mmol),咔唑(1.67g,10mmol),pd2(dba)3(280mg,0.3mmol),叔丁醇钠(2g,20mmol),三叔丁基磷(1.8ml,0.9mmol),然后加入200ml甲苯,100℃搅拌反应12小时,浓缩除去甲苯,然后加水,用二氯甲烷萃取,滤液浓缩,然后用二氯甲烷:石油醚=1∶2过柱纯化,最后得到白色固体4.06g,产率80%。
[0080]
2、合成硼羟基有机物b-7:
[0081]
在一个干燥的schlenck瓶中加入7-c(0.25g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.02g,产率10%。
[0082]
实施例8含硼羟基有机物b-8的合成
[0083]
含硼羟基有机物b-8的合成路线:
[0084][0085]
1、合成中间体8-c:
[0086]
在一个干燥的双口瓶里放置2-b(5.47g,11mmol),咔唑(1.67g,10mmol),pd2(dba)3(280mg,0.3mmol),叔丁醇钠(2g,20mmol),三叔丁基磷(1.8ml,0.9mmol),然后加入200ml甲苯,100℃搅拌反应12小时,浓缩除去甲苯,然后加水,用二氯甲烷萃取,滤液浓缩,然后用二氯甲烷:石油醚=1∶2过柱纯化,最后得到白色固体4.30g,产率80%。
[0087]
2、合成硼羟基有机物b-8:
[0088]
在一个干燥的schlenck瓶中加入8-c(0.27g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.02g,产率10%。
[0089]
实施例9含硼羟基有机物b-9的合成
[0090]
含硼羟基有机物b-9的合成路线:
[0091][0092]
1、合成中间体9-c:
[0093]
在一个干燥的双口瓶里放置1-b(3.72g,8mmol),9-苯基-9h-咔唑-3-硼酸哪醇酯(cas:1126522-69-7)(3.25g,8.8mmol),pd[(pph)3]4(0.28g,0.24mmol),抽真空充氮气循环三次,然后加入32ml 1,4-二氧气六环和16ml k2co3(2m)水溶液,105℃搅拌反应12小时,冷却到室温,用二氯甲烷萃取,浓缩除去二氧六环,加入大量二氯甲烷过硅胶,滤液浓缩,然后用二氯甲烷和石油醚的混合溶剂重结晶,最后得到白色固体3.95g,产率85%。
[0094]
2、合成硼羟基有机物b-9:
[0095]
在一个干燥的schlenck瓶中加入9-c(0.29g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.04g,产率15%。
[0096]
实施例10含硼羟基有机物b-10的合成
[0097]
含硼羟基有机物b-10的合成路线:
[0098][0099]
1、合成中间体10-c:
[0100]
在一个干燥的双口瓶里放置2-b(3.98g,8mmol),9-苯基-9h-咔唑-3-硼酸哪醇酯(cas:1126522-69-7)(3.25g,8.8mmol),pd[(pph)3]4(0.28g,0.24mmol),抽真空充氮气循环三次,然后加入32ml 1,4-二氧气六环和16ml k2co3(2m)水溶液,105℃搅拌反应12小时,冷
却到室温,用二氯甲烷萃取,浓缩除去二氧六环,加入大量二氯甲烷过硅胶,滤液浓缩,然后用二氯甲烷和石油醚的混合溶剂重结晶,最后得到白色固体3.92g,产率80%。
[0101]
2、合成硼羟基有机物b-10:
[0102]
在一个干燥的schlenck瓶中加入10-c(0.31g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.03g,产率12%。
[0103]
实施例11含硼羟基有机物b-11的合成
[0104]
含硼羟基有机物b-11的合成路线:
[0105][0106]
1、合成中间体11-c:
[0107]
在一个干燥的双口瓶里放置1-b(3.72g,8mmol),9-萘基-9h-咔唑-3-硼酸哪醇酯(3.69g,8.8mmol),pd[(pph)3]4(0.28g,0.24mmol),抽真空充氮气循环三次,然后加入32ml 1,4-二氧气六环和16ml k2co3(2m)水溶液,105℃搅拌反应12小时,冷却到室温,用二氯甲烷萃取,浓缩除去二氧六环,加入大量二氯甲烷过硅胶,滤液浓缩,然后用二氯甲烷和石油醚的混合溶剂重结晶,最后得到白色固体4.14g,产率82%。
[0108]
2、合成硼羟基有机物b-11:
[0109]
在一个干燥的schlenck瓶中加入11-c(0.32g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.05g,产率16%。
[0110]
实施例12含硼羟基有机物b-12的合成
[0111]
含硼羟基有机物b-12的合成路线:
[0112][0113]
1、合成中间体12-c:
[0114]
在一个干燥的双口瓶里放置2-b(3.98g,8mmol),9-萘基-9h-咔唑-3-硼酸哪醇酯(3.69g,8.8mmol),pd[(pph)3]4(0.28g,0.24mmol),抽真空充氮气循环三次,然后加入32ml 1,4-二氧气六环和16ml k2co3(2m)水溶液,105℃搅拌反应12小时,冷却到室温,用二氯甲烷萃取,浓缩除去二氧六环,加入大量二氯甲烷过硅胶,滤液浓缩,然后用二氯甲烷和石油醚的混合溶剂重结晶,最后得到白色固体4.14g,产率78%。
[0115]
2、合成硼羟基有机物b-12:
[0116]
在一个干燥的schlenck瓶中加入12-c(0.33g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.05g,产率15%。
[0117]
实施例13含硼羟基有机物b-13的合成
[0118]
含硼羟基有机物b-13的合成路线:
[0119][0120]
1、合成中间体13-c:
[0121]
在一个干燥的双口瓶里放置1-b(5.11g,11mmol),9,10-二氢-9,9-二甲基吖啶(2.10g,10mmol),pd2(dba)3(280mg,0.3mmol),叔丁醇钠(2g,20mmol),三叔丁基磷(1.8ml,0.9mmol),然后加入200ml甲苯,100℃搅拌反应12小时,浓缩除去甲苯,然后加水,用二氯甲烷萃取,滤液浓缩,然后用二氯甲烷∶石油醚=1∶2过柱纯化,最后得到白色固体4.10g,产率75%。
[0122]
2、合成硼羟基有机物b-13:
[0123]
在一个干燥的schlenck瓶中加入13-c(0.27g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.03g,产率13%。
[0124]
实施例14含硼羟基有机物b-14的合成
[0125]
含硼羟基有机物b-14的合成路线:
[0126][0127]
1、合成中间体14-c:
[0128]
在一个干燥的双口瓶里放置2-b(5.47g,11mmol),9,10-二氢-9,9-二甲基吖啶(2.10g,10mmol),pd2(dba)3(280mg,0.3mmol),叔丁醇钠(2g,20mmol),三叔丁基磷(1.8ml,0.9mmol),然后加入200ml甲苯,100℃搅拌反应12小时,浓缩除去甲苯,然后加水,用二氯甲烷萃取,滤液浓缩,然后用二氯甲烷∶石油醚=1∶2过柱纯化,最后得到白色固体4.05g,产率70%。
[0129]
2、合成硼羟基有机物b-14:
[0130]
在一个干燥的schlenck瓶中加入14-c(0.29g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.04g,产率15%。
[0131]
实施例15含硼羟基有机物b-15的合成
[0132]
含硼羟基有机物b-15的合成路线:
[0133][0134]
1、合成中间体15-c:
[0135]
在一个干燥的双口瓶里放置1-b(5.11g,11mmol),5-苯基-5,11-二氢吲哚并[3,2-b]咔唑(3.32g,10mmol),pd2(dba)3(280mg,0.3mmol),叔丁醇钠(2g,20mmol),三叔丁基磷(1.8ml,0.9mmol),然后加入200ml甲苯,100℃搅拌反应12小时,浓缩除去甲苯,然后加水,用二氯甲烷萃取,滤液浓缩,然后用二氯甲烷∶石油醚=1∶2过柱纯化,最后得到白色固体4.69g,产率70%。
[0136]
2、合成硼羟基有机物b-15:
[0137]
在一个干燥的schlenck瓶中加入15-c(0.34g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.03g,产率10%。
[0138]
实施例16含硼羟基有机物b-16的合成
[0139]
含硼羟基有机物b-16的合成路线:
[0140][0141]
1、合成中间体16-c:
[0142]
在一个干燥的双口瓶里放置2-b(5.47g,11mmol),5-苯基-5,11-二氢吲哚并[3,2-b]咔唑(3.32g,10mmol),pd2(dba)3(280mg,0.3mmol),叔丁醇钠(2g,20mmol),三叔丁基磷(1.8ml,0.9mmol),然后加入200ml甲苯,100℃搅拌反应12小时,浓缩除去甲苯,然后加水,用二氯甲烷萃取,滤液浓缩,然后用二氯甲烷∶石油醚=1∶2过柱纯化,最后得到白色固体4.91g,产率70%。
[0143]
2、合成硼羟基有机物b-16:
[0144]
在一个干燥的schlenck瓶中加入16-c(0.25g,0.5mmol),在氮气流下加入5ml干燥的间二甲苯,抽真空充氮气循环三次,转至-40℃温度下冷却搅拌10分钟,在氮气流下缓慢逐滴滴加n-buli(0.65mmol,0.26ml(2.5m)),-40℃温度下搅拌反应1小时,逐渐升温至室温搅拌反应1小时。然后冷却至-40℃,滴加bbr3(0.65mmol,0.061ml),-40℃温度下搅拌反应30分钟后转移至室温搅拌反应1小时。冰浴冷却至0℃,10分钟后滴加n,n-二异丙基乙胺(1.03mmol,0.175ml),0℃条件下搅拌反应10分钟后,逐渐升温至100℃温度下搅拌反应12小时。反应结束后冷却至室温,加入醋酸钾去离子水溶液进行猝灭,然后加去离子水和二氯甲烷溶剂进行萃取,浓缩有机相,并减压除去大部分间二甲苯溶剂,加入石油醚析出固体,抽滤并干燥得黄色固体0.04g,产率12%。
[0145]
实验例
[0146]
1、含硼羟基有机物x射线单晶结构表征
[0147]
含硼羟基有机物b-3的单晶是通过用乙醇溶剂向其二氯甲烷溶液中缓慢扩散得到的,其结构如图1所示,含硼的多元环单元显示出很好的平面性,即两个苯环平面的扭转角为4.3
°
,明显低于氧桥三苯胺单元两个苯环之间的扭转角(4.9
°
和34.9
°
),这表明含硼的多元环单元具有很好的刚性。此外,值得注意的是,该晶体中硼羟基中的氢原子与邻近的苯氧醚基团中的氧原子形成了明显的氢键,并且键长为这样也能大大增强该化合物的稳定性。
[0148]
含硼羟基有机物b-4的单晶也是通过用乙醇溶剂向其二氯甲烷溶液中缓慢扩散得到的,其结构如图2所示,含硼的多元环单元显示出很好的平面性,即两个苯环平面的扭转角为4.3
°
,明显低于氧桥三苯胺单元两个苯环之间的扭转角(10.6
°
和35.1
°
),这表明含硼的多元环单元也具有一定的刚性。此外,值得注意的是,该晶体中硼羟基中的氢原子与邻近的苯硫醚基团中的硫原子形成了明显的氢键,并且键长为这在一定程度上也可以增强该化合物的稳定性。
[0149]
2、oled器件的制备和表征:
[0150]
具有ito/npd(60nm)/b-1~b-16(5-15wt%):adn(85-95wt%)(15nm)/tpbi(65nm)/lif(1nm)/al(150nm)/阴极的oled器件的制备步骤如下:
[0151]
a、阳极导电玻璃基片ito(氧化铟锡)的清洗:首次使用时,可用多种溶剂进行清洗,例如氯仿、酮、异丙醇进行清洗,然后进行紫外臭氧等离子处理;
[0152]
b、npd(n,n
′-
二-1-萘基-n,n
′-
二苯联苯胺)为空穴传输层htl(60nm),b-1~b-16和adn(9-(1-萘基)-10-(2-萘基)蒽)共同作为发光层eml(25nm),其中b-1~b-16作为客体材料以5-15wt%的重量比掺杂在主体材料adn中,tpbi(1,3,5-三(1-苯基-1h-苯并咪唑-2-基)苯)为电子传输层etl(65nm):在高真空(1
×
10-6
毫巴,mbar)中热蒸镀而成;
[0153]
c、阴极:lif/al(1nm/150nm)在高真空(1
×
10-6
毫巴)中热蒸镀而成;
[0154]
d、封装:器件在氮气手套箱中用紫外线硬化树脂封装。
[0155]
该oled器件的电流电压亮度(jvl)特性通过表征设备来表征,同时记录重要的参数如效率及外部量子效率。经检测,oled的最大外部量子效率(eqe)为25%,具体如下:
[0156]
complexb-1b-2b-3b-4b-5b-6b-7b-8b-9b-10eqe15%13%25%20%14%12%15%14%21%19%
[0157]
进一步的优化,如器件结构的优化,htm,etm及主体材料的组合优化,将进一步提
高器件的性能,特别是效率,驱动电压及寿命。进一步的优化,如器件结构的优化,htm,etm及主体材料的组合优化,将进一步提高器件的性能,特别是效率,驱动电压及寿命。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1