包含血清来源蛋白质的多孔性细胞支架及制备方法与流程
1.涉及一种包含血清来源蛋白质的多孔性细胞支架及其制备方法。
背景技术:
2.多孔性支架作为用于伤口治愈、灼伤治愈、药物传递及损伤组织再生的支架而被广泛使用。特别是用于损伤组织再生的支架,要求适合于将从少量组织碎片中提取、分离的细胞培养成充足量的结构和稳定性,需具有体内移植后不出现副作用的生物合适性和生物降解性。因此,用于有效实现细胞再生和生长的生物降解性支架需具有组织细胞能够粘着于支架表面而形成三维结构的组织的多孔性结构,水分和细胞生长因子等移动容易,需适合细胞的附着和生长。另外,多孔性支架移植到体内后,需与周围组织良好融合,没有炎症反应等副作用,在组织再生后自行进行生物降解,不残留异物质,具有较高生物适合性。因此,生物合适性、生物降解性以及机械物性优秀的多孔性支架是组织再生与复原所必需的。
3.细胞培养相关生物医药品产业市场自2011年之后每年呈现两位数增长势头。特别是2014年,形成了1200亿美元以上的市场,但在韩国国内,三维细胞培养相关专业人才匮乏,依赖于外国机构。三维细胞培养技术是一门前景光明的尖端技术,不仅是药物效能和毒性检索,还应用于人造器官开发等,据bcc调查估计,2016年市场规模达到60亿美元左右。保持每年10%以上增长势头,预计2019年增长到80亿美元规模。另外,组织工程学及再生相关市场(含基于细胞的人造器官)2016年全世界达到136亿美元规模,预计2021年将达到608亿美元,是有望实现年均34.9%高增长率的朝阳领域。
4.因此,要求研发具有高存活率和保管性、用于生产与实际人类组织类似地体现的细胞聚集体的多孔性细胞支架。
技术实现要素:
5.技术课题
6.一种形态提供一种包含血清来源蛋白质的多孔性细胞支架,所述血清来源蛋白质是对分离的血清或血浆蛋白质水溶液进行交联剂处理,使血清血浆蛋白质水溶液内蛋白质交联后,用还原剂还原而收得。
7.又一形态提供一种多孔性细胞支架及包括在所述多孔性细胞支架内分植的细胞的组织修复或再生用组合物。
8.又一形态提供一种评价候选物质的药理学活性或毒性的方法,包括:在多孔性细胞支架分植细胞并进行三维培养而形成三维细胞聚集体的步骤;及对所述三维细胞聚集体进行候选物质处理的步骤。
9.又一形态提供一种生产目标物质的方法,包括:在多孔性细胞支架分植细胞并进行三维培养而形成三维细胞聚集体的步骤;及从所述三维细胞聚集体的培养物或培养液分离目标物质的步骤。
10.又一形态提供一种制备包含血清来源蛋白质的多孔性细胞支架的方法,包括:对
分离的血清或血浆蛋白质水溶液进行交联剂处理,使血清或血浆蛋白质水溶液内蛋白质交联的步骤;用还原剂使交联的血清或血浆蛋白质水溶液内蛋白质反应而收得反应物的步骤;及将所述反应物均质化而收得血清来源蛋白质的步骤。
11.技术方案
12.为了达成所述目的,一种形态提供一种包含血清来源蛋白质的多孔性细胞支架,所述血清来源蛋白质是对分离的血清或血浆蛋白质水溶液进行交联剂处理,使血清血浆蛋白质水溶液内蛋白质交联后,用还原剂还原而收得。
13.本说明书中的术语“血清来源蛋白质”,可以意味着对通常用于组织培养的牛胎血清(fetal bovine serum:fbs)、小牛血清(bovine calf serum:bcs)或来源于其他动物(例如,哺乳类或人类)的血清进行交联剂处理,使血清内蛋白质交联而收得的蛋白质。另外,可以意味着利用作为血清内蛋白质的血清白蛋白、脂蛋白、触珠蛋白、转铁蛋白、铜蓝蛋白、免疫球蛋白、各种补体、血纤蛋白原、凝血酶原、纤溶酶原、激肽原、前激肽释放酶、纤连蛋白、α2
‑
hs
‑
糖蛋白、血管紧张素原、激素等,使血液中暂时存在的蛋白质的水溶液内蛋白质交联而收得的蛋白质。
14.本说明书中使用的交联剂包括右旋糖酐二醛(dextran dialdehyde)、1
‑
乙基
‑3‑
[3
‑
二甲基氨基丙基]碳二亚胺盐酸盐(1
‑
ethyl
‑3‑
[3
‑
dimethylaminopropyl]carboimide hydrochloride)、乙烯胺(vinylamine)、甲基丙烯酸2
‑
氨基乙酯(2
‑
aminoethyl methacrylate)、3
‑
氨基丙基甲基丙烯酰胺(3
‑
aminopropyl methacrylamide)、乙二胺(ethylene diamine)、乙二醇二甲基丙烯酸酯(ethylene glycol dimethacrylate)、甲基丙烯酸甲酯(methyl methacrylate)、n,n
‑
亚甲基双丙稀酰胺(n,n
′‑
methylene
‑
bisacrylamide)、n,n
’‑
亚甲基双甲基丙烯酰胺(n,n
′‑
methylenebis
‑
methacrylamide)、二烯丙基酒石二酰胺(diallyltartardiamide)、甲基丙烯酸烯丙酯(allyl(meth)acrylate)、低级亚烷基二醇二(甲基)丙烯酸酯(lower alkylene glycol di(meth)acrylate)、聚低级亚烷基二醇二(甲基)丙烯酸酯(poly lower alkylene glycol di(meth)acrylate)、低级亚烷基二(甲基)丙烯酸酯(lower alkylene di(meth)acrylate)、二乙烯醚(divinyl ether)、二乙烯砜(divinyl sulfone)、二乙烯苯(divinylbenzene)、三乙烯苯(trivinylbenzene)、三羟甲基丙烷三(甲基)丙烯酸酯(trimethylolpropane tri(meth)acrylate)、季戊四醇四(甲基)丙烯酸酯(pentaerythritol tetra(meth)acrylate)、双酚a二(甲基)丙烯酸酯(bisphenol a di(meth)acrylate)、亚甲基双(甲基)丙烯酰胺(methylenebis(meth)acrylamide)、邻苯二甲酸三丙烯酯(triallyl phthalate)、邻苯二甲酸二烯丙酯(diallyl phthalate)、烯丙基缩水甘油醚(allyl glycidyl ether)、烷基氯(alkyl choloride)、转谷氨酰胺酶(transglutaminase)、赖氨酰氧化酶(lysyl oxidase)、蛋白质二硫键异构酶(protein disulfide
‑
isomerase)、蛋白质二硫键还原酶(protein
‑
disulfide reductase)、巯基氧化酶(sulfhydryl oxidase)、脂氧合酶(lipoxygenase)、多酚氧化酶(polyphenol oxidase)、酪氨酸酶(tyrosinase)、过氧化物酶(peroxidase)、虫漆酶(laccase)、辣根过氧化物酶(horseradish peroxidase)及他们的组合,此外,只要是使蛋白质结合的物质,则均可应用。
[0015]
所述交联剂中的酶交联剂可以是任意微生物(例如,streptoverticillium mobaraense)来源的酶。
[0016]
本说明书中的术语“还原剂”意味着使血清内蛋白质的二硫键还原的物质。在本说明书中使用的还原剂包括β
‑
巯基乙醇(β
‑
mercaptoethanol)、二硫苏糖醇(dithiothreitol:dtt)、三(2
‑
羧乙基)膦(tris(2
‑
carboxyethyl)phosphine:tcep)、半胱氨酸(cysteine)、谷胱甘肽(glutathione)及三(3
‑
羟基丙基)膦(tris(3
‑
hydroxypropyl)phosphine:thpp),此外,只要是使蛋白质的二硫键还原的物质,则均可应用。
[0017]
一个具体例的多孔性细胞支架的气孔大小可以为50至600μm、100至550μm、150至500μm、200至450μm、250至400μm、300至350μm、50至300μm、100至250μm、150至200μm、300至600μm、350至550μm、400至500μm。
[0018]
一个具体例的多孔性细胞支架的弹性率可以为1至10kpa、2至8kpa、3至8kpa、1至5kpa、4至10kpa、6至10kpa、1至3kpa或4至6kp。
[0019]
一个具体例的多孔性细胞支架的空隙率可以为10至80%、20至80%、30至70%、40至60%、10至40%、10至30%、50至80%或60至80%。
[0020]
在另一具体例中,所述多孔性细胞支架可以出现向固体或半固体的可逆相变。另外,所述多孔性细胞支架可以为不溶性。
[0021]
一个具体例的多孔性细胞支架尤其适合于组织工程学、修复或再生。空隙率的差异可以使得能够实现不同细胞类型向多孔性细胞支架适宜部位的移动。在又一体现例中,空隙率的差异可以使得能够实现发育/修复/再生组织的适宜结构化所要求的、包含多孔性细胞支架的细胞类型中适宜的细胞与细胞的连接发育。例如,细胞处理的扩张可以通过多孔性细胞支架性物质的多样空隙率而更适宜地得到调节。因此,多孔性细胞支架可以包含任意的组织细胞。
[0022]
一个具体例的多孔性细胞支架的用途可以包括用于组织工程学、三维细胞培养或治疗性使用的细胞搬运用途。
[0023]
在一个具体例中,所述多孔性细胞支架可以分植了细胞。一个具体例的多孔性细胞支架内分植的细胞可以包括由细菌细胞、酵母细胞、哺乳类细胞、昆虫细胞及植物细胞构成的组。
[0024]
就所述细胞而言,例如,真核细胞可以为酵母、真菌、原生动物(protozoa)、植物、高等植物及昆虫、或两栖类的细胞、或cho、hela、hek293、及诸如cos
‑
1的哺乳动物的细胞,例如,可以为本行业一般使用的、经培养的细胞(in vitro)、移植的细胞(graft cell)及原代细胞培养(体外及离体(ex vivo)、及活体(in vivo)细胞、及包括人类在内的哺乳动物的细胞(mammalian cell)。另外,所述有机体可以为酵母、真菌、原生动物、植物、高等植物及昆虫、两栖类或哺乳动物。
[0025]
一个具体例的多孔性细胞支架内分植的细胞可以包括选自软骨细胞、纤维软骨细胞、骨细胞、成骨细胞、破骨细胞、滑膜细胞、骨髓细胞、神经细胞、脂肪细胞、间充质细胞、上皮细胞、肝细胞、肌肉细胞、基质细胞、血管细胞、干细胞、胚胎干细胞、间充质干细胞、来源于脂肪组织的前体细胞、外周血祖细胞、从成体组织中分离出的干细胞及他们的组合的某一种。
[0026]
所述多孔性细胞支架可以还包含用于诱导分植细胞的分化及增殖的生长因子、生长刺激剂、生理活性物质、或作为细胞结合介质物质的肽或多糖类等。
[0027]
在一个体现例中,所述生长因子或生长刺激剂可以包括:细胞附着介质,生物学活
性配体,整合蛋白结合序列,配体,多样的生长及/或分化制剂(例如,上皮细胞生长因子、igf
‑
i、igf
‑
ii、tgf
‑
[β]、生长及分化因子、基质来源因子sdf
‑
1,血管内皮生长因子、成纤维细胞生长因子、血小板来源生长因子、胰岛素来源生长因子及变形性生长因子、附甲状腺激素、附甲状腺激素相关肽、bfgf,神经生长因子(ngf)或肌肉形成因子(mmf)、肝素结合生长因子(hbgf)、变形性生长因子α或β、α成纤维细胞性生长因子(fgf)、上皮细胞生长因子(tgf)、血管内皮生长因子(vegf)、sdf
‑
1、tgf[β]超家庭因子、bmp
‑
2、bmp
‑
4、bmp
‑
6、bmp
‑
12、音猬因子、gdf5、gdf6、gdf8、pdgf),对特定生长因子上调产生影响的小分子、肌腱蛋白c、透明质酸、硫酸软骨素、纤连蛋白、饰胶蛋白聚糖、促凝血酶原激酶、凝血酶来源肽、tnfα/β、基质金属蛋白酶(mmp)、肝素结合位点、肝素、硫酸乙酰肝素、dna片段、dna质粒、短干扰rna(short interfering rna:sirna)、转染子或其任意的混合物。
[0028]
又一形态提供一种制备包含血清来源蛋白质的多孔性细胞支架的方法,包括:对分离的血清或血浆蛋白质水溶液进行交联剂处理而使血清或血浆蛋白质水溶液内蛋白质交联的步骤;用还原剂使交联的血清或血浆蛋白质水溶液内蛋白质反应而收得反应物的步骤;及将所述反应物均质化而收得血清来源蛋白质的步骤。
[0029]
在对所述分离的血清或血浆蛋白质水溶液进行交联剂的步骤中,交联剂的特异活度大致可以为2至100单位/mg、7至95单位/mg、12至90单位/mg、17至85单位/mg、22至80单位/mg、27至75单位/mg、32至70单位/mg、37至65单位/mg、42至60单位/mg、47至55单位/mg、2至50单位/mg、7至45单位/mg、12至40单位/mg、17至35单位/mg、22至30单位/mg、50至100单位/mg、55至95单位/mg、60至90单位/mg、65至85单位/mg、70至80单位/mg、2至30单位/mg、7至25单位/mg、12至20单位/mg、30至60单位/mg、35至55单位/mg、40至50单位/mg、60至100单位/mg、65至95单位/mg、70至90单位/mg、75至85单位/mg。
[0030]
在本说明书中,特异活度可以意味着每基质蛋白质(在本说明书中为血清或血清内蛋白质)单位的浓度。
[0031]
在使所述血清或血浆蛋白质水溶液内蛋白质与还原剂反应的步骤中,还原剂的浓度大致可以为5至50mm、10至45mm、15至40mm、20至35mm、25至30mm、5至25mm、10至20mm、25至50mm、30至45mm、35至40mm。与所述还原剂的反应可以在20至40℃下执行。
[0032]
在使所述反应物均质化而收得血清来源蛋白质的步骤中,所述均质化可以在组织粉碎机(homogenizer)中执行。所述步骤还可以包括在均质化后进行离心分离而回收血清来源蛋白质的悬浮液的步骤。
[0033]
在另一具体例中,可以还包括使所述血清来源蛋白质熟化的步骤。所述熟化的步骤可以包括:洗涤血清来源蛋白质的步骤;及将所述洗涤的血清来源蛋白质在1至15℃下熟化的步骤。
[0034]
在另一具体例中,所述方法可以还包括将所述熟化的血清来源蛋白质成型并冻结干燥的步骤。所述成型可以在希望的形状及大小的铸模中执行。所述冻结干燥可以包括在
‑
40℃至
‑
240℃下冻结1分钟至3小时时间后干燥的步骤。
[0035]
另外,所述方法可以包括用水溶液或有机溶剂洗涤干燥的血清来源蛋白质而洗涤蛋白质之外的杂质的步骤;或将所述洗涤的血清来源蛋白质在保存液中浸渍的步骤。
[0036]
一个具体例的多孔性细胞支架不仅可以稳定并连续地培养细胞,而且具有每种细胞可以表现出符合细胞特性的培养形态的效果。另外,一个具体例的多孔性细胞支架具有
利用在细胞培养皿及平板中培养的原有二维培养方法也能够长时间培养的效果。
[0037]
一种形态涉及包含多孔性细胞支架及在分植于所述多孔性细胞支架内的细胞的组织修复或再生用组合物。
[0038]
所述多孔性细胞支架内分植的细胞可以为三维培养的三维细胞聚集体。
[0039]
本说明书内术语“细胞治疗剂(cellular therapeutic agent)”,作为将从人类分离、培养及通过特殊操作而制备的细胞及组织用作治疗、诊断及预防目的的医药品(美国fta规定),意味着为了复原细胞或组织的功能,通过将活的自体、同种或异种细胞在体外增殖甄别或以其他方法使细胞生物学特性发生变化等一系列行为,将这种细胞用作疾病治疗、诊断及预防目的的医药品。
[0040]
术语“治疗”可以是指减轻、抑制或预防疾病、障碍、病情或其一种以上症状,或者包括上述内容在内,“药剂学有效量”可以意味着,满足减轻、抑制或预防疾病、障碍、病情或其一种以上症状的,在实施本技术提供的发明的过程中所利用的组合物的任意的量。
[0041]
术语“给药的”、“涂覆的”、“导入的”及“移植的”可以互换使用,意味着一个具体例的贴片或组合物借助于导致所需部位至少部分地局部化的方法或路径而配置到个体内。
[0042]
本说明书内术语“细胞聚集体”或“三维细胞聚集体”是指2个以上细胞密集的状态,既可以是组织状态,也可以是多细胞状态。各个细胞聚集体可以作为组织本身或一部分、或多细胞的聚集体而存在,可以包括从基质细胞分化的细胞类似
‑
组织体。
[0043]
本说明书内术语“三维(three
‑
dimensional)”可以意味着并非二维而是具有3个几何学参数(例如,长、宽、高或x、y、z轴)模型的立体。三维细胞聚集体可以意味着并非象普通细胞聚集体一样由细胞单一层形成的细胞聚集体,而是由多层细胞或球形等形成的细胞聚集体。
[0044]
所述组织可以为心脏、关节、骨骼、血管、胃、肝、皮肤、肾脏、软骨、肠、神经或胰脏。普通技术技术人员为了重建目标组织,可以将与之相符的体细胞或干细胞分植于所述多孔性细胞支架内。或者为了研究来源于相应组织的肿瘤细胞,可以应用相同的方法。
[0045]
一个具体例的多孔性细胞支架在生物体内移植时,具有高存活率,可以形成三维细胞聚集体或分化为组织,具有可以有用地用于组织修复或再生的效果。另外,一个具体例的多孔性细胞支架即使冻结和融解,也具有稳定的细胞培养能力,因而具有可以有用地用于细胞治疗剂的产品化的效果。
[0046]
所述三维细胞聚集体可以为可目视识别的大小的球形或片状,例如,可以是直径大致300至2000μm的球形三维细胞聚集体,在一个具体例中,可以为300至1000μm。所述球形三维细胞聚集体的直径可以根据一个具体例的培养方法,由普通技术人员调节为可目视识别的大小。另外,一个具体例的球形三维细胞聚集体可以在直径400μm内包含大致3.0
×
105至1.0
×
106个细胞。另外,在一个具体例中,所述三维细胞聚集体可以分泌多样的蛋白质及功能性物质。
[0047]
因此,一个具体例的三维细胞聚集体在供应细胞治疗剂或生理活性物质时,可以有用地用作细胞源(source),所述三维细胞聚集体的用途如下。
[0048]
如上所述,三维细胞聚集体由于能够分泌上皮细胞生长因子、多样的蛋白质及功能性物质,因而通过移植到需要其的个体,执行作为细胞供应源的作用,从而可以促进皮肤再生或血管新生。另外,通过促进组织再生或组织新生,也可以有用地用于心脏、胃、肝、皮
肤、肾脏、软骨、肠、神经或胰脏相关疾病的预防及治疗用药学组合物。
[0049]
所述心脏相关疾病例如可以包括心绞痛、心肌梗塞、心肌病、瓣膜疾病、主动脉疾病和心律不齐。所述胃相关疾病可以包括胃炎、胃溃疡、胃癌、胃腺瘤、幽门螺杆菌感染和胃malt淋巴瘤。所述肝相关疾病可以包括肝炎、结节病、脂肪肝、酒精性肝病、肝癌、肝硬化、妊娠中毒、非霍奇金淋巴瘤、威尔逊病、里氏综合征、其他新生儿黄疸、肝肿大、肝脓肿及肝血管瘤。所述皮肤相关疾病可以包括湿疹皮肤病、红斑、荨麻疹、轻度皮疹、丘疹鳞屑病、昆虫和寄生虫介导的疾病、浅表皮肤真菌病、细菌感染疾病、病毒性疾病、成人疾病、自身免疫性水疱病、结缔组织病、色素异常症、痤疮、酒糟鼻及皮肤肿瘤。所述肾脏相关疾病可以包括急性肾损伤(急性肾功能衰竭)、慢性肾脏病(慢性肾功能衰竭)、晚期慢性肾功能衰竭、慢性肾小球肾炎、快速进行性肾小球肾炎、急性肾小球肾炎、急性肾炎、急性间质性肾炎、慢性间质性肾炎、血尿、蛋白尿、无症状性泌尿功能障碍、肾病综合征、急性肾盂肾炎、肾小管缺陷、遗传性肾脏疾病、肾结石、肾积水、肾病性尿崩症、肾细胞癌、移行上皮细胞癌、血管平滑肌脂肪瘤、常染色体显性遗传性多囊性肾病、单纯性囊肿和肾结核。所述软骨相关疾病可以包括退行性关节炎、创伤后关节炎、可分离性骨软骨炎和骨软化症。所述肠相关疾病可以包括溃疡、肠炎、出血、肿瘤、肠粘连、肠梗阻、肠麻痹、结肠癌、结肠息肉、肠易激综合症、溃疡性结肠炎及克罗恩病、结核性肠炎、感染性腹泻及结肠炎、血管性肠疾病及结肠憩室病。所述神经相关疾病可以包括先天性畸形、癌症、感染、外伤、出血和自身免疫性疾病。所述胰脏相关疾病可以包括糖尿病、急性胰腺炎、慢性胰腺炎及胰腺癌。
[0050]
一个具体例的细胞治疗剂或药学组合物的给药量以构成有效成分的三维细胞聚集体为基准,大致可以为1.0
×
105至1.0
×
108细胞/kg(体重)或1.0
×
107至1.0
×
108细胞/kg(体重)。不过,给药量可以根据诸如制剂方法、给药方式、患者的年龄、体重、性别、疾病状态、饮食、给药时间、给药路径、排出速度及反应敏感性的因素而多样地处方,只要是从业人员,便可以考虑这些因素而适宜地调节给药量。给药次数可以为1次,或在临床上可接受的副作用范围内,可以为2次以上,对于给药部位,可以在1处或2处以上给药。对于人类之外的动物,也可以按每kg与人类相同的给药量给药,或者例如,按目标动物与人类的器官(心脏等)的容积比(例如,平均值)等,以换算上述给药量进行给药。作为一个具体例的治疗对象动物,可以例如人类及其之外的目标哺乳动物,具体而言,包括人类、猴子、小鼠、大白鼠、兔子、羊、牛、狗、马、猪及其他宠物等。
[0051]
一个具体例的细胞治疗剂或药学组合物可以包含细胞聚集体及药学上可接受的载体及/或添加物作为有效成分。例如,可以包含无菌水、生理盐水、常规缓冲液(磷酸、柠檬酸、其他有机酸等)、稳定剂、盐、抗氧化剂(抗坏血酸等)、表面活性剂、助悬剂、等渗剂或防腐剂等。为了局部给药,优选与生物聚合物(biopolymer)等有机物、羟磷灰石等无机物组合,具体而言,与胶原蛋白基质、聚乳酸聚合物或共聚物、聚乙二醇聚合物或共聚物及其化学衍生物等组合。在一个具体例的细胞治疗剂或药学组合物制备成适合注射的剂型的情况下,细胞聚集体可以溶解于药学上可接受的载体中或以溶解的溶液形态冻结。
[0052]
一个具体例的组织重建或修复用组合物、细胞治疗剂或药学组合物,根据其给药方法或剂型,当需要时,可以适宜地包含悬浮剂、助溶剂、稳定剂、等渗剂、防腐剂、防吸附剂、界面活性剂、稀释剂、赋形剂、ph调节剂、无痛剂、缓冲剂、还原剂、抗氧化剂等。包括如上示例的在内,适合于本发明的药学上可接受的载体及制剂在文献[雷明顿药物科学,第19
版,1995年]中详细记载。
[0053]
一个具体例的组织重建或修复用组合物、细胞治疗剂或药学组合物可以根据本发明所属技术领域的普通技术人员能够容易地实施的方法,利用药学上可接受的载体及/或赋形剂而制剂,从而制备成单位用量形态,或充入大容量容器内而制备。此时,剂型可以为油或水性介质中的溶液、悬浮液或乳化液形态,或者粉末、颗粒、片剂或胶囊形态。
[0054]
又一形态提供一种包含一个具体例的三维细胞聚集体的药物筛选用三维培养系统。
[0055]
又一形态提供一种评价候选物质的药理学活性或毒性的方法,包括:细胞分植于多孔性细胞支架进行三维培养而形成三维细胞聚集体的步骤;及对所述三维细胞聚集体进行候选物质处理的步骤。
[0056]
所述候选物质例如受检化合物或受检组合物,可以包括小分子化合物(small molecule compound)、抗体(antibody)、反义核苷酸(antisense nucleotide)、短干扰rna(short interfering rna:sirna)、短发夹rna(short hairpin rna:shrna)、核酸(nucleic acid)、蛋白质(protein)、肽(peptide)、其他提取物(extract)或天然物(nature product)。
[0057]
所述三维细胞聚集体具有模仿生物体内环境的人造细胞形态,可以有用地用于实际细胞形态及功能研究或治疗剂(例如,上述的皮肤疾病或血管疾病)等。因此,包含所述三维细胞聚集体的药物筛选用三维培养系统,在用于医药品或化妆品等的疾病治疗剂效能测试、或炎症及过敏测试等的实验中,可以替代动物实验。
[0058]
又一形态提供一种生产目标物质的方法,包括:在多孔性细胞支架分植细胞并进行三维培养而形成三维细胞聚集体的步骤;及从所述三维细胞聚集体的培养物或培养液分离目标物质的步骤。
[0059]
所述目标物质可以为目标蛋白质。
[0060]
所述培养可以在含有碳源的培养基中培养。
[0061]
本技术中使用的术语“碳源”意味着作为可以被宿主生物或生产细胞株代谢的微生物能量源,优选象可发酵碳底物、一般的供应源碳水化合物、复合营养物质等一样,特别是以纯化的形态或原料物质提供的选自由单糖、寡糖、多糖、包含丙三醇在内的醇类构成的组的供应源。根据本发明,碳源可以使用单一碳源或不同碳源的混合物。
[0062]
本技术中使用的术语“目标蛋白质(product of interest:poi)”是指在宿主细胞中借助于再组合技术而生产的多肽或蛋白质。更具体而言,蛋白质可以为不会在宿主细胞中自然产生的多肽(即,异源蛋白质),或对于宿主细胞虽然可以是天然性的(即,对宿主细胞而言的同源蛋白质),但例如借助于使用含有对poi进行编码的核酸序列的自我复制载体的转化而生产,或通过重组技术将对poi进行编码的核酸序列的一个以上拷贝整合到宿主细胞的基因组中而产生,或例如借助于启动子序列的一个以上调节序列的重组变形而产生,所述调节序列调节对poi进行编码的基因的表达。在一些情况下,本技术中使用的术语poi是指宿主细胞由借助于重组而表达的蛋白质介导的任意代谢产物。具体而言,poi为真核细胞蛋白质,优选地,为哺乳动物蛋白质。poi为真核细胞分泌的蛋白质,优选地,为作为酵母细胞分泌的蛋白质而生产的异源重组多肽或蛋白质。蛋白质例如为免疫球蛋白、免疫球蛋白片段、抑肽酶、组织因子路径抑制剂或其他蛋白酶抑制剂,以及胰岛素或胰岛素前
体、胰岛素类似物、生长激素、白介素、组织纤溶酶原激活剂、转化生长因子a或b、胰高血糖素、胰高血糖素样肽1(glp
‑
1)、胰高血糖素样肽2(glp
‑
2)、grpp(胰高血糖素样肽相关多肽)、因子vii、因子viii、因子xiii、血小板来源的生长因子1,血清白蛋白、酶(例如脂肪酶或蛋白酶),或具有与天然蛋白质相似功能的功能类似物、功能等效变体、衍生物及生物活性片段。poi在结构可以与天然蛋白质相似,可以通过在c
‑
及n
‑
末端之一或两者或在天然蛋白质的侧链中添加一个以上氨基酸、在天然氨基酸序列中的一个或多个不同部位取代一个以上氨基酸、在天然蛋白质的一端或两末端或者在氨基酸序列中的一个或一些部位缺失一个以上氨基酸,或在天然氨基酸序列中的一个以上部位插入一个以上氨基酸,从而从天然氨基酸衍生而来。对于上述提及的一些蛋白质,这种变形是公知的。
[0063]
根据本发明而生产的poi,可以为多聚体蛋白质,优选地,可以为二聚体或四聚体。poi是选自包含抗体或其片段的治疗性蛋白质、酶及肽、蛋白抗生物质、毒素融合蛋白、碳水化合物
‑
蛋白质结合体、结构蛋白质、调节蛋白质、疫苗及疫苗样蛋白或粒子、工艺酶、生长因子、激素及细胞因子或poi的代谢物质的重组或异源蛋白质。特定poi为抗体等的抗原结合分子或其片段。在特定poi中,包括单克隆抗体(mab)、免疫球蛋白(ig)或免疫球蛋白g类(igg)、重链抗体(hcab')或其片段,例如片段
‑
抗原结合(fab)、fd、单链可变片段(scfv)或其工程变体,例如fv二聚体(双抗体)、fv三聚体(三聚体)、fv四聚体或微型抗体及诸如vh或vhh或v
‑
nar等的单域抗体。
[0064]
可以使用重组宿主细胞株,将如上所述收得的转化体在适宜的培养基中培养,从培养物分离表达的生成物或代谢物质,以适当方法将其任意纯化而生产poi。
[0065]
通过将这种载体dna,例如质粒dna引入宿主内,并选择以高产率表达poi或宿主细胞代谢物的转化体,可以收得本发明的转化体。通过通常用于真核细胞转化的方法,例如电脉冲法、原生质体法、乙酸锂法、氯化钙法及其变形方法,处理宿主细胞以便能够引入外源dna。
[0066]
本发明的优选宿主细胞株保留了根据本发明使用的遗传特性,生产水平保持高水平,例如,即使在传代培养约20代、至少传代培养30代、至少传代培养50代后,也至少保持μg水平。
[0067]
本技术公开的方法可以追加包括在允许poi以分泌的形态或作为细胞内产物进行表达的条件下培养所述重组宿主细胞。随后,借助于重组而生产的poi或宿主细胞代谢物可以从细胞培养基中分离,并通过从业人员公知的技术追加纯化。
[0068]
根据本发明生产的poi可以使用相应技术领域的通常技术进行分离及纯化,这包括增加目标poi的浓度及/或减小至少一种杂质浓度。
[0069]
当poi由细胞分泌时,其可以使用相应技术领域的常规技术,从细胞培养基分离及纯化。重组表达生成物从宿主细胞的分泌,不是从酵母细胞破碎而释放出细胞内蛋白质时发生的蛋白质复杂混合物中回收,而是从培养上清液中回收,因此,鉴于包括促进纯化工序的理由,一般更有利。
[0070]
另外,所培养的转化体细胞,可以用超声或机械、酶或化学方法破碎,经poi分离及纯化,可以收得含有目标poi的细胞提取物。
[0071]
作为收得重组多肽或蛋白质生成物的分离及纯化方法,可以使用利用溶解度差异的方法(例如,盐析(salting out)及溶剂沉淀)、利用分子量差异的方法(例如,超声及凝胶
电泳)、利用电荷差异的方法(例如,离子交换色谱法)、利用特异亲和性的方法(例如,亲和性色谱法)、利用疏水性差的方法(例如,反相高性能液体色谱法)及利用等电点差异的方法(例如,等电点电泳)等方法。
[0072]
高度纯化的生成物本质上不含污染蛋白质,优选地具有至少90%纯度,更优选地至少具有95%或至少98%纯度、100%以下纯度。纯化生成物可以通过纯化细胞培养上清液等而从细胞碎片中收得。
[0073]
作为分离及纯化方法,优选以下标准方法:细胞破坏(poi从细胞内收得时),细胞(碎片)分离及精密过滤或者基于切向流动滤器(tff)的洗涤或离心分离,基于沉淀或热处理的poi纯化,基于酶消化的poi活化,基于色谱法(例如基于离子交换(iex)、疏水性相互作用色谱法(hic)、亲和性色谱法、尺寸排阻法(sec)或hplc色谱法)的poi纯化,浓缩poi沉淀及基于超滤步骤的洗涤。
[0074]
分离及纯化的poi可以根据通常方法进行鉴定,例如,蛋白质印迹、hplc、活性分析或elisa。
[0075]
一般而言,表达重组生成物的宿主细胞可以为适合于poi重组表达的任意真核细胞。哺乳动物细胞例如为bhk、cho(cho
‑
dg44、cho
‑
duxb11、cho
‑
dukx、cho
‑
k1、chok1sv、cho
‑
s)、hela、hek293、mdck、nih3t3、ns0、per.c6、sp2/0及vero细胞。用作宿主细胞的酵母的示例包括但不限于酿酒酵母属(例如,酿酒酵母)、毕赤酵母属(例如,巴斯德毕赤酵母或美多巴毕赤酵母)、komagataella属(k.pastoris、k.pseudopastoris或k.phaffii)、多形汉逊酵母或乳酸克鲁维酵母。
[0076]
发明效果
[0077]
一个具体例的多孔性细胞支架不仅能够稳定及持续地培养细胞,而且每种细胞可以表现出符合细胞特性的培养形态,模拟实际组织,具有稳定的培养及生物体内高存活率,具有可以有用地用于利用类器官的药物活性及毒性评价、细胞治疗剂或目标蛋白质的生产的效果。
附图说明
[0078]
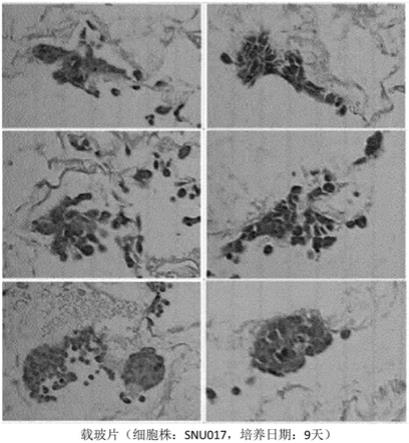
图1是利用一个具体例的多孔性细胞支架培养snu017胃癌细胞株9天时间的结果。
[0079]
图2是利用一个具体例的多孔性细胞支架培养siha宫颈癌细胞株14天时间的结果。
[0080]
图3是利用一个具体例的多孔性细胞支架培养hacs(软骨细胞)7天时间的结果。
[0081]
图4是利用一个具体例的多孔性细胞支架培养肠内分泌细胞13天时间的结果。
[0082]
图5是将利用一个具体例的多孔性细胞支架的肠内分泌细胞(enteroendocrine cell:eec)的三维细胞聚集体注入小鼠心包膜后一周的经过。
[0083]
图6是利用一个具体例的多孔性细胞支架培养肝癌细胞12天时间后实施冻结融解实验的结果。
[0084]
图7是针对利用一个具体例的多孔性细胞支架培养的肝癌细胞与阳性对照组培养的肝癌细胞的白蛋白,使用elisa方法比较表达量的图表。
具体实施方式
[0085]
下面,为了帮助理解本发明而提出了优选实施例。但是,下述实施例只是为了更容易理解本发明而提供的,并非本发明的内容特定于下述实施例。
[0086]
实施例1.多孔性细胞支架的制备
[0087]
利用血清来源蛋白质的多孔性细胞支架如下制备。
[0088]
首先,用交联剂使血清蛋白质交联,并用还原剂还原。具体而言,在100级以下的洁净棚中,将等量的牛胎血清或小牛血清用1mg/ml微生物谷氨酰胺转胺酶(特异活性单位20u/mg,西格玛奥瑞奇公司)进行处理。然后,添加作为还原剂的二硫苏糖醇(dithiothreitol:dtt,西格玛奥瑞奇公司)至最终浓度为15mm,在37℃下反应12小时,制备了反应物。然后,在所述反应物中添加洗涤缓冲液(6m尿素和0.1m乙酸钠,ph 5.0),用电动组织粉碎机(homogenizer d1000,benchmark scientific公司)均化后离心分离,回收血清来源蛋白质的悬浮液。用乳酸洗涤悬浮液后,使用高速搅拌器(maxti
◎
500s,daihan
‑
),以10,000rpm搅拌20分钟,在4℃下熟化8小时。为了将所述熟化的血清来源蛋白质成型为期望的形状,将其转移到铸模中,在
‑
80℃下冻结1小时后,冻结干燥24小时。之后,将干燥的血清来源蛋白质在常温下用100%乙醇和灭菌的三次蒸馏水分别洗涤5次,洗涤除血清来源蛋白质以外的杂质,制备了血清来源蛋白质的多孔性细胞支架。在随后的实验中,将所述血清来源蛋白质的多孔性细胞支架浸渍于保存液(1
×
pbs,细胞培养基,dw等)使用。
[0089]
所述制备的细胞支架的特性如表1所示。
[0090]
【表1】
[0091]
气孔大小平均直径约200μm(100至400μm)phpbs或组织培养基悬浮时约7.0至7.4保管温度常温
[0092]
实验例1.利用多孔性细胞支架的癌细胞三维培养
[0093]
利用所述实施例1制备的多孔性细胞支架培养癌细胞,确认培养稳定性及持续性。
[0094]
具体而言,为了从所述实施例1制备的多孔性细胞支架最大限度去除保存液,加入1
×
pbs并轻轻晃动漂洗,以便多孔性细胞支架充分浸没,然后去除1
×
pbs。再重复一次这种操作,去除保存液。然后,按5
×
105细胞数,将胃癌细胞株snu017(kclb)及宫颈癌细胞株siha(kclb)分植于多孔性细胞支架。然后,将所述分植了细胞的多孔性细胞支架在细胞培养液(rpmi、gibco公司)中,以37℃、co
2 5%的条件,在培养箱中培养。
[0095]
在培养的第9天及培养的第14天形成石蜡块,制作成载波片,执行h&e染色,执行组织检查,将其结果显示于图1及图2中。
[0096]
如图1所示,利用所述多孔性细胞支架将snu017细胞株培养9天时间的结果,确认了形成培养与在实际体内组织时类似的球形态的癌组织结构。
[0097]
另外,如图2所示,利用所述多孔性细胞支架培养siha细胞株14天时间的结果,确认了形成培养与在实际身体组织时类似的栅状组织形态的癌组织结构。
[0098]
实验例2.利用多孔性细胞支架的软骨细胞的三维培养
[0099]
软骨细胞是一般认为难以体外培养的细胞。在本实施例中,利用所述实施例1制备的多孔性细胞支架来培养软骨细胞,确认了培养稳定性及持续性。
[0100]
具体而言,除了按5
×
105细胞数分植从实际患者采集的软骨细胞(hacs)外,以与
所述实验例1相同的方法,三维培养软骨细胞。
[0101]
然后,对三维培养第7天的软骨细胞进行活细胞和死细胞染色。然后,利用共聚焦激光显微镜(lsm880 with airyscan,蔡司公司)确认染色的细胞,将其结果显示于图3中。在图3中,绿色代表活细胞,红色代表死细胞。
[0102]
图3的z1至z9意味着沿纵轴荧光拍摄每高度10μm的截面。
[0103]
如图3所示,在一周时间内未观察到显示为红色的死细胞,可以观察到稳定培养。在一个具体例的多孔性细胞支架中培养的患者来源软骨细胞表现出高生存率。
[0104]
实验例3.利用多孔性细胞支架的肠内分泌细胞的三维培养
[0105]
利用所述实施例1制备的多孔性细胞支架来培养肠内分泌细胞,确认培养稳定性及持续性。
[0106]
具体而言,除了按5
×
105细胞数分植从小鼠采集的肠内分泌细胞(enteroendocrine cell)外,以与所述实验例1相同的方法,三维培养肠内分泌细胞。
[0107]
然后,针对三维培养第11天及第13天的肠内分泌细胞,执行dapi和苏木精及伊红(h&e)染色。利用荧光显微镜(axiovert 200,蔡司公司)确认染色的细胞,将其结果显示于图4中。
[0108]
通常而言,肠内分泌细胞难以培养超过一周,而如图4所示可知,在一个具体例的多孔性细胞支架中培养的肠内分泌细胞的三维细胞聚集体,在无细胞状态低下的情况下,稳定培养超过2周。
[0109]
通过以上结果可知,一个具体例的多孔性细胞支架不仅可以稳定及持续地培养细胞,而且观察到符合每种细胞的细胞特性的培养形态。另外可知,即使以在细胞培养皿及平板中培养的原有二维培养方法,也具有能够长期培养的效果。
[0110]
实验例4.利用多孔性细胞支架的三维细胞聚集体的存活率
[0111]
在本实施例中,为了将所述实施例1制备的多孔性细胞支架应用于组织再生治疗,测量了肠内分泌细胞的三维细胞聚集体在心包膜中的存活率。
[0112]
具体而言,将与所述实施例3相同的细胞以相同方法培养后,利用汉密尔顿注射器移植到小鼠的心包膜。移植一周后,对小鼠实施安乐死,摘取、解剖心脏,直接观察剩余量。然后,只摘取移植的部分,测量其重量(wet weight),利用存活的细胞数确认存活率,形成石蜡块,制作成载波片,执行h&e染色,进行组织检查。将其结果显示于图5中。
[0113]
如图5所示,在无fbs情况下,将肠内分泌细胞在一个具体例的多孔性细胞支架中培养2周,将获得的细胞体移植到小鼠的心包膜,培养1周时间的结果,确认了超过约80%的生存率。
[0114]
考虑到通常在注入干细胞时生物体内存活率不足5%,可知一个具体例的多孔性细胞支架可以有用地用于面向组织再生的细胞治疗。
[0115]
实验例5.利用多孔性细胞支架的三维细胞聚集体的冻结融解试验
[0116]
在本实施例中,为了确认所述实施例1制备的多孔性细胞支架为了实际用于组织再生治疗的商用化而是否容易产品化及搬运,执行了冻结融解实验。
[0117]
具体而言,将肺癌细胞株nci
‑
h28和nci
‑
h2170(kclb)按5
×
105细胞数分植于一个具体例的多孔性细胞支架后,培养28天时间。冻结保管是在深度冷冻器中,在
‑
80℃下,在冻结液(介质:fbs:dmso为5:4:1)中保管30天,然后融解,培养12天时间。然后,对在所述支架
中培养的细胞执行h&e染色,将其结果显示于图6中。
[0118]
如图6所示,可以确认,一个具体例的多孔性细胞支架即使冻结或解冻,也可以实现细胞的再培养。
[0119]
这种结果意味着一个具体例的多孔性细胞支架具有有利于细胞治疗剂的产品化及搬运的效果。
[0120]
实验例6.利用多孔性细胞支架的蛋白质生产
[0121]
为了分析是否能够利用所述实施例1制备的多孔性细胞支架生产有用物质(目标蛋白质),对肝癌细胞的三维细胞聚集体的蛋白质生产能力进行了测量。
[0122]
具体而言,在24孔板中,按5
×
105细胞数分植hepg2细胞后,用mem(添加10%fbs)培养基培养7天、14天及21天。然后,在细胞培养液中,利用人alb固相夹心elisa(酶联免疫吸附试验)方法测量了白蛋白的浓度。作为对照组,执行通常的二维细胞培养方法。二维细胞培养在6孔板中执行。另外,作为阳性对照组,使用了matrigel(康宁公司,356231)及alvetex
tm
(reprocell公司,格拉斯哥,英国)。具体而言,除了使用上述可商业购买的三维细胞培养支架外,以与上述相同的方法培养了细胞。在所述对照组的细胞培养液中,测量了白蛋白的浓度,将其结果显示于图7中。
[0123]
如图7所示,一个具体例的多孔性细胞支架与阳性对照组使用及alvetex
tm
的情形相比,代表肝癌细胞激活程度的白蛋白的表达量更高。以上结果意味着一个具体例的多孔性细胞支架可以有用地用于目标物质(蛋白质)的生产。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1