结构和温度依赖性瓣状核酸内切酶底物的制作方法
结构和温度依赖性瓣状核酸内切酶底物
1.本技术要求于2019年9月16日提交的美国临时申请序列号62/901,085的优先权,所述申请以引用方式并入本文。
技术领域
2.本发明涉及瓣状核酸内切酶和使用核酸底物中的结构调节这些酶的酶促活性,所述结构在较低温度下阻遏报告切割位点处的酶促切割并且在升高的温度下改变结构以允许报告切割位点处的底物切割。
背景技术:
3.真细菌(eubacteria)、真核生物(eukarya)和古细菌(archaea)包含具有5'核酸外切酶和核酸内切酶功能、参与dna修复的酶。例如,在真细菌中的dna聚合酶i(dna pol i)的5'-核酸外切酶结构域中以及在真核生物和古细菌生物体的fen-1蛋白中发现了这些酶促活性。这些酶识别并切割包含双链和单链区域的多种核酸结构,优选的结构是由上游链3'端的模板化聚合酶延伸形成的置换5'链。包含与具有3'末端的上游链碱基配对且与具有单链5'瓣的下游链碱基配对的模板链的所得结构可称为瓣结构,并且识别并切割所述结构的酶通常可称为瓣状核酸内切酶或fen。(参见,例如,kaiser m.w.等人,j.biol.chem.274(30):21387-94(1999);shen,b.等人,bioessays 27:717-729,(2005);和finger d.l.等人,subcell biochem.62:301-326(2012),出于所有目的,所述文献各自以引用方式整体并入本文)最佳结构包含上游和下游双链体之间的重叠。重叠可以是序列重叠的一个或多个核苷酸,如在延伸引物端的序列复制置换的5'瓣的序列时将发生,或者它可以是物理的重叠,如在侵入性寡核苷酸的3'末端核苷酸与瓣链的下游双链体重叠时将发生,但不与相应的模板核苷酸互补,从而导致双瓣结构(参见,例如,kaiser,同上)。瓣状核酸内切酶识别瓣链的5'端,并且优选底物结构的切割通常发生在进入下游双链体中的一个核苷酸处,所述过程包括穿线或夹紧单链5'瓣以定位分子以进行精确切割(shen,同上)。
4.瓣状核酸内切酶可用于体外检测测定。例如,quarts和invader瓣测定利用古细菌瓣状核酸内切酶来切割合成的瓣状探针,以响应靶核酸链的存在。
技术实现要素:
5.本文提供了涉及瓣状寡核苷酸的组合物和方法,所述瓣状寡核苷酸被修饰以提供fen活性的控制,例如在测定中。例如,在一些实施方案中,对瓣状寡核苷酸的修饰是不耐热的,使得瓣状底物的切割在第一温度下被阻遏并且在升高的温度下被去阻遏,例如,当测定反应在孵育期内从室温移动至更高温度时。因此,在一些实施方案中,本技术提供了包含5'瓣修饰(例如,双链区,优选发夹形成区)的寡核苷酸,5'瓣修饰阻遏瓣状核酸内切酶在环境温度下在靶切割位点切割经修饰的寡核苷酸,并且在5'瓣修饰不阻遏切割的条件下(例如,在5'瓣不是双链或发夹形式的温度升高的条件下)可转化为可切割形式。
6.在一些实施方案中,本技术提供了一种组合物,其包含具有靶切割位点的5'发夹
侵入性切割结构,所述5'发夹切割结构包含5'瓣、下游双链茎和上游双链茎,从而限定侵入性切割结构,其中5'瓣包含发夹形成区,并且其中发夹形成区中发夹的形成抑制5'发夹侵入性切割结构在靶切割位点处的瓣状核酸内切酶切割。在某些实施方案中,5'发夹侵入性切割结构可在靶切割位点被fen-1核酸内切酶切割,优选被mg
++
瓣测定缓冲液中的afu fen-1切割。在优选的实施方案中,靶切割位点在下游双链茎中。
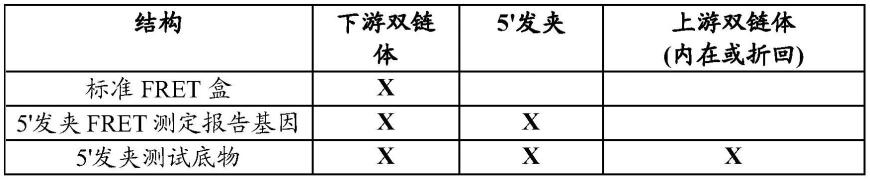
7.在某些优选的实施方案中,5'发夹侵入性切割结构选自:
8.i)包含侵入性寡核苷酸、5'发夹探针寡核苷酸和靶核酸的侵入性切割结构,其中5'发夹探针寡核苷酸退火到靶核酸上形成下游双链茎,并且侵入性寡核苷酸退火到靶核酸上形成上游双链茎;
9.ii)包含5'发夹报告基因和核酸分子的结构,5'发夹报告基因包含有包含5'发夹形成区的5'瓣、下游双链茎以及与核酸分子的3'末端部分互补的3'部分,其中核酸分子的3'末端部分退火到5'发夹报告基因的3'部分上形成侵入性切割结构的上游双链体;和
10.iii)寡核苷酸5'发夹测试底物,所述寡核苷酸包含有包含5'发夹形成区的5'瓣、下游双链茎和上游双链茎,从而限定侵入性切割结构。
11.在包含5'发夹报告基因和核酸分子的结构的一些实施方案中,核酸分子还包含5'发夹形成区。例如,在一些实施方案中,核酸分子是从5'发夹探针释放的5'瓣。
12.在一些实施方案中,5'发夹侵入性切割结构包含fret标记系统。优选地,fret标记系统的第一成员附接在5'发夹侵入性切割结构上的第一位置,并且fret标记系统的第二成员附接在5'发夹侵入性切割结构上的第二位置,并且靶切割位点在第一位置与第二位置之间。
13.fret标记系统成员的位置不限于5'发夹侵入性切割结构上的任何特定位点。在一些实施方案中,第一位置和第二位置在侵入性切割结构中(例如,沿着5'发夹侵入性切割结构中的一定长度的核酸)间隔不超过20个核苷酸,优选不超过10个核苷酸,更优选不超过9、8、7、6、5、4或3个核苷酸。
14.在一些实施方案中,5'发夹侵入性切割结构包含有包含3'阻断剂的寡核苷酸,并且在优选的实施方案中,3'阻断剂选自3'胺、3'磷酸酯、3'生物素、3'己二醇和3'双脱氧核苷酸。
15.在本技术的一些实施方案中,组合物包含溶液,例如缓冲液。在某些实施方案中,缓冲溶液包含阳离子,并且在优选的实施方案中,包含阳离子的缓冲溶液是mg
++
瓣测定缓冲液。
16.在一些实施方案中,上述任何组合物的技术还包括瓣状核酸内切酶。在优选的实施方案中,瓣状核酸内切酶包含fen-1核酸内切酶,优选热稳定fen-1核酸内切酶,更优选来自古细菌生物体的热稳定fen-1核酸内切酶。在特别优选的实施方案中,fen-1核酸内切酶包含afu fen-1、ave fen-1和pfu fen-1中的一种或多种。
17.在上述任何实施方案的实施方案中,预期组合物的实施方案可包含一种或多种pcr-瓣测定试剂,包括但不限于包含以下中的一种或多种的pcr-瓣测定试剂:dna聚合酶;脱氧核苷三磷酸;瓣状寡核苷酸;和引物。在一些实施方案中,pcr试剂还包含逆转录酶。
18.在一些实施方案中,本技术提供了一种组合物,其包含用于与核酸分子(例如,待检测的靶分子或瓣测定中的切割产物)一起形成侵入性切割结构的寡核苷酸5'发夹报告基
fen-1切割。在优选的实施方案中,靶切割位点在5'发夹报告基因的下游双链茎中,并且在特别优选的实施方案中,下游双链茎是包含环的发夹茎。在一些实施方案中,组合物还包含核酸分子,所述核酸分子包含与5'发夹报告基因的3'部分互补的3'末端部分。在优选的实施方案中,5'发夹报告基因的切割在室温下被阻遏。例如,在此类实施方案中,当组合物在室温下时,5'发夹报告基因的5'发夹形成区可以呈发夹形式。
32.在一些实施方案中,5'发夹报告基因包含标记。在某些实施方案中,5'发夹报告基因包含fret标记系统。在优选的实施方案中,fret标记系统的第一成员附接在5'发夹报告基因上的第一位置,并且fret标记系统的第二成员附接在5'发夹报告基因上的第二位置,并且靶切割位点在第一位置与第二位置之间。fret报告系统成员的位置不限于沿5'发夹报告分子链的任何特定距离,并且可以在分子的末端。在一些实施方案中,第一位置和第二位置沿5'发夹报告基因的长度间隔不超过20、19、18、17、16、15、14、13、12、11、10、9、8、7、6、5、4或3个核苷酸。
33.在一些实施方案中,5'发夹报告基因还包含3'阻断剂。优选地,3'阻断剂选自3'胺、3'磷酸酯、3'生物素、3'己二醇和3'双脱氧核苷酸。
34.在一些实施方案中,方法包括在反应混合物(例如,包含阳离子的反应混合物)中切割侵入性切割结构。在优选的实施方案中,反应混合物包含mg
++
瓣测定缓冲液。在优选的实施方案中,反应混合物包含瓣状核酸内切酶,例如,包含fen-1核酸内切酶,优选热稳定fen-1核酸内切酶,更优选来自古细菌生物体的热稳定fen-1核酸内切酶的瓣状核酸内切酶。在特别优选的实施方案中,fen-1核酸内切酶包含afu fen-1、ave fen-1和pfu fen-1中的一种或多种。
35.本技术还可应用于pcr-瓣测定中。因此,在一些实施方案中,反应混合物包含一种或多种pcr-瓣测定试剂。在某些优选的实施方案中,pcr-瓣测定试剂包含dna聚合酶、脱氧核苷三磷酸、瓣状寡核苷酸和引物中的一种或多种。在一些实施方案中,组合物包含靶核酸。
36.本技术还可应用于测试底物中,例如,用于表征瓣状核酸内切酶、瓣测定条件等。例如,在一些实施方案中,本技术提供了一种组合物,其包含用于形成具有靶切割位点的侵入性切割结构的寡核苷酸5'发夹测试底物,所述5'发夹测试底物包含5'瓣、下游双链茎和上游双链茎,从而限定可在靶切割位点被mg
++
瓣测定缓冲液中的afu fen-1核酸内切酶切割的侵入性切割结构,其中5'瓣包含发夹形成区,并且其中发夹形成区中发夹的形成抑制5'发夹测试底物在靶切割位点处的fen-1核酸内切酶切割。在优选的实施方案中,靶切割位点在5'发夹测试底物的下游双链茎中。在一些实施方案中,下游双链茎是包含环的发夹茎。在优选的实施方案中,5'发夹测试底物的切割在室温下被阻遏。例如,在此类实施方案中,当组合物在室温下时,5'发夹测试底物的5'发夹形成区可以呈发夹形式。
37.在一些实施方案中,5'发夹测试底物包含标记,诸如fret标记系统。在优选的实施方案中,fret标记系统的第一成员附接在5'发夹测试底物上的第一位置,并且fret标记系统的第二成员附接在5'发夹测试底物上的第二位置,其中靶切割位点在第一位置与第二位置之间。fret报告系统成员的位置不限于沿5'发夹测试底物分子链的任何特定距离,并且可以在分子的末端。在一些实施方案中,第一位置和第二位置沿5'发夹测试底物的长度间隔不超过20、19、18、17、16、15、14、13、12、11、10、9、8、7、6、5、4或3个核苷酸。
38.在一些实施方案中,组合物还包含有包含阳离子的缓冲溶液。在某些优选的实施方案中,包含阳离子的缓冲溶液是mg
++
瓣测定缓冲液。在一些实施方案中,组合物还包含瓣状核酸内切酶,例如,fen-1核酸内切酶,优选热稳定fen-1核酸内切酶,更优选来自古细菌生物体的热稳定fen-1核酸内切酶。在特别优选的实施方案中,fen-1核酸内切酶包含afu fen-1、ave fen-1和pfu fen-1中的一种或多种。
39.本文还提供了使用组合物(诸如上文所述的那些)的方法。例如,本技术的实施方案提供了一种测试瓣状核酸内切酶的方法,其包括:
40.i)提供用于形成具有靶切割位点的侵入性切割结构的寡核苷酸5'发夹测试底物,所述5'发夹测试底物包含:
41.a)5'瓣,
42.b)下游双链茎和上游双链茎,从而限定可在靶切割位点被mg
++
瓣测定缓冲液中的afu fen-1核酸内切酶切割的侵入性切割结构,
43.其中5'瓣包含发夹形成区,并且其中发夹形成区中发夹的形成抑制5'发夹测试底物在靶切割位点处的fen-1核酸内切酶切割;
44.ii)将5'发夹测试底物暴露于反应混合物中的瓣状核酸内切酶;和
45.iii)检测5'发夹测试底物的切割存在或不存在。
46.在优选的实施方案中,靶切割位点在5'发夹测试底物的下游双链茎中,并且在某些特别优选的实施方案中,下游双链茎是包含环的发夹茎。
47.在一些实施方案中,5'发夹测试底物包含标记,诸如fret标记系统。在优选的实施方案中,fret标记系统的第一成员附接在5'发夹测试底物上的第一位置,并且fret标记系统的第二成员附接在5'发夹测试底物上的第二位置,其中靶切割位点在第一位置与第二位置之间。fret报告系统成员的位置不限于沿5'发夹测试底物分子链的任何特定距离,并且可以在分子的末端。在一些实施方案中,第一位置和第二位置沿5'发夹测试底物的长度间隔不超过20、19、18、17、16、15、14、13、12、11、10、9、8、7、6、5、4或3个核苷酸。
48.在一些实施方案中,方法包括在反应混合物(例如,包含阳离子的反应混合物)中切割5'发夹测试底物。在优选的实施方案中,反应混合物包含mg
++
瓣测定缓冲液。在优选的实施方案中,反应混合物包含瓣状核酸内切酶,例如,包含fen-1核酸内切酶,优选热稳定fen-1核酸内切酶,更优选来自古细菌生物体的热稳定fen-1核酸内切酶的瓣状核酸内切酶。在特别优选的实施方案中,fen-1核酸内切酶包含afu fen-1、ave fen-1和pfu fen-1中的一种或多种。在优选的实施方案中,5'发夹测试底物的切割在室温下被阻遏。例如,在此类实施方案中,当组合物在室温下时,5'发夹测试底物的5'发夹形成区可以呈发夹形式。
49.定义
50.为了有利于理解本技术,在下文中定义了大量术语和短语。附加的定义在整个详细描述中阐述。
51.在整个说明书和权利要求中,除非上下文清楚地另有指明,否则以下术语采用与本文明确相关联的含义。如本文所用的短语“在一个实施方案中”不一定指相同的实施方案,尽管它可能指相同的实施方案。此外,如本文所用的短语“在另一个实施方案中”不一定指不同的实施方案,尽管它可能指不同的实施方案。因此,如下文所述,在不脱离本技术的范围或精神的情况下,本技术的各种实施方案可容易地组合。
11156;ballabio等人,(1990)human genetics 84(6)571-573;hayden等人,(2008)bmc genetics 9:80;所述文献各自以引用方式整体并入本文)、嵌套式pcr、重叠延伸pcr(参见例如higuchi等人,(1988)nucleic acids research 16(15)7351-7367;以引用方式整体并入本文)、实时pcr(参见例如higuchi等人,(1992)biotechnology 10:413-417;higuchi等人,(1993)biotechnology 11:1026-1030;所述文献各自以引用方式整体并入本文)、逆转录pcr(参见例如,bustin,s.a.(2000)j.molecular endocrinology 25:169-193;以引用方式整体并入本文)、固相pcr、热不对称交错pcr和递减pcr(参见例如don等人,nucleic acids research(1991)19(14)4008;roux,k.(1994)biotechniques 16(5)812-814;hecker等人,(1996)biotechniques 20(3)478-485;所述文献各自以引用方式整体并入本文)。多核苷酸扩增也使用数字pcr实现(参见例如kalinina等人,nucleic acids research.25;1999-2004,(1997);vogelstein和kinzler,proc natl acad sci usa.96;9236-41,(1999);国际专利公布号wo05023091a2;美国专利公布号20070202525;所述文献各自以引用方式整体并入本文)。
58.术语“聚合酶链反应”(“pcr”)是指k.b.mullis美国专利号4,683,195、4,683,202和4,965,188的方法,所述文献描述了一种用于在未克隆或纯化的情况下增加基因组或其他dna或rna的混合物中靶序列区段的浓度的方法。这种用于扩增靶序列的方法由以下各项组成:将大量的两种寡核苷酸引物引入到含有期望靶序列的dna混合物中,之后在dna聚合酶存在下引入热循环的精确序列。两种引物与双链靶序列的相应链互补。为了实现扩增,使混合物变性并且然后使引物退火到其在靶分子内的互补序列上。在退火后,使用聚合酶延伸引物以便形成一对新的互补链。变性、引物退火和聚合酶延伸的步骤可重复许多次(即,变性、退火和延伸构成一个“循环”;可存在许多个“循环”),以获得高浓度的期望靶序列的扩增区段。期望靶序列的扩增区段的长度通过引物相对于彼此的相对位置来确定,并且因此,此长度为可控制的参数。就过程的重复方面来说,所述方法称为“聚合酶链反应”(“pcr”)。因为靶序列的期望扩增区段在混合物中变成主要序列(就浓度而言),所以它们被称为“pcr扩增的”并且是“pcr产物”或“扩增子”。本领域技术人员将理解,术语“pcr”涵盖最初描述的使用例如实时pcr、嵌套式pcr、逆转录pcr(rt-pcr)、单一引物和任意引物pcr等的方法的许多变体。
59.如本文所用,术语“核酸检测测定”是指确定感兴趣的核酸的核苷酸组成的任何方法。核酸检测测定包括但不限于dna测序法、探针杂交法、结构特异性切割测定法(例如,“invader”瓣测定或侵入性切割测定,(hologic,inc.)描述于,例如,美国专利号5,846,717、5,985,557、5,994,069、6,001,567、6,090,543和6,872,816;lyamichev等人,nat.biotech.,17:292(1999),hall等人,pnas,usa,97:8272(2000)中,以及组合pcr/侵入性切割测定(hologic,inc.,例如,美国专利公布2006/0147955和2009/0253142中),出于所有目的,所述文献各自以引用方式整体并入本文);酶错配切割法(例如,variagenics,美国专利号6,110,684、5,958,692、5,851,770,以引用方式整体并入本文);聚合酶链反应(pcr),如上所述;支化杂交法(例如,chiron,美国专利号5,849,481、5,710,264、5,124,246和5,624,802,以引用方式整体并入本文);滚环式复制(例如,美国专利号6,210,884、6,183,960和6,235,502,以引用方式整体并入本文);nasba(例如,美国专利号5,409,818,以引用方式整体并入本文);分子信标技术(例如,美国专利号6,150,097,以引用方式整体并
入本文);e-传感器技术(美国专利号6,248,229、6,221,583、6,013,170和6,063,573,以引用方式整体并入本文);循环探针技术(例如,美国专利号5,403,711、5,011,769和5,660,988,以引用方式整体并入本文);dade behring信号扩增法(例如,美国专利号6,121,001、6,110,677、5,914,230、5,882,867和5,792,614,以引用方式整体并入本文);连接酶链反应(例如,barany proc.natl.acad.sci usa 88,189-93(1991));以及夹心杂交法(例如,美国专利号5,288,609,以引用方式整体并入本文)。
60.在一些实施方案中,靶核酸被扩增(例如,通过pcr)并且扩增的核酸同时使用侵入性切割测定来检测。被配置用于执行检测测定(例如侵入性切割测定)的测定与扩增测定的组合描述于美国专利号9,096,893 b2(申请序列号13/941,122)中,并如图1所示,出于所有目的,所述专利以引用方式整体并入本文。因为产生的靶扩增子的每个拷贝都切割fret盒的许多拷贝,所以称所述测定除靶扩增之外还产生“信号扩增”。还参见allawi ht等人j of clin microbio 2006;第44卷,第9期:3443-3447。另外的扩增加上侵入性切割检测配置,称为quarts法,描述于美国专利号8,361,720、8,715,937和8,916,344中,出于所有目的,所述专利以引用方式整体并入本文。
[0061]“瓣状寡核苷酸”是指可在检测测定(诸如侵入性切割测定)中被瓣状核酸内切酶切割的寡核苷酸。在优选的实施方案中,瓣状寡核苷酸与其他核酸(例如,靶核酸或模板核酸和侵入性寡核苷酸)一起形成侵入性切割结构。瓣测定试剂可任选地含有侵入性寡核苷酸和瓣状寡核苷酸结合的靶核酸或模板核酸。在特别优选的实施方案中,瓣测定试剂包含如本文所讨论的mg
++
瓣测定缓冲液。
[0062]
如本文所用,术语“瓣状核酸内切酶”是指切割核酸瓣状结构(例如,侵入性切割结构)的结构特异性溶核酶。瓣状核酸内切酶包括,例如,真细菌的dna聚合酶i蛋白的5'-核酸外切酶结构域以及真核生物和古细菌的fen-1蛋白。(kaiser等人,同上)。瓣状核酸内切酶可切割另外的结构,例如,假-y、5'悬突(overhang)和间隙结构。参见例如shen,b.,bioessays 27:717-729(2005)和finger,ld.,subcell biochem.62:301-326(2012),所述文献各自以引用方式整体并入本文。
[0063]
如本文参考酶所用,术语“fen-1”是指如由fen-1(瓣状结构特异性核酸内切酶1)基因编码的、来自真核生物或古细菌生物体的非聚合酶瓣状核酸内切酶。参见例如kaiser等人,同上,wo 02/070755和美国专利号us 7,122,364,出于所有目的,所述文献和专利以引用方式整体并入本文。术语“fen-1活性”是指fen-1酶的任何酶促活性。fen-1核酸内切酶还包含经修饰的fen-1蛋白,例如,包含来自不同生物体的fen-1酶部分的嵌合蛋白(chimerical protein)和包含一个或多个突变(例如,取代、缺失、插入等)的酶,如wo 02/070755和美国专利号us 7,122,364中所述。术语“fen1”在本文中可与“fen1”互换使用。
[0064]
如本文所用,术语“pcr-瓣测定”与术语“pcr-侵入性切割测定”可互换使用,并且是指通过以下方式来组合pcr靶扩增和扩增的dna的检测的测定配置:形成包含扩增的靶dna的第一重叠切割结构和包含来自第一重叠切割结构的切割的5'瓣的第二重叠切割结构以及标记的报告基因寡核苷酸,例如“fret盒”或5'发夹fret报告基因寡核苷酸。在如本文所用的pcr-瓣测定中,测定试剂包含:混合物,其含有dna聚合酶、fen-1核酸内切酶;初级探针,其包含与靶核酸互补的部分;以及fret盒或5'发夹fret报告基因,并且通过pcr扩增靶核酸,并且同时检测扩增的核酸(即,检测发生在靶扩增的过程期间)。pcr-瓣测定包括美国
专利号8,361,720;8,715,937;和8,916,344中描述的quarts测定和美国专利号9,096,893的扩增测定(例如,如所述专利的图1所示)。lqas测定是使用具有较长的靶特异性区域的探针寡核苷酸(长探针定量扩增信号,“lqas”)的瓣测定,并且telqas测定将lqas探针寡核苷酸与预扩增步骤组合(靶富集长探针定量扩增信号),如美国专利号10,648,025和wo 2020/112869中所述,所述专利各自以引用方式整体并入本文。
[0065]
如本文参考5'发夹形成区以及侵入性切割结构的切割减少所用,术语“阻遏”及其派生词与“抑制”及其派生词可互换使用以表示切割的减少或抑制,例如,通过瓣状核酸内切酶,例如,通过在5'发夹形成区中形成发夹。阻遏和抑制通常表示切割的可逆抑制或减少,而不限于抑制或减少侵入性切割结构的切割的任何特定机制。
[0066]
如本文所用,术语“pcr-瓣测定试剂”是指用于在pcr-瓣测定中检测靶序列的一种或多种试剂,所述试剂包含能够在含有dna聚合酶、fen-1核酸内切酶和fret盒或5'发夹fret报告基因的混合物中、在靶序列存在的情况下参与靶核酸的扩增和瓣状切割结构的形成的核酸分子。
[0067]
如本文所用,术语“侵入性切割结构”是指包含模板核酸、上游核酸(例如,侵入性寡核苷酸,或折回并杂交以形成发夹的模板链的3'部分)和iii)下游核酸(例如,探针,或折回并杂交以形成发夹的模板链的5'部分)的切割结构,其中上游核酸和下游核酸退火到模板链的相邻区域(即,在链上彼此邻近的模板链区域,不被插入核苷酸或碱基对分隔)上,并且其中在上游核酸的3'端与下游核酸与模板核酸之间形成的双链体之间形成重叠。在以下情况下发生重叠:来自上游和下游核酸的一个或多个碱基占据与模板链中的特定核苷酸相同的位置,无论上游核酸的一个或多个重叠碱基是否与模板链中的相应核苷酸互补,并且无论那些碱基是否是自然碱基或非自然碱基。在一些实施方案中,与下游双链体重叠的上游核酸的3'部分是非碱基化学部分,诸如芳族环结构,例如,如例如美国专利号6,090,543中所公开的,所述专利以引用方式整体并入本文。如本文参考侵入性切割结构所用,术语“上游双链体”是指在模板链与具有3'端的杂交上游核酸链之间形成的双链体,并且术语“下游双链体”是指在模板链与具有5'端的杂交下游核酸之间形成的双链体,使得重叠的瓣状核酸内切酶底物由上游和下游核酸链的相邻杂交区域形成。在一些实施方案中,上游核酸、下游核酸或两者是与模板链相同的核酸链的一部分。参见例如图1a、图1b和图1c,其展示了分别由3条核酸链、2条核酸链或1条核酸链形成的侵入性切割结构的上游和下游双链体区。在一些实施方案中,核酸链中的一条或多条可通过非核酸化学键联(例如,多碳链)彼此附接。参见例如美国专利号8,445,238,其以引用方式整体并入本文。
[0068]
如本文参考侵入性切割结构的切割所用,术语“靶切割位点”是指核酸结构(例如,侵入性切割结构)上通过识别结构为切割底物的结构特异性核酸酶(例如,fen-1核酸内切酶)切割的一个或多个优选位点。例如,如kaiser等人所讨论的,5'瓣状核酸内切酶(包括fen-1核酸内切酶)通常在下游核酸中切割侵入性切割结构,通常在第一个碱基配对核苷酸之后,即,进入下游双链体中的一个核苷酸。在本文所述的优选实施方案中,靶切割位点可用作瓣测定中的报告切割位点。例如,在某些优选的实施方案中,fret标记系统的供体和受体部分(例如,荧光团和猝灭剂部分)被定位,使得它们在靶切割位点处的侵入性切割结构被切割时分离,使得反应混合物中荧光的增加报告靶切割位点处的切割。本技术不受fret系统的部分在切割结构上的任何特定放置的限制。例如,在一些实施方案中,fret系统的部
分在靠近报告切割位点侧翼的位置处(例如在报告切割位点任一侧的1个、2个或几个核苷酸内)附接至探针或报告基因,而在其他实施方案中,fret系统的部分间隔更宽,例如在核酸链上间隔5个、6个、7个、8个、9个、10个核苷酸等。在一些实施方案中,fret系统的一个或多个部分位于或接近在侵入性切割结构中切割的核酸链的末端。在优选的实施方案中,侵入性切割结构可在靶切割位点被mg
++
瓣测定缓冲液中的来自闪烁古生球菌(archaeoglobus fulgidus)的fen-1核酸内切酶(“afu fen-1”)切割,如下所讨论。还参见例如kaiser等人的美国专利号6,562,611和kaiser m.w.等人(1999)j.biol.chem.,274:21387,出于所有目的,所述专利和文献以引用方式整体并入本文。
[0069]
如本文参考瓣状核酸内切酶的核酸底物结构所用,“5'发夹”是指发夹或发夹形成序列,所述发夹或发夹形成序列与靶切割位点在同一条链上,并且沿着同一条核酸链在靶切割位点的5'方向上。5'发夹不限于靶切割位点的5'链上的任何特定位置。在一些实施方案中,5'发夹形成区可包含5'瓣的5'末端核苷酸,而在其他实施方案中,5'发夹形成区可位于5'发夹形成序列的一侧或两侧(即,在5'和/或3'方向)上的非自互补区域的侧翼。在一些实施方案中,整个5'瓣由发夹形成序列构成。
[0070]
如参考瓣结构(例如,侵入性切割结构)的核酸链所用,术语“模板”是指这样的链,上游和下游核酸或核酸区域与所述链杂交以形成侵入性切割结构。虽然模板链可用作通过聚合酶延伸引物模板(例如,在pcr瓣状核酸内切酶测定中),但所述术语的使用不限于聚合测定或反应。
[0071]
如本文所用,术语“3'端阻断剂”是指3'端修饰(例如,寡核苷酸上的3'端修饰),在3'端阻断剂存在于切割结构中的上游核酸的3'端上时,所述3'端修饰抑制瓣状核酸内切酶切割侵入性切割结构。例如,如果3'胺、3'磷酸酯(3'-po4)、3'生物素、3'c6(6-碳乙二醇间隔物,也称为“3'己二醇”)和3'双脱氧核苷酸存在于上游核酸上,则它们抑制瓣切割。参见例如kaiser等人,同上。
[0072]
如本文所用,术语“mg
++
瓣测定缓冲液”是指用于瓣状核酸内切酶的缓冲溶液,其包括mg
++
作为缓冲液中主要或基本上唯一的二价阳离子,使得在缓冲液中执行的测定反应(例如,瓣测定)表现出mg
++
的存在的特征(例如,与例如y结构、假y结构相比,一些瓣状核酸内切酶对侵入性切割结构的高特异性),并且不表现出与其他二价阳离子的存在相关的特征(例如,与使用mn
++
和mg
++
或使用mn
++
取代mg
++
相关的瓣状核酸内切酶的替代切割活性),例如,如kaiser等人所述,同上。在一些实施方案中,与标准pcr缓冲液相比,瓣测定缓冲液具有非常低的kcl或没有kcl,并且包含升高的mg
++
(例如,本技术的瓣测定缓冲液包含》6mm,优选》7mm,更优选7.5mm mg
++
,而pcr缓冲液通常包含约1.5mm至2.5mm mg
++
)。
[0073]
如本文所用,术语“瓣测定试剂”或“侵入性切割测定试剂”是指执行对底物的瓣测定或侵入性切割测定所需的所有试剂的集合。如本领域已知的,瓣测定通常包括用于形成侵入性切割结构的寡核苷酸、瓣状核酸内切酶和任选的fret盒或5'发夹fret报告基因。
[0074]
如本文所用,术语“fret”是指荧光共振能量转移,这是其中部分(例如,荧光团)例如在其本身中或从荧光团到非荧光团(例如,猝灭剂分子)转移能量的过程。在一些情况下,fret涉及通过短范围(例如,约10nm或更小)偶极-偶极相互作用将能量转移到低能量受体荧光团的激发的供体荧光团。在其他情况下,fret涉及来自供体的荧光能量的损失和受体荧光团中的荧光增加。在仍其他形式的fret中,能量可以从激发的供体荧光团交换至非荧
光分子(例如,猝灭分子)。fret是本领域的技术人员已知的并且已得到描述(参见例如stryer等人,1978,ann.rev.biochem.,47:819;selvin,1995,methods enzymol.,246:300;orpana,2004 biomol eng 21,45-50;olivier,2005 mutant res 573,103-110,所述文献各自以引用方式整体并入本文)。
[0075]
如本文所用,术语“fret系统”是指一起充当用于基于fret的分子(例如,瓣状寡核苷酸或测定报告分子)分析的供体-受体或供体-猝灭剂配偶体的一对或一组部分。虽然在一个特定位置用荧光团展示并且在特定的第二位置用猝灭剂或其他fret受体部分展示本技术的实施方案,例如,在如图1至图5所展示的fret测定报告基因中,但所展示的实施方案作为本技术的非限制性实例提供。可应用于本技术中的fret系统的部分不限于这些放置,并且可例如在位置中转换,可定位在所展示的分子的不同部分上,或者可包含相同或不同的另外的供体或受体部分。
[0076]
如本文所用,术语“报告切割位点”是指在瓣状核酸内切酶测定中生成信号的切割位点。例如,被配置成使用fret效应来指示5'瓣被瓣状核酸内切酶释放的瓣状寡核苷酸可包含荧光团部分和猝灭剂部分,当瓣状寡核苷酸与靶分子杂交时,所述部分被定位成通过瓣状核酸内切酶切割分离。荧光团和猝灭剂部分之间的切割将fret系统部分分离并且去除荧光团的猝灭效应,使得通过来自荧光团的荧光的增加来报告(即,使可检测到)成功的切割。因此,fret系统的荧光团和猝灭剂部分之间的位点是报告切割位点,而所述寡核苷酸上的可被瓣状核酸内切酶活性切割但不在fret部分之间的任何位点都不会是报告切割位点。在优选的实施方案中,测定中使用的底物结构中的“报告切割位点”是测定中使用的瓣状核酸内切酶的靶切割位点。
[0077]
如本文所用,术语“fret盒”是指含有荧光团部分和猝灭荧光团的附近猝灭剂部分的发夹寡核苷酸。切割的瓣(例如,来自pcr-瓣测定中的靶特异性探针的切割)与fret盒的杂交产生了瓣状核酸内切酶的次级底物,例如fen-1酶。一旦形成这种底物,含有5'荧光团的碱基可以被瓣状核酸内切酶从盒中切割,从而生成荧光信号。在优选的实施方案中,fret盒包含未配对的3'部分,切割产物(例如,切割的瓣状寡核苷酸的一部分)可以与未配对的3'部分杂交以形成可被fen-1核酸内切酶切割的侵入性切割结构。
[0078]
如本文所用,核酸“发夹”是指含有在一端由环闭合的链内碱基配对茎的核酸区域。在优选的实施方案中,环包含多个未配对的核苷酸。发夹可例如在核酸链包含两个彼此充分互补以形成多个碱基对,优选连续碱基对(例如,2、3、4、5、6、7、8、9、10或更多个连续碱基对)的部分时形成。5'发夹fret报告基因、5'发夹瓣状寡核苷酸或3-发夹瓣状核酸内切酶底物的5'发夹在5'发夹的茎中包含至少两个、优选至少3个连续碱基对。
[0079]
术语“发夹形成区”和“发夹形成序列”在本文中可互换使用,并且是指包含可碱基配对形成双链“茎”区域的自互补序列的核酸链区域,茎的链任选地在一端通过环序列连接。发夹区的茎通常包含至少两个连续碱基对,优选标准的沃森-克里克(watson-crick)碱基对。由发夹形成区的自互补序列形成的发夹的茎不限于任何特定数量的连续或非连续碱基对。在一些实施方案中,茎可包含3个、4个、5个、6个、7个...10个、20个、30个...50个、100个、150个或它们之间的任何整数,或更多个碱基对。在一些实施方案中,茎可包含一种或多种碱基类似物并且发夹可以包含一个或多个非标准碱基对。在发夹报告分子(例如,fret盒、5'发夹fret报告分子和单分子底物)中,不同的发夹可具有不同的优选茎长度。例如,在
瓣状切割底物中形成下游双链体的发夹形成区优选包含互补序列,其可形成10个或更多个碱基对,优选10个或更多个连续碱基对,优选沃森-克里克碱基对,以用于通过瓣状核酸内切酶进行有效切割,而为瓣状核酸内切酶提供上游双链体的发夹的茎区可以显著更短,例如,少至2或3个碱基对。(参见例如kaiser m.w.等人,同上)。在优选的实施方案中,形成5'发夹的发夹形成区被选择为在茎中形成多个碱基对,茎在一些条件(例如,低于测定反应温度)下阻遏靶切割位点处的切割并且在其他条件下(例如,在测定反应温度下)不阻遏靶切割位点处的切割。在一些实施方案中,发夹茎可以包含错配、缺失、插入、凸出的核苷酸、侧茎(例如,形成3向和4向连接)等。发夹茎环的环端可包含核苷酸序列,或者可包含非核苷酸连接物,例如,一个或多个无碱基间隔物或接头、碳链等。
[0080]
在一些实施方案中,可使用茎的环端的稳定环,例如,dna四环(antao等人,nucl.acids res.,19:5901[1991])或三环(hiraro等人,nuc.acids res.,22:576[1994])。对于合成的发夹探针(诸如fret盒、5'发夹fret报告基因和5'发夹测试底物),在发夹形成区中考虑的设计元素包括自互补区的长度、如由沃森-克里克碱基配对预测的发夹或茎/环结构的稳定性、非标准碱基和碱基对的存在以及任何特定稳定环序列(例如,四环[tinoco等人,同上]或三环[hirao等人,同上])的存在或不存在。
[0081]
如本文所用,术语“5'发夹fret报告基因”是指一类fret盒,其包含在靶切割位点上游的5'发夹形成区,并且包含在报告基因在靶切割位点被切割时分离的fret标记部分。在某些实施方案中,5'发夹fret报告基因包含可以在侵入性切割结构中形成下游双链体的区域。在优选的实施方案中,5'发夹fret报告基因还包含可以与核酸链的3'末端部分杂交以形成侵入性切割结构的上游双链体的区域,使得5'发夹fret报告基因在切割不被5'发夹阻遏的条件下(例如,在5'发夹形成分区不是发夹形式的条件下)可在靶切割位点被切割。在特别优选的实施方案中,与一种或多种另外的核酸复合以形成侵入性切割结构的5'发夹fret报告基因在切割不被5'发夹阻遏的条件下可被mg
++
瓣测定缓冲液中的afu fen-1切割。如本文所用,术语“5'发夹测试底物”(例如,瓣状核酸内切酶的测试底物)是指单链核酸,优选合成的核酸,其形成在某些条件下可被瓣状核酸内切酶,优选fen-1瓣状核酸内切酶切割的结构,并且含有5'发夹形成区。在优选的实施方案中,5'发夹测试底物形成分子内结构,其在5'发夹可能存在的条件下(例如,在低温下)不可被fen-1核酸内切酶切割或切割效果很差,并且在5'发夹不太可能存在的条件下(例如,在较高温度下)可被相同的核酸内切酶切割。在优选的实施方案中,由5'发夹测试底物形成的结构在对侵入性切割结构具有最大特异性的条件下(例如,在包含mg
++
作为反应中基本上唯一的二价阳离子和/或基本上不含mn
++
的缓冲液中)可使用afu fen-1核酸内切酶进行切割。优选地,5'发夹测试底物包含形成侵入性切割结构的上游和下游双链体以及在靶切割位点上游的5'发夹形成区的序列,即,本技术的测试底物可以形成3个发夹:上游双链发夹、下游双链发夹以及5'发夹,例如,如图8a所示。在一些实施方案中,5'发夹测试底物包含在测试底物在靶切割位点被切割时分离的fret标记部分。在优选的实施方案中,5'发夹测试底物在切割不被5'发夹阻遏的条件下(例如,在5’发夹形成区不是发夹形式的条件下)可在靶切割位点被切割。在特别优选的实施方案中,5'发夹测试底物在切割不被5'发夹阻遏的条件下可被mg
++
瓣测定缓冲液中的afu fen-1切割。
[0082]
如本文所用,术语“引物退火”是指允许寡核苷酸引物与模板核酸链杂交的条件。
引物退火的条件随引物的长度和序列而变化,并且通常基于针对引物确定或计算的tm。例如,涉及热循环的扩增方法中的退火步骤涉及将热变性步骤之后的温度降低到基于引物序列的tm的温度,降低温度的时间足以允许这种退火。
[0083]
如本文所用,术语“可扩增核酸”用于指代可通过任何扩增方法扩增的核酸。预期“可扩增核酸”通常将包含“样品模板”。
[0084]
如本文参考核酸扩增或信号扩增的检测所用,术语“实时”是指检测或测量反应进行中时(例如,孵育或热循环期间)的反应中的产物或信号的积累。这种检测或测量可连续发生,或者它可在扩增反应过程期间的多个离散点时发生,或者它可为组合。例如,在聚合酶链反应中,可在全部或部分热循环期间连续发生检测(例如,荧光检测),或者可在一个或多个循环期间的一个或多个点时瞬时发生检测。在一些实施方案中,pcr的实时检测通过确定多个循环中的每个循环中的或每个循环中的同一点(例如,循环中的时间点或循环中的温度步骤)时的荧光水平来实现。扩增的实时检测也可称为扩增反应“期间”的检测。
[0085]
如本文所用,术语“核酸丰度”是指存在于样品或等分试样中的特定靶核酸序列的量。所述量通常是指质量(例如,μg)、每单位体积的质量(例如,μg/μl);拷贝数(例如,1000个拷贝、1阿托摩尔)或每单位体积的拷贝数(例如,1000个拷贝/ml、1阿托摩尔/μl)。核酸丰度也可以表示为相对于已知浓度或拷贝数的标准量的量。核酸丰度的测量可以基于本领域技术人员理解为核酸丰度的合适定量表示的任何基础,所述定量表示包括物理密度或样品、光密度、折射性质、染色性质,或基于可检测标记(例如,荧光标记)的强度。
[0086]
术语“扩增子”或“扩增产物”是指通过扩增过程诸如pcr过程生成的核酸(通常是dna)区段。所述术语也用于指代通过采用rna聚合酶(诸如nasba、tma等)的扩增方法产生的rna区段。
[0087]
如参考热循环扩增反应所用,术语“扩增图”是指指示扩增的信号(例如荧光信号)与循环数的图。当用于指代非热循环扩增方法时,扩增图通常是指信号积累随时间变化的图。
[0088]
如参考扩增图所用,术语“基线”是指在孵育之前来自组装扩增反应的检测信号,或者在pcr的情况下,在初始循环中来自组装扩增反应的检测信号,其中信号几乎没有变化。
[0089]
如本文参考在热循环的扩增反应期间的实时检测所用,术语“c
t”或“阈值循环”是指检测信号(例如,荧光)通过固定阈值时的分数循环数。
[0090]
如本文参考对照反应所用,术语“无模板对照”和“无靶对照”(或“ntc”)是指不含模板或靶核酸的反应或样品。它用于验证扩增质量。
[0091]
如本文所用,术语“样品模板”是指来源于对靶标的存在进行分析的样品的核酸。相比之下,“背景模板”用于指代可能存在于或可能不存在于样品中的样品模板以外的核酸。背景模板的存在通常是无意的。这可能是残留污染(carryover)的结果,或者可能是由于存在试图从样品中纯化去除的核酸污染物。例如,来自待检测生物体之外的生物体的核酸可作为背景存在于测试样品中。
[0092]“怀疑含有”核酸的样品可能含有或不含有靶核酸分子。
[0093]
如本文所用,术语“样品”以其最广泛的意义使用。例如,在一些实施方案中,样品意图包括样本或培养物(例如,微生物培养物),而在其他实施方案中,样品意图包括生物样
品和环境样品(例如,怀疑包含靶序列、基因或模板)。在一些实施方案中,样品可包括合成来源的样本。样品可以是未纯化的,或可以是部分或完全纯化的或以其他方式处理的。
[0094]
本技术不受所使用或所分析的生物样品的类型限制。本技术对于多种生物样品有用,包括但不限于从人(例如,成人、婴儿或胚胎)或动物(例如,牛、家禽、小鼠、大鼠、狗、猪、猫、马等)获得的组织(例如,器官(例如,心脏、肝脏、脑、肺、胃、肠、脾、肾、胰和生殖器官)、腺体、皮肤和肌肉)样品、细胞(例如,血细胞(例如,淋巴细胞或红细胞)、肌肉细胞、肿瘤细胞和皮肤细胞)样品、气体样品、体液(例如,血液或其部分、血清、血浆、尿液、精液、唾液等)样品或固体(例如,粪便)样品。在一些实施方案中,生物样品可以是固体食物和/或饲料产品和/或诸如乳制品、蔬菜、肉类和肉类副产品以及废物的成分。生物样品可从以下的全部中获取:家畜的各种家系,以及野性或野生动物,包括但不限于诸如有蹄动物、熊、鱼、兔类、啮齿类、鳍脚类动物等的动物。
[0095]
生物样品还包括活组织检查和组织切片(例如,肿瘤、生长物、皮疹、感染的活组织检查或切片或石蜡包埋切片)、医学或医院样品(例如,包括但不限于血液样品、唾液、口腔拭子、脑脊液、胸膜液、乳汁、初乳、淋巴液、痰液、呕吐物、胆汁、精液、卵母细胞、宫颈细胞、羊水、尿液、粪便、毛发和汗液)、实验室样品(例如,亚细胞部分)和法医样品(例如,血液或组织(例如,飞溅物或残留物)、含有核酸的毛发和皮肤细胞)以及考古样品(例如,化石生物体、组织或细胞)。
[0096]
环境样品包括但不限于环境材料,诸如地表物质、土壤、水(例如,淡水或海水)、藻类、地衣、地质样品、含有核酸的含空气材料、晶体和工业样品,以及从食品和乳制品加工器械、装置、设备、器具、一次性和非一次性物品中获得的样品。
[0097]
样品可通过任何期望或合适的方法制备。在一些实施方案中,使用美国专利号9,000,146中所述的方法直接从体液、粪便或其他样品中分析核酸,出于所有目的,所述专利以引用方式整体并入本文。
[0098]
然而,不将上述实例理解为限制适用于本技术的样品(例如,怀疑包含靶序列、基因或模板(例如,其存在或不存在可以使用本技术的组合物和方法来确定))类型。
[0099]
如本文所用,术语“核酸序列”和“核酸分子”是指寡核苷酸、核苷酸或多核苷酸及其片段或部分。所述术语涵盖包括dna和rna核苷酸类似物的序列,包括上文列出的那些,并且还包括但不限于:4-乙酰胞嘧啶、8-羟基-n6-甲基腺苷、氮丙啶胞嘧啶(aziridinylcytosine)、假异胞嘧啶、5-(羧羟基-甲基)尿嘧啶、5-氟尿嘧啶、5-溴尿嘧啶、5-羧甲基胺甲基-2-硫尿嘧啶、5-羧甲基-胺甲基尿嘧啶、二氢尿嘧啶、肌苷、n6-异戊烯基腺嘌呤、1-甲基腺嘌呤、1-甲基假尿嘧啶、1-甲基鸟嘌呤、1-甲基肌苷、2,2-二甲基-鸟嘌呤、2-甲基腺嘌呤、2-甲基鸟嘌呤、3-甲基胞嘧啶、5-甲基胞嘧啶、n6-甲基腺嘌呤、7-甲基鸟嘌呤、5-甲氨基甲基尿嘧啶、5-甲氧基-氨基-甲基-2-硫尿嘧啶、β-d-甘露糖基q核苷(mannosylqueosine)、5'-甲氧基羰基甲基尿嘧啶、5-甲氧基尿嘧啶、2-甲硫基-n6-异戊烯基腺嘌呤、尿嘧啶-5-氧基乙酸甲酯、尿嘧啶-5-氧基乙酸、氧基丁氧核苷(oxybutoxosine)、假尿嘧啶、q核苷、2-硫胞嘧啶、5-甲基-2-硫尿嘧啶、2-硫尿嘧啶、4-硫尿嘧啶、5-甲基尿嘧啶、n-尿嘧啶-5-氧基乙酸甲酯、尿嘧啶-5-氧基乙酸、假尿嘧啶、q核苷、2-硫胞嘧啶、2,6-二氨基嘌呤和吡唑并[3,4-d]嘧啶,诸如鸟嘌呤类似物6氨基1h-吡唑并[3,4d]嘧啶4(5h)酮(ppg或ppg,也称为super g)和腺嘌呤类似物4氨基1h-吡唑并[3,4d]嘧啶(ppa或ppa)。也可
以使用黄嘌呤类似物1h-吡唑并[5,4d]嘧啶4(5h)-6(7h)-二酮(ppx)。这些碱基类似物,当存在于寡核苷酸中时,加强杂交并改善错配判别。所有互变异构形式的自然存在的碱基、经修饰的碱基和碱基类似物都可包括在本技术的寡核苷酸缀合物中。可用于本技术中的其他经修饰的碱基包括6-氨基-3-丙-1-炔基-5-氢吡唑并[3,4-d]嘧啶-4-酮,pppg;6-氨基-3-(3-羟基丙-1-炔基)-5-氢吡唑并[3,4-d]嘧啶-4-酮,hopppg;6-氨基-3-(3-氨基丙-1-炔基)-5-氢吡唑并[3,4-d]嘧啶-4-酮,nh2pppg;4-氨基-3-(丙-1-炔基)吡唑并[3,4-d]嘧啶,pppa;4-氨基-3-(3-羟基丙-1-炔基)吡唑并[3,4-d]嘧啶,hopppa;4-氨基-3-(3-氨基丙-1-炔基)吡唑并[3,4-d]嘧啶,nh
2 pppa;3-丙-1-炔基吡唑并[3,4-d]嘧啶-4,6-二氨基,(nh2)2pppa;2-(4,6-二氨基吡唑并[3,4-d]嘧啶-3-基)乙炔-1-醇,(nh2)2pppaoh;3-(2-氨基乙炔基)吡唑并[3,4-d]嘧啶-4,6-二胺,(nh2)2pppanh2;5-丙-1-炔基-1,3-二氢嘧啶-2,4-二酮,pu;5-(3-羟基丙-1-炔基)-1,3-二氢嘧啶-2,4-二酮,hopu;6-氨基-5-丙-1-炔基-3-二氢嘧啶-2-酮,pc;6-氨基-5-(3-羟基丙-1-炔基)-1,3-二氢嘧啶-2-酮,hopc;和6-氨基-5-(3-氨基丙-1-炔基)-1,3-二氢嘧啶-2-酮,nh2pc;5-[4-氨基-3-(3-甲氧基丙-1-炔基)吡唑[3,4-d]嘧啶基]-2-(羟甲基)氧戊环(oxolan)-3-醇,ch
3 opppa;6-氨基-1-[4-羟基-5-(羟甲基)氧戊环-2-基]-3-(3-甲氧基丙-1-炔基)-5-氢吡唑并[3,4-d]嘧啶-4-酮,ch3opppg;4,(4,6-二氨基-1h-吡唑并[3,4-d]嘧啶-3-基)-丁-3-炔基-1-醇,super a;6-氨基-3-(4-羟基-丁-1-炔基)-1,5-二氢-吡唑并[3,4-d]嘧啶-4-酮;5-(4-羟基-丁-1-炔基)-1h-嘧啶-2,4-二酮,super t;3-碘-1h-吡唑并[3,4-d]嘧啶-4,6-二胺((nh2)2ppai);3-溴-1h-吡唑并[3,4-d]嘧啶-4,6-二胺((nh2)2ppabr);3-氯-1h-吡唑并[3,4-d]嘧啶-4,6-二胺((nh2)2ppacl);3-碘-1h-吡唑并[3,4-d]嘧啶-4-基胺(ppai);3-溴-1h-吡唑并[3,4-d]嘧啶-4-基胺(ppabr);以及3-氯-1h-吡唑并[3,4-d]嘧啶-4-基胺(ppacl)。所述术语涵盖:提供替代氢键构型的碱基类似物(例如,s.benner的美国专利号6,001,983中所述的异-c和异-g以及其他非标准碱基对);非氢键类似物(例如,非极性芳族核苷类似物,诸如b.a.schweitzer和e.t.kool,j.org.chem.,1994,59,7238-7242,b.a.schweitzer和e.t.kool,j.am.chem.soc.,1995,117,1863-1872所述的2,4-二氟甲苯);“万能”碱基,诸如5-硝基吲哚和3-硝基吡咯;和万能嘌呤和万能嘧啶(诸如分别为“k”和“p”核苷酸;p.kong等人,nucleic acids res.,1989,17,10373-10383,p.kong等人,nucleic acids res.,1992,20,5149-5152)。核苷酸类似物包括修饰形式的脱氧核糖核苷酸以及核糖核苷酸。
[0100]
核酸序列或分子可以是基因组来源或合成来源的dna或rna,其可以是单链或双链并且代表有义链或反义链。因此,核酸序列可以是dsdna、ssdna、混合ssdna、混合dsdna、制成ssdna的dsdna(例如,通过解链、变性、解旋酶等)、a-、b-或z-dna、三链dna、rna、ssrna、dsrna、混合ssrna和混合dsrna、制成ssrna的dsrna(例如,通过解链、变性、解旋酶等)、信使rna(mrna)、核糖体rna(rrna)、转运rna(trna)、催化rna、snrna、微rna或蛋白核酸(pna)。
[0101]
本技术不受所利用的核酸(例如,序列或分子(例如,靶序列和/或寡核苷酸))的类型或来源的限制。例如,核酸序列可以是扩增或产生的序列(例如,通过合成(例如,聚合(例如,引物延伸(例如,rna-dna杂交引物技术))和逆转录(例如,将rna逆转录成dna))和/或扩增(例如,聚合酶链反应(pcr)、滚环扩增(rca)、基于核酸序列的扩增(nasba)、转录介导扩增(tma)、连接酶链反应(lcr)、循环探针技术、q-β复制酶、链置换扩增(sda)、分支dna信号扩增(bdna)、杂交捕获和解旋酶依赖性扩增)来扩增或产生核酸序列)。
[0102]
除非本文另有说明,否则术语“核苷酸”和“碱基”在用于指代核酸序列时可互换使用。“核碱基”是杂环碱基,诸如腺嘌呤、鸟嘌呤、胞嘧啶、胸腺嘧啶、尿嘧啶、肌苷、黄嘌呤、次黄嘌呤或其杂环衍生物、类似物或互变异构体。核碱基可以是自然存在的或合成的。核碱基的非限制性实例是腺嘌呤、鸟嘌呤、胸腺嘧啶、胞嘧啶、尿嘧啶、黄嘌呤、次黄嘌呤、8-氮杂嘌呤、在位置8被甲基或溴取代的嘌呤、9-氧代-n6-甲基腺嘌呤、2-氨基腺嘌呤、7-脱氮黄嘌呤、7-脱氮鸟嘌呤、7-脱氮腺嘌呤、n4-桥亚乙基胞嘧啶(ethanocytosine)、2,6-二氨基嘌呤、n6-桥亚乙基-2,6-二氨基嘌呤、5-甲基胞嘧啶、5-(c3-c6)-炔基胞嘧啶、5-氟尿嘧啶、5-溴尿嘧啶、硫尿嘧啶、假异胞嘧啶、2-羟基-5-甲基-4-三唑并吡啶、异胞嘧啶、异鸟嘌呤、肌苷、7,8-二甲基咯嗪、6-二氢胸腺嘧啶、5,6-二氢尿嘧啶、4-甲基吲哚、桥亚乙基腺嘌呤(ethenoadenine)以及描述于美国专利号5,432,272和6,150,510以及pct申请wo 92/002258、wo 93/10820、wo 94/22892和wo 94/24144以及fasman(“practical handbook of biochemistry and molecular biology”,第385-394页,1989,crc press,boca raton,lo)中的非自然存在的核碱基,所述文献全部以引用方式整体并入本文。
[0103]
如本文所用,术语“寡核苷酸”定义为包含两个或更多个核苷酸(例如,脱氧核糖核苷酸或核糖核苷酸),优选至少5个核苷酸,更优选至少约10个至15个核苷酸,并且更优选至少约15个至30个核苷酸的分子或更长的分子(例如,寡核苷酸长度通常小于200个残基(例如,15个至100个核苷酸),然而,如本文所用,所述术语也旨在涵盖更长的多核苷酸链)。确切尺寸将取决于许多因素,继而取决于寡核苷酸的最终功能或用途。寡核苷酸通常由其长度指示。例如,24个残基的寡核苷酸被称为“24聚体”。寡核苷酸可以通过自杂交或通过与其他多核苷酸杂交来形成二级和三级结构。此类结构可以包括但不限于双链体、发夹、十字形、弯曲和三链体。寡核苷酸可以任何方式生成,所述方式包括化学合成、dna复制、逆转录、pcr或其组合。在一些实施方案中,形成侵入性切割结构的寡核苷酸在反应中生成(例如,通过在酶促延伸反应中延伸引物)。
[0104]
因为单核苷酸以使得一个单核苷酸戊糖环的5'磷酸酯通过磷酸二酯键联在一个方向上附接至其相邻的3'氧的方式反应制成寡核苷酸,所以如果寡核苷酸的5'磷酸酯不与单核苷酸戊糖环的3'氧连接,则寡核苷酸的一端被称为“5'末端”或“5'端”,并且如果寡核苷酸的3'氧不与随后的单核苷酸戊糖环的5'磷酸酯连接,则寡核苷酸的一端被称为“3'末端”或“3'端”。如本文所用,即使在更大的寡核苷酸内部,核酸序列也可以称为具有5'端和3'端。不同于核酸分子的3'和5'端,核酸序列的3'和5'端不必位于分子链的3'和5'末端。如果当以5'至3'的方向沿核酸链移动时,第一区域的3'端在第二区域的5’端之前,则称沿核酸链的第一区域在另一个区域的上游。
[0105]
当两个不同的、不重叠的寡核苷酸退火到同一线性互补核酸序列的不同区域上,并且一个寡核苷酸的3'端指向另一个寡核苷酸的5'端时,前者可被称为“上游”寡核苷酸并且后者可被称为“下游”寡核苷酸。
[0106]
如本文所用,“碱基配对规则”是指由沃森和克里克建立的核苷酸碱基配对规则。在标准沃森-克里克几何结构中,大嘌呤(a和g碱基)与小嘧啶碱基(t和c)碱基配对,其中a与t(或u)配对,并且g与c配对,使得a-t碱基对与g-c碱基对的尺寸基本上相同。这意味着由a-t(或a-u)或g-c碱基对形成的dna梯的横档(rungs)在螺旋上都具有相同的长度。根据碱基配对的标准沃森-克里克规则,a-t和a-u碱基对在碱基部分之间形成两个氢键,而g-c碱
基对形成三个氢键。
[0107]
核苷酸可以非标准方式,诸如以“摇摆”碱基配对的方式配对,其中形成一个或多个氢键,但碱基对的几何结构不符合标准沃森-克里克几何结构。最常见的摇摆碱基对是g-t(或u)碱基配对,其中在g和t(或g和u)之间形成单个氢键。非沃森-克里克碱基配对还包括由肌苷(i)与c、t或a形成的碱基对、嘌呤碱基对a-g(或i)、a-a和g-c以及反向沃森-克里克碱基对a-t,其中t环从正常的沃森-克里克对旋转180
°
。参见例如hyone-myong eun,enzymology primer for recombinant dna technology,academic press,(1996)。
[0108]
如本文所用,“标准碱基对/碱基配对”是指具有标准沃森-克里克几何结构并涵盖a-t、a-u和g-c碱基对的碱基对。所述术语涵盖这些核苷酸的经修饰类似物的碱基配对,其中修饰(例如,附接的染料或其他部分)基本上不改变碱基之间的氢键(例如,氢键的数量、位置或受体/供体对)。如本文所用,“非标准碱基对/碱基配对”是指不属于具有标准沃森-克里克几何结构的标准碱基配对的核苷酸(例如,自然核苷酸、核苷酸类似物)之间的配对。
[0109]
如本文所用,术语“互补”或“互补性”用于指代通过碱基配对规则相关的多核苷酸(例如,两个或更多个核苷酸(例如,寡核苷酸或靶核酸)的序列)。例如,序列“5'-a-g-t-3'”与序列“3'-t-c-a-5'”互补。互补性可为“部分的”,其中仅一些核酸碱基根据碱基配对规则匹配。或者,在核酸碱基之间可存在“完全”或“总体”互补性。核酸链之间的互补程度对核酸链之间的杂交的效率和强度具有显著影响。这在扩增反应以及取决于两个或更多个核酸链的缔合的检测方法中特别重要。任一术语也可用于指代单个核苷酸,尤其是在多核苷酸的上下文中。例如,寡核苷酸中的特定核苷酸可能因其与另一核酸序列(例如,靶序列)中的核苷酸的互补性或缺乏互补性而被注意到,这与其余的寡核苷酸和核酸序列之间的互补性形成对比或比较。
[0110]
如本文所用的核酸序列的互补序列是指寡核苷酸,当与核酸序列比对使得一个序列的5'端与另一个序列的3'端配对时,所述寡核苷酸处于“反平行缔合”。如上文所讨论的,核苷酸类似物可包括在本技术的核酸中并且包括例如肌苷、7-脱氮鸟嘌呤、异-c和异-g。互补性不必是完美的;稳定的双链体可含有错配的碱基对或不匹配的碱基。核酸技术领域的技术人员可考虑多个变量来凭经验确定双链体稳定性,所述变量包括例如寡核苷酸的长度、寡核苷酸序列的碱基组成和序列、离子强度以及错配碱基对的发生率。如本文所用,术语“标记”是指可以被检测到或可以导致可检测响应的任何部分(例如,化学物种)。在一些优选的实施方案中,标记的检测提供可量化的信息。标记可以是任何已知的可检测部分,例如像放射性标记(例如,放射性核素)、配体(例如,生物素或抗生物素蛋白)、发色团(例如,赋予可检测颜色的染料或颗粒)、半抗原(例如,洋地黄毒苷)、质量标记、乳胶珠、金属颗粒、顺磁标记、发光化合物(例如,生物发光、磷光或化学发光标记)或荧光化合物。
[0111]
标记还可包含用于检测的磷光体颗粒。在特别优选的实施方案中,磷光体颗粒是上转换磷光体颗粒(参见例如ostermayer,f.w.preparation and properties of infrared-to-visible conversion phosphors.metall.trans.752,747-755[1971])。在一些实施方案中,掺杂稀土的陶瓷颗粒用作磷光体颗粒。磷光体颗粒可通过任何合适的方法来检测,所述方法包括但不限于上转换磷光技术(up-converting phosphor technology,upt),其中上转换磷光体将低能红外(ir)辐射转移到高能可见光。虽然本发明不限于任何特定机制,但在一些实施方案中,upt通过多光子吸收和随后的掺杂剂依赖性磷光发射将红
外光上转换为可见光。参见例如2002年6月4日授权于zarling等人的美国专利号6,399,397;van de rijke等人,nature biotechnol.19(3):273-6[2001];corstjens等人,iee proc.nanobiotechnol.152(2):64[2005],各自以引用方式整体并入本文。
[0112][0113]
如本文所用,参考信号(例如,来自不同标记的信号)的术语“不同”是指可以例如通过光谱性质(诸如荧光发射波长、颜色、吸光度、质量、尺寸、荧光偏振性质、电荷等)或通过与另一部分(诸如化学试剂、酶、抗体等)相互作用的能力彼此区分的信号。
[0114]
标记可以直接或间接连接至寡核苷酸或其他生物分子。直接标记可以通过将标记与寡核苷酸连接的键或相互作用(包括共价键或非共价相互作用,诸如氢键、疏水和离子相互作用)或通过形成螯合物或配位复合物来发生。间接标记可以通过使用桥联部分或“接头”(诸如抗体或另外的寡核苷酸,它们是直接或间接标记的)来发生。
[0115]
标记可以单独使用或与可以抑制(例如,猝灭)、激发或转移(例如,移动)标记(例如,发光标记)的发射光谱(例如,荧光共振能量转移(fret))的部分组合使用。
[0116]“聚合酶”是通常用于连接3'-oh 5'-三磷酸核苷酸、低聚物和它们的类似物的酶。聚合酶包括但不限于模板依赖性dna依赖性dna聚合酶、dna依赖性rna聚合酶、rna依赖性dna聚合酶和rna依赖性rna聚合酶。聚合酶包括但不限于t7 dna聚合酶、t3 dna聚合酶、t4 dna聚合酶、t7 rna聚合酶、t3 rna聚合酶、sp6 rna聚合酶、dna聚合酶1、klenow片段、thermophilus aquaticus dna聚合酶、tth dna聚合酶、vent dna聚合酶(new england biolabs)、deep vent dna聚合酶(new england biolabs)、bst dna聚合酶大片段、stoeffel片段、9
°
n dna聚合酶、pfu dna聚合酶、tfl dna聚合酶、repliphi phi29聚合酶、tli dna聚合酶、真核生物dna聚合酶β、端粒酶、therminator聚合酶(new england biolabs)、kod hifi dna聚合酶(novagen)、kod1 dna聚合酶、q-β复制酶、末端转移酶、amv逆转录酶、m-mlv逆转录酶、phi6逆转录酶、hiv-1逆转录酶、通过生物勘探发现的新型聚合酶以及us 2007/0048748、美国专利号6,329,178;6,602,695;和6,395,524(以引用方式并入)中引用的聚合酶。这些聚合酶包括野生型、突变体同种型和基因工程变体。
[0117]“dna聚合酶”是由脱氧核苷酸单体(dntp)产生dna的聚合酶。如本文所用,“真细菌dna聚合酶”是指来自真细菌的pol a型dna聚合酶(修复聚合酶),包括但不限于来自大肠杆菌(e.coli)的dna聚合酶i、来自水生栖热菌(thermus aquaticus)的taq dna聚合酶和来自栖热菌属(thermus)的其他成员的dna pol i酶,以及其他真细菌物种等。
[0118]
如本文所用,如参考核酸链或核酸链上的位点所用,术语“靶”是指待检测或表征的核酸物种或核酸序列或结构。
[0119]
因此,如本文所用,“非靶”(例如,当它用于描述诸如dna的核酸时)是指可能存在于反应中但不是通过反应的检测或表征的对象的核酸。在一些实施方案中,非靶核酸可指代存在于例如不含靶序列的样品中的核酸,而在一些实施方案中,非靶可指代外源核酸,即不源自含有或怀疑含有靶核酸的样品并且被添加到反应中(例如,以使酶(例如,聚合酶)活性归一化以降低反应中的酶性能的变异性)的核酸。
[0120]
如本文所用,术语“扩增试剂”是指除引物、核酸模板和扩增酶外,扩增所需的那些试剂(脱氧核糖核苷三磷酸、缓冲液等)。通常,将扩增试剂与其他反应组分一起放置并包含在反应容器中。
[0121]
如本文所用,术语“对照”在用于指代核酸检测或分析时是指用于与实验靶(例如,浓度未知的核酸)比较的、具有已知特征(例如,已知序列、已知每个细胞的拷贝数)的核酸。对照可以是内源性的,优选不变的基因,测定中的测试核酸或靶核酸可以针对所述基因进行归一化。样品与样品变化的此类归一化对照可在例如样品处理、测定效率等中出现并且允许准确的样品与样品数据比较。对照也可以是外部的。例如,在定量测定(诸如qpcr、quarts等)中,“校准物”或“校准对照”是具有已知序列(例如,具有与实验靶核酸的部分相同的序列)和已知浓度或一系列浓度(例如,用于在定量pcr中生成校准曲线的连续稀释对照靶)的核酸。通常,使用与对实验dna使用的相同的试剂和反应条件分析校准对照。在某些实施方案中,校准物的测量与实验测定同时进行,例如在同一热循环仪中进行。在优选的实施方案中,多个校准物可包括在单个质粒中,使得以等摩尔量容易地提供不同的校准物序列。在特别优选的实施方案中,消化质粒校准物(例如,使用一种或多种限制性酶)以从质粒载体中释放校准物部分。参见例如wo 2015/066695,其以引用方式包括在本文中。
[0122]
如本文所用,术语“鱼dna”是指从鱼中分离的大量(例如,基因组)dna,例如,如美国专利号9,212,392中所述。大量纯化的鱼dna为可商购获得的,例如以鳕鱼和/或鲱鱼精dna(roche applied science,mannheim,germany)或鲑鱼dna(usb/affymetrix)形式提供。“鱼dna”不同于分离形式的(例如,已经单独地合成或已经从鱼基因组的其他dna中分离)、来自鱼的任何特定基因。
[0123]
如本文所用,术语“试剂盒”是指递送材料的任何递送系统。在核酸纯化系统和反应测定的上下文中,此类递送系统包括允许存储、运输试剂和装置(例如,适当容器中的离液盐、颗粒、缓冲液、变性剂、寡核苷酸、过滤器等)和/或支持材料(例如,样品处理或样品存储容器、用于执行程序的书面指令等)或将它们从一个位置递送至另一个位置的系统。例如,试剂盒包括一个或多个套罩(例如,盒),其含有相关反应试剂和/或支持材料。如本文所用,术语“片段化试剂盒”是指包含两个或更多个单独容器的递送系统,每个容器含有总试剂盒组分的子部分。这些容器可一起或单独递送至预定接受者。例如,第一容器可含有用于样品收集的材料和缓冲液,而第二容器含有捕获寡核苷酸和变性剂。术语“片段化试剂盒”旨在涵盖含有根据联邦食品、药物和化妆品法案(federal food,drug,and cosmetic act)的部分520(e)来监管的分析物特异性试剂(asr)的试剂盒,但是不限于此。实际上,包含各自含有总试剂盒组分的子部分的两个或更多个单独容器的任何递送系统包括在术语“片段化试剂盒”中。相比之下,“组合试剂盒”是指在单个容器(例如,容纳每个期望组分的单个盒)中包含反应测定的所有组分的递送系统。术语“试剂盒”包括片段化试剂盒和组合试剂盒。
[0124]
如本文所用,术语“系统”是指出于特定目的使用的制品的集合。在一些实施方案中,制品包含使用说明书,作为例如制品、纸、在线(例如,网站或网址)、可记录介质(例如,磁盘、cd、dvd、闪存驱动器等)上供应的信息。在一些实施方案中,说明书将用户引导至在线位置(例如网站)以查看、收听和/或下载说明书。在一些实施方案中,说明书或其他信息作为例如用于计算机或用于移动装置(诸如智能电话)的应用程序(“app”)提供。
附图说明
[0125]
参照以下附图,本技术的这些和其他特征、方面和优点将变得更加容易理解:
[0126]
图1a、图1b和图1c分别提供了由三条核酸链、两条核酸链或一条核酸链形成的侵入性切割结构的示意图。
[0127]
图1d提供了包含fret盒报告基因寡核苷酸的组合的pcr-侵入性切割测定(“pcr-瓣测定”)(例如,quarts测定)的示意图。
[0128]
图2示出了示例性pcr-瓣测定的核酸序列和示意性结构,其中瓣通过瓣状寡核苷酸的切割而释放,并且瓣与fret盒寡核苷酸的3'区域杂交以形成第二种切割结构。瓣-fret盒复合物的切割将荧光团与猝灭剂部分分离,并导致来自荧光团的可检测荧光增加。
[0129]
图3a至图3d展示了三种5'发夹fret报告分子。图3a示出了5'发夹fret报告分子1、2和3的线性序列,并且示出每种5'发夹fret报告分子上的5'发夹的二级结构的示意性表示在图3b、图3c和图3d中示出。用于5'发夹fret报告分子1、2和3的5'部分中的不同茎导致报告分子的这些部分的计算解链温度不同。
[0130]
图4a至图4c提供了5'发夹fret测定报告分子在可切割的和被抑制的切割配置中的示意性表示。虽然不将本技术限制于任何特定的作用机制,但可在低温下形成5'发夹,从而在测定反应混合物不处于优选反应温度下时抑制荧光团和猝灭剂部分之间的报告切割位点处的瓣状核酸内切酶切割(如图4a至图4b所示)。在瓣测定反应温度(通常高于5'发夹的计算解链温度)下,报告切割位点处的瓣状核酸内切酶切割不被抑制,并且可以发生切割以从猝灭剂附近释放荧光团,从而导致来自荧光团的荧光信号增加(图4c)。
[0131]
图5提供了掺入5'发夹fret测定报告基因的pcr-瓣测定(例如,quarts测定)的示意图。
[0132]
图6a提供了比较来自标准fret盒和来自两个5'发夹fret报告基因(发夹1和发夹2)的背景荧光的图表,所述标准fret盒和5'发夹fret报告基因在不存在靶引物的情况下用于连续侵入性信号扩增反应中。
[0133]
图6b提供了比较来自标准fret盒和来自两个5'发夹fret报告基因(发夹1和发夹2)的信号的图表,所述标准fret盒和5'发夹fret报告基因在存在靶引物的情况下用于连续侵入性信号扩增反应中。
[0134]
图7a、图7b、图7c和图d提供了比较来自标准fret盒(图7a)和来自三个5'发夹fret报告基因(图7b、图7c和图7d,分别示出了发夹1、2和3的数据)的图表,所述标准fret盒和5'发夹fret报告基因用于与侵入性切割化学组合的实时pcr反应中(长探针定量扩增信号,lqas)。fret测定报告基因被设计成有和没有5'发夹,并且在使用标准fret盒展示高背景信号的测定设计中进行测试(图7a)。包括5'发夹导致背景信号减少(图7b、图7c和图7d),从而导致更清晰的扩增曲线和改善的信噪比。
[0135]
图8a和图8b提供了瓣状核酸内切酶的5'发夹测试底物的示意图。除了5'发夹形成区和下游双链发夹形成区之外,测试底物还包括配置成形成上游双链体的3'发夹形成区,以定位底物寡核苷酸的3'端以充当侵入性切割结构中的侵入性寡核苷酸。
[0136]
图9提供了5'发夹测试底物的实施方案的预测二级结构,其中指示了上游和下游双链体、靶切割位点以及阻遏性5'瓣中的5'发夹。
[0137]
图10提供了示出使用有或没有阻遏性5'发夹的、在35℃下孵育的单分子底物的荧光的图表。
[0138]
图11a和图11b提供了展示与在缺乏阻遏性5'发夹的底物上测量的瓣状核酸内切
酶活性(图11a)相比,5'发夹结构阻遏报告切割位点处的瓣状核酸内切酶切割的活性(图11b)的图表。
[0139]
图12提供示出在作为被切割5'发夹测试底物v3的量的直接量度的反应期间测量的荧光信号的图表,如下所述。
[0140]
图13a和图13b展示了示出导致线性标准曲线的微分响应的标准物质(例如,5'发夹测试底物)的滴定。所述标准曲线提供了用于确定未知批次的酶的相对性能的方式。将反应线性部分的随时间增加的荧光速率(log[rfu/s])与酶浓度(log[fen-1(nm)])作图。
[0141]
图14a展示了通过具有5'发夹形成区的探针寡核苷酸与上游侵入性寡核苷酸杂交而在靶链上形成的侵入性切割结构。在瓣测定反应温度(通常高于5'发夹的计算解链温度)下,靶切割位点处的瓣状核酸内切酶切割不被抑制,并且可以发生切割以从探针寡核苷酸释放5'瓣臂。释放的瓣可以与标准fret盒和5'发夹fret报告分子形成侵入性切割结构,分别如图14b和图14c所示。
[0142]
图14b和图14c是由释放的瓣状寡核苷酸和标准fret盒(图14b)或5'发夹fret报告分子(图14c)形成的侵入性切割结构的示意图。
[0143]
图15a至图15p提供了比较来自连续侵入性切割测定的信号的图表,所述测定具有不同量的靶dna并且使用标准探针或5'发夹探针以及标准fret盒或5'发夹fret盒,如图14a、图14b和图14c示意性所示,如实施例3中所述。
具体实施方式
[0144]
本技术涉及可被瓣状核酸内切酶切割的结构。特别地,本技术涉及形成可以被例如温度的改变操纵以调节或抑制瓣状核酸内切酶在报告切割位点的切割的核酸结构。
[0145]
设计核酸检测测定的一个方面是选择在靶分析物不存在时产生最少量背景信号并且在靶分析物存在的情况下产生独特报告信号的反应组分和条件。在瓣状核酸内切酶测定中,信号生成的一个方面是瓣状寡核苷酸和报告分子(诸如fret盒)的特异性切割。因此,在瓣状核酸内切酶测定中最小化背景的一个方面是使用足够高的反应温度,使得来自测试样品的核酸与测定的检测寡核苷酸(例如,引物、瓣状寡核苷酸)之间的杂交非常特异。通常,热稳定性酶用于此类测定,使得测定反应可以在最小化或消除测定寡核苷酸的非特异性结合的反应温度下执行。
[0146]
用于高温测定(诸如pcr和pcr-瓣状核酸内切酶测定)的测定反应混合物通常在远低于最终反应温度的温度下(例如在室温下或在冰上)组装。在这些较低的温度下,报告寡核苷酸的切割可以非特异性方式发生,例如通过在不太严格的条件下的错误杂交。
[0147]
在一个方面,本技术提供了经修饰的寡核苷酸底物,其在低温下阻遏瓣状核酸内切酶在靶或报告切割位点的切割,但允许在所选择的测定反应温度或温度范围下的报告切割位点处的切割。在一些实施方案中,经修饰的测定寡核苷酸(例如,瓣状寡核苷酸或fret测定报告基因)包含5'瓣区域,5'瓣区域包括在较低温度下抑制报告切割位点处的切割的结构和部分,但在执行测定的温度下失去所述结构或部分,使得报告切割位点处的切割可以发生。在优选的实施方案中,经修饰的测定寡核苷酸包含5'发夹。
[0148]
在一些实施方案中,本技术可用于瓣状核酸内切酶测定中,包括例如pcr-瓣测定,诸如美国专利号8,361,720;8,715,937;和8,916,344中描述的quarts测定和美国专利号9,
096,893的扩增测定。参见例如图1,其提供了pcr-瓣测定的实施方案的示意图。如图所示,在靶链区域的扩增期间,靶特异性探针被瓣状核酸内切酶切割以释放5'瓣。在二级反应中,释放的5'瓣用作荧光共振能量转移(fret)盒上的侵入性寡核苷酸以再次产生被瓣状核酸内切酶识别的结构。当单个fret盒上的荧光团和猝灭剂通过切割分离时,产生高于背景荧光的可检测荧光信号。因此,这种第二种结构的切割导致荧光增加,从而指示靶核酸的存在。在多个不同的靶待检测的实施方案中,fret盒可对每个待检测的等位基因或基因座具有不同的标记(例如,可通过发射或激发波长的差异来分辨,或可通过时间分辨荧光检测来分辨),使得可以在单个反应中检测不同的等位基因或基因座。在此类实施方案中,用于多个靶序列的瓣测定寡核苷酸可组合在单个反应混合物中,从而允许来自同一样品中的每个等位基因或基因座的信号的比较。
[0149]
本文的技术提供了用于瓣状核酸内切酶的经修饰底物。在特定实施方案中,测定寡核苷酸(例如,瓣状寡核苷酸或fret报告基因)包含瓣测定反应中的待切割寡核苷酸的5'瓣中的发夹结构,优选dna发夹。
[0150]
通过考虑存在的发夹数量,本技术容易与标准fret测定报告基因进行对比,因为标准fret盒通常含有单个发夹(参见例如图2),而本技术的5'发夹分子通常由两个或三个发夹组成。
[0151][0152]
虽然本技术在本文中通过参考含有5'发夹的分子用fret系统标记的实施方案来讨论,但本技术不限于此类实施方案。还预期将本技术应用于未标记的寡核苷酸和结构以及使用不同类型的标记的寡核苷酸和结构,并且所述应用在本技术的范围内。
[0153]
在本技术的开发过程中,已经观察到5'发夹的存在通过减少背景切割来改善侵入性切割化学。本技术可以掺入到瓣状切割底物中(例如掺入到fret盒结构中)以改善瓣测定反应(包括pcr-瓣测定反应)中的信噪分离。修饰为具有5'发夹的fret盒通常包含两个发夹:调节报告切割位点处的切割的5'发夹和形成是侵入性切割结构的特征的下游双链体的发夹,如图4a示意性所示。为方便起见,这种经修饰的fret盒可称为“5'发夹fret报告基因”。
[0154]
5'发夹fret报告基因含有经计算形成具有低于反应孵育温度的解链温度的发夹的5'瓣中的序列。当这种5'发夹fret报告基因在室温下与瓣状核酸内切酶混合时,切割受到限制。虽然本技术不限于任何特定的作用机制,但数据表明,随着反应的孵育温度增加到超过阻遏性发夹的解链点,发夹解链,从而提供单链5'臂,fen酶可以在所述单链5'臂上穿线以到达fret标记系统部分之间的报告切割位点。因此,当达到或超过阻遏性臂的解链温度时,瓣状核酸内切酶可以切割报告分子以将荧光团与含有猝灭剂的底物的部分分离,从而导致荧光信号的可测量增加。
[0155]
本技术还可用作包含三个可用于例如表征瓣状核酸内切酶活性的发夹的多合一测试底物的一部分。图8a提供了这种3-发夹测试底物的示意图。在优选的实施方案中,3-发
夹底物包含fret标记系统,其中荧光团和猝灭剂可通过报告切割位点处的瓣状核酸内切酶切割而分离。如上文针对瓣状核酸内切酶测定所述,当这种含有5'发夹的底物在低温下(例如在室温下)与瓣状核酸内切酶混合时,切割被抑制。切割可以通过升高反应混合物的温度来引发。虽然不将本技术限制于任何特定的作用机制,但测试底物的5'发夹经计算在升高的反应温度下解链,使得瓣状核酸内切酶可到达报告切割位点,并且测试底物在报告切割位点被切割。因此,5'发夹测试底物允许切割测定反应的精确引发。使用fret标记系统的另一个优点是允许在反应中发生测试底物的切割时实时检测测试底物的切割。组合来说,3-发夹测试底物的特征允许酶活性的精确表征。
[0156]
本技术还可应用于同步引发多个测定(例如,在不同反应容器中或在多孔测定板的不同孔中)中。在此类实施方案中,反应混合物可在不同时间组装并且可通过基本上同时升高所有容器中的温度来引发。例如,当测定试剂的移液过程使得用于多种不同反应混合物的试剂的同时混合不切实际或不可能时,这种通过温度移动的同步反应引发是有用的。
[0157]
在一些实施方案中,不同的5'发夹结构用于提供不同的测定开始时间。例如,5'发夹fret报告基因可配置成含有在不同温度下解链的5'发夹。使用具有在40℃、50℃和60℃下解链的5'阻遏性发夹的fret报告基因,可以在低于40℃的温度下组装一组反应,然后可通过将温度升高至40℃、50℃然后60℃(时间定义为适合特定实验的需要)来随意引发不同的反应。
[0158]
在一些实施方案中,切割活性的5'发夹调节用于调整表现出不同反应速率的测定的切割速率。例如,使用不同的fret标记系统(例如,不同的荧光团-猝灭剂组合)可改变瓣状核酸内切酶对不同的fret报告基因表现出的切割活性,所述fret报告基因原本具有相同的一级序列和预测的二级结构。预期不同的5'发夹修饰(例如,具有不同长度或稳定性的发夹)可用于使不同fret报告基因(例如,具有不同荧光团的fret报告基因)中的切割速率归一化中。此实施方案可应用于例如使用多种不同染料的多重测定中,并且其中可能期望所有fret报告基因以大约相同的速率被切割。
[0159]
表征瓣状核酸内切酶
[0160]
本技术还可应用于其他类型的测定(例如,用于表征瓣状核酸内切酶活性的测定)中。由一个或多个寡核苷酸(通常为合成寡核苷酸)构成的模型核酸结构可用于被设计来检测或测量瓣状核酸内切酶活性(例如,在怀疑具有此类活性的酶(例如,dna聚合酶、修复核酸酶)中或在怀疑产生此类酶的生物体中)和检测瓣状核酸内切酶活性(例如,在不同测定条件下)的测定中。例如,各种合成瓣结构已用于表征重组fen-1核酸内切酶的活性和结构特异性(参见例如lyamichev等人的美国专利号7,122,364和kaiser m.w.等人j.biol.chem.,274:21387(1999),所述专利和文献各自以引用方式整体并入本文)。lyamichev和kaiser测试的结构不包含本技术的5'发夹结构。
[0161]
本文的技术提供了一种3-发夹底物,其包含可用于表征瓣状核酸内切酶活性的侵入性切割结构的上游双链体和下游双链体,如图8a所示。虽然不将本技术限制于任何特定的作用机制,但观察到5'发夹的存在阻遏下游双链体中的优选位点的侵入性切割,所述优选位点如图8a中的报告切割位点所示。随着反应的孵育温度升高并且超过阻遏性5'发夹的计算解链温度,形成用于瓣状核酸内切酶切割的优选结构并引发切割反应(参见图8b)。
[0162]
当使用fret标记系统时,靶切割位点处的切割将荧光团与猝灭剂分离,从而导致
荧光增加。这种信号可以实时监测,并且对应于反应中的瓣状核酸内切酶切割活性。
[0163]
在一些实施方案中,5'发夹报告基因和测试底物可包括含有碱基类似物、间隔物(例如,9-碳间隔物)和/或碱基类似物(例如,非标准碱基、脱碱基糖或接头等)的5'发夹。在一些实施方案中,5'臂可配置成利用阻断瓣状核酸内切酶到达靶切割位点的替代方法。例如,预期了将短寡核苷酸退火到单链5'臂上的双分子方法,或者5'臂可以不耐热的方式与阻断部分缀合,其中缀合的阻断剂在升高的温度下释放或以其他方式呈中性。
[0164]
实验实施例
[0165]
quarts和lqas/telqas瓣测定技术将基于聚合酶的靶dna扩增过程与侵入性基于切割的信号扩增过程组合。quarts技术描述于例如美国专利号8,361,720;8,715,937;8,916,344和9,212,392中,并且使用具有较长靶特异性区域的探针寡核苷酸(长探针定量扩增信号,“lqas”)的瓣测定描述于美国专利10,648,025中,出于所有目的,所述专利各自以引用方式整体并入本文。在本文所述的quarts测定中,瓣状寡核苷酸具有12个碱基的靶特异性区域,而lqas测定使用具有至少13个碱基的靶特异性区域的瓣状寡核苷酸,并使用不同的热循环程序进行扩增。由quarts和lqas反应生成的荧光信号以与实时pcr相似的方式监测,从而允许定量样品中的靶核酸的量。
[0166]
示例性quarts pcr-瓣测定反应通常包含大约200-600nm(例如,500nm)的每种引物和检测探针、大约100nm的侵入性寡核苷酸、大约600-700nm的每种fret盒(fam,例如,如由hologic,inc.在商业上供应;hex,例如,如由biosearch technologies在商业上供应;和quasar 670,例如,如由biosearch technologies在商业上供应,并且包含“黑洞”猝灭剂(“black hole”quencher),例如,bhq-1、bhq-2或bhq-3,biosearch technologies)、6.675ng/μl的fen-1核酸内切酶(例如,2.0,hologic,inc.)、30μl反应体积中的1个单位的taq dna聚合酶(例如,dna聚合酶,promega corp.,madison,wi)、10mm的3-(正吗啉代)丙磺酸(mops)、7.5mm的mgcl2和250μm的每种dntp。
[0167]
示例性quarts循环条件如下所示:
[0168][0169]
示例性lqas反应通常包含大约200-600nmol/l的每种引物、大约100nmol/l的侵入性寡核苷酸、大约500nmol/l的每种瓣状寡核苷酸探针和fret盒。lqas反应可例如经受以下热循环条件:
[0170][0171][0172]
靶向的预扩增
[0173]
预扩增通常以多种形式进行,即多种不同的靶核酸一起扩增。例如在含有以下各项的反应混合物中进行预扩增:7.5mm mgcl2、10mm mops、0.3mm tris-hcl、ph 8.0、0.8mm kcl、0.1μg/μl bsa、0.0001%tween-20、0.0001%igepal ca-630、250μm每种dntp、寡核苷酸引物(例如,对于12种靶、12个引物对/24个引物,以等摩尔量计(包括但不限于例如200-500nm每种引物的范围),或者其中单个引物浓度被调整以平衡不同靶区域的扩增效率)、0.025个单位/μl hotstart gotaq浓度以及20体积%至50体积%的亚硫酸氢盐处理的靶dna(例如,10μl靶dna到50μl反应混合物中或者50μl靶dna到125μl反应混合物中)。选择对于反应的体积和扩增容器适当的热循环时间和温度。例如,反应可如下循环:
[0174][0175]
在热循环之后,将预扩增反应的等分试样(例如,10μl)在10mm tris、0.1mm edta中在具有或不具有鱼dna的情况下稀释到500μl。将稀释的预扩增的dna的等分试样(例如,10μl)用于quarts pcr-瓣测定中,例如,如上所述。还参见2015年10月30日提交的美国专利申请序列号62/249,097;2016年10月26日提交的申请序列号15/335,096;以及2016年10月26日提交的pct/us16/58875,出于所有目的,所述专利各自以引用方式整体并入本文。
[0176]
组合的预扩增和lqas测定被称为telqas测定(“靶富集长探针定量扩增信号”)。
[0177]
使用预扩增样品,quarts和telqas反应设置如下:
[0178][0179]
*10x寡核苷酸混合物=2μm每种引物和5μm每种探针和fret寡核苷酸
[0180]
**20x酶混合物含有1个单位/μl gotaq热启动聚合酶(promega)、292ng/μl cleavase 2.0瓣状核酸内切酶(hologic)。
[0181]
如上所述,quarts测定中的瓣状寡核苷酸具有12个碱基的靶特异性区域,而lqas测定使用具有至少13个碱基的靶特异性区域的瓣状寡核苷酸,并经受不同的热循环条件。
[0182]
quarts反应经受以下热循环条件:
[0183][0184]
lqas/telqas反应经受以下热循环条件:
[0185][0186]
用于rna检测的lqas/telqas(“rt-lqas”或“rt-telqas”)
[0187]
示例性rt-lqas反应含有20u的mmlv逆转录酶(mmlv-rt)、219ng的2.0、1.5u的dna聚合酶、200nm的每种引物、500nm的每种探针和fret寡核苷酸、10mm mops缓冲液、ph 7.5、7.5mm mgcl2和250μm的每种dntp。示例性方案如下:
[0188]
1.从-20℃冷冻机中取出所需的寡核苷酸混合物并使其解冻。
[0189]
2.在室温下将对照从-80℃解冻一小段时间,然后放置在冰上。
[0190]
3.在室温下将样品板从-80℃解冻一小段时间,然后放置在冰上。
[0191]
4.在适当尺寸的管中制备寡核苷酸混合物的主混合物。
[0192]
5.在h2o中以1:20稀释mmlv-rt
[0193][0194]
6.按照板布局,使用矩阵移液器或八通道p20移液器将20μl主混合物移液到96孔rt-lqas板中。
[0195]
7.加载10μl样品(靶核酸)、对照、校准物(用于校准的稀释系列)(按照板布局)。
[0196]
8.封闭板并短暂离心。
[0197]
9.在以下反应条件下运行板
[0198]
反应通常在配置成实时收集荧光数据的热循环仪上运行(例如,连续地,或在一些或所有循环中的同一点)。例如,roche lightcycler480仪器或applied biosystem quantstudiodx实时pcr仪器可在以下条件下使用:
[0199][0200]
在一些实施方案中,rt-lqas测定可包括多重逆转录和预扩增的步骤,以例如预扩增样品中的2、5、10、12或更多个靶(或多于1个靶的任何数量的靶),如上所述,并且可称为“rt-telqas”。在优选的实施方案中,rt-预扩增在含有以下各项的反应混合物中进行:例如,20u的mmlv逆转录酶、1.5u的dna聚合酶、10mm mops缓冲液、ph7.5、7.5mm mgcl2、250μm的每种dntp和寡核苷酸引物(例如,对于12种靶、12个引物对/24个引物,以等摩尔量计(例如,200nm每种引物),或者其中单个引物浓度被调整以平衡不同靶的扩增效率)。选择对于反应的体积和扩增容器适当的热循环时间和温度。例如,反应可如下循环:
[0201]
[0202]
在热循环之后,将rt-预扩增反应的等分试样(例如,10μl)在10mm tris、0.1mm edta中在具有或不具有鱼dna的情况下稀释到500μl。将稀释的预扩增的dna的等分试样(例如,10μl)用于lqas/telqas pcr-瓣测定中,如上所述。在一些实施方案中,使用另外量的相同引物对来执行lqas/telqas pcr瓣测定。
[0203]
实施例1
[0204]
连续侵入性切割和pcr-瓣状核酸内切酶测定中的标准fret盒与5'发夹fret报告基因的比较
[0205]
修饰标准fret盒设计(例如参见图2)以包括两种不同的5'发夹中的一种(参见图3a至图3d)。在存在或不存在被测定寡核苷酸识别的靶dna的情况下,在连续侵入性切割测定中,这两种5'发夹fret报告基因与标准fret盒(无5'发夹)一起进行测试。每个5'发夹测定报告基因使用fam作为荧光团并使用black hole1(“bhq1,”biosearch technologies)作为猝灭剂,如图3所示掺入到t核苷酸上。如hall jg等人,proc natl acad sci usa 97:8272-8277(2000)所述执行连续侵入性切割测定,并且实时测量荧光信号。结果在图6a(无靶对照)和图6b(有靶)中示出。
[0206]
这些数据表明,在反应中有或没有靶dna的情况下,使用没有5'发夹的fret盒导致荧光水平更高。虽然5'发夹fret报告基因在模板阳性反应中表现出较低的荧光信号,但相对于对照fret盒,阴性和阳性模板反应之间的分离增加了。对于不同的fret测定报告基因设计中的每一种,计算每种fret报告基因的信噪比以确定来自阳性(有靶模板)和阴性(没有靶模板)反应的信号之间的分离。
[0207][0208]
fret报告基因时间(分钟)信噪比对照(标准fret盒)2255.455'发夹122513.215'发夹222513.60
[0209]
这些数据表明,使用含有5'发夹形成序列的fret报告分子导致信号和噪声之间的分离更大。更大的分离主要是由于在阴性(没有靶)样品组中生成的背景信号减少。
[0210]
pcr-瓣测定反应
[0211]
将用于实时pcr-瓣状核酸内切酶测定(lqas测定,如上所述)中的fret盒用包括5'发夹的fret测定报告基因替换。5'发夹fret报告基因1、2和3的一级结构在图3a中示出,并且二级结构在图3b至图3d中示出。具有和不具有5'发夹形成序列的fret测定报告基因在pcr-瓣测定反应中进行比较。这些数据在图7a(使用标准fret盒)、图7b(使用5'发夹fret报告基因1)、图7c(使用5'发夹fret报告基因2)和图7d(使用5'发夹fret报告基因3)中示出。这些数据表明,使用任何5'发夹fret报告基因的反应的背景斜率降低(图7b至图7d)。当将这些反应与无模板对照反应进行比较时,背景斜率的降低导致信噪比的改善。
[0212]
下文示出了在这些瓣测定反应中测试的三种5'发夹fret报告分子的序列。这些报告基因包含具有不同计算解链温度的不同5'发夹设计,如下所示。
[0213][0214]
实施例2
[0215]
单分子瓣状核酸内切酶底物
[0216]
比较了没有和有抑制切割的5'发夹的单分子底物上的切割反应。每种底物包含荧光团和猝灭剂,如图8示意性所示。单分子测试底物的二级结构的实例在图9中示出。这种分子的线性序列在下表中示为“v3”。所述设计的其他迭代包括含有9-碳间隔物(c9)的5'发夹、一组无碱基内部修饰(ds)或双分子方法,其中较短的寡核苷酸退火到单链5'-臂上。
[0217]
实时监测荧光随时间推移的变化提供了酶促活性的直接指示。反应的线性部分的鉴定允许线性回归分配指示瓣状核酸内切酶活性的rfu/s值(参见图10)。
[0218]
测定包含单分子底物、瓣状核酸内切酶、mgcl2或mncl2和缓冲剂中的一种。载体蛋白,诸如牛血清白蛋白(bsa)也可以用于所述测定中。为了执行测定,将参考批次的瓣状核酸内切酶以标准曲线稀释。然后稀释未知的酶(例如,fen-1核酸内切酶)以靶向参考滴定的中心。以下是可使用的反应浓度的实例。
[0219]
表1:瓣状核酸内切酶测试反应制剂
[0220]
试剂反应浓度水namops,ph 7.510mmmgcl27.5mm底物5μm酶15-150nm
[0221]
将酶稀释液与底物、缓冲液和mgcl2混合。然后将这些反应在监测动态荧光的等温温度下孵育。检测到的荧光随时间增加的速率是酶活性的直接指示。因此,参考滴定基于可用于生成标准曲线的酶浓度提供微分响应(图12)。这种标准曲线可用于执行线性回归以确定未知批次的酶的相对活性百分比。
[0222]
下表提供了示例性单分子底物的一级序列:
[0223]
v1(fams和faml)=无阻遏性臂(无5'发夹)
[0224]
v2(ds)=具有用于5'发夹环的“dspacer”内部修饰的5'发夹寡核苷酸。
[0225]
v2(c9)=具有用于5'发夹环的“spacer9”内部修饰的5'发夹寡核苷酸。
[0226]
v2(hp)=具有用作5'发夹中的环序列的“t”的5'发夹寡核苷酸。
[0227]
表2:单分子侵入性切割测试底物
[0228][0229][0230]
图10中的图表示出了在使用具有或不具有阻遏性5'臂的单个底物的35℃温度下的孵育期间测量的荧光。测试使用上文的v3测试底物或具有相同序列但缺乏5'发夹部分的对照fret盒,并使用2.0(hologic,inc.)来进行。含有阻遏性发夹的寡核苷酸在整个孵育期间表现出一致的低荧光,而不具有阻遏性臂的底物表现出较高的初始荧光,这指示了在将反应混合物转移至反应板期间发生的切割。这些数据还表明,缺乏阻遏性臂的底物的荧光随时间推移而增加,这表明在这种低孵育温度下发生持续的切割。
[0231]
图11中的数据展示了5'结构在靶切割位点阻遏酶促切割的能力。使用上文的v3测试底物或缺乏上述5'发夹的对照fret盒进行测试。所述图表示出了对于不具有(图11a)或具有(图11b)阻遏性臂的单个底物进行的反应,在53℃的孵育温度下测量的荧光。含有阻遏性5'发夹的寡核苷酸在数据收集开始时表现出低荧光,这表明在反应设置期间成功阻遏了酶促切割,而没有阻遏性臂的底物表现出更高的初始荧光,这指示在反应设置期间发生了切割。5'阻遏性臂还导致在酶浓度范围(0-40nm)内产生更好的斜率均匀性和分离。
[0232]
图12示出了在反应期间测量的荧光信号是被切割的底物(上文的测试底物v3)的量的直接量度。因此,荧光随时间的定量(rfu/s)是酶活性的直接量度。反应的线性部分的鉴定允许确定给定反应的rfu/s值。为了做到这一点,使用来自每个反应的原始荧光数据来
确定数据集中每个时间点的一阶导数。一阶导数提供了变化率的直接指示。然后使用一阶导数数据来鉴定每个反应的最大值,所述最大值用于将导数数据表示为%最大值。将阈值应用于%最大值数据以确定每个反应的rfu数据的线性子集,其可以用于线性回归中以确定每个反应的rfu/s活性。图12展示了与%最大值一阶导数(红色圆圈)一起绘制的反应曲线(蓝色十字)。反应曲线的突出显示部分用于线性回归。
[0233]
图13展示了执行标准物质的滴定示出了导致线性标准曲线的微分响应。所述标准曲线提供了用于确定未知批次的酶的相对性能的方式。将反应线性部分的随时间增加的荧光速率(rfu/s)与酶浓度作图。
[0234]
使用阻遏性5'修饰(例如,5'发夹)减少环境温度下的靶切割位点处的切割。因为用于测定中的底物是单分子,所以不需要退火反应,并且确保猝灭剂和荧光团的等摩尔。因此,使用具有fret标记系统的3-发夹单分子底物(例如,如图8和图9所示)的测定提供了实时监测瓣状核酸内切酶活性的方式,减少了背景切割,并且提供了用户友好的设置。用于表征瓣状核酸内切酶活性的先前的测定没有控制反应的开始并且在不需要杂交的情况下实时监测。本技术提供了一种可再现的并提供更高敏感度的测定。
[0235]
执行测试以确定所述测定是否能够区分各批次的瓣状核酸内切酶的不同活性水平。针对参考稀释系列测试了低、中和高性能批次的afu fen-1核酸内切酶(如通过quarts测定性能确定)。结果在下表中示出。
[0236]
表3:酶性能判别(对v3测试底物,表2)
[0237][0238][0239]
结果表明,使用5'阻遏性臂测试底物的测定具有使用针对标准曲线的线性回归来区分高、中和低性能批次的酶的能力。所述测定的进一步表征包括涉及多个操作员、仪器和试剂批次的多地点研究,其示出了所述测定优异的再现性,所有运行的%cv为7-8%(数据未示出)。
[0240]
此测定提供了可在60分钟内执行的简单的工作流程。数据收集和分析是简单易懂的,并且最小化可影响结果的变量。例如,不需要温度循环、寡核苷酸杂交或taq聚合。另外,与终点技术相比,使用动态荧光以实时检测酶活性提供了更敏感的活性评估方法。
[0241]
实施例3
[0242]
侵入性切割结构中的探针寡核苷酸上的5'发夹瓣
[0243]
连续侵入性切割测定使用初级探针寡核苷酸上的、fret报告寡核苷酸上的和两者上的5'发夹进行测试。还比较了具有不同热稳定性(即,具有59℃(“高”温)或51℃(“低”温)的计算温度)的5'发夹的初级探针寡核苷酸如hall jg等人,proc natl acad sci usa 97:8272-8277(2000)所述执行连续侵入性切割测定,不同的是反应首先在靶切割位点处的切割应被阻断的温度下孵育,然后移动到5'发夹应该展开并且靶切割位点处的切割应该发生
的温度。以一分钟的间隔实时测量荧光信号。
[0244]
在下文讨论的实验中,“探针”是指连续侵入性切割反应中的靶特异性瓣测定探针,有时也称为“初级探针”。含有lass4_4482基因区域的经消化的血浆dna用作测定中的靶材料。
[0245]
用于连续侵入性切割测定的寡核苷酸如下:
[0246][0247]
使用10%漂白剂清洁工作台区域,然后用去离子水冲洗并允许风干。在风干时,用6%过氧化氢擦拭移液器。从冷藏中取出寡核苷酸和试剂并使它们在室温下平衡30分钟。
[0248]
试剂如下制备:
[0249]
1.制备bsa的稀释液:
[0250][0251]
2.制备正向引物/侵入性寡核苷酸的1:10稀释液
[0252]
3.制备用于待测试的每种测定配置的10x寡核苷酸混合物:
[0253][0254]
4.测试了寡核苷酸的以下组合:
[0255]
i.对照混合物-所有标准组分(fret测定报告基因或探针上无发夹)
[0256]
ii.发夹fret+标准探针
[0257]
iii.发夹探针+标准fret盒
[0258]
iv.发夹fret+发夹探针
[0259]
使用标准或发夹fret(arm 5fam)和发夹探针的矩阵来设置连续侵入性切割反应。设置标准arm 7fam fret和arm 7探针的对照混合物以进行比较。反应如下组装:
[0260]
5.制备10x反应混合物:
[0261][0262][0263]
6.制备连续侵入性切割测定反应混合物:
[0264][0265]
7.将20μl的主混合物转移到96孔lightcycler板的孔中。
[0266]
8.将10ul的靶dna转移到板孔中。“无靶”对照反应含有鱼dna稀释剂。
[0267]
9.封闭板并在板旋转器中短暂旋转。
[0268]
10.按照以下参数在quantstudio dx上运行板,反应体积为30ul。
[0269]
循环条件
[0270][0271]
如上所述,测定板在40℃或50℃下孵育180分钟,每分钟收集一次数据。此孵育期示出了在5'发夹被配置成阻断靶切割位点处的切割的温度下,阻断探针和发夹fret测定报告基因的切割的功效。然后将板在63℃下孵育240分钟,每分钟收集一次数据。此孵育期示出了连续侵入性切割测定试剂在生成信号以响应不同量的靶dna方面的功效。“高”dna反应含有2x109链的靶dna,“中”dna反应含有2x108链的靶dna,并且“低”dna反应含有2x107链的靶dna。
[0272]
使用多组分数据评估扩增曲线。确定每个孔的线性拟合(rfu/循环)并在混合物之间进行比较。结果在图15a至图15p中示出,其中规格反应配置在每个标题栏中示出。放大“缩放”图以示出50℃(阻遏)孵育和63℃(未阻遏)切割测定条件之间的过渡。这些数据表明,当反应移动到更高的“未阻遏”温度时,初级探针上的5
′
发夹抑制背景并且不抑制测定。
[0273]
参考文献
[0274]
1.kaiser m,et al.j biol chem.1999.vol 274,no 30,21387-21394.
[0275]
2.dorjsuren d,et al.nucleic acids research.2011.vol 39,no 2 el 1
[0276]
3.lyamichev v,et al.biochemistry.2000.39,9523-9532.
[0277]
4.tsutakawa s,et al.cell.2011.145,198-211.
[0278]
5.tumey n,et al.bioorg&med chem let.2004.15,277-281.
[0279]
6.hall jg,et al.proc natl acad sci usa 2000;97:8272-8277.sensitive detection of dna polymorphisms by the serial invasive signal amplification reaction.
[0280]
7.allawi ht,et al.j of clin microbio 2006;vol 44,no.9:3443-3447.invader plus method detects herpes simplex virus in cerebrospinal fluid and simultaneously differentiates types 1 and 2.
[0281]
本技术中引用的所有文献和类似的材料,包括但不限于专利、专利申请、文章、书籍、论文和因特网网页,出于任何目的以引用的方式明确地整体并入。除非另外定义,否则本文中使用的所有技术性和科学性术语具有与本文所描述的各种实施方案所属领域中的普通技术人员通常所理解的相同的含义。当引入的参考文献中的术语的定义与本教义中提供的定义不同时,以本教义中提供的定义为主。
[0282]
本技术的所描述的组合物、方法和用途的各种修改和变化对于本领域技术人员是显而易知的,而不背离所描述的技术的范围和精神。虽然已结合具体的示例性实施方案描述了本技术,但应理解的是,要求保护的本发明不应不适当地局限于这些具体的实施方案。事实上,对药理学、生物化学、医学科学或相关领域的技术人员来说显而易见的用于执行本发明的所描述模式的各种修改意图在以下权利要求的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1