具有硫磷酰胺晶体结构的树枝状大分子及其衍生物
1.本发明涉及一种新的具有硫磷酰胺晶体结构的树枝状大分子及其衍生物,其制备方法和用途。
背景技术:
2.树枝状大分子是由单体构成的大分子,这些单体在多官能核心周围通过支化过程结合。
3.树枝状大分子,也称为“级联分子”或“分子树”,是具有确定结构的高度支化的官能聚合物。这些大分子实际是聚合物,这是因为它们基于重复单元的结合。然而,树枝状大分子由于它们的树状结构所赋予的固有特性而与传统聚合物有本质的不同。树枝状大分子的分子量和形状可以得到精确控制,并且所有官能团都位于树状结构的末端,形成一个平面,使其易于使用。
4.树枝状大分子是通过重复一系列反应逐步构建的,从而使每个可重复单元和末端官能团倍增。每一系列反应都形成所谓的“新一代”。树状结构是通过重复一系列反应来获得的,这可以在每个反应循环结束时获得新一代和数量递增的相同分支。几代之后,由于外围存在大量末端官能团,因此树枝状大分子通常呈现出高度支化和多官能团的球状。
5.因此,这些结构特征加强了它们在生物学和医学中的应用(cloninger m.j.curr.opin.chem.biol.2002年第6期,742-748页)。树枝状大分子可用作药物载体,能够提高其水溶性,增强药物透过生物屏障的输送能力,并确保药物的组织中的分配(lee c.c.等人nat.biotechnol.2005年第23期,1517-1526页;cheng y.等人front.biosci.2008年第13期,1447-1471页)。
6.具体地,在过去的几十年中,含磷树枝状大分子因其诸多特性而引起了研究人员越来越多的兴趣,特别是在生物学和纳米医学领域(caminade a.-m.等人,phosphorous dendrimers in biology and nanomedicine:syntheses,characterization,and properties,jenny stanford publishing,2018年第1版)
7.尤其是,具有氮杂双膦酸盐表面的含磷树枝状大分子(abp树枝状大分子)能够激活单核细胞并诱导抗炎反应(wo 2010/013086 a1;portevin d.等人,j.transl.med.2009年第7期,82页)。更具体地,抗炎特性已经在类风湿性多关节炎动物模型中得到了验证,其中已知单核细胞在炎症和破骨细胞生成中起着主要作用(hayder m.等人,sci.trans.med.2011年第3期,81ra35)。abp树枝状大分子的抗炎作用也已在葡萄膜炎(fruchon等人molecules,2013年第18期,9305-9316页)和多发性硬化(caminade a.-m.nat.commun.2015年第6期,7722页)的模型中得到了验证。
8.然而,这些聚磷腙型含磷树枝状大分子在其结构中具有腙型链,对生理ph值下的水解敏感。实际上,已知芳香腙对生物介质中的水解敏感,具体是血浆中的水解(kovarikova,p.等人,j.pharm.biomed.anal.,2008年第47期,360-370页)。还已经证明,树枝状大分子,例如具有聚磷腙骨架和酪胺衍生的氨基二亚甲基膦酸(单钠盐)末端的abp树
枝状大分子,在生理ph值和37℃的温度下,48小时后约降解10%(hayder m.等人,biomacromolecules,2018年第19期,712-720页)。
9.因此,需要在生理ph值下具有良好稳定性的新型含磷树枝状大分子。
技术实现要素:
10.本发明涉及一种n代树枝状大分子或其药学上可接受的盐,包括:
[0011]-化合价为m的核心
§
,其中m是大于或等于1的整数;
[0012]-围绕核心的树状代链,用结构式(cg)表示:
[0013]
[化学式1]
[0014][0015]
其中:
[0016]
a是o或s;
[0017]
b是可选地被c1-c6-烷基或卤素取代的芳基或杂芳基;
[0018]
d选自c1-c12-烷基、c1-c12-卤代烷基、芳基、杂芳基、(ch
2-ch
2-o)
a-ch3、ch2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nr’r”、ch
2-(ch
2-ch
2-o)
c-ch
2-ch
2-ch
2-nr’r”,其中a、b、c各自是1到12的整数,r’和r”各自选自h、c1-c12-烷基、c1-c12-卤代烷基,叔-丁基氧羰基、芴基甲氧羰基、甲氧羰基、叔-丁基羰基、对甲苯磺酰基、甲基磺酰基、三氟甲基磺酰基、烯丙基、苄基、三苯甲基,
[0019]
[化学式2]
[0020][0021]
并且
[0022]
[化学式3]
[0023][0024]
其中z1是单键或1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是杂原子,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是阳离子;
[0025]
e是o或s;
[0026]-用结构式(ci)表示的每代链端部的中间链:
[0027]
[化学式4]
[0028]-g-j-l-[0029]
ꢀꢀꢀ
(ci)
[0030]
其中:
[0031]
g是o或s;
[0032]
j是可选地被c1-c6-烷基或卤素取代的芳基或杂芳基;
[0033]
l是1至6个链节的直链或支链烃链,一个或多个链节可选地可以是杂原子;
[0034]-用结构式(t)表示的每个中间链端部的端基:
[0035]
[化学式5]
[0036][0037]
其中:
[0038]
v是ch或n;
[0039]
w1是h、c1-c12-烷基或
[0040]
[化学式3]
[0041][0042]
其中z1是单键或1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是杂原子,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是阳离子;
[0043]
w2是c1-c12-烷基或
[0044]
[化学式3]
[0045][0046]
其中z1是单键或1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是杂原子,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是阳离子;
[0047]
其中n是1到12的整数。
[0048]
根据另一方面,提出了根据本发明的树枝状大分子的制备方法,依次包括以下步骤:
[0049]
(a)制备以下结构式的中间体:
[0050]
[化学式29]
[0051][0052]
或其某种药学上可接受的盐,
[0053]
其中:
[0054]
§
、a、b、d定义如下:
[0055]
(b)使步骤(a)中获得的中间体与p(e)x3反应,其中e是o或s,x是卤素;
[0056]
(c)使步骤(b)中获得的产物与包含中间链和端基的片段反应。
[0057]
还提出了根据本发明的树枝状大分子的制备方法,依次包括以下步骤:
[0058]
(a)制备包含代链、中间链和端基的片段,结构式如下:
[0059]
[化学式33]
[0060][0061]
或其某种药学上可接受的盐,
[0062]
其中:
[0063]
a、b、d、e、g、j、l、v、w1和w2例如定义如下;
[0064]
(b)使步骤(a)中获得的片段与卤化核心
§
反应。
[0065]
根据另一方面,提出了一种药物组合物,其含有至少一种根据本发明的树枝状大分子以及药学上可接受的赋形剂。
[0066]
最后,本发明涉及根据本发明的树枝状大分子用于治疗炎性疾病。
[0067]
下面通过详细说明来阐述其他特征、详情及优点。
具体实施方式
[0068]
如上所述,本发明涉及一种n代树枝状大分子或其药学上可接受的盐,包括:
[0069]-化合价为m的核心
§
,其中m是大于或等于1的整数,具体地在1到12之间,更具体地在1到8之间,甚至更具体地在3到6之间,更具体地m是选自3、4、6的整数;
[0070]-围绕核心的树状代链,用结构式(cg)表示:
[0071]
[化学式1]
[0072][0073]
其中:
[0074]
a是o或s,具体地a是o;
[0075]
b是可选地被c1-c6-烷基或卤素取代的芳基或杂芳基,具体地,b是可选地被c1-c6-烷基或卤素取代的芳基,更具体地,b是可选地被c1-c6-烷基或卤素取代的苯基,甚至更具体地,b是可选地被c1-c4-烷基、氯或氟取代的苯基,甚至更具体地是苯基;
[0076]
d选自c1-c12-烷基、c1-c12-卤代烷基、芳基、杂芳基、(ch2–
ch2–
o)a–
ch3、ch2–
(ch2–
ch2–
o)a–
ch3、(ch2)b–
nr’r”、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nr’r”,其中a、b、c各自是1到12的整数,r’和r”各自选自h、c1-c12-烷基、c1-c12-卤代烷基、叔-丁基氧羰基、芴基甲氧羰基、甲氧羰基、叔-丁基羰基、对甲苯磺酰基、甲基磺酰基、三氟甲基磺酰基、烯丙基、苄基、三苯甲基,
[0077]
[化学式2]
[0078][0079]
并且
[0080]
[化学式3]
[0081]
其中z1是单键或1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是杂原子,并且r1和r2各自选自h、c1-c6-烷基和m+,其中m+是阳离子;具体地,d选自c1-c12-烷基、c1-c12-卤代烷基、(ch2–
ch2–
o)a–
ch3、ch2–
(ch2–
ch2–
o)a–
ch3、(ch2)b–
nr’r”、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nr’r”,其中a,b、c各自是1到12的整数,并且r’和r”各自选自h、c1-c12-烷基、c1-c12-卤代烷基、叔-丁基氧羰基,
[0082]
[化学式2]
[0083][0084]
并且
[0085]
[化学式3]
[0086][0087]
其中z1是单键或1至6个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c4-烷基、na
+
、k
+
;更具体地,d选自c1-c10-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nr’r”、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nr’r”,其中a、b、c各自是1到10的整数,并且r’和r”各自选自h,
[0088]
[化学式2]
[0089][0090]
并且
[0091]
[化学式3]
[0092][0093]
其中z1是1至4个链节的直链烃链,并且r1和r2各自选自h、c1-c2-烷基、na
+
;更具体地,d选自c1-c8-烷基、(ch2)
b-nhr’、ch
2-(ch
2-ch
2-o)
c-ch
2-ch
2-ch
2-nhr’,其中b和c各自是1到8的整数,r’是h或
[0094]
[化学式2]
[0095]
以及
[0096]
e是o或s,具体地e是o;
[0097]-用结构式(ci)表示的每代链端部的中间链:
[0098]
[化学式4]
[0099]-g-j-l-[0100]
ꢀꢀꢀ
(ci)
[0101]
其中:
[0102]
g是o或s,具体地g是o;
[0103]
j是可选地被c1-c6-烷基或卤素取代的芳基或杂芳基,具体地,j是可选地被c1-c6-烷基或卤素取代的芳基,更具体地j是可选地被c1-c6-烷基或卤素取代的苯基,甚至更具体地,j是可选地被c1-c4-烷基、氯或氟取代的苯基,甚至更具体地是苯基,
[0104]
l是1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是选自n、o、s的杂原子,具体地,l是1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是选自n、o的杂原子,更具体地,l是1至4个链节的直链或支链烃链,甚至更具体地,l是1至4个链节的直链烃链,甚至更具体地,l是1至2个链节的直链烃链,还是更具体地,l是ch2或ch
2-ch2;
[0105]-用结构式(t)表示的每个中间链端部的端基:
[0106]
[化学式5]
[0107][0108]
其中:
[0109]
v是ch或n,具体地v是n;
[0110]
w1是h、c1-c12-烷基或
[0111]
[化学式3]
[0112][0113]
其中z1是单键或1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是杂原子,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是阳离子;具体地w1是h、c1-c10-烷基或
[0114]
[化学式3]
[0115][0116]
其中z1是单键或1至6个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是元素周期表中ia、iia、iib或iiia族元素的阳离子或含氮碱基的阳离子;更具体地,w1是h、c1-c8-烷基或
[0117]
[化学式3]
[0118][0119]
其中z1是1至4个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c4-烷基、na
+
、k
+
;更具体地,w1是h、c1-c6-烷基或
[0120]
[化学式3]
[0121][0122]
其中z1是1至2个链节的直链烃链,并且r1和r2各自选自h、c1-c2-烷基和na
+
;
[0123]
w2是c1-c12-烷基或
[0124]
[化学式3]
[0125][0126]
其中z1是单键或1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是杂原子,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是阳离子;具体地w2是c1-c10-烷基或
[0127]
[化学式3]
[0128][0129]
其中z1是单键或1至6个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是元素周期表中ia、iia、iib或iiia族元素的阳离子或含氮碱基的阳离子;更
具体地,w2是h、c1-c8-烷基或
[0130]
[化学式3]
[0131][0132]
其中z1是1至4个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c4-烷基、na
+
、k
+
;更具体地,w2是c1-c6-烷基或
[0133]
[化学式3]
[0134][0135]
其中z1是1至2个链节的直链烃链,并且r1和r2各自选自h、c1-c2-烷基和na
+
;
[0136]
其中n是1到12的整数,具体地n是1到10的整数,更具体地n是1到8的整数,更具体地n是1到6的整数,甚至更具体地n是1到5的整数。
[0137]
因此,本发明的树枝状大分子或其药学上可接受的盐包含结构式(ci)的中间链,末端为处于结构式(cg)的每个代链的端部的结构式(t)的端基。
[0138]
本发明的树枝状大分子或其药学上可接受的盐因此包含m个与核心
§
连接的分支,这些分支中的每一个由一个或多个结构式(cg)的代链构成,在其端部包含结构式(ci)的中间链,中间链的末端为结构式(t)的端基。
[0139]
发明人的贡献在于证明了树枝状大分子中存在如上定义的结构式(cg)的代链,该代链可以提高树枝状大分子在生理ph值下的稳定性。
[0140]
在一种实施方式中,存在于本发明的树枝状大分子中的核心
§
选自戊糖、己糖和结构式如下的基团:
[0141]
[化学式6]
[0142][0143]
[化学式7]
[0144][0145]
[化学式8]
[0146][0147]
[化学式9]
[0148]
以及
[0149]
[化学式10]
[0150][0151]
具体地,存在于本发明的树枝状大分子中的核心
§
选自结构式如下的基团:
[0152]
[化学式6]
[0153][0154]
[化学式7]
[0155]
以及
[0156]
[化学式8]
[0157][0158]
更具体地,存在于本发明的树枝状大分子中的核心
§
是结构式如下的基团:
[0159]
[化学式7]
[0160][0161]
在一种实施方式中,本发明的树枝状大分子的特征在于,m是1到8的整数。具体地,本发明的树枝状大分子的特征在于,m是选自3、4、6的整数。更具体地,本发明的树枝状大分子的特征在于,m等于6。
[0162]
在一种实施方式中,本发明的树枝状大分子的特征在于,n是1到5的整数。
[0163]
在一种实施方式中,本发明的树枝状大分子的特征在于,在结构式(cg)中,a是o。
[0164]
在一种实施方式中,本发明的树枝状大分子的特征在于,在结构式(cg)中,b是可选地被c1-c6-烷基或卤素取代的苯基,具体地,b是可选地被c1-c4-烷基、氯或氟取代的苯基,甚至更具体地,b是苯基。
[0165]
在一种实施方式中,本发明的树枝状大分子的特征在于,在结构式(cg)中,e是s。
[0166]
在一种实施方式中,本发明的树枝状大分子的特征在于,在结构式(ci)中,g是o。
[0167]
在一种实施方式中,本发明的树枝状大分子的特征在于,在结构式(ci)中,j是可选地被c1-c6-烷基或卤素取代的苯基,具体地,j是可选地被c1-c4-烷基、氯或氟取代的苯基,甚至更具体地,j是苯基。
[0168]
在一种实施方式中,本发明的树枝状大分子的特征在于,在结构式(ci)中,l是(ch2)d,其中d是1到6的整数,d是1到4的整数,更具体地,d是1到2的整数。
[0169]
在一种实施方式中,本发明的树枝状大分子的特征在于,在结构式(t)中,v是n。
[0170]
在一种实施方式中,本发明的树枝状大分子的特征在于,在结构式(t)中,w1是h以及w2是c1-c12-烷基。
[0171]
在一种实施方式中,本发明的树枝状大分子的特征在于,在结构式(t)中,w1和w2是
[0172]
[化学式3]
[0173][0174]
其中z1是单键或1至6个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是元素周期表中ia、iia、iib或iiia族元素的阳离子或含氮碱基的阳离子。具体地,m选自钠、钾、钙、钡、锌、镁、锂和铝原子。更具体地,m
+
选自na
+
、k
+
、li
+
。甚至更具体地,m
+
是na
+
或k
+
。
[0175]
在一种实施方式中,本发明的树枝状大分子的特征在于,在结构式(t)中,w1和w2是
[0176]
[化学式3]
[0177][0178]
其中z1是ch2,并且r1和r2各自选自h、甲基和na
+
。
[0179]
换言之,本发明涉及一种树枝状大分子,结构式为(i);
[0180]
[化学式11]
[0181][0182]
或其药学上可接受的盐,
[0183]
其中:
[0184]
a是o或s,具体地a是o;
[0185]
b是可选地被c1-c6-烷基或卤素取代的芳基或杂芳基,具体地,b是可选地被c1-c6-烷基或卤素取代的芳基,更具体地,b是可选地被c1-c6-烷基或卤素取代的苯基,甚至更具体地,b是可选地被c1-c4-烷基、氯或氟取代的苯基,甚至更具体地是苯基;
[0186]
d选自c1-c12-烷基、c1-c12-卤代烷基、芳基、杂芳基、(ch2–
ch2–
o)a–
ch3、ch2–
(ch2–
ch2–
o)a–
ch3、(ch2)b–
nr’r”、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nr’r”,其中a、b、c各自是1到12的整数,r’和r”各自选自h、c1-c12-烷基、c1-c12-卤代烷基、叔-丁基氧羰基、芴基甲氧羰基、甲氧羰基、叔-丁基羰基、对甲苯磺酰基、甲基磺酰基、三氟甲基磺酰基、烯丙基、苄基、三苯甲基,
[0187]
[化学式2]
[0188][0189]
并且
[0190]
[化学式3]
[0191][0192]
其中z1是单键或1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是杂原子,并且r1和r2各自选自h、c1-c6-烷基和m+,其中m+是阳离子;具体地,d选自c1-c12-烷基、c1-c12-卤代烷基、(ch2–
ch2–
o)a–
ch3、ch2–
(ch2–
ch2–
o)a–
ch3、(ch2)b–
nr’r”、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nr’r”,其中a,b、c各自是1到12的整数,并且r’和r”各自选自h、c1-c12-烷基、c1-c12-卤代烷基、叔-丁基氧羰基,
[0193]
[化学式2]
[0194][0195]
并且
[0196]
[化学式3]
[0197][0198]
其中z1是单键或1至6个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c4-烷基、na
+
、k
+
;更具体地,d选自c1-c10-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nr’r”、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nr’r”,其中a、b、c各自是1到10的整数,并且r’和r”各自选自h,
[0199]
[化学式2]
[0200][0201]
并且
[0202]
[化学式3]
[0203][0204]
其中z1是1至4个链节的直链烃链,并且r1和r2各自选自h、c1-c2-烷基、na
+
;更具体地,d选自c1-c8-烷基、(ch2)
b-nhr’、ch
2-(ch
2-ch
2-o)
c-ch
2-ch
2-ch
2-nhr’,其中b和c各自是1到8的整数,r’是h或
[0205]
[化学式2]
[0206][0207]
e是o或s,具体地e是o;
[0208]
g是o或s,具体地g是o;
[0209]
j是可选地被c1-c6-烷基或卤素取代的芳基或杂芳基,具体地,j是可选地被c1-c6-烷基或卤素取代的芳基,更具体地j是可选地被c1-c6-烷基或卤素取代的苯基,甚至更具体地,j是可选地被c1-c4-烷基、氯或氟取代的苯基,甚至更具体地是苯基,
[0210]
l是1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是选自n、o、s
的杂原子,具体地,l是1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是选自n、o的杂原子,更具体地,l是1至4个链节的直链或支链烃链,甚至更具体地,l是1至4个链节的直链烃链,甚至更具体地,l是1至2个链节的直链烃链,还是更具体地,l是ch2或ch
2-ch2;
[0211]
v是ch或n,具体地v是n;
[0212]
w1是h、c1-c12-烷基或
[0213]
[化学式3]
[0214][0215]
其中z1是单键或1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是杂原子,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是阳离子;具体地w1是h、c1-c10-烷基或
[0216]
[化学式3]
[0217][0218]
其中z1是单键或1至6个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是元素周期表中ia、iia、iib或iiia族元素的阳离子或含氮碱基的阳离子;更具体地,w1是h、c1-c8-烷基或
[0219]
[化学式3]
[0220][0221]
其中z1是1至4个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c4-烷基、na
+
、k
+
;更具体地,w1是h、c1-c6-烷基或
[0222]
[化学式3]
[0223][0224]
其中z1是1至2个链节的直链烃链,并且r1和r2各自选自h、c1-c2-烷基和na
+
;
[0225]
w2是c1-c12-烷基或
[0226]
[化学式3]
[0227][0228]
其中z1是单键或1至6个链节的直链或支链烃链,其中一个或多个链节可选地可以是杂原子,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是阳离子;具体地w2是c1-c10-烷
基或
[0229]
[化学式3]
[0230][0231]
其中z1是单键或1至6个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是元素周期表中ia、iia、iib或iiia族元素的阳离子或含氮碱基的阳离子;更具体地,w2是h、c1-c8-烷基或
[0232]
[化学式3]
[0233][0234]
其中z1是1至4个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c4-烷基、na
+
、k
+
;更具体地,w2是c1-c6-烷基或
[0235]
[化学式3]
[0236][0237]
其中z1是1至2个链节的直链烃链,并且r1和r2各自选自h、c1-c2-烷基和na
+
;
[0238]
m是1到8的整数,具体地m是选自3、4、6的正整数,更具体地m等于6;
[0239]
n是1到12的整数,具体地n是1到10的整数,更具体地n是1到8的整数,更具体地n是1到6的整数,甚至更具体地n是1到5的整数。
[0240]
§
选自戊糖、己糖和结构式如下的基团:
[0241]
[化学式6]
[0242][0243]
[化学式7]
[0244][0245]
[化学式8]
[0246][0247]
[化学式9]
[0248]
以及
[0249]
[化学式10]
[0250][0251]
具体地,
§
选自结构式如下的基团:
[0252]
[化学式6]
[0253][0254]
[化学式7]
[0255]
以及
[0256]
[化学式8]
[0257][0258]
更具体地,
§
是结构式如下的基团:
[0259]
[化学式7]
[0260][0261]
根据第一改型,本发明的树枝状大分子的特征在于,在结构式(t)中,v是n,w1是h。
[0262]
在这种情况下,本发明的树枝状大分子可以用如下结构式(ii)来表示:
[0263]
[化学式12]
[0264][0265]
或其药学上可接受的盐,
[0266]
其中:
[0267]
§
、a、b、d、e、g、j、l、w2、m和n例如定义如上或者如结构式(i),并且
[0268]
{}n是指所述树枝状大分子的第n代链的树状结构。
[0269]
结构式(ii)的优选树枝状大分子是其中
§
、a、b、d、e、g、j、l、w2、m和n定义如下的树枝状大分子:
[0270]
§
选自结构式如下的基团:
[0271]
[化学式6]
[0272][0273]
[化学式7]
[0274]
以及
[0275]
[化学式8]
[0276][0277]
具体地,
§
是结构式如下的基团:
[0278]
[化学式7]
[0279][0280]
a是o或s,具体地a是o;
[0281]
b是可选地被c1-c6-烷基或卤素取代的芳基或杂芳基,具体地,b是可选地被c1-c6-烷基或卤素取代的芳基,更具体地,b是可选地被c1-c6-烷基或卤素取代的苯基,甚至更具体地,b是可选地被c1-c4-烷基、氯或氟取代的苯基,甚至更具体地,b是苯基;
[0282]
d选自c1-c12-烷基、c1-c12-卤代烷基、(ch
2-ch
2-o)
a-ch3、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nr’r”、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nr’r”,其中a、b、c各自是1到12的整数,r’和r”各自选自h、c1-c12-烷基、c1-c12-卤代烷基、叔-丁基氧羰基,
[0283]
[化学式2]
[0284][0285]
并且
[0286]
[化学式3]
[0287][0288]
其中z1是单键或1至6个链节的直链或支链烃链,并且r1和r2各自选自h、c1-c4-烷基、na
+
和k
+
;具体地,d选自c1-c10-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’r”,其中a、b、c各自是1到10的整数,并且r’是h或
[0289]
[化学式2]
[0290][0291]
更具体地,d选自c1-c8-烷基、ch
2-(ch
2-ch
2-o)
a-ch3,其中a是1到8的整数,甚至更具体地,d是c1-c8-烷基,还是更具体地,d选自甲基、己基和辛基;非常具体地,d是甲基;
[0292]
e是o或s,具体地e是s;
[0293]
g是o或s,具体地g是o;
[0294]
j是可选地被c1-c6-烷基或卤素取代的芳基或杂芳基,具体地,j是可选地被c1-c6-烷基或卤素取代的芳基,更具体地j是可选地被c1-c6-烷基或卤素取代的苯基,甚至更具体地,j是可选地被c1-c4-烷基、氯或氟取代的苯基,甚至更具体地是苯基,
[0295]
l是1至6个链节的直链或支链烃链,其中每个链节可选地可以是杂原子,具体地,l是1至6个链节的直链或支链烃链,更具体地,l是1至4个链节的直链或支链烃链,甚至更具体地,l是1至4个链节的直链烃链,甚至更具体地,l是1至2个链节的直链烃链,还是更具体地,l是ch2;
[0296]
w2是c1-c12-烷基,具体地,w2是c1-c10-烷基,更具体地,w2是c1-c8-烷基,更具体地,w2是c1-c4-烷基,还是更具体地,w2是甲基;
[0297]
m是大于或等于1的整数,具体地m是1到12的整数,更具体地m是1到8的整数,更具体地m是3到6的整数,甚至更具体地m是选自3、4、6的整数。
[0298]
n是1到12的整数,具体地n是1到10的整数,更具体地n是1到8的整数,更具体地n是1到6的整数,甚至更具体地n是1到5的整数。
[0299]
根据一种具体的实施方式,本发明的树枝状大分子的特征在于,n等于1。在这种情况下,本发明的树枝状大分子是结构式(ii1)的树枝状大分子:
[0300]
[化学式13]
[0301][0302]
或其药学上可接受的盐,
[0303]
其中:
[0304]
§
、a、b、d、e、g、j、l、w2、m例如被定义为如结构式(ii)所示。
[0305]
根据一种具体的实施方式,本发明的树枝状大分子的特征在于,n等于2。在这种情况下,本发明的树枝状大分子是结构式(ii2)的树枝状大分子:
[0306]
[化学式14]
[0307][0308]
或其药学上可接受的盐,
[0309]
其中:
[0310]
§
、a、b、d、e、g、j、l、w2、m例如被定义为如结构式(ii)所示。
[0311]
根据一种具体的实施方式,本发明的树枝状大分子的特征在于,n等于3。在这种情况下,本发明的树枝状大分子是结构式(ii3)的树枝状大分子:
[0312]
[化学式15]
[0313][0314]
或其药学上可接受的盐,
[0315]
其中:
[0316]
§
、a、b、d、e、g、j、l、w2、m例如被定义为如结构式(ii)所示。
[0317]
根据一种具体的实施方式,本发明的树枝状大分子的特征在于,n等于4。在这种情况下,本发明的树枝状大分子是结构式(ii4)的树枝状大分子:
[0318]
[化学式16]
[0319][0320]
或其药学上可接受的盐,
[0321]
其中:
[0322]
§
、a、b、d、e、g、j、l、w2、m例如被定义为如结构式(ii)所示。
[0323]
根据一种具体的实施方式,本发明的树枝状大分子的特征在于,n等于5。在这种情况下,本发明的树枝状大分子是结构式(ii5)的树枝状大分子:
[0324]
[化学式17]
[0325][0326]
或其药学上可接受的盐,
[0327]
其中:
[0328]
§
、a、b、d、e、g、j、l、w2和m例如被定义为如结构式(ii)所示。
[0329]
结构式(ii)的优选树枝状大分子是结构式(iia)的树枝状大分子:
[0330]
[化学式18]
[0331][0332]
或其药学上可接受的盐,
[0333]
其中:
[0334]
a、b、d、e、g、j、l、w2、m例如是根据结构式(ii)定义的,
[0335]
{}n是指所述树枝状大分子的第n代链的树状结构,并且
[0336]
[p=n]3是指以下结构式的核心:
[0337]
[化学式7]
[0338][0339]
结构式(iia)的优选树枝状大分子是其中a、b、d、e、g、j、l、w2和n定义如下的树枝状大分子:
[0340]
a是o或s,具体地a是o;
[0341]
b是可选地被c1-c6-烷基或卤素取代的苯基,具体地,b是苯基;
[0342]
d是c1-c12-烷基,具体地,d是c1-c10-烷基,更具体地,d是c1-c8-烷基,甚至更具体地,d选自甲基、己基和辛基,还是更具体地,d是甲基;
[0343]
e是o或s,具体地e是s;
[0344]
g是o或s,具体地g是o;
[0345]
j是可选地被c1-c6-烷基或卤素取代的苯基,具体地,j是苯基;
[0346]
l是1至4个链节的直链或支链烃链,具体地,l是1至4个链节的直链烃链,更具体地,l是1至2个链节的直链烃链,还是更具体地,l是ch2;
[0347]
w2是c1-c8-烷基,更具体地,w2是c1-c4-烷基,还是更具体地,w2是甲基;
[0348]
n是1到6的整数,具体地,n是1到5的整数。
[0349]
结构式(ii)的其他优选树枝状大分子是结构式(iib)的树枝状大分子:
[0350]
[化学式19]
[0351][0352]
或其药学上可接受的盐,
[0353]
其中:
[0354]
b、d、j、l、w2、n例如是根据结构式(ii)定义的,
[0355]
{}n是指所述树枝状大分子的第n代链的树状结构,并且
[0356]
[p=n]3是指以下结构式的核心:
[0357]
[化学式7]
[0358][0359]
结构式(iib)的优选树枝状大分子是其中b、d、j、l、w2和n定义如下的树枝状大分子:
[0360]
b是可选地被c1-c6-烷基或卤素取代的苯基,具体地,b是苯基;
[0361]
d是c1-c12-烷基,具体地,d是c1-c10-烷基,更具体地,d是c1-c8-烷基,甚至更具体地,d选自甲基、己基和辛基,还是更具体地,d是甲基;
[0362]
j是可选地被c1-c6-烷基或卤素取代的苯基,具体地,j是苯基;
[0363]
l是1至4个链节的直链或支链烃链,具体地,l是1至4个链节的直链烃链,更具体地,l是1至2个链节的直链烃链,还是更具体地,l是ch2;
[0364]
w2是c1-c8-烷基,更具体地,w2是c1-c4-烷基,还是更具体地,w2是甲基;
[0365]
n是1到6的整数,具体地,n是1到5的整数。
[0366]
结构式(ii)的其他优选树枝状大分子是结构式(iic)的树枝状大分子:
[0367]
[化学式20]
[0368][0369]
或其药学上可接受的盐,
[0370]
其中:
[0371]
d、w2、n例如是根据结构式(ii)定义的,
[0372]
{}n是指所述树枝状大分子的第n代链的树状结构,并且
[0373]
[p=n]3是指以下结构式的核心:
[0374]
[化学式7]
[0375][0376]
结构式(iic)的优选树枝状大分子是其中d、w2、n定义如下的树枝状大分子:
[0377]
d是c1-c12-烷基,具体地,d是c1-c10-烷基,更具体地,d是c1-c8-烷基,甚至更具体地,d选自甲基、己基和辛基,还是更具体地,d是甲基;
[0378]
w2是c1-c8-烷基,更具体地,w2是c1-c4-烷基,还是更具体地,w2是甲基;
[0379]
n是1到6的整数,具体地,n是1到5的整数。
[0380]
根据第二改型,本发明的树枝状大分子的特征在于,在结构式(t)中,w1和w2是
[0381]
[化学式3]
[0382][0383]
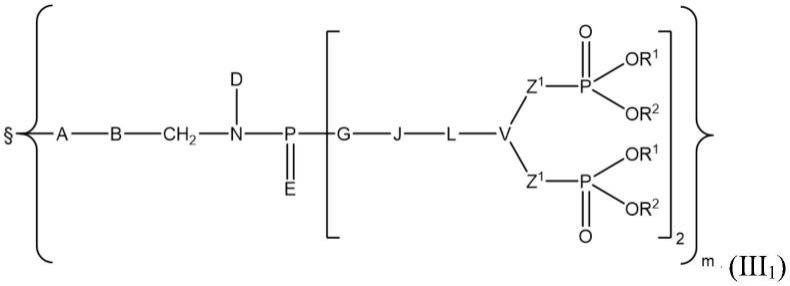
在这种情况下,本发明的树枝状大分子可以用如下结构式(iii)来表示:
[0384]
[化学式21]
[0385][0386]
或其药学上可接受的盐,
[0387]
其中:
[0388]
§
、a、b、d、e、g、j、l、v、z1、r1、r2、m和n例如定义如上或者如结构式(i)所示,并且
[0389]
{}n是指所述树枝状大分子的第n代链的树状结构。
[0390]
结构式(iii)的优选树枝状大分子是其中
§
、a、b、d、e、g、j、l、v、z1、r1、r2、m和n定义如下的树枝状大分子:
[0391]
§
选自结构式如下的基团:
[0392]
[化学式6]
[0393][0394]
[化学式7]
[0395]
以及
[0396]
[化学式8]
[0397][0398]
具体地,
§
是结构式如下的基团:
[0399]
[化学式7]
[0400][0401]
a是o或s,具体地a是o;
[0402]
b是可选地被c1-c6-烷基或卤素取代的芳基或杂芳基,具体地,b是可选地被c1-c6-烷基或卤素取代的芳基,更具体地,b是可选地被c1-c6-烷基或卤素取代的苯基,甚至更具体地,b是可选地被c1-c4-烷基、氯或氟取代的苯基,甚至更具体地,b是苯基;
[0403]
d选自c1-c12-烷基、(ch
2-ch
2-o)
a-ch3、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中a、b、c各自是1到12的整数,r’是h或
[0404]
[化学式2]
c6-烷基或卤素取代的芳基,更具体地j是可选地被c1-c6-烷基或卤素取代的苯基,甚至更具体地,j是可选地被c1-c4-烷基、氯或氟取代的苯基,甚至更具体地是苯基,
[0421]
l是1至6个链节的直链或支链烃链,其中每个链节可选地可以是杂原子,具体地,l是1至6个链节的直链或支链烃链,更具体地,l是1至4个链节的直链或支链烃链,甚至更具体地,l是1至4个链节的直链烃链,甚至更具体地,l是1至2个链节的直链烃链,还是更具体地,l是ch
2-ch2;
[0422]
v是ch或n,具体地v是n;
[0423]
z1是单键或1至6个链节的直链或支链烃链,其中每个链节可选地可以是杂原子,具体地,z1是单键或1至6个链节的直链或支链烃链,更具体地,z1是单键或1至4个链节的直链或支链烃链,甚至更具体地,z1是1至4个链节的直链烃链,甚至更具体地,z1是1至2个链节的直链烃链;
[0424]
r1和r2各自选自h、c1-c6-烷基和m
+
,其中m
+
是阳离子,具体地,r1和r2各自选自h、c1-c4-烷基和m
+
,其中m
+
是元素周期表中ia、iia、iib或iiia族元素的阳离子或含氮碱基的阳离子,更具体地,r1和r2各自选自h、c1-c4-烷基、na
+
和k
+
;
[0425]
m是大于或等于1的整数,具体地m是1到12的整数,更具体地m是1到8的整数,更具体地m是3到6的整数,甚至更具体地m是选自3、4、6的整数。
[0426]
n是1到12的整数,具体地n是1到10的整数,更具体地n是1到8的整数,更具体地n是1到6的整数,甚至更具体地n是1到5的整数。
[0427]
根据一种具体的实施方式,本发明的树枝状大分子的特征在于,n等于1。在这种情况下,本发明的树枝状大分子是结构式(iii1)的树枝状大分子:
[0428]
[化学式22]
[0429][0430]
或其药学上可接受的盐,
[0431]
其中:
[0432]
§
、a、b、d、e、g、j、l、v、z1、r1、r2、m例如被定义为如结构式(iii)所示。
[0433]
根据一种具体的实施方式,本发明的树枝状大分子的特征在于,n等于2。在这种情况下,本发明的树枝状大分子是结构式(iii2)的树枝状大分子:
[0434]
[化学式23]
[0435][0436]
或其药学上可接受的盐,
[0437]
其中:
[0438]
§
、a、b、d、e、g、j、l、v、z1、r1、r2、m例如被定义为如结构式(iii)所示。
[0439]
根据一种具体的实施方式,本发明的树枝状大分子的特征在于,n等于3。在这种情况下,本发明的树枝状大分子是结构式(iii3)的树枝状大分子:
[0440]
[化学式24]
[0441][0442]
或其药学上可接受的盐,
[0443]
其中:
[0444]
§
、a、b、d、e、g、j、l、v、z1、r1、r2、m例如被定义为如结构式(iii)所示。
[0445]
根据一种具体的实施方式,本发明的树枝状大分子的特征在于,n等于4。
[0446]
根据一种具体的实施方式,本发明的树枝状大分子的特征在于,n等于5。
[0447]
根据一种具体的实施方式,本发明的树枝状大分子是双官能的。在这种情况下,树枝状大分子的代链上包含一个官能团,端基上包含一个或多个官能团。
[0448]
双官能树枝状大分子是结构式(iii)的树枝状大分子,其中d定义如下:
[0449]
d是(ch2)
b-nhr’或ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中b和c各自是1到12的整数,r’是
[0450]
[化学式2]
[0451][0452]
具体地,d是(ch2)
b-nhr’或ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中b和c各自是1到10的整数,r’是
[0453]
[化学式2]
[0454][0455]
具体地,d是(ch2)
b-nhr’或ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中b和c各自是1到8的整数,r’是
[0456]
[化学式2]
[0457][0458]
结构式(iii)的优选树枝状大分子是结构式(iiia)的树枝状大分子:
[0459]
[化学式25]
[0460][0461]
或其药学上可接受的盐,
[0462]
其中:
[0463]
a、b、d、e、g、j、l、v、z1、r1、r2、n例如是根据结构式(iii)定义的,
[0464]
{}n是指所述树枝状大分子的第n代链的树状结构,并且
[0465]
[p=n]3是指以下结构式的核心:
[0466]
[化学式7]
[0467][0468]
结构式(iiia)的优选树枝状大分子是其中a、b、d、e、g、j、l、v、z1、r1、r2、n定义如下的树枝状大分子:
[0469]
a是o或s,具体地a是o;
[0470]
b是可选地被c1-c6-烷基或卤素取代的苯基,具体地,b是苯基;
[0471]
d选自c1-c12-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中a、b、c各自是1到12的整数,r’是h或
[0472]
[化学式2]
[0473][0474]
具体地d选自c1-c10-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中a、b、c各自是1到10的整数,r’是h或
[0475]
[化学式2]
[0476][0477]
更具体地,d选自c1-c8-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch
2-(ch
2-ch
2-o)
c-ch
2-ch
2-ch
2-nhr’,其中a、b、c各自是1到8的整数,r’是h或
[0478]
[化学式2]
[0479][0480]
甚至更具体地,d选自c1-c8-烷基、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中b和c各自是1到6的整数,r’是h或
[0481]
[化学式2]
[0482][0483]
还是更具体地,d选自甲基、己基和辛基、(ch2)
2-nhr’、ch
2-(ch
2-ch
2-o)
3-ch
2-ch
2-ch
2-nhr’,其中r’是
[0484]
[化学式2]
[0485][0486]
e是o或s,具体地e是s;
[0487]
g是o或s,具体地g是o;
[0488]
j是可选地被c1-c6-烷基或卤素取代的苯基,具体地,j是苯基;
[0489]
l是1至4个链节的直链或支链烃链,具体地,l是1至4个链节的直链烃链,更具体地,l是1至2个链节的直链烃链,还是更具体地,l是ch
2-ch2;
[0490]
v是ch或n,具体地v是n;
[0491]
z1是1至4个链节的直链烃链,具体地,z1是1至2个链节的直链烃链;
[0492]
r1、r2、r3和r4各自选自h、c1-c6-烷基、na
+
、k
+
,具体地,r1和r2各自选自h、c1-c4-烷基、na
+
,更具体地,r1和r2各自选自h、c1-c2-烷基、na
+
,更具体地,r1和r2各自选自h、甲基或na
+
;
[0493]
n是1到6的整数,具体地,n是1到5的整数。
[0494]
结构式(iii)的其他优选树枝状大分子是结构式(iiib)的树枝状大分子:
[0495]
[化学式26]
[0496][0497]
或其药学上可接受的盐,
[0498]
其中:
[0499]
b、d、e、j、l、v、z1、r1、r2、n例如是根据结构式(iii)定义的,
[0500]
{}n是指所述树枝状大分子的第n代链的树状结构,并且
[0501]
[p=n]3是指以下结构式的核心:
[0502]
[化学式7]
[0503][0504]
结构式(iiib)的优选树枝状大分子是其中b、d、e、j、l、v、z、r1、r2、n定义如下的树枝状大分子:
[0505]
b是可选地被c1-c6-烷基或卤素取代的苯基,具体地,b是苯基;
[0506]
d选自c1-c12-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中a、b、c各自是1到12的整数,r’是h或
[0507]
[化学式2]
[0508][0509]
具体地d选自c1-c10-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中a、b、c各自是1到10的整数,r’是h或
[0510]
[化学式2]
[0511][0512]
更具体地,d选自c1-c8-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch
2-(ch
2-ch
2-o)
c-ch
2-ch
2-ch
2-nhr’,其中a、b、c各自是1到8的整数,r’是h或
[0513]
[化学式2]
[0514][0515]
甚至更具体地,d选自c1-c8-烷基、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中b和c各自是1到6的整数,r’是h或
[0516]
[化学式2]
[0517][0518]
还是更具体地,d选自甲基、己基和辛基、(ch2)
2-nhr’、ch
2-(ch
2-ch
2-o)
3-ch
2-ch
2-ch
2-nhr’,其中r’是
[0519]
[化学式2]
[0520][0521]
e是o或s,具体地e是s;
[0522]
j是可选地被c1-c6-烷基或卤素取代的苯基,具体地,j是苯基;
[0523]
l是1至4个链节的直链或支链烃链,具体地,l是1至4个链节的直链烃链,更具体
地,l是1至2个链节的直链烃链,还是更具体地,l是ch
2-ch2;
[0524]
v是ch或n,具体地v是n;
[0525]
z1是1至4个链节的直链烃链,具体地,z1是1至2个链节的直链烃链;
[0526]
r1和r2各自选自h、c1-c6-烷基、na
+
、k
+
,具体地,r1和r2各自选自h、c1-c4-烷基、na
+
,更具体地,r1和r2各自选自h、c1-c2-烷基、na
+
,更具体地,r1和r2各自选自h、甲基或na
+
;
[0527]
n是1到6的整数,具体地,n是1到5的整数。
[0528]
结构式(iii)的其他优选树枝状大分子是结构式(iiic)的树枝状大分子:
[0529]
[化学式27]
[0530][0531]
或其药学上可接受的盐,
[0532]
其中:
[0533]
b、d、e、j、l、r1、r2、n例如是如下定义的或是根据结构式(iii)定义的,
[0534]
{}n是指所述树枝状大分子的第n代链的树状结构,并且
[0535]
[p=n]3是指以下结构式的核心:
[0536]
[化学式7]
[0537][0538]
结构式(iiic)的优选树枝状大分子是其中b、d、e、j、l、r1、r2、n定义如下的树枝状大分子:
[0539]
b是可选地被c1-c6-烷基或卤素取代的苯基,具体地,b是苯基;
[0540]
d选自c1-c12-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中a、b、c各自是1到12的整数,r’是h或
[0541]
[化学式2]
[0542][0543]
具体地d选自c1-c10-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中a、b、c各自是1到10的整数,r’是h或
[0544]
[化学式2]
[0545][0546]
更具体地,d选自c1-c8-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中a、b、c各自是1到8的整数,r’是h或
[0547]
[化学式2]
[0548][0549]
甚至更具体地,d选自c1-c8-烷基、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中b和c各自是1到6的整数,r’是h或
[0550]
[化学式2]
[0551][0552]
还是更具体地,d选自甲基、己基和辛基、(ch2)
2-nhr’、ch
2-(ch
2-ch
2-o)
3-ch
2-ch
2-ch
2-nhr’,其中r’是
[0553]
[化学式2]
[0554][0555]
e是o或s,具体地e是s;
[0556]
j是可选地被c1-c6-烷基或卤素取代的苯基,具体地,j是苯基;
[0557]
l是1至4个链节的直链或支链烃链,具体地,l是1至4个链节的直链烃链,更具体地,l是1至2个链节的直链烃链,还是更具体地,l是ch
2-ch2;
[0558]
r1和r2各自选自h、c1-c6-烷基、na
+
、k
+
,具体地,r1和r2各自选自h、c1-c4-烷基、na
+
,更具体地,r1和r2各自选自h、c1-c2-烷基、na
+
,更具体地,r1和r2各自选自h、甲基或na
+
;
[0559]
n是1到6的整数,具体地,n是1到5的整数。
[0560]
结构式(iii)的其他优选树枝状大分子是结构式(iiid)的树枝状大分子:
[0561]
[化学式28]
[0562][0563]
或其药学上可接受的盐,
[0564]
其中:
[0565]
d、r1、r2、n例如是如下定义的或是根据结构式(iii)定义的,
[0566]
{}n是指所述树枝状大分子的第n代链的树状结构,并且
[0567]
[p=n]3是指以下结构式的核心:
[0568]
[化学式7]
[0569][0570]
结构式(iiid)的优选树枝状大分子是其中d、e、r1、r2、n定义如下的树枝状大分子:
[0571]
d选自c1-c12-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中a、b、c各自是1到12的整数,r’是h或
[0572]
[化学式2]
[0573][0574]
具体地d选自c1-c10-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中、b、c各自是1到10的整数,r’是h或
[0575]
[化学式2]
[0576][0577]
更具体地,d选自c1-c8-烷基、ch
2-(ch
2-ch
2-o)
a-ch3、(ch2)
b-nhr’、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nhr’,其中a、b、c各自是1到8的整数,r’是h或
[0578]
[化学式2]
[0579][0580]
甚至更具体地,d选自c1-c8-烷基、(ch2)b-nhr’、ch2
–
(ch2
–
ch2
–
o)c
–
ch2
–
ch2
–
ch2
–
nhr’,其中b和c各自是1到6的整数,r’是h或
[0581]
[化学式2]
[0582][0583]
还是更具体地,d选自甲基、己基和辛基、(ch2)
2-nhr’、ch
2-(ch
2-ch
2-o)
3-ch
2-ch
2-ch
2-nhr’,其中r’是
[0584]
[化学式2]
[0585][0586]
r1和r2各自选自h、c1-c6-烷基、na
+
、k
+
,具体地,r1和r2各自选自h、c1-c4-烷基、na
+
,更具体地,r1和r2各自选自h、c1-c2-烷基、na
+
,更具体地,r1和r2各自选自h、甲基或na
+
;
[0587]
n是1到6的整数,具体地,n是1到5的整数。
[0588]
根据一种具体的实施方式,本发明的树枝状大分子的代链是相同的。
[0589]
根据另一种具体的实施方式,本发明的树枝状大分子的代链是不同的。具体地,本发明的树枝状大分子的代链因每一代的胺基团的性质而不同。换言之,在结构式(cg)中,d在树枝状大分子的每一代中都是不同的。因此将其称为“层块”型树枝状大分子。
[0590]
根据该具体实施方式,“层块”型树枝状大分子可以用如下结构式(iv)表示:
[0591]
[化学式29]
[0592][0593]
或其药学上可接受的盐,
[0594]
其中:
[0595]
§
、a、b、e、g、j、l、v、w1、w2、m例如定义如上或者如结构式(i)所示,并且
[0596]
d’和d”各自选自c1-c12-烷基、c1-c12-卤代烷基、芳基、杂芳基、(ch2–
ch2–
o)a–
ch3、ch2–
(ch2–
ch2–
o)a–
ch3,(ch2)b–
nr’r”、ch2–
(ch2–
ch2–
o)c–
ch2–
ch2–
ch2–
nr’r”,其中a、b、c各自是1到12的整数,r’和r”各自选自h、c1-c12-烷基、c1-c12-卤代烷基、叔-丁基氧羰基、芴基甲氧羰基、甲氧羰基、叔-丁基羰基、对甲苯磺酰基、甲基磺酰基、三氟甲基磺酰基、烯丙基、苄基、三苯甲基,
[0597]
[化学式2]
[0598][0599]
并且
[0600]
[化学式3]
[0601][0602]
其中z1是单键或1至6个链节的直链或支链烃链,一个或多个链节可选地可以是杂原子,r1和r2各自选自h、c1-c6-烷基和m+,其中m+是阳离子;具体地,d’和d”各自选自c1-c12-烷基、c1-c12-卤代烷基、芳基、杂芳基、(ch2–
ch2–
o)a–
ch3、ch2–
(ch2–
ch2–
o)a–
ch3,其中a是1到12的整数;更具体地,d’和d”各自选自c1-c12-烷基、c1-c12-卤代烷基、(ch2–
ch2–
o)a–
ch3、ch2–
(ch2–
ch2–
o)a–
ch3,其中a是1到12的整数;更具体地,d’和d”各自选自c1-c12-烷基、(ch2–
ch2–
o)a–
ch3,其中a是1到12的整数;更具体地,d’和d”各自选自c1-c12-烷基、(ch2–
ch2–
o)a–
ch3,其中a是1到6的整数;更具体地,d’和d”各自选自c1-c12-烷基、(ch2–
ch2–
o)a–
ch3,其中a是1到4的整数;更具体地,d’和d”各自选自c1-c12-烷基、(ch2–
ch2–
o)a–
ch3,其中a是1到3的整数;更具体地,d’是c1-c12-烷基,而d”是c1-c12-烷基或(ch2–
ch2–
o)a–
ch3,其中a是1到3的整数;更具体地,d’是甲基,而d”是辛基或(ch2–
ch2–
o)a–
ch3。
[0603]
本发明的特别优选的化合物是下表1中列出的那些:
[0604]
[表1]
[0605]
[0606]
[0607]
[0608]
[0609][0610]
有利地,与现有技术的多磷腙类型的含磷树枝状大分子相比,根据本发明的树枝状大分子在生理ph值下具有改进的稳定性。具体地,本发明的树枝状大分子,特别是氨基膦酸末端的树枝状大分子(单钠),在ph值为7.2、7、5或4,温度为25℃的情况下,储存4至8个月后,不会出现任何化学降解。
[0611]
制备方法
[0612]
本专利申请还涉及如前所述的树枝状大分子的制备方法。
[0613]
本发明的树枝状大分子可以通过应用或修改本身已知的和/或本领域技术人员力所能及的任何方法来制备。
[0614]
本发明的树枝状大分子可以通过发散法或半内敛法来制备。
[0615]
在第一替代方案中,该树枝状大分子是通过发散法制备的。
[0616]
因此,根据该替代方案,本发明的树枝状大分子可以通过依次包括以下步骤的方法来制备:
[0617]
(a)制备以下结构式的中间体:
[0618]
[化学式30]
[0619][0620]
或其某种药学上可接受的盐,
[0621]
其中:
[0622]
§
、a、b、d例如定义如上或者如结构式(i)所示;
[0623]
(b)使步骤(a)中获得的中间体与p(e)x3反应,其中e是o或s,优选地e是s,x是卤素,优选地x是cl;
[0624]
(c)使步骤(b)中获得的产物与包含中间链和可选地包含端基的片段反应。
[0625]
具体地,步骤(a)的实施是通过使卤化核心
§
与包含胺或铵官能团的代链前体反应,或与包含醛官能团的代链前体反应,然后将醛官能团转化为胺或铵官能团。
[0626]
具体地,步骤(a)中使用的卤化核心
§
选自结构式如下的基团:
[0627]
[化学式31]
[0628][0629]
[化学式32]
[0630][0631]
并且
[0632]
[化学式33]
[0633][0634]
其中x是卤素,优选地x是cl。更具体地,步骤(a)中使用的卤化核心
§
是
[0635]
[化学式32]
[0636][0637]
其中x是卤素,优选地x是cl。
[0638]
在一种实施方式中,该方法在步骤(a)之后还包括以下步骤,使步骤(a)中获得的产物与包含胺或铵官能团的代链前体反应,或与包含醛官能团的代链前体反应,然后将醛官能团转化为胺或铵官能团,并重复步骤(b)。
[0639]
在第二替代方案中,树枝状大分子是通过半内敛法制备的。
[0640]
因此,根据该替代方案,本发明的树枝状大分子可以通过依次包括以下步骤的方法来制备:
[0641]
(a)制备包含代链、中间链和端基的片段,结构式如下:
[0642]
[化学式34]
[0643][0644]
其中:
[0645]
a、b、d、e、g、j、l、v、w1和w2例如定义如上或者如结构式(i)所示;
[0646]
(b)使步骤(a)中获得的片段与卤化核心
§
反应。
[0647]
具体地,步骤(b)中使用的卤化核心
§
选自结构式如下的基团:
[0648]
[化学式30]
[0649][0650]
[化学式32]
[0651][0652]
并且
[0653]
[化学式33]
[0654][0655]
其中x是卤素,优选地x是cl。更具体地,步骤(a)中使用的卤化核心
§
是
[0656]
[化学式32]
[0657][0658]
其中x是卤素,优选地x是cl。
[0659]
有利地,步骤(b)是在-100℃到50℃之间,具体地在-78℃到30℃之间的温度下实施的。
[0660]
有利地,步骤(b)是在选自非极性溶剂和非质子极性溶剂的溶剂中实施的。具体地,步骤(b)是在选自醚类溶剂和含氯溶剂的溶剂中实施的。更具体地,步骤(b)是在选自四氢呋喃、乙醚、二恶烷、二氯甲烷和氯仿的溶剂中实施的。甚至更具体地,步骤(b)是在四氢呋喃中实施的。
[0661]
药物组合物
[0662]
本技术还涉及一种药物组合物,包含如前所述的树枝状大分子,具体是结构式(iii)或其子结构式的树枝状大分子,以及药学上可接受的赋形剂。
[0663]
术语“药学上可接受的”仅指药物组合物的成分彼此相容且对患者无害。在一种实施方式中,药学上可接受的赋形剂在施用于动物,优选施用于人时不会产生副作用、过敏或其他不良反应。施用于人时,制剂必须达到无菌性、致热性、一般安全性和标准纯度的标准,例如监管机构制定的标准,如fda或ema。
[0664]
药学上可接受的赋形剂尤其可以是本领域技术人员已知的任何赋形剂。
[0665]
除了本发明的树枝状大分子作为活性成分之外,该药物组合物还可以包含一种或多种其他治疗剂和/或活性成分,例如抗炎剂、抗感染剂或免疫抑制剂。
[0666]
治疗用途
[0667]
本专利申请的目标还包括本发明,的树枝状大分子,具体是结构式(iii)或其子结构式的树枝状大分子,或如上所述的药物组合物,该组合物用作药物,更具体地用于治疗或预防有此需要的受试者所患的炎性疾病。
[0668]
根据另一个方面,本发明涉及一种治疗或预防炎性疾病的方法,包括向受试者施用有效治疗剂量的本发明的树枝状大分子,具体是结构式(iii)或其子结构式的树枝状大分子,或根据本发明的药物组合物。优选地,受试者是动物,优选哺乳动物,更优选患有炎性疾病的人类。
[0669]
本发明还涉及本发明的树枝状大分子,具体是结构式(iii)或其结构式的树枝状大分子,或如上所述的药物组合物,用于制造治疗或预防炎性疾病的药物。
[0670]
根据一种实施方式,所述炎性疾病选自慢性炎性疾病、自身免疫造成的炎性疾病以及促炎和癌症相关的炎性症状。
[0671]
根据一种具体实施方式,慢性炎性疾病选自类风湿性关节炎、银屑病、葡萄膜炎和多发性硬化症。
[0672]
根据一种实施方式,本发明的树枝状大分子,具体是结构式(iii)或其子结构式的树枝状大分子,或本发明的药物组合物,可以用作药物,具体地用于治疗或预防炎性疾病,例如与至少一种其他治疗剂联合施用于前述受试者。此类其他治疗剂包括但不限于抗炎剂、抗感染剂或免疫抑制剂。树枝状大分子和其他治疗剂可以同时施用或在不同时间、同时或分开施用。
[0673]
因此,本发明的治疗方法和药物组合物可以使用本发明的树枝状大分子,具体是结构式(iii)或其子结构式的树枝状大分子,或单药疗法的本发明的药物组合物,但是这些方法和组合物也可以通过多药疗法的形式使用,其中本发明的一种或多种树枝状大分子与一种或多种其他治疗剂联合共同施用。
[0674]
定义
[0675]
下面的定义和解释涉及本技术中使用的术语和表达,包括说明书以及权利要求。
[0676]
对于本发明化合物的描述,除非另有说明,否则所使用的术语和表达应该根据以下定义进行解释。
[0677]
单独或作为其他基团的一部分的术语“卤素”或“卤代”是指氟、氯、溴或碘。优选的卤素基团是氯和氟,更优选的是氟。
[0678]
单独或作为其他基团的一部分的术语“烷基”是指结构式c
nh2n+1
的烃基,其中n是大于或等于1的整数。
[0679]
单独或作为其他基团的一部分的术语“卤代烷基”或“卤代氧烷基”是指如上定义的烷基,其中一个或多个氢原子被如上定义的卤素基团所取代。根据本发明的卤代烷基可以是直链或支链的,并且包括但不限于结构式c
nf2n+1
的基团,其中n是大于或等于1的整数,优选1到10的整数。优选的卤代烷基包括三氟甲基、二氟甲基、氟甲基、五氟乙基、七氟-正丙基、九氟-正丁基、1,1,1-三氟-正丁基、1,1,1-三氟-正戊基、1,1,1-三氟-正己基、三氟甲基。
[0680]
单独或作为其他基团的一部分的术语“环烷基”是指具有3至12个碳原子,尤其是5至10个碳原子,更具体是6至10个碳原子的饱和单环、二环或三环烃基。合适的环烷基包括但不限于环丙基、环丁基、环戊基、环己基、环庚基、环辛基、降冰片基,金刚烷基,尤其是金刚烷胺-l-基、金刚烷胺-2-基、1-十氢化萘基。
[0681]
单独或作为其他基团的一部分的术语“芳基”是指具有单环(苯基)或稠合在一起的多个芳环(例如萘基)的多不饱和芳烃基团,通常含5至12个原子,优选6至10个原子,其中至少一个环是芳环。特别优选的芳基是苯基。
[0682]
单独或作为其他基团的一部分的术语“杂芳基”是指芳环或含有一个至两个稠合芳环的环系统,但不限于此,通常含有5至12个原子,其中至少一个环是芳环,并且其中一个或多个这些环中的一个或多个碳原子被氧、氮和/或硫原子所取代,氮和硫的杂原子可能被氧化,并且氮的杂原子可能被季铵化。优选但并非限制性的杂芳基是吡啶基、吡咯基、呋喃基、苯硫基。
[0683]
含有碱性官能团的本发明化合物可以是药学上可接受的盐的形式。含有一个或多个碱性官能团的本发明化合物的药学上可接受的盐尤其包括它们的酸式盐。合适的酸式盐是由形成无毒盐的酸形成。盐的实例包括乙酸盐、己二酸盐、天冬氨酸盐、苯甲酸盐、苯磺酸盐、碳酸氢盐/碳酸盐、硫酸氢盐/硫酸盐、硼酸盐、氨磺酸盐、枸橼酸盐、环磺酸盐、乙二磺酸盐、乙磺酸盐、甲酸盐、富马酸盐、葡庚糖酸盐、葡萄糖酸盐、葡萄糖醛酸盐、六氟磷酸盐、海苯酸盐、盐酸盐/氯化物、氢溴酸盐/溴化物、氢碘酸盐/碘化物、羟乙基磺酸盐、乳酸盐、苹果酸盐、马来酸盐、丙二酸盐、甲磺酸盐、甲基硫酸盐、萘酸盐、2-萘酸盐、烟酸盐、硝酸盐、乳清酸盐、草酸盐、棕榈酸盐、双羟萘酸盐、磷酸盐/磷酸氢盐/磷酸二氢盐、焦谷氨酸盐、糖酸盐、硬脂酸盐、琥珀酸盐、单宁酸盐、酒石酸盐、甲苯磺酸盐、三氟乙酸盐和xinofoate。盐的具体示例包括盐酸盐/氯化物和三氟乙酸盐。
[0684]
本发明化合物的药学上可接受的盐例如可以按如下所述制备得到:
[0685]
(i)使本发明化合物与所需的酸反应;或者
[0686]
(ii)通过与合适的酸反应或通过合适的离子交换柱,将本发明化合物的一种盐转化为另一种。
[0687]
所有这些反应通常都是在溶液中进行的。盐可以从溶液中沉淀出来,并经过滤回收或者可以通过溶剂蒸发来回收。盐的电离度可以从完全电离到几乎不电离不等。
[0688]
本发明化合物可以以溶剂合物的形式存在,即以与一种或多种溶剂分子例如乙醇或水的结合或组合的形式存在。溶剂是水时,使用术语“水合物”。
[0689]
对本发明化合物的所有引用也指其溶剂化物。
[0690]
本发明化合物是如上定义的结构式i的化合物和它们的溶剂化物,其中包括它们的所有多晶型物和结晶形式、它们的前药和带有同位素标记的化合物或溶剂化物。
[0691]
术语“受试者”是指动物,更具体地是哺乳动物。优选地,受试者是人。在本发明中,受试者可以是患者,即在患病期间接受医疗护理、经过或已经经过治疗或监控的人。
[0692]
术语“人”是指男女和处于任何发育阶段(即新生儿、婴儿、少年、青少年和成人)的受试者。在一种实施方式中,包括青少年或成年人,优选成年人。
[0693]
术语“治疗”(动词)和“治疗”(名词)应该按它们的一般含义进行理解,因此包括病理状况的改善和消除。
[0694]
术语“预防”(动词)和“预防”(名词)是指避免或延迟疾病或病症和相关症状的出现,从而排除患者患上疾病或病症,或降低受试者患上疾病或病症的风险。
[0695]
术语“有效治疗剂量”或“有效剂量”是指活性成分(根据本发明的树枝状大分子)的剂量,足以使施用了该剂量的患者达到预期的治疗或预防结果。在本技术中,有效治疗剂量是指足以产生抗炎作用的树枝状大分子的剂量。
[0696]
对照下面的示例将更好地理解本发明。这些示例代表了本发明的部分实施方式,但任何情况下均不是对本发明范围的限制。附图用于说明实验结果。
附图说明
[0697]
图1
[0698]
[图1]示出了树枝状大分子1-g
”’
1-hcl的结构(化合物1)。
[0699]
图2
[0700]
[图2]示出了树枝状大分子1-g
”’
1-htfa的结构(化合物2)。
[0701]
图3
[0702]
[图3]示出了树枝状大分子1-g
”’
2-htfa的结构(化合物3)。
[0703]
图4
[0704]
[图4]示出了树枝状大分子1-g
”’
3-htfa的结构(化合物4)。
[0705]
图5
[0706]
[图5]示出了树枝状大分子1-g
”’
4-htfa的结构(化合物5)。
[0707]
图6
[0708]
[图6]示出了树枝状大分子3-g
’1(ome)的结构(化合物6)。
[0709]
图7
[0710]
[图7]示出了树枝状大分子3-g
’1(oh)的结构(化合物7)。
[0711]
图8
[0712]
[图8]示出了树枝状大分子3-g
’1(ona)的结构(化合物8)。
[0713]
图9
[0714]
[图9]示出了树枝状大分子4-g
’1(ome)的结构(化合物9)。
[0715]
图10
[0716]
[图10]示出了树枝状大分子4-g
’1(oh)的结构(化合物10)。
[0717]
图11
[0718]
[图11]示出了树枝状大分子4-g
’1(oh)的结构(化合物11)。
[0719]
图12
[0720]
[图12]示出了树枝状大分子5-g
’1(ome)的结构(化合物12)。
[0721]
图13
[0722]
[图13]示出了树枝状大分子5-g
’1(oh)的结构(化合物13)。
[0723]
图14
[0724]
[图14]示出了树枝状大分子5-g
’1(ona)的结构(化合物14)。
[0725]
图15
[0726]
[图15]示出了树枝状大分子11a-g1(nh-nac)的结构(化合物15)。
[0727]
图16
[0728]
[图16]示出了树枝状大分子11b-g1(nh-nac)的结构(化合物16)。
[0729]
图17
[0730]
[图17]示出了树枝状大分子11c-g1(nh-nac)的结构(化合物17)。
[0731]
图18
[0732]
[图18]示出了树枝状大分子11a-g1(nh-nac/po3hna)的结构(化合物18)。
[0733]
图19
[0734]
[图19]示出了树枝状大分子11b-g1(nh-nac/po3hna)的结构(化合物19)。
[0735]
图20
[0736]
[图20]示出了树枝状大分子11c-g1(nh-nac/po3hna)的结构(化合物20)。
[0737]
图21
[0738]
[图21]示出了树枝状大分子12-g
”’
2-htfa的结构(化合物21)。
{1h})核磁共振进行的。
[0763]
溶剂、试剂和起始物购自知名化学品供应商,例如sigma aldrich、acros organics、fluorochem、eurisotop、vwr international、sopachem和polymer。除非另有说明,否则溶剂在使用前经蒸馏纯化。除非另有说明,否则试剂和起始物无需进一步纯化即可使用。
[0764]
使用了以下缩写:
[0765]
dcm:二氯甲烷,
[0766]
dipea:二异丙胺,
[0767]
eq.或equiv.:倍量,
[0768]
etoac:乙酸乙酯,
[0769]
etoh:乙醇,
[0770]
meoh:甲醇,
[0771]
rmn:核磁共振,
[0772]
ta:室温,
[0773]
tfa:三氟乙酸,
[0774]
thf:四氢呋喃。
[0775]
合成1至5代树枝状大分子
[0776]
示意图1描述了第1代树枝状大分子的反应示意图。
[0777]
[示意图1]
[0778][0779]
rmn分配时使用的编号:
[0780]
[化学式35]
[0781][0782]
利用n3p3cl6(macromolecules,1981年第14期,1616-1622页)合成化合物1-g
’0[0783]
[化学式36]
[0784][0785]
在室温下,向n3p3cl6(2000mg,5.75mmol)的thf(200ml)溶液中依次加入k2co3(14.3g,103.5mmol)和4-羟基苯甲醛(4634mg,37.95mmol)。在室温下搅拌72小时后,对混合物过滤,然后浓缩至干。粗残余物用meoh洗涤4到5次,得到白色粉末状的化合物1-g
’0,产率81%。
[0786]
rmn1h(300mhz,cdcl3):δ(ppm)9.83(s,6h,cho),7.74(d,3j
hh
=8.6hz,12h,c
03
h),7.12(d,3j
hh
=8.5hz,12h,c
02
h)。
[0787]
rmn 31
p-{1h}(121mhz,cdcl3):δ(ppm)7.15(s,p0)。
[0788]
rmn 13
c-{1h}(75mhz,cdcl3):δ(ppm)190.47(s,cho),154.44(dd,2j
cp=
5.1hz,4j
cp
=2.5hz,c
01
),133.74(s,c
04
),131.38(s,c
03
),121.21(d,3j
cp
=2.5hz,c
02
)。
[0789]
利用1-g
’0合成化合物1-g”0
[0790]
[化学式37]
[0791][0792]
在室温下,向化合物1-g
’0(500mg,0.580mmol)的thf(50ml)溶液中加入8m甲胺的etoh(1.3ml,10.45mmol)溶液。室温下搅拌过夜后,对混合物浓缩至干,得到白色粉末状的树枝状大分子1-g”0
。
[0793]
rmn 1
h(300mhz,cd3cn):δ(ppm)8.24(d,4j
hh
=1.7hz,6h,ch=n),7.55(d,3j
hh
=8.6hz,12h,c
03
h),6.99(d,3j
hh
=8.5hz,12h,c
02
h),3.50(s,18h,n-ch3)
[0794]
rmn 31
p-{1h}(121mhz,cd3cn):δ(ppm)8.66(s,p0).
[0795]
rmn 13
c-{1h}(75mhz,cd3cn):δ(ppm)160.80(s,c=n),151.57(dd,2j
cp
=5.1hz,4j
cp
=2.5hz,c
01
),133.94(s,c
04
)129.13(c
03
),120.66(dd,3j
cp
=3.2hz,5j
cp
=1.8hz,c
02
),47.29(s,ch3).
[0796]
合成化合物1-ab-boc
[0797]
[化学式38]
[0798][0799]
向4-羟基苯甲醛(1000mg,8.188mmol)的thf(50ml)溶液中加入甲胺溶液(8m甲胺的etoh溶液)(3.07ml,24.56mmol)。在室温下搅拌过夜后,反应结束。化合物1未经分离直接用于后续操作。
[0800]
rmn 1
h(400mhz,cd3od):δ(ppm)8.16(s,1h,ch=n),7.52(d,j=8.7hz,2h,c
03
h),6.77(d,j=8.6hz,2h,c
02
h),2.40(s,3h,ch3)。
[0801]
[化学式39]
[0802][0803]
然后将nabh4(371mg,9.81mmol)加入到反应介质中。在室温下搅拌12小时后,对混合物减压浓缩至干。然后将粗残余物溶于hcl溶液(1m的meoh溶液)(29.43ml,29.43mmol)中。在室温下搅拌3小时后,对溶液过滤,然后减压浓缩,得到白色粉末。粉末用3
×
50ml的ch2cl2洗涤,得到白色粉末状的相应盐酸胺,产率98%。
[0804]
rmn 1
h(300mhz,cd3od):δ(ppm)7.35(d,3j
hh
=8.7hz,2h,c
03
h),6.87(d,3j
hh
=8.7hz,2h,c
02
h),4.10(s,2h,ch2),2.69(s,3h,ch3)。
tbutyl),52.00(sl,ch2nboc),51.28(sl,ch2nboc),34.07(s,n-ch3),28.43(s,c(ch3)3).
[0822]
利用n3p3cl6合成化合物1-g
’”
0-boc
[0823]
[化学式43]
[0824][0825]
向六氯环三磷腈(0.5mmol)的thf(50ml)溶液中,依次加入cs2co3(6.30mmol)和化合物1-ab-boc(3.15mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。然后利用ch2cl2/etoac混合物,通过硅胶色谱法纯化粗残余物,得到白色粉末状的树枝状大分子1-g
’”
0-boc,产率86%。
[0826]
rmn 31
p-{1h}(162mhz,cdcl3):δ(ppm)8.2(s,p0).
[0827]
利用1-g”0
合成化合物1-g
’”
0-hcl
[0828]
[化学式44]
[0829][0830]
向树枝状大分子1-g”0
(500mg,0.53mmol)的thf/meoh混合物(25/5)ml溶液中加入nabh4(201mg,5.32mmol)。在室温下搅拌过夜后,对混合物浓缩至干。粗残余物用200ml的dcm稀释,然后用50ml蒸馏水洗涤一次。回收有机相,用na2so4干燥,过滤并减压浓缩。然后将产物溶于其中添加有9.5ml hcl(1m hcl的meoh溶液)的meoh(30ml)。在室温下搅拌2小时后,对溶液过滤,然后减压浓缩。然后残余物用25ml的ch2cl2洗涤3次,得到白色粉末状的产物1-g
’”
0-hcl(质子化hcl的形式)。
[0831]
rmn 1
h(400mhz,cd3od):δ(ppm)7.54(d,3j
hh
=8.5hz,12h,c
03
h),7.05(d,3j
hh
=8.3hz,12h,c
02
h),4.27(s,12h,ch2nh),2.75(s,18h,n-ch3).
[0832]
rmn 31
p-{1h}(162mhz,cd3od):δ(ppm)8.29(s,p0).
[0833]
rmn 13
c-{1h}(101mhz,cd3od):δ(ppm)151.07(dd,2j
cp
=5.1hz,4j
cp
=2.5hz,c
01
),131,46(s,c
03
),128.71(s,c
04
),121.12(dd,3j=3.2,5j=1.7hz,(s,c
02
),51.30(s,ch2nh),31.88(s,n-ch3).
[0834]
利用1-g
’”
0-boc合成化合物1-g
”’
0-htfa
[0835]
[化学式45]
[0836][0837]
在室温下,将化合物1-g
”’
0-boc(300mg)在10ml的ch2cl2/tfa(50/50)混合物中溶解60分钟,然后将反应混合物蒸发至干,得到化合物1-g
”’
0-htfa(质子化tea的形式)。
[0838]
rmn 31
p-{1h}(162mhz,cd3od):δ(ppm)8.3(s,p0).
[0839]
利用1-g
’”
0-htfa或1-g
’”
0-hcl合成1-g
’”0[0840]
[化学式46]
[0841][0842]
将化合物1-g
”’
0-htfa或1-g
”’
0-hcl(300mg)溶于其中添加有25ml的naoh溶液(2m)的25ml蒸馏水中。然后水相用200ml的ch2cl2提取3次。然后有机相经na2s04干燥,过滤和真空浓缩,得到透明油状的树枝状大分子1-g
”’0,产率80%。
[0843]
rmn 1
h(400mhz,cdcl3):δ(ppm)7.12(d,3j
hh
=8.5hz,12h,c
03
h),6.91(d,3j
hh
=8.3hz,12h,c
02
h),3.69(s,12h,ch2nh),2.43(s,18h,n-ch3).
[0844]
rmn 31
p-{1h}(162mhz,cdcl3):δ(ppm)8.71(s,p0).
[0845]
rmn 13
c-{1h}(101mhz,cdcl3):δ(ppm)149.55(dd,2j
cp
=5.1hz,4j
cp
=2.5hz,c
01
),136.70(s,c
03
),128.99(s,c
04
),120.82(dd,3j=3.4,5j=1.7hz,c
02
),55.43(s,ch2nh),36.06(s,n-ch3).
[0846]
利用1-g
”’0合成化合物1-g1[0847]
[化学式47]
[0848][0849]
室温下,在30分钟内,向pscl3(3.109ml,30.60mmol)的ch2cl2(100ml)溶液中逐滴加入存在et3n(0.740ml,5.31mmol)的树枝状大分子1-g
’”
0(800mg,0.85mmol)的ch2cl2(25ml)溶液。室温下搅拌3小时后,对混合物减压浓缩至干。然后将粗残余物溶于200ml的ch2c12,再经硅胶过滤,得到白色粉末状的树枝状大分子1-g1,产率82%。
[0850]
rmn 1
h(300mhz,cdcl3):δ(ppm)7.22(d,3j
hh
=8.5hz,12h,c
03
h),6.99(d,3j
hh
=8.3hz,12h,c
02
h),4.60(d,3j
hp
=15.1hz,12h,ch2nh),2.82(d,3j
hp
=16.2hz,18h,n-ch3).
[0851]
rmn 31
p-{1h}(121mhz,cdcl3):δ(ppm)64.12(s,p1),8.35(s,p0).
[0852]
rmn 13
c-{1h}(75mhz,cdcl3):δ(ppm)150.26(dd,2j
cp
=5.1hz,4j
cp
=2.5hz,c
01
),132.73(d,3j
cp
=6.5hz,c
04
),129,17(s,c
03
),121.29
–
121.15(m,c
02
),54.18(d,2j
cp
=5.5hz,ch2nh),35.11(d,2j
cp
=2,5hz,n-ch3).
[0853]
利用1-g
’”
0-htfa或1-g
’”
0-hcl合成1-g1[0854]
[化学式47]
[0855][0856]
向冷却至-78℃的化合物1-g
”’
0-htfa或1-g
”’
n-hcl(0.05mmol)的ch2cl2(25ml)溶液中,其中含有碱,优选非亲质子的有机碱,如dipea(每个末端质子化胺2至3倍量,即2*
0.05*2ny至3*0.05*2ny mmol),极快地加入pscl3(每个末端质子化胺5至10倍量,即5*0.05*2ny至10*0.05*2ny mmol)。混合物缓慢升温至室温。在室温下搅拌过夜后,将反应混合物减压蒸发至干。粗残余物用200ml的ch2cl2稀释,并经硅胶过滤。然后溶液用mgso4干燥并减压浓缩。得到的残余物用chcl3/链烷混合物(1/10)洗涤3次,得到白色粉末状的产物g1。
[0857]
利用1-g1合成化合物1-g
’1[0858]
[化学式48]
[0859][0860]
向树枝状大分子1-g1(300mg,0.171mmol)的thf(30ml)溶液中依次加入cs2co3(1341mg,4.11mmol)和4-羟基苯甲醛(314.2mg,2.57mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。然后通过硅胶色谱法(洗脱液梯度为50/50-60/40etoac/己烷)纯化产物,得到白色粉末状的树枝状大分子1-g’1,产率73%。
[0861]
rmn 1
h(400mhz,cdcl3):δ(ppm)9.96(s,12h,cho),7.88(d,3j
hh
=8.5hz,24h,c
13
h),7.33(d,3j
hh
=8.3hz,24h,c
12
h),7.18(d,3j
hh
=8.5hz,12h,c
03
h),6.97(d,3j
hh
=8.5hz,12h,c
02
h),4.49(d,3j
hp
=13.4hz,12h,ch2nh),2.83(d,3j
hp
=10.6hz,18h,n-ch3).
[0862]
rmn 31
p-{1h}(162mhz,cdcl3):δ(ppm)66.34(s,p1),8.35(s,p0).
[0863]
rmn 13
c-{1h}(101mhz,cdcl3):δ(ppm)190.65(s,cho),155.31(d,2j
cp
=7.3hz,c
11
),150.14(dd,2j
cp
=5.1hz,4j
cp
=2.5hz,c
01
),133.66(d,3j
cp
=4.4hz,c
04
),133.57(d,5j
cp
=1.3hz,c
14
),131.48(s,c
13
),129.42(s,c
03
),121.63(d,3j
cp
=5.0hz,c
12
),121.01(m,c
02
),53.67(d,2j
cp
=7.8hz,ch2nh),33.72(d,2j
cp
=1.5hz,n-ch3).
[0864]
利用1-g
”’0合成化合物1-g
’1[0865]
[化学式48]
[0866][0867]
存在dipea(1.5mmol)的情况下,向化合物1-g
”’0(0.1mmol)的thf溶液(30ml)中加入化合物1-ab
2-cho(0.63mmol)。在室温下搅拌过夜后,对混合物减压蒸发至干。然后通过硅胶色谱法纯化粗残余物,得到白色粉末状的化合物1-g
’1。
[0868]
利用1-g
”’
0-htfa或1-g
”’
0-hcl合成化合物1-g
’1[0869]
[化学式48]
[0870]
[0871]
存在dipea(1.8mmol)的情况下,向化合物1-g
”’
0-tfa或1-g
”’
0-hcl(0.1mmol)的thf(30ml)溶液中加入化合物1-ab
2-cho(0.63mmol)。在室温下搅拌过夜后,对混合物减压蒸发至干。然后通过硅胶色谱法纯化粗残余物,得到白色粉末状的化合物1-g
’1。
[0872]
利用1-g
’1合成化合物1-g”1
[0873]
[化学式49]
[0874][0875]
向化合物1-g
’1(200mg,0.072mmol)的thf(20ml)溶液中加入8m甲胺的etoh(320μl,2.59mmol)溶液。室温下搅拌过夜后,对混合物减压浓缩至干,得到白色粉末状的树枝状大分子1-g”1
。产率是可定量的。
[0876]
rmn 1
h(300mhz,cd2cl2):δ(ppm)8.25(d,4j
hh
=1.6hz,12h,ch=n),7.71(d,3j
hh
=8.5hz,24h,c
13
h),7.32
–
7.10(m,36h,c
12
h,c
03
h),6.96(d,3j
hh
=8.4hz,12h,c
02
h),4.48(d,3j
hp
=13.0hz,12h,ch2n0h),3.48(d,4j
hh
=1,5hz,36h,c=n
1-ch3),2.80(d,3j
hp
=10.7hz,18h,n
0-ch3).
[0877]
rmn 31
p-{1h}(121mhz,cd2cl2):δ(ppm)67.60(s,p1),8.59(s,p0).
[0878]
利用1-g”1
合成树枝状大分子1-g
’”
1-hcl
[0879]
[化学式50]
[0880][0881]
向化合物1-g”1(155mg,0.053mmol)的thf(20ml)溶液中加入1m bh3.thf的thf(792μl,0.792mmol)溶液。在室温下搅拌过夜后,加入4ml的meoh。搅拌一小时后,对反应混合物减压浓缩至干。然后将粗残余物溶于1m hcl的meoh溶液(1908μl,1.908mmol)。然后溶液经过滤并减压浓缩至干。获得的粉末随后用10ml的ch2cl2洗涤3次,得到白色粉末状的化合物1-g
”’
1-hcl(质子化形式),产率90%。
[0882]
rmn 1
h(300mhz,cd3od):δ(ppm)7.59(d,3j
hh
=8.5hz,24h,c
13
h),7.28(m,36h,c
12
h,c
03
h),6.92(d,3j
hh
=8.4hz,12h,c
02
h),4.51(d,3j
hp
=14.0hz,12h,ch2n0h),4.21(s,24h,ch2n1h),2.82(d,3j
hp
=10.5hz,18h,n
0-ch3),2.73(s,36h,n
1-ch3).
[0883]
rmn 31
p-{1h}(121mhz,cd3od):δ(ppm)67.97(s,p1),9.07(s,p0).
[0884]
rmn 13
c(75mhz,cd3od):δ(ppm)151.81(d,2j
cp
=7.4hz,c
11
),149.79(dd,2j
cp
=4.4hz,4j
cp
=3,0hz,c
01
),134.33(d,3j
cp
=4,5hz,c
04
),131.35(s,c
13
),129.26(s,c
03
),128.33(d,5j
cp
=1.2hz,c
14
),121.61(d,3j
cp
=4.5hz,c
12
),120.65(s,c
02
),53.01(d,2j
cp
=6.9hz,ch2n0h),51.46(s,ch2n1h),33.00(d,2j
cp
=1.6hz,n
0-ch3),31.85(s,n
1-ch3).
[0885]
树枝状大分子1-g
”’
1-hcl的结构如[图1]所示。
[0886]
利用1-g1合成化合物1-g
”’
1-boc
[0887]
[化学式51]
[0888][0889]
向化合物1-g1(1000mg,0.571mmol)的thf(50ml)溶液中依次加入cs2co3(5570mg,17.14mmol)和化合物1-ab-boc(2035mg,8.57mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。然后利用ch2cl2/etoac混合物,通过硅胶色谱法纯化粗残余物,得到白色粉末状的树枝状大分子1-g
”’
1-boc,产率76%。
[0890]
rmn 1
h(300mhz,cdcl3):δ(ppm)7.26
–
7.11(m,60h,c
13
h,c
12
h,c
03
h),6.94(d,3j
hh
=8.4hz,12h,c
02
h),4.47(d,3j
hp
=12.6hz,12h,ch2n0h),4.38(s,24h,ch2n1h),2.87
–
2.71(m,54h,n
0-ch3,n
1-ch3),1.47(s,108h,boc).
[0891]
rmn 31
p-{1h}(121mhz,cdcl3):δ(ppm)68.11(s,p1),8.46(s,p0).
[0892]
rmn 13
c-{1h}(75mhz,cdcl3):δ(ppm)156.07(s,co),155.66(s,co),150.22
–
149.91(m,c
11
,c
01
),135.02(s,c
14
),134.06(d,3j
cp
=4.4hz,c
04
),129.30(s,c
03
),128.63(sl,c
13
),121.09(d,3j
cp
=4.8hz,c
12
),120.95(s,c
02
),79.72(s,o-c-tbutyl),53.56(d,2j
cp
=7.1hz,ch2n0h),51.64(d,j=56.7hz,ch2n1boc),33.93(s,n
1-ch
3)
,33.65(d,2j
cp
=1.7hz,n
0-ch3),28.45(s,c(ch3)3).
[0893]
利用1-g
’”
0-htfa或1-g
’”
0-hcl合成化合物1-g
’”
1-boc
[0894]
[化学式51]
[0895][0896]
存在dipea(3mmol)的情况下,向化合物1-g
’”1(0.1mmol)的thf溶液(30ml)中加入化合物1-ab
2-boc(1.26mmol)。在室温下搅拌过夜后,对混合物减压蒸发至干。然后通过硅胶色谱柱纯化粗残余物,得到白色粉末状的化合物1-g
’”1。
[0897]
利用1-g
’”0合成化合物1-g
”’
1-boc
[0898]
[化学式51]
[0899][0900]
存在dipea(3.6mmol)的情况下,向化合物1-g
’”
1-tfa或1-g
’”
1-hcl(0.1mmol)的thf(30ml)溶液中加入化合物1-ab
2-boc(1.26mmol)。在室温下搅拌过夜后,对混合物减压蒸发至干。然后通过硅胶色谱柱纯化粗残余物,得到白色粉末状的化合物1-g
’”1。
[0901]
利用1-g
’”
1-boc合成树枝状大分子1-g
”’
1-htfa
[0902]
[化学式52]
[0903][0904]
将化合物1-g
’”nboc(200mg)溶于ch2cl2/三氟乙酸70/30混合物(30ml)。在室温下搅拌30分钟后,将混合物减压浓缩至干。然后残余物用3ml的ch2cl2共蒸发5次,得到白色粉末状的树枝状大分子1-g
”’
n-htfa。
[0905]1h rmn(400mhz,cd3cn)δ(ppm):2.64(s),2.77(d,j=10.8hz),4.11(s),4.47(d,j=13.4hz),6.93(d,j=8.4hz),7.23(d,j=9.7hz),7.47(d,j=8.6hz).
[0906]
31
p-{1h}rmn(162mhz,cd3cn)δ(ppm):9.09(s,p0),67.80(s,p1).
[0907]
树枝状大分子1-g
”’
1-htfa的结构如[图2]所示。
[0908]
利用1-g
’”
1-htfa或1-g
’”
1-hcl合成1-g2[0909]
[化学式53]
[0910][0911]
向冷却至-78℃,并存在dipea(246μl,1.386mmol)的1-g
’”
1-htfa(200mg,0.046mmol)或1-g
’”
1-hcl的ch2cl2(25ml)溶液中,极快地加入pscl3(337μl,3.32mmol)。添加后,使混合物缓慢回升至室温。在室温下搅拌过夜后,对混合物减压蒸发至干。粗残余物用200ml的ch2cl2稀释,并经硅胶过滤。然后溶液用mgso4干燥并减压浓缩。然后残余物用chcl3/戊烷混合物(1/10)洗涤3次,得到白色粉末状的产物1-g2。产率为73%。
[0912]
rmn 1
h(500mhz,cdcl3):δ(ppm)7.33(d,3j
hh
=8.5hz,24h,c
13
h),7.26
–
7.11(m,36h,c
03
h,c
12
h),6.93(d,3j
hh
=8,4hz,12h),4.60(d,3j
hp
=14.9hz,24h,ch2n1h),4.50(d,3j
hp
=12.8hz,12h,ch2n0h),2.92
–
2.77(m,54h,n
1-ch3,n
0-ch3).
[0913]
rmn 31
p-{1h}(202mhz,cdcl3):δ(ppm)67.86(s,p1),63.95(s,p2),8.49(s,p0).
[0914]
rmn 13
c-{1h}(126mhz,cdcl3):δ(ppm)150.68(d,2j
cp
=7.5hz,c
11
),150.02(dd,2j
cp
=5.2hz,4j
cp
=2.5hz,c
01
),133.99(d,3j
cp
=4.6hz,c
04
),132.73(d,3j
cp
=6.6hz,c
14
),129.33(s,c
13
,c
03
),121.41(d,3j
cp
=4.8hz,s,c
12
),120.97(s,c
02
),54.21(d,2j
cp
=5.3hz,ch2n1h),53.64(d,2j
cp
=7.4hz,ch2n0h),35.15(s,n
1-ch3),33.74(d,n
0-ch3).
[0915]
利用1-g
’”
1-htfa或1-g
’”
1-hcl合成1-g
’2[0916]
[化学式54]
[0917][0918]
存在dipea(3.6mmol)的情况下,向化合物1-g
’”
1-htfa或1-g
’”
1-hcl(0.1mmol)的thf(30ml)溶液中加入化合物1-ab
2-boc(1.26mmol)。在室温下搅拌过夜后,对混合物减压
蒸发至干。然后通过硅胶色谱柱纯化粗残余物,得到白色粉末状的化合物1-g
’2。
[0919]
rmn 1
h(400mhz,cdcl3):δ(ppm)9.93(s,12h),9.94(s,12h),7.87(dd,j=8.5,2.1hz,48h),7.34(d,j=8.5hz,48h),7.26(s,24h),7.19(d,j=8.5hz,12h),7.11(d,j=8.3hz,24h),6.95(d,j=8.4hz,12h),4.54
–
4.44(m,36h),2.86(d,j=10.8hz,36h),2.78(d,j=10.6hz,18h).
[0920]
rmn 31
p-{1h}(162mhz,cdcl3):δ(ppm)67.91(s,p1),66.33(s,p2),8.43(s,p0).
[0921]
利用1-g2合成化合物1-g
’2[0922]
[化学式54]
[0923][0924]
向树枝状大分子1-g2(0.15mmol)的thf(30ml)溶液中依次加入cs2co3(7.2mmol)和4-羟基苯甲醛(2.5mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。然后通过硅胶色谱法(洗脱液梯度为50/50-60/40etoac/己烷)纯化产物,得到白色粉末状的树枝状大分子1-g
’2,产率73%。
[0925]
示意图2描述了利用第1代树枝状大分子获得的第2至5代树枝状大分子的反应示意图。
[0926]
[示意图2]
[0927][0928]
利用1-g
’”
n-1-htfa与合成子1-ab
2-boc合成化合物1-g
’”
n-boc的一般过程
[0929]
向200mg的树枝状大分子1-g
”’
(n-1)-htfa的三氟乙酸盐的ch2cl2溶液中(50-100ml),其中含有et3n(n=1,0.696mmol,n=2,1.392mmol,n=3,2.784mmol,n=4,5.569mmol,n=5,11.14mmol),加入化合物ab
2-boc(n=1,0.633mmol,n=2,1.265mmol,n=3,2.531mmol,n=4,5.062mmol,n=5,10.13mmol)。在室温下搅拌过夜后,对混合物浓缩至干。产率在50%到90%之间。
[0930]
n=1、2、3时,粗残余物经硅胶过滤,其中洗脱液为etoac/ch2cl2(梯度为5/95至30/70),得到油状化合物1-g
”’
n-boc。
[0931]
n=4、5时,粗残余物用10ml乙腈洗涤2次,得到粉末状化合物1-g
”’
n-boc。
[0932]
表征1-g
’”
2-boc:
[0933]
[化学式55]
[0934][0935]
rmn 1
h(600mhz,cd2cl2):δ(ppm)7.40
–
6.91(m,168h,ch-arom),4.63
–
4.47(d,3j
hp
=12.6hz,36h,ch2n0h,ch2n1h),4.40(s,48h,ch2n2h),3.14
–
2.84(m,54h,n
0-ch3,n
1-ch3),2.81(s,72h,n
2-ch3),1.47(sl,216h,boc).
[0936]
rmn 31
p-{1h}(243mhz,cd2cl2):δ(ppm)68.38(s,p2),68.03(s,p1),8.39(s,p0).
[0937]
rmn 13
c-{1h}(151mhz,cd2cl2):δ(ppm)155.59(d,nc(o)otbutyl),150.43(m,c
11
,c
01
),150.06(d,3j
cp
=7.5hz,c
21
),135.37(s,c
24
),134.28(s,c
04
,c
14
),129.41(m,c
03
,c
13
)128.56(d,c
23
),120.7-121.07(m,c
02
,c
12
,c
22
),79.34(s,o-c-tbutyl),51.57(d,ch2n2),33.81(s,n
2-ch3),33.64(s,n
1-ch3),33.58(s,n
0-ch3),28.14(s,c(ch3)3).
[0938]
表征1-g
’”
3-boc:
[0939]
[化学式56]
[0940][0941]
rmn 1
h(600mhz,cd2cl2):δ(ppm)7.41
–
6.97(m,10h,ch-arom),4.49
–
4.65(m,10h,ch2n0h,ch2n1h,ch2n2h),4.41(s,11h,ch2n3h),3.01
–
2.88(m,1h,n
0-ch3,n
1-ch3,n
2-ch3),2.82(s,18h,n
3-ch3),1.49(d,50h,boc).
[0942]
rmn 31
p-{1h}(243mhz,cd2cl2):δ(ppm)68.42(s,p3),68.14(m,p1,p2),8.28(s,p0).
[0943]
rmn 13
c-{1h}(151mhz,cd2cl2):δ(ppm)155.64(d,nc(o)otbutyl),150.50(m,c
11
,c
01,c21
),150.11(m,c
31
)135.41(s,c
34
),134.30(s,c
04
,c
14
,c
24
),129.45(s,c
03
,c
13
,c
23
),128.61(s,c
33
),121.40
–
120.71(m,c
02
,c
12
,c
22
,c
32
),79.39(s,o-c-tbutyl),51.72-51.62(m,ch2n),33.86-33.61(m,n
0-ch3,n
1-ch3,n
2-ch3,n
3-ch3),28.19(s,c(ch3)3).
[0944]
表征1-g
’”
4-boc:
[0945]
[化学式57]
[0946][0947]
rmn 1
h(400mhz,cdcl3):δ(ppm)7.40
–
7.04(m,744h,ch-arom),4.51
–
4.28(m,372h,ch2n0,ch2n1,ch2n2,ch2n3,ch2n4),3.03
–
2.68(m,558h,n
0-ch3,n
1-ch3,n
2-ch3,n
3-ch3,n
4-ch3),
1.46(s,864h,boc).
[0948]
rmn 31
p-{1h}(162mhz,cdcl3):δ(ppm)68.16(s,p4),67.94(m,p1,p2,p3),7.85(s,p0).
[0949]
rmn 13
c-{1h}(101mhz,cdcl3):δ(ppm)155.84(d,nc(o)otbutyl),150.62
–
150.27(m,c
11
,c
01,c21
,c
31
),150.09(d,2j
cp
=7.5hz,c
41
),135,00(s,c
44
),134,30(d,3j
cp
=3,7hz,c
04
,c
14
,c
24
,c
34
),129.47(m,c
03
,c
13
,c
23
,c
33
),128.63(m,c
43
),121.11(d,3j
cp
=4.3hz,c
02
,c
12
,c
22
,c
32
,c
42
),79.70(s,o-c-tbutyl),53.64
–
53.58(m,ch2n1,ch2n2,ch2n3)52.31
–
50.86(m,ch2n4)33.94-33.75(m,n
0-ch3,n
1-ch3,n
2-ch3,n
3-ch3,n
3-ch3),28.46(s,c(ch3)3).
[0950]
表征1-g
’”
5-boc:
[0951]
[化学式58]
[0952][0953]
rmn 1
h(300mhz,cdcl3):δ(ppm)7.45
–
6.92(m,1512h,ch-arom),4.43(m,756h,ch2n0,ch2n1,ch2n2,ch2n3,ch2n4,ch2n5),2.81(m,1134h,n
0-ch3,n
1-ch3,n
2-ch3,n
3-ch3,n
4-ch3,n
5-ch3),1.45(s,1728h,boc).
[0954]
rmn 31
p-{1h}(162mhz,cdcl3):δ(ppm)68.16(s,p4),67.94(m,p1,p2,p3),7.85(s,p0).
[0955]
利用1-g
’”
n-boc合成树枝状大分子1-g
’”
n-htfa的一般过程
[0956]
将化合物1-g
’”nboc(200mg)溶于ch2cl2/三氟乙酸70/30混合物(30ml)。在室温下搅拌30分钟后,将混合物减压浓缩至干。然后残余物用3ml的ch2cl2共蒸发5次,得到白色粉末状的树枝状大分子1-g
”’
n-htfa。产率高于90%。
[0957]
表征1-g
”’
1-htfa:
[0958]
[化学式52]
[0959][0960]1h rmn(400mhz,cd3cn)δ(ppm):2.64(s),2.77(d,j=10.8hz),4.11(s),4.47(d,j=13.4hz),6.93(d,j=8.4hz),7.23(d,j=9.7hz),7.47(d,j=8.6hz).
[0961]
31
p-{1h}rmn(162mhz,cd3cn)δ(ppm):9.09(s,p0),67.80(s,p1).
[0962]
树枝状大分子1-g
”’
1-htfa的结构如[图2]所示。
[0963]
表征1-g
’”
2-htfa:
[0964]
[化学式59]
[0965][0966]
rmn 1
h(600mhz,cd2cl2):δ(ppm)7.40
–
6.91(m,168h,ch-arom),4.63
–
4.47(d,3j
hp
=12.6hz,36h,ch2n0h,ch2n1h),4.40(s,48h,ch2n2h),3.14
–
2.84(m,54h,n
0-ch3,n
1-ch3),2.81(s,72h,n
2-ch3),1.47(sl,216h,boc).
[0967]
31
p-{1h}rmn(121mhz,cd3cn)δ(ppm):9.12(s,p0),67.74(s,p2),68.38(s,p1).
[0968]
树枝状大分子1-g
”’
2-htfa的结构如[图3]所示。
[0969]
表征1-g
’”
3-htfa:
[0970]
[化学式60]
[0971][0972]
31
p-{1h}rmn(162mhz,cd3cn)δ(ppm):9.10(s,p0),67.71(s,(p3),68.33(s,p1,p2).
[0973]
树枝状大分子1-g
”’
3-htfa的结构如[图4]所示。
[0974]
表征1-g
”’
4-htfa:
[0975]
[化学式61]
[0976][0977]
31
p-{1h}rmn(162mhz,cd3cn)δ(ppm):8.97(s,p0),67.72(s,p4),68.30(s,p1,p2,p3)。
[0978]1h rmn(400mhz,cd3cn)δ(ppm):2.58-2.74(m,558h,n
0-ch3,n
1-ch3,n
2-ch3,n
3-ch3,n
4-ch3),4.06
–
4,58(m,372,ch2n0,ch2n1,ch2n2,ch2n3,ch2n4),6.65
–
7.87(m,744h,ch-arom).
[0979]
树枝状大分子1-g
”’
4-htfa的结构如[图5]所示。
[0980]
发散法合成带有双-膦酸盐末端的第1代树枝状大分子
[0981]
示意图3描述了发散法合成带有双-膦酸盐末端的第1代树枝状大分子的反应示意图。
[0982]
[示意图3]
[0983][0984]
利用1-g1合成化合物3-g
’1(ome)
[0985]
[化学式62]
[0986][0987]
向前述制备的化合物1-g1(1mmol)的thf(30ml)溶液中,其中含cs2co3(24mmol),加入衍生自酪胺的苯酚氨基双亚甲基膦酸酯(参见wo 2005/052031 a1)(12mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。粗残余物用最少量的thf稀释,然后用大量乙醚洗涤。减压干燥后,得到透明油状的树枝状大分子3-g
’1(ome),产率95%。
[0988]
31
p-{1h}rmn(243mhz,cdcl3)δ(ppm):8.40(s,n=p),26.85(s,po),68.32(s,ps);
[0989]1h rmn(600mhz,cdcl3)δ(ppm):2.75(d,3j
hh
=10.1hz,24h,c
14-ch2),2.77(d,3j
hp
=7.6hz,18h,ch3),3.06(d,3j
hh
=7.7hz,24h,c
14-ch
2-ch2),3.19(d,2j
hp
=9.4hz,48h,ch
2-p),3.73(d,3j
hp
=10.6hz,144h,pome),6.94(d,3j
hh
=8.2hz,12h,c
02
h),7.07(d,3j
hh
=8.1hz,24h,c
12
h),7.18(br d,3j
hh
=8.2hz,36h,c
03 and c
13
h);
[0990]
13
c-{1h}rmn(151mhz,cdcl3)δ(ppm):33.05(s,ch2),33.64s,(ch3n),49.46(dd,1j
cp
=157.3,3j
cp
=7.2hz,ch
2-p),53.56-51.75(m,poch3),53.47(d,2j
cp
=10.3hz,c
14-ch2),58.22(t,3j
cp
=7.7hz,c
14-ch
2-ch2),120.91(br d,3j
cp
=4.4hz,c
02 and c
12
),129.30(s,c
03
),129.87(s,c
13
),134.10(br d,2j
cp
=4.5hz,c
04
),136.22(s,c
14
),149.35(d,2j
cp
=7.5hz,c
11
),150.01(br s,c
01
).
[0991]
树枝状大分子3-g
’1(ome)的结构如[图6]所示。
[0992]
利用3-g
’1(ome)合成化合物3-g
’1(oh)
[0993]
[化学式63]
[0994][0995]
在0℃,向树枝状大分子3-g
’1(ome)(1g,0.17mmol)的无水ch3cn(30ml)溶液中逐滴加入brtms(1.34,10.2mmol)。搅拌过夜后,对混合物减压浓缩至干。残余物在meoh(10ml)中搅拌一小时,然后用meoh(20ml)洗涤2次,再用et2o(20ml)洗涤1次。得到的固体物减压至干,得到白色粉末状的树枝状大分子3-g
’1(oh),产率是可定量的。
[0996]
31
p rmn(162mhz,d2o)δ(ppm):7.36(sl,poh),8.35(sl,poh),68.53(sl,ps).
[0997]
树枝状大分子3-g
’1(oh)的结构如[图7]所示。
[0998]
化合物3-g
’1(oh)随后被转化为3-g
’1(ona)
[0999]
利用3-g
’1(oh)合成化合物3-g
’1(ona)
[1000]
[化学式64]
[1001][1002]
在搅拌下,向3-g
’1(oh)的水混悬液中加入24倍量的0.1m的naoh水溶液。剩余溶液经0.4μm微过滤器过滤,然后冻干,得到白色粉末状化合物3-g
’1(ona),产率90%。
[1003]
31
p-{1h}rmn(162mhz,d2o/cd3cn)δ(ppm):6.93(s,po),9.59(s,n=p),68.77(s,ps);
[1004]1h rmn(600mhz,d2o/cd3cn)δ(ppm):2.76(d,3j
hp
=10.7hz,18h,ch3),3.13(t,3j
hh
=8.8hz,24h,c
14-ch2),3.47(d,2j
hp
=11.9hz,48h,ch
2-p),3.72(t,3j
hh
=8.6hz,24h,c
14-ch
2-ch2),4.47(d,2j
hp
=13.5hz,12h,c
04-ch2),6.91(d,2j
hh
=8.1hz,12h,c
02
h),7.15(d,2j
hh
=8.1hz,24h,c
12
h),7.29(d,2j
hh
=8.3hz,12h,c
03
h),7.38(d,2j
hh
=8.2hz,24h,c
13
h);
[1005]
13
c-{1h}rmn(151mhz,d2o/cd3cn)δ(ppm):29.07(s,c
14-ch2),33.58(s,ch3),52.91(d,1j
cp
=127.6hz,ch
2-p),52.94(s,c
04-ch2),57.81(s,c
14-ch
2-ch2),121.14(br s,c
02
),121.42(d,3j
cp
=4.4hz c
12
),129.61(s,c
03
),130.59(s,c
13
),133.95(s,c
14
),134.89(s,c
04
),149.18(s,c
01
),149.60(d,3j
cp
=7.6hz,c
11
)ppm.
[1006]
树枝状大分子3-g
’1(ona)的结构如[图8]所示。
[1007]
利用1-g
’0合成化合物4-g”0
[1008]
[化学式65]
[1009][1010]
向化合物1-g
’0(2g,2.32mmol)的thf(40ml)溶液中加入1-氨基己烷(5.5ml,41.8mmol)。室温下搅拌过夜后,对混合物浓缩至干,然后用meoh洗涤3到4次,得到白色粉末状的树枝状大分子4-g”0
,产率是可定量的。
[1011]
31
p-{1h}rmn(121mhz,cd2cl2)δ(ppm):8.46(s,p=n).
[1012]1h rmn(300mhz,cd2cl2)δ(ppm):0.79
–
1.10(m,18h,-ch3),1.29
–
1.47(m,36h,-ch
2-),1.68
–
1.77(m,12h,-ch
2-),3.63(td,3j
hh
=7.1,4j
hh
=1.3hz,12h,-ch
2-n),7.00(d,3j
hh
=8.4hz,12h,c
02
h),7.58(d,3j
hh
=8.7hz,12h,c
03
h),8.23(s,6h,ch=n).
[1013]
利用4-g”0
合成化合物4-g
’”0[1014]
[化学式66]
[1015][1016]
向树枝状大分子4-g”0(2g,1.4mmol)的thf/meoh混合物(30/10ml)溶液中加入nabh4(672mg,17.75mmol)。在室温下搅拌过夜后,对混合物浓缩至干。粗残余物用200ml的dcm稀释,然后用50ml蒸馏水洗涤一次。回收有机相,用na2so4干燥,过滤并减压浓缩。然后将产物溶于其中添加有20ml hcl(1m hcl的meoh溶液)的meoh(30ml)。2小时后且无需搅拌,对溶液过滤,然后减压浓缩。然后残余物用25ml的dcm洗涤3次,得到白色粉末。产物溶于其中添加有25ml naoh(2m)溶液的dcm/thf(75/25ml)混合物,然后用200ml的dcm提取4到5次。回收有机相,经na2s04干燥,过滤,真空浓缩,得到透明油状的树枝状大分子4-g
’”
0,产率78%。
[1017]
31
p-{1h}rmn(121mhz,cdcl3)δ(ppm):8.72(s,p=n).
[1018]1h rmn(300mhz,cdcl3)δ(ppm):0.73
–
1.09(m,18h,ch
3-)),1.13
–
1.42(m,48h,-ch
2-),1.45
–
1.55(m,12h,-ch
2-),2.60(t,3j
hh
=7.2hz,12h,-ch
2-n),3.73(s,12h,c
04-ch
2-),6.90(d,3j
hh
=8.4hz,12h,c
02
h),7.13(d,3j
hh
=8.6hz,12h,c
03
h).
[1019]
利用4-g
’”0合成化合物4-g1[1020]
[化学式67]
[1021][1022]-70℃下,在30分钟内向pscl3(4ml,39.36mmol)的dcm(100ml)溶液中逐滴加入树枝状大分子4-g
”’0(1g,0.72mmol)的dcm溶液(40ml),其中存在et3n(0.91ml,6.57mmol)。搅拌过夜后,对反应混合物减压浓缩至干。然后将粗残余物溶于200ml的dcm,再经硅胶过滤,得到透明油状的树枝状大分子4-g1,产率35%。
[1023]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.36(s,p=n),63.09(s,ps).
[1024]1h rmn(400mhz,cdcl3)δ(ppm):0.89(t,3j
hh
=6.9hz,18h,-ch3),1.23
–
1.47(m,36h,-ch
2-),1.57
–
1.64(m,12h,-ch
2-),3.23(dt,3j
hp
=18.0,3j
hh
=7.8hz,12h,-ch
2-n),4.63(d,3j
hp
=16.9hz,12h,c
04-ch
2-),6.99(d,3j
hh
=8.4hz,12h,c
02
h),7.23(d,3j
hh
=8.5hz,12h,c
03
h).
[1025]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):14.01(s,ch
3-),22.53(s,-ch
2-),26.33(s,-ch
2-),26.90(d,2j
cp
=2.9hz,-ch
2-n),31.36(s,-ch
2-),47.38(s,-ch
2-),50.11(d,2j
cp
=4.8hz,,c
04-ch
2-),121.22(br s,c
02
),129.16(s,c
03
),132.67(d,3j
cp
=5.0hz,c
04
),150.22(dd,2j
cp
=5.1,4j
cp
=2.5hz,c
01
)
[1026]
利用1-g4合成化合物4-g
’1(ome)
[1027]
[化学式68]
[1028][1029]
向化合物4-g1(1mmol)的thf(30ml)溶液中,其中含cs2co3(24mmol),加入衍生自酪胺的苯酚氨基双亚甲基膦酸酯(参见wo2005/052031a1)(12mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。粗残余物用最少量的thf稀释,然后用大量乙醚洗涤。减压干燥后,得到透明油状的树枝状大分子4-g
’1(ome),产率是可定量的。
[1030]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.23(s,p=n),26.89(s,pome),68.00(s,ps).
[1031]1h rmn(400mhz,cdcl3)δ(ppm):0.78(t,3j
hh
=6.6hz,18h,ch
3-),1.10
–
1.26(m,36h,-ch
2-),1.41
–
1.47(m,12h,-ch
2-),2.75(t,3j
hh
=7.6hz,24h,-ch
2-c
14
),3.04(t,3j
hh
=7.7hz,24h,-ch
2-n),3.09
–
3.15(m,12h,-ch
2-np),3.19(d,2j
hp
=9.3hz,18h,-ch
2-p),3.65
–
3.79(m,144h,pome),4.53(d,3j
hp
=13.1hz,12h,-ch
2-c
04
),6.95(d,3j
hh
=8.1hz,12h,c
02
h),7.06(d,3j
hh
=8.2hz,24h,c
12
h),7.16(d,3j
hh
=8.2hz,24h,c
12
h),7.22(d,3j
hh
=8.3hz,24h,c03
h).
[1032]
树枝状大分子4-g
’1(ome)的结构如[图9]所示。
[1033]
利用4-g
’1(ome)合成化合物4-g
’1(oh)
[1034]
[化学式69]
[1035][1036]
在0℃,向树枝状大分子4-g1(ome)(1g,0.16mmol)的无水ch3cn(30ml)溶液中加入brtms(1.25,9.48mmol)。搅拌过夜后,对混合物减压浓缩至干。残余物在meoh(10ml)中搅拌一小时,然后用meoh(20ml)洗涤2次,再用et2o(20ml)洗涤1次。得到的固体物减压至干,得到白色粉末状的树枝状大分子4-g
’1(oh),产率是可定量的。
[1037]
31
p-{1h}rmn(162mhz,d2o)δ(ppm):8.20(sl,poh).
[1038]
树枝状大分子4-g
’1(oh)的结构如[图10]所示。
[1039]
化合物4-g
’1(oh)随后被转化为4-g
’1(ona)
[1040]
利用4-g
’1(oh)合成化合物4-g
’1(ona)
[1041]
[化学式70]
[1042][1043]
在搅拌下,向4-g
’1(oh)的水混悬液中加入24倍量的0.1m的naoh水溶液。剩余溶液经0.4μμ微过滤器过滤,然后冻干,得到白色粉末状化合物4-g
’1(ona),产率88%。
[1044]
31
p-{1h}rmn(162mhz,d2o)δ(ppm)6.64(s,pohona),9.50(s,p=n),68.66(s,ps).
[1045]
树枝状大分子4-g
’1(ona)的结构如[图11]所示。
[1046]
利用1-g
’0合成化合物5-g”0
[1047]
[化学式71]
[1048][1049]
向化合物1-g
’0(2g,2.32mmol)的thf(40ml)溶液中加入1-氨基己烷(6.8ml,41.8mmol)。室温下搅拌过夜后,对混合物浓缩至干,然后用meoh洗涤3到4次,得到白色粉末状的树枝状大分子5-g”0
,产率是可定量的。
[1050]
31
p-{1h}rmn(121mhz,cd2cl2)δ(ppm):8.46(s,p=n).
[1051]1h rmn(300mhz,cd2cl2)δ(ppm):0.73
–
1.13(m,18h,ch
3-),1.19
–
1.45(m,60h,-ch
2-),1.78
–
1.66(m,12h,-ch
2-),3.62(td,3j
hh
=7.1,4j
hh
=1.3hz,12h,ch2n),6.99(d,3j
hh
=8.6hz,12h,c
02
h),7.58(d,3j
hh
=8.7hz,12h,c
03
h),8.22(s,6h,ch=n).
[1052]
13
c-{1h}rmn(75mhz,cd2cl2)δ(ppm):13.86(s,ch
3-),22.66(s,-ch
2-),27.43(s,-ch
2-),29.31(s,-ch
2-),29.47(s,-ch
2-),31.04(s,-ch
2-),31.88(s,-ch
2-),61.67(s,-ch2n),120.93(d,3j
cp
=2.9hz,c
02
h),129.19(s,c
03
h),133.78(s,c
04
),151.80(d,2j
cp
=7.6hz,c
01
),158.93(s,-c=n-).
[1053]
利用5-g”0
合成化合物5-g
’”0[1054]
[化学式72]
[1055][1056]
向树枝状大分子5-g”0
(2g,1.3mmol)的thf/meoh混合物(30/10ml)溶液中加入nabh4(594mg,15.68mmol)。在室温下搅拌过夜后,对混合物浓缩至干。粗残余物用200ml的dcm稀释,然后用50ml蒸馏水洗涤一次。回收有机相,用na2so4干燥,过滤并减压浓缩。然后将产物溶于其中添加有20ml hcl(1m hcl的meoh溶液)的meoh(30ml)。2小时后且无需搅拌,对溶液过滤,然后减压浓缩。然后残余物用25ml的dcm洗涤3次,得到白色粉末。产物溶于其中添加有25ml naoh(2m)溶液的dcm/thf(75/25ml)混合物,然后用200ml的dcm提取4到5次。回收有机相,经na2s04干燥,过滤,真空浓缩,得到透明油状的树枝状大分子5-g
’”0,产率65%。
[1057]
31
p-{1h}rmn(121mhz,cd2cl2)δ(ppm):8.92(s,p=n).
[1058]1h rmn(300mhz,cd2cl2)δ(ppm):0.70
–
1.13(m,18h,ch
3-),1.23
–
1.45(m,60h,-ch
2-),1.46
–
1.66(m,12h,-ch
2-),2.64(t,3j
hh
=7.1hz,12h,-ch2n),3.77(s,12h,c
04-ch
2-),6.91(d,3j
hh
=8.4hz,12h,c
02
h),7.22(d,3j
hh
=8.5hz,12h,c
03
h).
[1059]
13
c-{1h}rmn(75mhz,cd2cl2)δ
‘
(ppm):13.88(s,ch
3-),22.68(s,-ch
2-),27.41(s,-ch
2-),29.33(s,-ch
2-),29.60(s,-ch
2-),30.11(s,-ch
2-),31.88(s,-ch
2-),49.55(s,-ch
2-),53.31(s,-ch
2-),115.12
–
124.47(m,c
02
),129.03(s,c
03
),137.59(s,c
04
),149.37(dd,2j
cp
=5.1,4j
cp
=2.5hz,c
01
).
[1060]
利用5-g
’”0合成化合物5-g1[1061]
[化学式73]
[1062][1063]-70℃下,在30分钟内向pscl3(4ml,39.36mmol)的dcm(100ml)溶液中逐滴加入树枝状大分子5-g
’”0(1g,0.64mmol)的dcm溶液(40ml),其中存在et3n(0.81ml,5.84mmol)。搅拌过夜后,对反应混合物减压浓缩至干。然后将粗残余物溶于200ml的dcm,再经硅胶过滤,得到透明油状的树枝状大分5-g1,产率25%。
[1064]
31
p-{1h}rmn(162mhz,cd2cl2)δ(ppm):8.42(s,p=n),63.04(s,ps).
[1065]1h rmn(400mhz,cd2cl2)δ(ppm):0.91(t,3j
hh
=6.7hz,18h,-ch3),1.14
–
1.40(m,72h,-ch
2-),1.59
–
1.68(m,24h,-ch
2-),3.00
–
3.50(m,12h,-ch
2-n),4.67(d,3j
hp
=17.0hz,12h,c
04-ch
2-),7.02(d,3j
hh
=8.3hz,12h,c
02
h),7.29(d,3j
hh
=8.4hz,12h,c
03
h).
[1066]
利用5-g1合成化合物5-g
’1(ome)
[1067]
[化学式74]
[1068][1069]
向化合物5-g1(1mmol)的thf(30ml)溶液中,其中含cs2co3(24mmol),加入衍生自酪胺的苯酚氨基双亚甲基膦酸酯(参见wo2005/052031a1)(12mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。粗残余物用最少量的thf稀释,然后用大量乙醚洗涤。减压干燥后,得到透明油状的树枝状大分子5-g
’1(ome),产率是可定量的。
[1070]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.22(s,p=n),26.89(s,pome),68.01(s,ps)。
[1071]1h rmn(400mhz,cdcl3)δ(ppm):0.83(t,3j
hh
=7.0hz,18h,ch3),1.01
–
1.41(m,60h,ch2),1.45(br s,12h,ch2),2.77(t,3j
hh
=7.5hz,24h,c
14-ch
2-),3.06(t,3j
hh
=7.7hz,24h,
ch2n),3.09
–
3.15(m,12h,ch2nps),3.20(d,2j
hp
=9.3hz,48h,ch2p),3.74(d,3j
hp
=10.6,1.5hz,72h,pome),3.75(d,3j
hp
=10.6,1.5hz,72h,pome),4.55(d,3j
hp
=13.1hz,12h,c
04-ch
2-),6.96(d,3j
hh
=8.2hz,12h,c
02
h),7.02
–
7.12(m,24h,c
12
h),7.18(d,3j
hh
=8.5hz,24h,c
13
h),7.24(d,3j
hh
=8.4hz,12h,c
03
h).
[1072]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):14.11(s,ch3),22.61(s,ch2),26.81(s,ch2),27.62(s,ch2),29.18(s,ch2),31.72(s,ch2),33.07(s c
14-ch
2-),45.74(br s,ch2ns),49.45(dd,1j
cp
=157.2,3j
cp
=7.1hz,ch2p),49.46(br s,c
04-ch
2-),52.59
–
52.71(m,pome),58.30(t,3j
cp
=7.7hz,ch2n),120.90(s,c
02
h),121.02(d,2j
cp
=4.7hz,c
02
h),129.39(s,c
03
h),129.77(s,c
13
h),134.28(s,c
04
),136.09(s,c
14
),149.54(d,2j
cp
=7.8hz,c
11
),150.00(d,2j
cp
=4.5hz,c
01
).
[1073]
树枝状大分子5-g
’1(ome)的结构如[图12]所示。
[1074]
利用5-g
’1(ome)合成化合物5-g
’1(oh)
[1075]
[化学式75]
[1076][1077]
在0℃,向树枝状大分子5-g1(ome)(1g,0.15mmol)的无水ch3cn(30ml)溶液中加入brtms(1.22,9mmol)。搅拌过夜后,对混合物减压浓缩至干。残余物在meoh(10ml)中搅拌一小时,然后用meoh(20ml)洗涤2次,再用et2o(20ml)洗涤1次。得到的固体物减压至干,得到白色粉末状的树枝状大分子5-g
’1(oh),产率是可定量的。
[1078]
31
p-{1h}rmn(162mhz,d2o)δ(ppm):7.19(sl,poh).
[1079]
树枝状大分子5-g
’1(oh)的结构如[图13]所示。
[1080]
化合物5-g
’1(oh)随后被转化为5-g
’1(ona)。
[1081]
利用5-g
’1(oh)合成化合物5-g
’1(ona)
[1082]
[化学式76]
[1083][1084]
在搅拌下,向5-g
’1(oh)的水混悬液中加入24倍量的0.1m的naoh水溶液。剩余溶液经0.4μμ微过滤器过滤,然后冻干,得到白色粉末状化合物5-g
’1(ona),产率85%。
[1085]
31
p-{1h}rmn(243mhz,d2o)δ(ppm):6.64(s,n=p),9.50(s,po),68.66(s,ps).
[1086]
树枝状大分子5-g
’1(ona)的结构如[图14]所示。
[1087]
半内敛法合成带有双膦酸盐末端的1代树枝状大分子
[1088]
示意图4描述了半内敛法合成带有双膦酸盐末端的1代树枝状大分子的反应示意图:
[1089]
[示意图4]
[1090][1091]
化合物3a
[1092]
[化学式77]
[1093][1094]
向4-((四氢-2h-吡喃-2-基)氧基)苯甲醛(fu h.等人,molecules,2014年第16期,17715-17726页)(1g,4.83mmol)的thf(30ml)溶液中,加入甲胺溶液(8m甲胺的etoh溶液)(1.8ml,14.49mmol)。室温下搅拌过夜后,对混合物浓缩至干,得到无色油状的产物3a,产率95%。
[1095]1h rmn(300mhz,cd3od)δ(ppm):1.39
–
1.74(m,3h,-ch
2-),1.75
–
1.92(m,2h,-ch
2-),1.90
–
2.06(m,1h,-ch
2-o),3.55
–
3.62(m,1h,-ch
2-o),3.79
–
3.87(m,1h,-ch
2-),5.46(t,3j
hh
=3.1hz,1h,o-ch-o),7.08(d,3j
hh
=8.8hz,2h,c
02
h),7.63(d,3j
hh
=8.8hz,2h,c
03
h),8.21(q,4j
hh
=1.6hz,1h,-ch=n-).
[1096]
13
c-{1h}rmn(75mhz,cd3od)δ(ppm):18.46(s,-ch
2-),24.89(s,-ch
2-),29.95(s,-ch
2-),46.32(s,ch
3-),61.73(s,-ch
2-o),96.10(s,-ch-o),116.17(s,c
02
),129.22(s,c
04
),129.30(s,c
03
),159.41(s,c
04
),163.46(s,c=n).
[1097]
化合物3b
[1098]
[化学式78]
[1099][1100]
在一只fisher porter试管中,加入化合物3a溶液(1g,4.5mmol)、10%pd/c(225mg)和meoh(40ml)。对试管缓慢抽真空以排出空气。然后将h2压力调至5bar。反应混合物在室温下搅拌2小时。缓慢减压后,回收反应混合物,过滤并减压浓缩。残余物经硅胶色谱法纯化(洗脱液:acoet),得到透明油状的化合物3b,产率80%。
[1101]1h rmn(300mhz,cdcl3)δ(ppm):1.33
–
1.72(m,3h,-ch
2-),1.77
–
1.82(m,2h,-ch
2-),1.87
–
2.07(m,1h,-ch
2-o),2.36(s,3h,ch3),3.50
–
3.57(m,1h,-ch
2-o),3.61(s,2h,-ch
2-n),3.76
–
3.99(m,1h,-ch
2-),5.34(t,3j
hh
=3.3hz,1h,o-ch-o),6.96(d,3j
hh
=8.6hz,2h,c
02
h),7.09
–
7.26(m,2h,c
02
h).
[1102]
13
c-{1h}rmn(75mhz,cdcl3)δ(ppm):18.78(s,-ch
2-),25.16(s,-ch
2-),30.33(s,-ch
2-),35.63(s,-ch3),55.31(s,-ch
2-n),61.96(s,-ch
2-o),96.38(s,o-ch-o),116.36(s,c
02
),129.25(s,c
03
),132.78(s,c
03
),156.12(s,c
04
).
[1103]
化合物4b
[1104]
[化学式79]
[1105][1106]
向4-((四氢-2h-吡喃-2-基)氧基)苯甲醛(1g,4.83mmol)的thf(30ml)溶液中加入1-氨基己烷(1.9ml,14.49mmol)。在室温下搅拌过夜后,对混合物减压蒸发至干。在一只fisher porter试管中,加入得到的残余物、10%pd/c(241mg)和meoh(40ml)。对试管缓慢抽真空下以排出氧气。然后将h2压力调至5bar。反应混合物在室温下搅拌2小时。缓慢减压后,回收反应混合物,过滤并减压浓缩。残余物经硅胶色谱法纯化(洗脱液:acoet),得到透明油状的化合物4b,产率70%。
[1107]1h rmn(300mhz,cdcl3)δ(ppm):0.76
–
1.05(m,3h,-ch3),1.17
–
1.43(m,3h,-ch
2-),1.43
–
1.59(m,3h,-ch
2-),1.59
–
1.76(m,3h,-ch
2-),1.75
–
1.95(m,3h,-ch
2-),1.90
–
2.04(m,3h,-ch
2-),2.61(t,3j
hh
=7.1hz,2h,-ch2n),3.56
–
3.63(m,1h,-ch
2-o),3.72(s,2h,c
04-ch
2-),3.88
–
3.96(m,1h,-ch
2-o),,5.40(t,3j
hh
=3.3hz,1h,o-ch
2-o),7.01(d,3j
hh
=8.6hz,2h,c
02
h),7.23(d,3j
hh
=8.6hz,2h,c
03
h).
[1108]
13
c-{1h}rmn(75mhz,cdcl3)δ(ppm):14.04(s,ch
3-),18.82(s,-ch
2-),22.62(s,-ch
2-),25.24(s,-ch
2-),27.06(s,-ch
2-),30.09(s,-ch
2-),30.39(s,-ch
2-),31.80(s,-ch
2-),49.46(s,-ch
2-),53.54(s,-ch2n),61.97(s,-ch
2-o),96.41(s,o-ch-o),116.36(s,c
02
),129.12(s,c
03
),133.72(s,c
04
),156.01(s,c
01
).
[1109]
化合物5b
[1110]
[化学式80]
[1111][1112]
向4-((四氢-2h-吡喃-2-基)氧基)苯甲醛(1g,4.83mmol)的thf(30ml)溶液中加入1-氨基己烷(2.4ml,14.49mmol)。在室温下搅拌过夜后,对混合物减压蒸发至干。在一只fisher porter试管中,加入得到的残余物、10%pd/c(241mg)和meoh(40ml)。对试管缓慢抽真空下以排出氧气。然后将h2压力调至5bar。反应混合物在室温下搅拌2小时。缓慢减压后,回收反应混合物,过滤并减压浓缩。残余物经硅胶色谱法纯化(洗脱液:acoet),得到透明油状的化合物5b,产率76%。
[1113]1h rmn(400mhz,cdcl3)δ(ppm):0.90(t,3j
hh
=6.8hz,3h,-ch3),1.28
–
1.34(m,10h,-ch
2-),1.45
–
1.53(m,3h,-ch
2-),1.54
–
1.79(m,2h,-ch
2-),1.85
–
1.90(m,2h,-ch
2-),1.97
–
2.15(m,1h,-ch
2-),2.62(t,3j
hh
=7.1hz,2h,-ch2n),3.59
–
3.64(m,1h,-ch
2-o),3.74(s,ch
2-c
04
),3.91
–
3.97(m,1h,-ch
2-o),5.42(t,3j
hh
=3.4hz,1h,-ch-o),7.02(d,3j
hh
=8.6hz,2h,c
02
h),7.24(d,3j
hh
=8.5hz,1h,c
03
h).
[1114]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):14.11(s,ch
3-),18.85(s,-ch
2-),22.67(s,-ch
2-),25.24(s,-ch
2-),27.40(s,-ch
2-),29.28(s,-ch
2-),29.55(s,-ch
2-),30.12(s,-ch
2-),30.41(s,-ch
2-),31.84(s,-ch
2-),49.47(s,-ch
2-),53.56(s,-ch2n),62.04(s,-ch2o),96.45(s,o-ch-o),116.39(s,c
02
),129.18(s,c
02
),133.70(s,c
04
),156.02(s,c
01
).
[1115]
化合物3c
[1116]
[化学式81]
[1117][1118]
在30分钟内,向pscl3(2.2ml,22.6mmol)的dcm(100ml)溶液中逐滴加入树枝状大分子3b(1g,4.52mmol)的dcm溶液(40ml),其中存在et3n(0.62ml,4.52mmol)。室温下搅拌4小时后,对反应混合物减压浓缩至干。然后将粗残余物溶于200ml的dcm,再经硅胶过滤,得到透明油状的化合物3c,产率85%。
[1119]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):63.18(s,ps).
[1120]
化合物4c
[1121]
[化学式82]
[1122][1123]-70℃下,在30分钟内向pscl3(1.73ml,17.18mmol)的dcm(100ml)溶液中逐滴加入树枝状大分子4b(1g,3.43mmol)的dcm(40ml)溶液,其中存在et3n(0.47ml,3.43mmol)。搅拌过夜后,对反应混合物减压浓缩至干。然后将粗残余物溶于200ml的dcm,再经硅胶过滤,得到透明油状的树枝状大分4c,产率73%。
[1124]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):63.01(s,ps).
[1125]1h rmn(400mhz,cdcl3)δ(ppm):0.79
–
0.98(m,3h,-ch3),1.15
–
1.33(m,6h,-ch
2-),1.54
–
1.75(m,5h,-ch
2-),1.82
–
1.93(m,2h,-ch
2-),1.95
–
2.06(m,1h,-ch
2-),3.20
–
3.36(m,2h,-ch
2-n),3.56
–
3.68(m,1h,-ch
2-o),3.88
–
3.94(m,1h,-ch
2-o),4.57(d,3j
hp
=16.1hz,2h,c
04-ch
2-),5.41(t,3j
hh
=3.4hz,1h,o-ch-o),7.04(d,3j
hh
=8.6hz,2h,c
02
h),7.25(d,3j
hh
=8.6hz,1h,c
03
h).
[1126]
化合物5c
[1127]
[化学式83]
[1128][1129]-70℃下,在30分钟内向pscl3(1.58ml,15.67mmol)的dcm(100ml)溶液中逐滴加入树枝状大分子5b(1g,3.13mmol)的dcm(40ml)溶液,其中存在et3n(0.43ml,3.13mmol)。搅拌过夜后,对反应混合物减压浓缩至干。然后将粗残余物溶于200ml的dcm,再经硅胶过滤,得到透明油状的化合物4c,产率70%。
[1130]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):62.92(s,ps).
[1131]1h rmn(400mhz,cdcl3)δ(ppm):0.90(t,3j
hh
=6.9hz,3h),1.16
–
1.42(m,10h,-ch
2-),1.52
–
1.78(m,5h,-ch
2-),1.85
–
1.96(m,2h,-ch
2-),1.99
–
2.09(m,1h,-ch
2-),3.21
–
3.32(m,2h,-ch
2-n),3.57
–
3.71(m,1h,-ch
2-o),3.90
–
3.96(m,1h,-ch
2-o),4.59 3jhp
=16.1hz,2h,c
04-ch
2-),5.43(t,3j
hh
=3.3hz,1h,o-ch
2-o),7.06(d,3j
hh
=8.6hz,2h,c
02
h),7.27(d,3j
hh
=8.5hz,2h,c
02
h).
[1132]
化合物3d
[1133]
[化学式84]
[1134][1135]
向化合3c(1mmol)的thf(30ml)溶液中,其中含cs2co3(4mmol),加入衍生自酪胺的苯酚氨基双亚甲基膦酸酯(参见wo2005/052031a1)(2mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。然后利用洗脱液混合物(meoh/etoac),通过硅胶色谱法纯化粗残余物,减压除去溶剂后,得到透明油状的化合物3d,产率85%。
[1136]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):26.95(s,pome),68.48(s,p=n).
[1137]1h rmn(400mhz,cdcl3)δ(ppm):1.58
–
1.72(m,3h,-ch2),1.81
–
1.94(m,2h,-ch
2-),1.96
–
2.05(m,1h,-ch
2-),2.78
–
2.83(m,7h,c
14-ch2,ch3n-),3.09(t,3j
hh
=7.6hz,4h,-ch2n-),3.22(d,3j
hh
=8.9hz,8h,),3.55
–
3.67(m,1h,ch
2-o),3.75(d,3j
hp
=10.3hz,24h,pome),3.89
–
3.95(m,1h,ch
2-o),4.44(d,3j
hp
=12.0hz,2h),5.41(t,3j
hh
=3.3hz,1h,o-ch
2-o),6.99(d,3j
hh
=8.6hz,2h,c
02
h),7.12(d,3j
hh
=8.4,4h,c
12
h),7.16
–
7.25(m,6h,c
03
h,c
13
h).
[1138]
化合物4d
[1139]
[化学式85]
[1140][1141]
向化合物4c(1mmol)的thf(30ml)溶液中,其中含cs2co3(4mmol),加入衍生自酪胺的苯酚氨基双亚甲基膦酸酯(参见wo2005/052031a1)(2mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。然后利用洗脱液混合物(meoh/etoac),通过硅胶色谱法纯化粗残余物,减压除去溶剂后,得到透明油状的化合物4d,产率81%。
[1142]
31
p-{1h}rmn(121mhz,cdcl3)δ(ppm):26.60(s,pome),67.70(s,ps).
[1143]
化合物5d
[1144]
[化学式86]
[1145]
[1146]
向化合物5c(1mmol)的thf(30ml)溶液中,其中含cs2co3(4mmol),加入衍生自酪胺的苯酚氨基双亚甲基膦酸酯(参见wo2005/052031a1)(2mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。然后利用洗脱液混合物(meoh/etoac),通过硅胶色谱法纯化粗残余物,减压除去溶剂后,得到透明油状的化合物5d,产率75%。
[1147]
31
p-{1h}rmn(121mhz,cdcl3)δ(ppm):26.92(s,pome),68.02(s,ps).
[1148]
化合物3e
[1149]
[化学式87]
[1150][1151]
向化合物3d(1mmol)的meoh(30ml)溶液中加入甲基苯磺酸吡啶鎓(1.5mmol)。反应混合物在室温下搅拌过夜。减压除去溶剂,残余物经硅胶色谱法纯化(洗脱液:meoh/acoet),减压除去溶剂后得到透明油状的化合物3e,产率80%。
[1152]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):26.76(s,pome),68.38(s,ps).
[1153]
化合物4e
[1154]
[化学式88]
[1155][1156]
向化合物4d(1mmol)的meoh(30ml)溶液中加入甲基苯磺酸吡啶鎓(1.5mmol)。反应混合物在室温下搅拌过夜。减压除去溶剂,残余物经硅胶色谱法纯化(洗脱液:meoh/acoet),减压除去溶剂后得到透明油状的化合物3e,产率78%。
[1157]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):26.70(s,pome),68.2(s,ps).
[1158]1h rmn(300mhz,cdcl3)δ(ppm):0.74
–
0.91(m,3h,ch
3-),1.11
–
1.39(m,6h,-ch
2-),1.58(br s,2h,-ch
2-),2.75(t,3j
hh
=7.8hz,4h,c
14-ch
2-),2.91
–
3.17(m,6h,-ch2n-,-ch2n-),3.74(d,3j
hp
=10.6,12h,pome),3.75(d,3j
hp
=10.6,12h,pome),4.38(d,3j
hh
=14.1hz,2h,c
04-ch
2-),6.61(d,3j
hh
=8.5hz,2h,c
02
h),6.70(d,3j
hh
=8.6hz,2h,c
03
h),6.91
–
7.21(m,8h,c
12
h,c
13
h),8.80(s,1h,oh).
[1159]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):13.99(s,ch
3-),22.57((s,-ch
2-),26.57(s,ch
2-),27.00(s,ch
2-),31.50(s,ch
2-),33.20(s,ch
2-),44.66(br s,ch
2-np),48.96(d,2j
cp
=8.3hz,c
04-ch
2-),49.51(dd,1j
cp
=157.7,2j
cp
=7.3hz,-ch
2-p),52.78(m,poch3),58.38(t,3j
cp
=7.4hz,-ch
2-n),114.87(s,c
02
),121.33(d,3j
cp
=4.8hz,c
12
),127.57(d,3j
cp
=3.5hz,c
04
),129.64(s,c
13
),129.76(s,c
03
),135.73(s,c
14
),149.33(d,2j
hp
=7.2hz,c
11
),156.70(s,c
01
).
[1160]
化合物5e
[1161]
[化学式89]
[1162][1163]
向化合物5d(1mmol)的meoh(30ml)溶液中加入甲基苯磺酸吡啶鎓(1.5mmol)。反应混合物在室温下搅拌过夜。减压除去溶剂,残余物经硅胶色谱法纯化(洗脱液:meoh/acoet),减压除去溶剂后得到透明油状的化合物5e,产率82%。
[1164]
31
p-{1h}rmn(121mhz,cdcl3)δ(ppm):26.72(s,pome),68.41(s,ps).
[1165]
利用3e合成化合物3-g
’1(ome)
[1166]
[化学式62]
[1167][1168]
向化合物3e(1g,1.04mmol)的thf(30ml)溶液中,其中含cs2co3(794mg,2.08mmol),加入六氯环三磷腈(60mg,0.17mmol)。在45℃下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。得到透明油状的树枝状大分子3-g
’1,产率90%。
[1169]
31
p-{1h}rmn(243mhz,cdcl3)δ(ppm):8.40(s,n=p),26.85(s,po),68.32(s,ps);
[1170]1h rmn(600mhz,cdcl3)δ(ppm):2.75(d,3j
hh
=10.1hz,24h,c
14-ch2),2.77(d,3j
hp
=7.6hz,18h,ch3),3.06(d,3j
hh
=7.7hz,24h,c
14-ch
2-ch2),3.19(d,2j
hp
=9.4hz,48h,ch
2-p),3.73(d,3j
hp
=10.6hz,144h,pome),6.94(d,3j
hh
=8.2hz,12h,c
02
h),7.07(d,3j
hh
=8.1hz,24h,c
12
h),7.18(br d,3j
hh
=8.2hz,36h,c
03 and c
13
h);
[1171]
13
c-{1h}rmn(151mhz,cdcl3)δ(ppm):33.05(s,ch2),33.64s,(ch3n),49.46(dd,1j
cp
=157.3,3j
cp
=7.2hz,ch
2-p),53.56-51.75(m,poch3),53.47(d,2j
cp
=10.3hz,c
14-ch2),58.22(t,3j
cp
=7.7hz,c
14-ch
2-ch2),120.91(br d,3j
cp
=4.4hz,c
02 and c
12
),129.30(s,c
03
),129.87(s,c
13
),134.10(br d,2j
cp
=4.5hz,c
04
),136.22(s,c
14
),149.35(d,2j
cp
=7.5hz,c
11
),150.01(br s,c
01
).
[1172]
利用4e合成化合物4-g
’1(ome)
[1173]
[化学式68]
[1174][1175]
向化合物4e(1g,0.97mmol)的thf(30ml)溶液中,其中含cs2co3(632mg,1.94mmol),加入六氯环三磷腈(56mg,0.16mmol)。在45℃下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。得到透明油状的树枝状大分子4-g
’1,产率85%。
[1176]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.23(s,p=n),26.89(s,pome),68.00(s,ps).
[1177]1h rmn(400mhz,cdcl3)δ(ppm):0.78(t,3j
hh
=6.6hz,18h,ch
3-),1.10
–
1.26(m,36h,-ch
2-),1.41
–
1.47(m,12h,-ch
2-),2.75(t,3j
hh
=7.6hz,24h,-ch
2-c
14
),3.04(t,3j
hh
=7.7hz,24h,-ch
2-n),3.09
–
3.15(m,12h,-ch
2-np),3.19(d,2j
hp
=9.3hz,18h,-ch
2-p),3.65
–
3.79(m,144h,pome),4.53(d,3j
hp
=13.1hz,12h,-ch
2-c
04
),6.95(d,3j
hh
=8.1hz,12h,c
02
h),7.06(d,3j
hh
=8.2hz,24h,c
12
h),7.16(d,3j
hh
=8.2hz,24h,c
12
h),7.22(d,3j
hh
=8.3hz,24h,c
03
h).
[1178]
利用5e合成化合物5-g
’1(ome)
[1179]
[化学式74]
[1180][1181]
向化合物5e(1g,0.94mmol)的thf(30ml)溶液中,其中含cs2co3(616mg,1.9mmol),加入六氯环三磷腈(54mg,0.15mmol)。在45℃下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。得到透明油状的树枝状大分子5-g
’1,产率88%。
[1182]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.22(s,p=n),26.89(s,pome),68.01(s,ps)。
[1183]1h rmn(400mhz,cdcl3)δ(ppm):0.83(t,3j
hh
=7.0hz,18h,ch3),1.01
–
1.41(m,60h,ch2),1.45(br s,12h,ch2),2.77(t,3j
hh
=7.5hz,24h,c
14-ch
2-),3.06(t,3j
hh
=7.7hz,24h,ch2n),3.09
–
3.15(m,12h,ch2nps),3.20(d,2j
hp
=9.3hz,48h,ch2p),3.74(d,3j
hp
=10.6,1.5hz,72h,pome),3.75(d,3j
hp
=10.6,1.5hz,72h,pome),4.55(d,3j
hp
=13.1hz,12h,c
04-ch
2-),6.96(d,3j
hh
=8.2hz,12h,c
02
h),7.02
–
7.12(m,24h,c
12
h),7.18(d,3j
hh
=8.5hz,24h,c
13
h),7.24(d,3j
hh
=8.4hz,12h,c
03
h).
[1184]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):14.11(s,ch3),22.61(s,ch2),26.81(s,ch2),
27.62(s,ch2),29.18(s,ch2),31.72(s,ch2),33.07(s c
14-ch
2-),45.74(br s,ch2ns),49.45(dd,1j
cp
=157.2,3j
cp
=7.1hz,ch2p),49.46(br s,c
04-ch
2-),52.59
–
52.71(m,pome),58.30(t,3j
cp
=7.7hz,ch2n),120.90(s,c
02
h),121.02(d,2j
cp
=4.7hz,c
02
h),129.39(s,c
03
h),129.77(s,c
13
h),134.28(s,c
04
),136.09(s,c
14
),149.54(d,2j
cp
=7.8hz,c
11
),150.00(d,2j
cp
=4.5hz,c
01
).
[1185]
半内敛法合成带有双官能1代树枝状大分子
[1186]
示意图5描述了半内敛法合成双官能1代树枝状大分子的反应示意图:
[1187]
[示意图5]
[1188][1189]
合成化合物7a、7b、7c
[1190]
向(4-甲酰基苯基)碳酸叔丁酯(5mmol)的dcm(50ml)溶液中加入化合物6a、b或c(5.25mmol)。在室温下搅拌过夜后,反应结束。化合物7a、b或c未经分离直接用于后续操作。
[1191]
表征化合物7a:
[1192]
[化学式90]
[1193][1194]1h rmn(400mhz,cd3cn)δ(ppm)1.39(s,9h boc-nh),1.55(s,9hboc-o),3.34(q,3j
hh
=6.1hz,2h,ch2nhboc),3.65(m,2h,ch=n-ch2),5,42(s,nhboc)7.25(d,3j
hh
=8.6hz,2h,c02
h),7.80(d,3j
hh
=8.6hz,2h,c
03
h),8.30(s,1h,ch=n).
[1195]
表征化合物7b:
[1196]
[化学式91]
[1197][1198]1h rmn(400mhz,cd2cl2)δ(ppm)1.45(s,9h,boc-nh),1.57(s,9h,boc-oph),3.21(q,3j
hh
=6.3hz,2h,ch2nhboc),3.47
–
3.75(m,2h,ch=n-ch2),7.23(d,3j
hh
=8.7hz,2h,c
02
h),7.78(d,3j
hh
=8.6hz,2h,c
03
h),8.32(s,1h,hc=n).
[1199]
表征化合物7c:
[1200]
[化学式92]
[1201][1202]
化合物7c直接用于后续步骤。
[1203]
合成化合物8a、8b、8c
[1204]
在5bar的氢气环境下,向化合物7a、b、c(5mmol)的无水乙醇(50ml)溶液中入10%的pd/c(250mg)。在室温下搅拌1.5小时后,反应结束。然后通过硅胶纯化化合物8a、b、c,其中洗脱液梯度dcm/meoh,产率70%至80%。
[1205]
表征化合物8a:
[1206]
[化学式93]
[1207][1208]1h rmn(400mhz,cdcl3)δ(ppm)1.45(s,4h),1.56(s,2h),2.74(t,j=5.8hz,1h),3.19
–
3.27(m,3h),3.77(s,1h),5.01(s,1h),7.12(d,3j
hh
=9.5hz,0h),7.31(d,3j
hh
=8.3hz,1h).
[1209]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm)27.69(s,boc-o-ph),28.41(s,boc-nh),48.45(s,n0ch2ch2),52.82(s,ch2ch2nhboc),79.33(sl,nhcoc(ch3)3),83.50(s,ococ(ch3)3),121.21(s,c
02
),129.03(s,c
03
),137.58(s,c
04
),150.05(s,c
01
),151.96(s,oc(o)coc(ch3)3),156.19(s,nhc(o)coc(ch3)3).
[1210]
表征化合物8b:
[1211]
[化学式94]
[1212][1213]1h rmn(300mhz,cd2cl2)δ(ppm):1.51(m,26h,ch2ch2ch2ch2,boc-o,boc-nh),2.63(t,j=7.1hz,2h,n0ch2),3.09(q,j=6.8hz,2h,ch2nhboc),3.80(s,2h,c
04
ch2),4.83(s,1h,nhboc),7.12(d,3j
hh
=8.5hz,2h,c
02
h),7.37(d,3j
hh
=8.5hz,2h,c
03
h).
[1214]
表征化合物8c:
[1215]
[化学式95]
[1216][1217]1h rmn(300mhz,cdcl3)δ(ppm):1.43(s,9h,nhboc),1.55(s,9h,nhboc),1.65
–
1.92(m,4h,n0ch2ch2,ch2ch2nhboc),2.45(s,nh),2.73(t,3j
hh
=6.8hz,2h,n0ch2),3.21(q,3j
hh
=5.3hz,2h,ch2nhboc),3.38
–
3.70(m,12h,ch2o),3.78(s,2h,c
04
ch2),5.13(s,1h,nhboc),7.11(d,3j
hh
=8.5hz,2h,c
02
h),7.33(d,3j
hh
=8.1hz,2h,c
03
h).
[1218]
合成化合物9a、9b、9c
[1219]
在30分钟内,向带有分子筛的pscl3(12mmol)的ch2cl2(100ml)溶液中,逐滴加入化合物8a、b、c(4mmol)的含et3n(
6mm
ol)的ch2cl2(30ml)溶液。室温下搅拌2到12小时后,将混合物减压浓缩至干。然后通过硅胶纯化粗残余物,其中洗脱液梯度为100
→
98/2dcm/thf,得到透明油状的化合物9a、b、c,产率70-85%。
[1220]
表征化合物9a:
[1221]
[化学式96]
[1222][1223]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):64.17.
[1224]1h rmn(400mhz,cdcl3)δ(ppm):1.46(s),1.58(s),3.20
–
3.61(m),4.68(d,j=15.3hz),7.20(d,j=8.5hz),7.41(d,j=8.1hz).
[1225]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):27.69,28.40,37.42,46.47,50.11,79.77,83.82,121.78,129.35,132.41(d,j=5.6hz),150.96,151.74,155.80.
[1226]
表征化合物9b:
[1227]
[化学式97]
[1228][1229]1h rmn(400mhz,cd2cl2)δ(ppm):1.23
–
1.38(m),1.45(s),1.57(s),1.60
–
1.78(m),3.08(q,j=6.6hz),3.20
–
3.43(m),4.68(d,j=16.6hz),7.20(d,j=8.5hz),7.41(d,j=8.5hz).
[1230]
31
p-{1h}rmn(162mhz,cd2cl2)δ(ppm):63.16.
[1231]
13
c-{1h}rmn(101mhz,cd2cl2)δ(ppm):26.25(d,j=4.5hz),26.85(d,j=3.1hz),27.41,28.14,29.89,40.32,47.40(d,j=2.4hz),50.21(d,j=4.5hz),78.56,83.49,121.66,129.05,133.15(d,j=5.5hz),150.89,151.69,155.76.
[1232]
表征化合物9c:
[1233]
[化学式98]
[1234][1235]1h rmn(300mhz,cdcl3)δ(ppm):1.45(s),1.58(s),1.76(p,j=6.2hz),1.85
–
1.99(m),3.10
–
3.29(m),3.31
–
3.76(m),4.66(d,j=16.5hz),4.97(s),7.19(d,j=8.6hz),7.38(d,j=8.5hz).
[1236]
31
p-{1h}rmn(121mhz,cdcl3)δ(ppm):63.07.
[1237]
合成化合物10a、10b、10c
[1238]
向化合物9a、b、c(4mmol)的thf(30ml)溶液中,依次加入cs2co3(16.4mmol)和衍生自酪胺的苯酚氨基双亚甲基膦酸酯(8.2mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。然后通过硅胶色谱柱(洗脱液梯度为2.5/97.5-5/95meoh/dcm)纯化产物,得到透明油状的化合物10a、b、c,产率60-80%。
[1239]
表征化合物10a:
[1240]
[化学式99]
[1241][1242]
31
p-{1h}rmn(162mhz,c6d6)δ(ppm):26.67(s,pome),68.58(s,ps).
[1243]
表征化合物10b:
[1244]
[化学式100]
[1245][1246]
31
p-{1h}rmn(121mhz,cdcl3)δ(ppm):26.70(s,pome),68.65(s,ps).
[1247]
表征化合物10c:
[1248]
[化学式101]
[1249][1250]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):26.68(s,pome),68.80(s,ps).
[1251]
合成化合物11a、11b、11c
[1252]
向化合物10(mmol)的meoh(10ml)溶液中加入过量的甲胺的etoh(8m)溶液。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。然后通过硅胶色谱柱(洗脱液梯度为2.5/97.5-5/95meoh/dcm)纯化产物,得到透明油状的化合物11,产率80%。
[1253]
表征化合物11a:
[1254]
[化学式102]
[1255][1256]
31
p-{1h}rmn(121mhz,cdcl3)δ(ppm):26.68,68.75.
[1257]
表征化合物11b:
[1258]
[化学式103]
[1259]
[1260]
31
p-{1h}rmn(121mhz,cdcl3)δ(ppm):26.68,68.75.
[1261]
表征化合物11c:
[1262]
[化学式104]
[1263][1264]
31
p-{1h}rmn(121mhz,cdcl3)δ(ppm):26.71,68.80.
[1265]
合成化合物11a-g1(nhboc)、11b-g1(nhboc)和11c-g1(nhboc)
[1266]
向n3p3cl6(0,1mmol)的thf溶液中加入化合物11a、b、c(0.72mmol)和碳酸铯(1.45mmol)。在40℃的温度下搅拌过夜后,对混合物离心、过滤,减压浓缩。然后通过硅胶色谱法纯化产物,得到透明油状的化合物11a、b、c-g1(nhboc)。产率为60%到80%。
[1267]
表征化合物11a-g1(nhboc):
[1268]
[化学式105]
[1269][1270]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.08(s,p0),26.88(s,pome),68.56(s,p1).
[1271]1h rmn(400mhz,cdcl3)δ(ppm):1.37(s,54h,nhboc),2.66
–
2.88(m,c
14
ch2,24h),3.00
–
3.11(m,c
14
ch
2 ch2,24h),3.21(m,60h,ch2pome,ch2nhboc),3.28
–
3.37(m,n0ch2),3.75(d,3j
hp
=10.6hz,144h,pome),4.58(d,3j
hp
=12.1hz,12h,c
04
ch2),5.09(s,6h,nhboc),6.97(d,3j
hh
=8.2hz,12h,c
02
),7.08(d,3j
hh
=7.1hz,24h,c
12
),7.18(d,3j
hh
=8.4hz,24h,c
13
),7.26(d,3j
hh
=8.4hz,12h,c
03
).
[1272]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):28.41(s,boc),33.06(s,c
14
ch2)38,23(s,nch2ch2),45,25(s,nch2ch2),48.66(dd,1j
cp
=157.2,3j
cp
=7.1hz,ch2pome),49,57(sl,c
04
ch2),52.29
–
53.00(m,pome),58.27(t,3j
cp
=7,7hz,c
14
ch2ch2),79.11(s,oc(ch3)3),120.96(s,c
02
),121.14(d,3j
cp
=4.5hz,c
12
),129.69(s,c
03
),129.83(s,c
13
),133.89(s,c
04
),136.31(s,c
14
),149.37(d,2j
cp
=7.9hz,c
11
),150.19(s,c
01
),155.86(s,c=o).
[1273]
表征化合物11b-g1(nhboc):
[1274]
[化学式106]
[1275][1276]
31
p-{1h}rmn(162mhz,meod)δ(ppm):8.92年第27.42期,68.63页。
[1277]
表征化合物11c-g1(nhboc):
[1278]
[化学式107]
[1279][1280]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.11(s,p0),26.87(s,pome),68.15(s,p1).
[1281]1h rmn(400mhz,cdcl3)δ(ppm):1.41(s,54h,nhboc),1.59
–
1.82(m,24h,ch2ch2ch2),2.77(m,c
14
ch2,24h),3.05(t,3j
hh
=7.7hz,24h,c
14
ch2ch2),3.12
–
3.38(m,84h,nch2pome,ch2nhboc,n0ch2),3.41
–
3.64(m,60h,ch2o),3.74(3j
hp
=10.6hz,144h,pome),4.55(d,3j
hp
=12.1hz,12h,c
04
ch2),5.15(s,nhboc)6.95(d3j
hh
=8.2hz,12h,c
02
),7.06(d,3j
hh
=7.1hz,24h,c
12
),7.17(d,3j
hh
=8.4hz,24h,c
13
),7.24(d,3j
hh
=8.4hz,12h,c
03
).
[1282]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):27.98(bochnch2ch2ch2),28.45(s,boc),29.66(n0ch2ch2),33.03(s,c
14
ch2),38.42(s,n0ch2ch2),43.05(s,ch2nhboc),49.44(1j
cp
=157.4,3j
cp
=7.1hz,ch2pome),49,65(sl,c
04
ch2),52.33
–
52.97(m,pome),58.30(t,3j
cp
=7,7hz,c
14
ch2ch2),68.49(s,ch2o),69.43(s,ch2o),70.08(s,ch2o)70.12(s,ch2o),70.44(s,ch2o),70.49(s,ch2o),78.75(s,oc(ch3)3),120.88(s,c
02
),121.07(d,3j
cp
=4.7hz,c
12
),129.44(s,c
03
),129.80(s,c
13
),134.24(s,c
04
),136.16(s,c
14
),149.49(d,2j
cp
=7.9hz,c
11
),150.01(s,c
01
),156.04(s,c=o).
[1283]
合成化合物11a-g1(nh2)、11b-g1(nh2)和11b-g1(nh2)
[1284]
向化合物11a、b、c-g1(nhboc)的dcm(5ml)溶液中加入三氟乙酸(5ml)。搅拌10分钟后,将混合物蒸发至干,然后用3ml的dcm共蒸发5次,得到透明油状三氟乙酸盐形式的化合物11a、b、c-g1(nh2)。产率高于90%。
[1285]
表征化合物11a-g1(nh2):
[1286]
[化学式108]
[1287][1288]
31
p-{1h}rmn(243mhz,cd3cn)δ(ppm):8.74(s,p0),26.00(s,pome),68.65(s,p1).
[1289]1h rmn(600mhz,cd3cn)δ(ppm):2.81(t,3j
hh
=7.6hz,24h,c
14
ch2),2.92(m,12h,n0ch2),3.05(t,3j
hh
=7.7hz,24h,c
14
ch
2 ch2),3.26(d,2j
hp
=10.4hz,48h,ch2pome),3.49
–
3.56(m,12h,pnch2ch2nh
3+
),3.73(dd,2j
hp
=10.7,j=1.5hz,144h,pome),4.55(d,3j
hp
=12.8hz,12h,c
04
ch2),6.91(d,3j
hh
=8.3hz,12h,c
02
),7.11(d,3j
hh
=8.0hz,24h,c
12
),7.17
–
7.28(m,36h,c
13
,c
03
).
[1290]
13
c-{1h}rmn(151mhz,cd3cn)δ(ppm):31.38(s,c
14
ch2),37.34(s,nch2ch2),42.63(s,nch2ch2),48.66(dd,1j
cp
=157.2hz,3j
cp
=7.1hz,ch2pome),49.60(sl,c
04
ch2),53.01(d,2j
cp
=7.2hz,pome),58.10(t,3j
cp
=7,7hz,c
14
ch2ch2),115.13(q,1j
cf
=286.3hz,coocf3),120.81(s,c
02
),121.24(d,3j
cp
=4.5hz,c
12
),129.74(s,c
03
),130.10(s,c
13
),134.07(s,c
04
),136.98(s,c
14
),148.98(d,2j
cp
=7.9hz,c
11
),149.88(sl,c
01
),157.99(q,2j
cf
=40.1hz,coocf3).
[1291]
表征化合物11b-g1(nh2):
[1292]
[化学式109]
[1293][1294]
31
p-{1h}rmn(162mhz,cd3cn)δ(ppm):8.71,27.42,68.21.
[1295]
表征化合物11c-g1(nh2):
[1296]
[化学式110]
[1297]
[1298]1h rmn(400mhz,cd3cn)δ(ppm):1.73(m,12h,pnch2ch2),1.76
–
1.86(m,12h,ch2ch2nhboc),2.87(m,24h,c
14
ch2),3.03(m,12h,n0ch2ch2),3.13
–
3.22(m,24h,c
14
ch2ch2),3.31(m,24h,ch2o),3.38(m,12h,ch2ch2nhboc),3.42
–
3.65(m,ch2pome,och2ch2o,),3.79(d,2j
hp
=10.9hz,144h,pome),4.59(d,3j
hp
=12.8hz,12h,c
04
ch2),6.92(d,3j
hh
=8.3hz,12h,c
02
h),7.14(d,3j
hh
=7.8hz,24h,c
12
h),7.24(d,3j
hh
=8.4hz,24h,c
13
h),7.27
–
7.36(d,3j
hh
=8.3hz,12h,c
03
h).
[1299]
31
p-{1h}rmn(162mhz,cd3cn)δ(ppm):8.89(s,p0),24.44(s,pome),68.26(s,p1).
[1300]
合成化合物11a-g1(nh-nac)、11b-g1(nh-nac)和11c-g1(nhnac)
[1301]
向树枝状大分子11-g1(nh2)(0.05mmol)的dcm/thf混合物溶液中加入dipea,直至ph值为中性。然后得到(n-乙酰基-s-((3-((2,5-二氧代吡咯烷-1-基)氧基)-3-氧代丙基)硫代)半胱氨酸(0.35mmol)的thf溶液。在室温下搅拌3小时后,对混合物浓缩至干。粗残余物然后用15ml的acoet洗涤3次,用acoet/thf 70/30混合物洗涤2次,得到树枝状大分子11-g1(nh-nac)。产率在75%到95%之间。
[1302]
(n-乙酰基-s-((3-((2,5-二氧代吡咯烷-1-基)氧基)-3-氧代丙基)硫代)半胱氨酸是根据cleland j.l.等人描述的过程获得的(bioeng.transl.med.2018年,第3期,87-101页)。
[1303]
[化学式111]
[1304][1305]1h rmn(400mhz,thf)δ(ppm):1.93(s,3h,ch3),2.79(s,4h,c(o)ch2ch2c(o)),2.99
–
3.33(m,6h,sch2ch
*
,c(o)ch2ch2s),4.77(ddd,3j
hh
=8.0,7.3,4.8hz,1h,ch
*
),7.52(d,3j
hh
=7.9hz,1h,nhc(o)ch3).
[1306]
表征化合物11a-g1(nh-nac):
[1307]
[化学式112]
[1308][1309]1h rmn(600mhz,cdcl3)δ(ppm):2.01(s,18h,nhcoch3),2.37
–
2.42(m,12h,-sch2ch2conh),2.72
–
2.94(m,36h,-sch2ch2conh,c
14
ch2),2.96
–
3.42(m,108h,c
14
ch
2 ch2,nch2ch2nhco,-sch2ch
*
,ch2pome),3.75(d,2j
hp
=10.5hz,144h,pome),4.61(d,3j
hp
=12.7hz,12h,,c
04
ch2),4.80(m,6h,ch
*
),6.82
–
7.01(m,12h,c
02
h),7.09(d,3j
hh
=8.0hz,24h,c
12
h),7.20(d,3j
hh
=7.9hz,24h,c
13
h),7.29(d,3j
hh
=8.4hz,12h,c
03
h).
[1310]
31
p-{1h}rmn(243mhz,cdcl3)δ(ppm):8.46(s,p0),26.84(s,pome),68.42(s,p1).
[1311]
13
c-{1h}rmn(151mhz,cdcl3)δ(ppm):23.01(s,nhcoch3),32.98(s,c
14
ch2),33.97(s,sch2ch2nhco),35.81(s,sch2ch2nhco),37.41(s,nch2ch2nhco),41.52(s,sch2ch
*
),44.78(nch2ch2nhco),49.48(dd,1j
cp
=157.2,3j
cp
=7.1hz,ch2pome),49.62(sl,c
04
ch2),52.14(s,sch2ch
*
),52.86(d,2j
cp
=7.2hz,pome),58.22(t,,3j
cp
=7,7hz,c
14
ch2ch2),121.12(s,c
02
,c
12
),129.84(s,c
03
),129.98(s,c
13
),133.84(s,c
04
),136.42(s,c
14
),149.29(d,2j
cp
=7.9hz,c
11
),150.09(sl,c
01
),170.64(sl,nhcoch2ch2s),171.67(sl,nhcoch3),171.87(sl,cooh).
[1312]
树枝状大分子11a-g1(nh-nac)的结构如[图15]所示。
[1313]
表征化合物11b-g1(nh-nac):
[1314]
[化学式113]
[1315][1316]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.41(s,p0),26.61(s,pome),68.21(s,p1).
[1317]
树枝状大分子11b-g1(nh-nac)的结构如[图16]所示。
[1318]
表征化合物11c-g1(nh-nac):
[1319]
[化学式114]
[1320][1321]1h rmn(400mhz,cdcl3)δ(ppm):1.65
–
1.80(m,24h,ch2ch2ch2),2.00(s,18h,nhcoch3),2.53(m,12h,-sch2ch2conh),2.69
–
2.79(m,24h,c
14
ch2),2.86
–
2.96(m,12h,-sch2ch2conh),2.96
–
3.08(m,30h,c
14
ch2ch2,-sch2ch
*
),3.09
–
3.57(m,,n0ch2,c=onhch2,-sch2ch
*
,ch2pome,ch2o),3.72(d,2j
hp
=10.5hz,144h,pome),4.54(d,3j
hp
=13.3hz,12h,c
04
ch2),4.66(m,6h,ch
*
),6.94
–
7.26(m,84h,nhco,nhcoch3,c
02
h,c
12
h,c
03
h,c
13
h).
[1322]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.13(s,p0),26.84(s,pome),68.06(s,p1).
[1323]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):23.12(s,18h,nhcoch3),27.99(c=ohnch2ch2),29.05(s,n0ch2ch2),32.96(s,c
14
ch2),34.45(s,sch2ch2nhco),35.89(s,sch2ch2nhco),37.44(s,nch2ch2nhco),42.26(s,sch2ch
*
),43.12(ch2ch2nhco),49.42(dd,1j
cp
=157.7,3j
cp
=7.3hz,ch2pome),49.66(sl,c
04
ch2),52.54
–
52.89(m,pome),52.94(sl,,sch2ch
*
),58.25(t,3j
cp
=7.5hz,c
14
ch2ch2),68.45(s,ch2o),69.44(s,ch2o),70.03(s,ch2o),70.36(s,ch2o),70.44(s,ch2o),120.87(s,c
02
),121.04(d,3j
cp
=4.6hz,c
12
),129.47(s,c
03
),129.82(s,c
13
),134.28(s,c
04
),136.17(s,c
14
),149.46(d,2j
cp
=7.9hz,c
11
),149.99(s,c
01
),170.36(sl,nhcoch2ch2s),171.23(sl,nhcoch3),172.75(sl,cooh).
[1324]
树枝状大分子11c-g1(nh-nac)的结构如[图17]所示。
[1325]
合成化合物11a-g1(nh-nac/po3hna)、11b-g1(nh-nac/po3hna)和11c-g1(nh-nac/po3hna)
[1326]
在0℃下,向树枝状大分子11-g1(nh
2-nac)(0.01mmol)的乙腈(10ml)溶液中逐滴加入溴代三甲基硅烷(0.7mmol)。在室温下搅拌过夜后,对溶液浓缩至干。然后将甲醇(4ml)加入到干残余物中。搅拌一小时后,对得到的粉末过滤,然后用5ml甲醇洗涤2次。然后在表面添加膦酸1倍量的naoh,将树枝状大分子转化为其钠盐。产率高于95%。
[1327]
表征化合物11a-g1(nh-nac/po3hna):
[1328]
[化学式115]
[1329][1330]
31
p-{1h}rmn(243mhz,d2o/cd3cn)δ(ppm):7.23(s,p0),9.59(s,pohna),68.64(s,p1).
[1331]1h rmn(600mhz,d2o/cd3cn)δ(ppm):1.96(s,18h,nhcoch3),2.32(sl,12h,12h,-sch2ch2conh),2.73(sl,12h,sch2ch2conh),2.87(m,6h,ch2ch
*
),2.95
–
3.33(m,1h,c
14
ch2ch2,nch2ch2nhco,-sch2ch
*
),3.50
–
3.73(m,54h,c
14
ch2ch2,ch2poh),4.41
–
4.61(m,18h,c
04
ch2,nhchcooh),6.85(s,12h,c
02
h),7.05(m,24h,c
12
h),7.26(sl,36h,c
13
h,c
03
h).
[1332]
13
c-{1h}rmn(151mhz,d2o/cd3cn)δ(ppm):22.05(s,18h,nhcoch3),28.86(s,c
14
ch2),33.16(s,-sch2ch2conh),35.13(s,sch2ch2nhco),37.38(s,nch2ch2nhco),39.62(s,sch2ch
*
),44.90(nch2ch2nhco),49.67(sl,c
04
ch2),52.09(s,ch2poh),53.02(s,sch2ch
*
),57.35(sl,c
14
ch2ch2),121.18(s,c
02
),121.62(s,c
12
),129.92(s,c
03
),130.48(s,c
13
),133.55(s,c
14
),134.42(s,c
04
),149.39(m,c
01
),149.71(m,c
11
),173.20(sl,nch2ch2nhco),173.48(s,nhcoch3),175.00(sl,cooh).
[1333]
树枝状大分子11a-g1(nh-nac/po3hna)的结构如[图18]所示。
[1334]
表征化合物11b-g1(nh-nac/po3hna):
[1335]
[化学式116]
[1336][1337]
31
p-{1h}rmn(243mhz,d2o/cd3cn)δ(ppm):7.17(s,p0),9.51(s,pohna),68.69(s,p1).
[1338]
树枝状大分子11b-g1(nh-nac/po3hna)的结构如[图19]所示。
[1339]
表征化合物11c-g1(nh-nac/po3hna):
[1340]
[化学式117]
[1341][1342]1h rmn(400mhz,d2o)δ(ppm):1.63
–
1.80(m,24h,ch2ch2ch2),2.43
–
2.66(m,12h,sch2ch2conh),2.75
–
3.82(m,192h,ch2),4.48
–
4.62(m,36h,c
04
ch2,ch
*
),6.78
–
7.48(m,72h,ch-arom).
[1343]
31
p-{1h}rmn(162mhz,d2o)δ(ppm):7.18(s,pohna),9.63(s,p0),68.33(s,p1).
[1344]
树枝状大分子11c-g1(nh-nac/po3hna)的结构如[图20]所示。
[1345]
合成“层块”型树枝状大分子
[1346]
示意图6描述了“层块”型树枝状大分子的反应示意图,其中d’是甲基,d”是(ch2–
ch2–
o)3–
ch3:
[1347]
[示意图6]
[1348][1349]
利用1-g1合成化合物12-g
”’
1-boc[化学式118]
[1350]
[1351]
向树枝状大分子1-g1(125mg,0.071mmol)的thf(20ml)溶液中依次加入cs2co3(693mg,2.130mmol)和12-ab-boc(394mg,1.065mmol)。在室温下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。然后将粗残余物溶于200ml的dcm,再经硅胶过滤,得到透明油状的树枝状大分12-g
’”
1-boc,产率56%。
[1352]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):28.44,33.65,46.19,50.23,51.06,59.02,69.72,70.62,71.94,79.83,120.99,128.35,128.91,129.32,134.08,150.07,155.78.
[1353]1h rmn(400mhz,cdcl3)δ(ppm):1.46
–
1.48(m,108h),2.78(d,j=11.0hz,18h),3.20
–
3.47(m,60h),3.47
–
3.89(m,120h),4.50(s,36h),6.98(d,j=8.6hz,12h),7.06
–
7.26(m,60h).
[1354]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.28,68.11.
[1355]
利用12-g
’”
1-boc合成化合物12-g
”’
1-htfa
[1356]
[化学式119]
[1357][1358]
将化合物12-g
’”
1-boc(120mg,0.021mmol)溶于ch2cl2/三氟乙酸50/50至70/30比例混合物(5ml)。在室温下搅拌30分钟后,将混合物减压浓缩至干。然后残余物用3ml的ch2cl2共蒸发5次,得到白色粉末状的树枝状大分子12-g
’”
1-htfa。产率高于90%。
[1359]1h rmn(400mhz,cdcl3)δ(ppm):2.70(d,j=11.0hz,18h),3.15(s,24h),3.30(s,36h),3.56
–
3.67(m,72h),3.77(s,24h),4.10(s,24h),4.37(d,j=12.2hz,12h),6.88(d,j=9.0hz,12h),7.15(t,j=6.8hz,36h),7.42(d,j=8.7hz,24h).
[1360]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):33.56,46.19,50.57,58.73,70.09(d,j=8.5hz),71.52,114.49(q),121.53,127.62,129.17,131.63,133.73,149.87,151.74(d,j=7.4hz),160.68.
[1361]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.94,66.97.
[1362]
利用12-g
’”
1-htfa与合成子1-ab
2-boc合成化合物12-g
’”
2-boc
[1363]
[化学式120]
[1364][1365]
在120mg树枝状大分子12-g
’”
1-htf(0.021mmol)三氟乙酸盐(0.021毫摩尔)的ch2cl2(20
à
50ml)和dipea(0.135ml,0.756mmol)的溶液中加入化合物1-ab
2-boc(180mg,0.315mmol).在35℃搅拌72小时后,在室温下将混合物减压浓缩至干。然后将粗残余物溶于200ml的乙酸乙酯,过滤并在乙醚/戊烷混合物中沉淀,得到黄色油状的树枝状大分子12-g
’”
2-boc,产率80%。
[1366]
31
p-{1h}rmn(121mhz,cdcl3)δ(ppm):8.42,67.78,68.00.
[1367]
利用12-g
’”
2-boc合成化合物12-g
”’
2-htfa
[1368]
[化学式121]
[1369][1370]
将化合物12-g
’”
2-boc(100mg,0.021mmol)溶于ch2cl2/三氟乙酸50/50至70/30比例混合物(5ml)。在室温下搅拌30分钟后,将混合物减压浓缩至干。然后残余物用3ml的ch2cl2共蒸发5次,得到黄色油状的树枝状大分子12-g
’”
2-htfa。产率高于90%。
[1371]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):8.91,66.81,67.1.
[1372]
树枝状大分子12-g
”’
2-htfa的结构如[图21]所示。
[1373]
示意图7描述了“层块”型树枝状大分子的反应示意图,其中d’是甲基,d”是辛基:
[1374]
[示意图7]
[1375][1376]
利用1-g1与合成子5e合成化合物13-g2(ome)
[1377]
[化学式122]
[1378][1379]
向化合5e(300mg,0.282mmol)的thf(15ml)溶液中,其中含cs2co3(184mg,0.564mmol),加入六化合物1-g1(41.2mg,0.0235mmol)。在40℃下搅拌过夜后,对混合物离心、过滤,然后减压浓缩。得到透明油状的树枝状大分子13-g2(ome),产率90%。
[1380]1h rmn(400mhz,cdcl3)δ(ppm):0.69
–
0.96(m,36h),1.08
–
1.40(m,120h),2.73
–
2.85(m,72h),3.06(t,j=7.8hz,48h),3.20(d,j=9.3hz,114h),3.74(d,j=10.3hz,288h),4.37
–
4.74(m,36h),6.89
–
7.39(m,168h).
[1381]
13
c-{1h}rmn(101mhz,cdcl3)δ(ppm):14.10(d,j=2.6hz),22.59,26.36
–
27.03(m),27.62,29.19(dd,j=14.2,6.5hz),31.74(d,j=7.1hz),33.14(d,j=18.8hz),44.59,45.86,48.29
–
49.03(m),49.51,50.28(t,j=7.5hz),52.26
–
52.97(m),57.83
–
58.79(m),121.01(d,j=4.8hz),121.39(d,j=4.7hz),127.63
–
130.62(m),135.73(d,j=1.9hz),136.09,149.32(d,j=7.2hz),149.53(d,j=7.3hz),150.42(d,j=7.7hz).
[1382]
31
p-{1h}rmn(162mhz,cdcl3)δ(ppm):7.97,26.84,68.07,68.68.
[1383]
树枝状大分子13-g2(ome)的结构如[图22]所示。
[1384]
根据本发明的树枝状大分子的稳定性评价
[1385]
对照现有技术的聚磷腙型的含磷树枝状大分子(wo 2005/052031a1),评价了根据本发明的树枝状大分子在生理ph下的稳定性。
[1386]
操作方法
[1387]
将化合物溶解在h2o/d2o的混合物(20-50mg/ml)。如有必要,每次rmn光谱记录间隔期间,调节ph值并将溶液在25℃下避光保存。
[1388]
结果表明,根据本发明的化合物3-g’1(ona)在ph=7.2下的稳定性远高于具有聚磷腙骨架和酪胺衍生的氨基二亚甲基膦酸(单钠盐)末端的abp参比化合物。rmn 31
p光谱表明,abp化合物在ph=7.2,25℃下4天后降解([图23]的光谱b,信号证明在约67ppm处发生水解,该信号随着时间的推移而增强,如光谱c、d、e所示)。在相同条件下,化合物3-g’1(ona)保持完全稳定,即使在溶液中存放8个月后也没有观察到副产物([图24]的光谱a至e)。
[1389]
结果表明,根据本发明的化合物3-g’1(ona)在ph=5下的稳定性远高于具有聚磷腙骨架和酪胺衍生的氨基二亚甲基膦酸(单钠盐)末端的abp参比化合物。rmn 31
p光谱表明,abp化合物在ph=5,25℃下4天后降解([图25]的光谱b,信号证明在约67ppm处发生水解,该信号随着时间的推移而增强,如光谱c、d、e所示)。从10天开始,在48ppm处也观察到了证明降解的第二个信号([图25]的光谱c,这个信号随着时间的推移而加强,如光谱c、d和e所示)在相同条件下,化合物3-g’1(ona)保持完全稳定,即使在溶液中存放8个月后也没有观察到副产物([图26]的光谱a至e)。
[1390]
结果表明,根据本发明的化合物4-g’1(ona)在ph=7下的稳定性远高于具有聚磷腙骨架和酪胺衍生的氨基二亚甲基膦酸(单钠盐)末端的abp参比化合物。rmn 31
p光谱表明,abp化合物在ph=7,25℃下4天后降解([图23]的光谱b,信号证明在约67ppm处发生水解,该信号随着时间的推移而增强,如光谱c、d、e所示)。在相同条件下,化合物4-g’1(ona)保持完全稳定,即使在溶液中存放4个月后也没有观察到副产物([图27]的光谱a至e)。
[1391]
结果表明,根据本发明的化合物5-g’1(ona)在ph=7下的稳定性远高于具有聚磷腙骨架和酪胺衍生的氨基二亚甲基膦酸(单钠盐)末端的abp参比化合物。rmn 31
p光谱表明,abp化合物在ph=7,25℃下4天后降解([图23]的光谱b,信号证明在约67ppm处发生水解,该信号随着时间的推移而增强,如光谱c、d、e所示)。在相同条件下,化合物5-g’1(ona)保持完全稳定,即使在溶液中存放4个月后也没有观察到副产物([图28]的光谱a至e)。
[1392]
结果表明,根据本发明的化合54-g’1(ona)在ph=5下的稳定性远高于具有聚磷腙骨架和酪胺衍生的氨基二亚甲基膦酸(单钠盐)末端的abp参比化合物。rmn 31
p光谱表明,abp化合物在ph=5,25℃下4天后降解([图25]的光谱b,信号证明在约67ppm处发生水解,该信号随着时间的推移而增强,如光谱c、d、e所示)。在相同条件下,化合物5-g’1(ona)保持完全稳定,即使在溶液中存放4个月后也没有观察到副产物([图29]的光谱a至e)。
[1393]
生物学评价
[1394]
对根据本发明的树枝状大分子3-g’1(ona)的原代人单核细胞激活进行了评价。
[1395]
操作方法
[1396]
由法国的血液机构(法国,图卢兹,efs)采集了健康献血者的人血。然后通过在20℃下以1200rpm离心20分钟,利用pancoll溶液(panbiotech gmbh),根据密度梯度从血液中分离出外周血单核细胞(pbmc:peripheral blood mononuclear cells)。使用untouched
tm
人单核细胞试剂盒(invitrogen),利用除单核细胞之外的所有血细胞(t细胞、b细胞、nk细胞、树突细胞、红细胞和粒细胞)的抗体,通过阴性选择从pbmc中分离出单核细胞。通过流式细胞术验证,带有抗cd 14-apc-cy7抗体(miltenyi biotec)的每名献血者的单核细胞纯度高于90%。
[1397]
在48孔检测板中,按100万/ml,将新鲜纯化的单核细胞重悬于100u/ml的rpmi 1640+glutamax、青霉素和链霉素以及10%胎牛血清(svf)中。在培养开始时按20μm的浓度添加树枝状大分子。在37℃下培养5天后,利用macsquant q10细胞仪(miltenyi biotec),通过流式细胞术分析单核细胞的形态。通过flowlogic
tm
软件(miltenyi biotec)分析所有细胞计数数据。
[1398]
[图30]示出了通过流式细胞术分析单核细胞形态(粒度和大小)的结果(在图中,每个点是一个细胞)。对3名献血者进行了测试,树枝状大分子的浓度为20μm。左列对应及未激活的对照单核细胞。右列对应经3-g’1(ona)树枝状大分子培养4天的单核细胞:被激活的单核细胞位于椭圆内。
[1399]
形态的变化(粒度和大小增加)反映了原代人单核细胞的激活。结果表明,树枝状大分子3-g’1(ona)引起原代人单核细胞的粒度和大小增加。此外,注意到,被激活单核细胞的椭圆内,单核细胞比例更高,该比例取决于献血者。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1