检测样本中标志物表达水平的试剂在制备用于检测或诊断乳腺癌的试剂盒中的应用的制作方法
1.本发明涉及生物标志物技术领域,具体而言,涉及检测样本中标志物表达水平的试剂在制备用于检测或诊断乳腺癌的试剂盒中的应用。
背景技术:
2.乳腺癌(breast cancer)是乳腺上皮细胞在多种致癌因子的作用下,发生增殖失控的现象,是全球女性死亡的第二大癌症,其治疗的主要挑战之一是乳腺癌细胞具有异质性,从而决定治疗策略的选择。
3.根据受体类型的不同,乳腺癌可被分为4种亚型:雌激素/孕激素受体阳性(er/pr)、人类表皮生长因子受体阳性(her2)和三阴性乳腺癌(triple negative breast cancer,tnbc);而根据病理及分子分型的不同可分为:管腔样a型[luminal a,(er/pr阳性,her2阴性)]、管腔样b型[luminal b,(er/pr阳性,her2阳性)]、her2阳性类型及基底样型(basal)1。
[0004]
如何对乳腺癌进行更有效地检测一直是如今亟待解决的问题之一。
[0005]
鉴于此,特提出本发明。
技术实现要素:
[0006]
本发明的目的在于提供检测样本中标志物表达水平的试剂在制备用于检测或诊断乳腺癌的试剂盒中的应用。
[0007]
本发明是这样实现的:
[0008]
第一方面,本发明实施例提供了检测样本中标志物表达水平的试剂在制备用于检测或诊断乳腺癌的试剂盒中的应用,所述标志物选自:氨基酸序列依次如seqidno.1~3所示的nans、ran和erh中的至少一种。
[0009]
第二方面,本发明实施例提供了检测样本中标志物表达水平的试剂在筛选用于治疗或改善乳腺癌药物中的应用,所述标志物选自:nans、ran和erh中的至少一种;所述应用不以疾病的治疗或诊断为直接目的。
[0010]
本发明具有以下有益效果:
[0011]
本发明提供了乳腺癌的蛋白标志物,标志物包括nans、ran和erh中的至少一种,这些标志物在乳腺癌组织及其癌旁组织中的差异性表达,可用于乳腺癌诊断、预后评估和/或筛药。
附图说明
[0012]
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这
些附图获得其他相关的附图。
[0013]
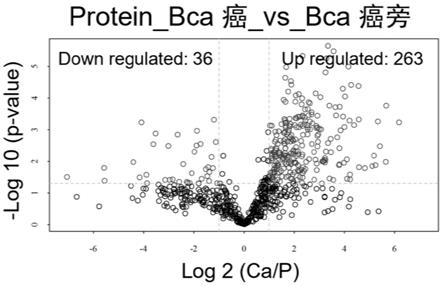
图1为实施例1乳腺癌癌组织与癌旁差异表达蛋白的鉴定和定量分析的结果,其中,bcaca代表癌组织,bcap代表癌旁组织;
[0014]
图2为实施例2中侵袭性乳腺导管癌中显著性差异表达的基因的检测结果;其中,num(t):癌组织样本数;num(n):癌旁组织样本数;*:p<0.05具有显著性差异;
[0015]
图3为实施例3中侵袭性乳腺癌差异表达的蛋白与乳腺癌患者无复发生存期相关性分析结果图;其中,low(n):n代表此基因低表达样本数;high(n):n代表此基因高表达样本数;hr(hazard ratio):风险率;
[0016]
图4为实施例4中qrt
‑
pcr方法验证乳腺癌癌组织与癌旁组织中差异基因的相对表达量的结果。
具体实施方式
[0017]
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0018]
首先,本发明实施例提供了检测样本中标志物表达水平的试剂在制备用于检测或诊断乳腺癌的试剂盒中的应用,所述标志物选自:氨基酸序列依次如seqidno.1~3所示的nans、ran和erh中的至少一种。
[0019]
具体地,nans的氨基酸序列为:5
’‑
mplelelcpgrwvggqhpcfiiaeigqnhqgdldvakrmirmakecgadcakfqkselefkfnrkalerpytskhswgktygehkrhlefshdqyrelqryaeevgifftasgmdemaveflhelnvpffkvgsgdtnnfpylektakkgrpmvissgmqsmdtmkqvyqivkplnpnfcflqctsayplqpedvnlrviseyqklfpdipigysghetgiaisvaavalgakvlerhitldktwkgsdhsaslepgelaelvrsvrlveralgsptkqllpcemacneklgksvvakvkipegtiltmdmltvkvgepkgyppedifnlvgkkvlvtveeddtimeelvdnhgkkiks
‑3’
。
[0020]
ran的氨基酸序列为:5
’‑
maaqgepqvqfklvlvgdggtgkttfvkrhltgefekkyvatlgvevhplvfhtnrgpikfnvwdtagqekfgglrdgyyiqaqcaiimfdvtsrvtyknvpnwhrdlvrvcenipivlcgnkvdikdrkvkaksivfhrkknlqyydisaksnynfekpflwlarkligdpnlefvampalappevvmdpalaaqyehdlevaqttalpdedddl
‑3’
。
[0021]
erh的氨基酸序列为:5
’‑
mshtillvqptkrpegrtyadyesvnecmegvckmyeehlkrmnpnspsitydisqlfdfiddladlsclvyradtqtyqpynkdwikekiyvllrrqaqqagk
‑3’
。
[0022]
经一系列创造性研究,本发明提供了一种新的用于检测或诊断乳腺癌的标志物,上述标志物在乳腺癌癌组织及其癌旁组织中差异性表达,通过对标志物的表达水平进行检测,能够用于乳腺癌的诊断、预后评估或筛药。
[0023]
优选地,所述标志物还可以包括:氨基酸序列依次如seqidno.4~14所示的lcp1、cct3、nme1、hsp90aa1、ywhaz、prdx1、stip1、hspa8、h2afy、hspe1和pdia3中的至少一种。
[0024]
具体地,lcp1的氨基酸序列为:5
’‑
margsvsdeemmelreafakvdtdgngyisfnelndlfkaaclplpgyrvreitenlmatgdldqdgrisfdefikifhglkstdvaktfrkainkkegicaiggtseqssvgtqhsyseeekyafvnwinkalendpdcrhvipmnpntndlfnavgdgivlckminlsvpdtidertinkkkltpftiq
enlnlalnsasaigchvvnigaedlkegkpylvlgllwqvikiglfadielsrnealiallregesledlmklspeelllrwanyhlenagcnkignfstdikdskayyhlleqvapkgdeegvpavvidmsglrekddiqraecmlqqaerlgcrqfvtatdvvrgnpklnlafianlfnrypalhkpenqdidwgalegetreertfrnwmnslgvnprvnhlysdlsdalvifqlyekikvpvdwnrvnkppypklggnmkklencnyavelgknqakfslvgiggqdlnegnrtltlaliwqlmrrytlnileeigggqkvnddiivnwvnetlreakksssissfkdpkistslpvldlidaiqpgsinydllktenlnddeklnnakyaismarkigarvyalpedlvevnpkmvmtvfaclmgkgmkrv
‑3’
。
[0025]
cct3的氨基酸序列为:5
’‑
mmghrpvlvlsqntkresgrkvqsgninaaktiadiirtclgpksmmkmlldpmggivmtndgnailreiqvqhpaaksmieisrtqdeevgdgttsviilagemlsvaehfleqqmhptvvisayrkalddmistlkkisipvdisdsdmmlniinssittkaisrwsslacnialdavkmvqfeengrkeidikkyarvekipggiiedscvlrgvminkdvthprmrryiknprivlldssleykkgesqtdieitreedftrilqmeeeyiqqlcediiqlkpdvvitekgisdlaqhylmranitairrvrktdnnriaracgarivsrpeelreddvgtgaglleikkigdeyftfitdckdpkactillrgaskeilsevernlqdamqvcrnvlldpqlvpgggasemavahaltekskamtgveqwpyravaqaleviprtliqncgastirlltslrakhtqencetwgvngetgtlvdmkelgiweplavklqtyktavetavlllriddivsghkkkgddqsrqggapdagqe
‑3’
。
[0026]
nme1的氨基酸序列为:5
’‑
mancertfiaikpdgvqrglvgeiikrfeqkgfrlvglkfmqasedllkehyvdlkdrpffaglvkymhsgpvvamvweglnvvktgrvmlgetnpadskpgtirgdfciqvgrniihgsdsvesaekeiglwfhpeelvdytscaqnwiye
‑3’
。
[0027]
hsp90aa1的氨基酸序列为:5
’‑
mpeetqtqdqpmeeeevetfafqaeiaqlmsliintfysnkeiflrelisnssdaldkiryesltdpskldsgkelhinlipnkqdrtltivdtgigmtkadlinnlgtiaksgtkafmealqagadismigqfgvgfysaylvaekvtvitkhnddeqyawessaggsftvrtdtgepmgrgtkvilhlkedqteyleerrikeivkkhsqfigypitlfvekerdkevsddeaeekedkeeekekeekesedkpeiedvgsdeeeekkdgdkkkkkkikekyidqeelnktkpiwtrnpdditneeygefyksltndwedhlavkhfsvegqlefrallfvprrapfdlfenrkkknniklyvrrvfimdnceelipeylnfirgvvdsedlplnisremlqqskilkvirknlvkkclelftelaedkenykkfyeqfskniklgihedsqnrkklsellryytsasgdemvslkdyctrmkenqkhiyyitgetkdqvansafverlrkhgleviymiepideycvqqlkefegktlvsvtkeglelpedeeekkkqeekktkfenlckimkdilekkvekvvvsnrlvtspccivtstygwtanmerimkaqalrdnstmgymaakkhleinpdhsiietlrqkaeadkndksvkdlvillyetallssgfsledpqthanriyrmiklglgideddptaddtsaavteempplegdddtsrmeevd
‑3’
。
[0028]
ywhaz的氨基酸序列为:5
’‑
mdknelvqkaklaeqaeryddmaacmksvteqgaelsneernllsvayknvvgarrsswrvvssieqktegaekkqqmareyrekietelrdicndvlsllekflipnasqaeskvfylkmkgdyyrylaevaagddkkgivdqsqqayqeafeiskkemqpthpirlglalnfsvfyyeilnspekacslaktafdeaiaeldtlseesykdstlimqllrdnltlwtsdtqgdeaeageggen
‑3’
。
[0029]
prdx1的氨基酸序列为:5
’‑
mssgnakighpapnfkatavmpdgqfkdislsdykgkyvvfffypldftfvcpteiiafsdraeefkklncqvigasvdshfchlawvntpkkqgglgpmniplvsdpkrtiaqdygvlkadegisfrglfiiddkgilrqitvndlpvgrsvdetlrlvqafqftdkhgevcpagwkpgsdtikpdvqkskeyfskqk
‑3’
。
[0030]
stip1的氨基酸序列为:5
’‑
meqvnelkekgnkalsvgniddalqcyseaikldphnhvlysnrsaayakkgdyqkayedgcktvdlkpdwgkgysrkaaaleflnrfeeakrtyeeglkheannpqlkeglqnmearlaerkfmnpfnmpnlyqklesdprtrtllsdptyrelieqlrnkpsdlgtklqdprimttlsvllgvdlgsmdeeeeia
tpppppppkketkpepmeedlpenkkqalkekelgndaykkkdfdtalkhydkakeldptnmtyitnqaavyfekgdynkcrelcekaievgrenredyrqiakayarignsyfkeekykdaihfynkslaehrtpdvlkkcqqaekilkeqerlayinpdlaleeknkgnecfqkgdypqamkhyteaikrnpkdaklysnraacytkllefqlalkdceeciqleptfikgytrkaaaleamkdytkamdvyqkaldldssckeaadgyqrcmmaqynrhdspedvkrramadpevqqimsdpamrlileqmqkdpqalsehlknpviaqkiqklmdvgliair
‑3’
。
[0031]
hspa8的氨基酸序列为:5
’‑
mskgpavgidlgttyscvgvfqhgkveiiandqgnrttpsyvaftdterligdaaknqvamnptntvfdakrligrrfddavvqsdmkhwpfmvvndagrpkvqveykgetksfypeevssmvltkmkeiaeaylgktvtnavvtvpayfndsqrqatkdagtiaglnvlriineptaaaiaygldkkvgaernvlifdlgggtfdvsiltiedgifevkstagdthlggedfdnrmvnhfiaefkrkhkkdisenkravrrlrtacerakrtlssstqasieidslyegidfytsitrarfeelnadlfrgtldpvekalrdakldksqihdivlvggstripkiqkllqdffngkelnksinpdeavaygaavqaailsgdksenvqdlllldvtplslgietaggvmtvlikrnttiptkqtqtfttysdnqpgvliqvyegeramtkdnnllgkfeltgippaprgvpqievtfdidangilnvsavdkstgkenkititndkgrlskediermvqeaekykaedekqrdkvssknslesyafnmkatvedeklqgkindedkqkildkcneiinwldknqtaekeefehqqkelekvcnpiitklyqsaggmpggmpggfpgggappsggassgptieevd
‑3’
。
[0032]
h2afy的氨基酸序列为:5
’‑
mssrggkkkstktsrsakagvifpvgrmlryikkghpkyrigvgapvymaavleyltaeilelagnaardnkkgrvtprhillavandeelnqllkgvtiasggvlpnihpellakkrgskgkleaiitpppakkakspsqkkpvskkaggkkgarkskkkqgevskaasadsttegtpadgftvlstkslflgqklnlihseisnlagfeveaiinptnadidlkddlgntlekkggkefveavlelrkkngplevagaavsaghglpakfvihcnspvwgadkceellektvknclaladdkklksiafpsigsgrngfpkqtaaqlilkaissyfvstmsssiktvyfvlfdsesigiyvqemakldan
‑3’
。
[0033]
hspe1的氨基酸序列为:5
’‑
magqafrkflplfdrvlversaaetvtkggimlpeksqgkvlqatvvavgsgskgkggeiqpvsvkvgdkvllpeyggtkvvlddkdyflfrdgdilgkyvd
‑3’
。
[0034]
pdia3的氨基酸序列为:5
’‑
mrlrrlalfpgvalllaaarlaaasdvleltddnfesrisdtgsaglmlveffapwcghckrlapeyeaaatrlkgivplakvdctantntcnkygvsgyptlkifrdgeeagaydgprtadgivshlkkqagpasvplrteeefkkfisdkdasivgffddsfseahseflkaasnlrdnyrfahtnveslvneyddngegiilfrpshltnkfedktvayteqkmtsgkikkfiqenifgicphmtednkdliqgkdlliayydvdyeknakgsnywrnrvmmvakkfldaghklnfavasrktfshelsdfglestageipvvairtakgekfvmqeefsrdgkalerflqdyfdgnlkrylksepipesndgpvkvvvaenfdeivnnenkdvliefyapwcghcknlepkykelgeklskdpniviakmdatandvpspyevrgfptiyfspankklnpkkyeggrelsdfisylqreatnppviqeekpkkkkkaqedl
‑3’
。
[0035]
优选地,所述检测标志物表达水平是指检测标志物mrna表达水平和检测标志物蛋白表达水平中的至少一种。
[0036]
优选地,所述试剂为引物、探针和芯片中的至少一种。在一些实施例中,本发明不对引物和探针的具体序列进行限定,只要是将能够对上述任意标志物或标志物的组合的表达水平进行检测的试剂用于制备检测或诊断乳腺癌的试剂盒,则属于本技术的保护范围。
[0037]
优选地,所述试剂包括分别用于检测nans、ran和erh的引物对1~3中的至少一对;引物对1的碱基序列如seqidno.15
‑
16所示;引物对2的碱基序列如seqidno.17
‑
18所示;引物对3的碱基序列如seqidno.19
‑
20所示。
[0038]
优选地,所述试剂还包括分别用于检测lcp1、cct3、nme1、hsp90aa1、ywhaz、prdx1、
control)target为1e6,maximum it为50ms,动态排除时间(dynamic exclusion)为60.0s。多肽和多肽碎片的质量电荷比按照下列方法采集:每次全扫描(full scan)后采集20个碎片图谱(ms2 scan),ms2 activation type为hcd,isolation window为2m/z,二级质谱分辨率17,500at 200m/z,normalized collision energy为30ev,underfill为0.1%。
[0054]
四、蛋白质鉴定和定量分析
[0055]
质谱分析原始数据为raw文件,用软件maxquant软件(版本号1.5.3.17)进行查库鉴定及定量分析。
[0056]
结果如图1所示。由图1可知,与癌旁比较,癌组织中差异表达上调的蛋白是263个,下调的蛋白是36个。
[0057]
在上述乳腺癌癌组织中表达上调的蛋白中,设置差异倍数大于2倍且p<0.05为具有显著性差异的条件,共筛选出23个癌组织中特异性表达的蛋白,如表1所示,分别是:lcp1、arf1、cct3、vdac1、nans、nme1、hsp90aa1、ran、ywhaz、ckap4、erh、prdx1、sfn、tubb、stip1、snrpd3、hspa8、nme2、h2afy、hspe1、hdgf、srp9和pdia3。
[0058]
表1乳腺癌肿瘤组织与癌旁组织比较表达上调的蛋白
[0059][0060]
备注:protein_id:蛋白编码;protein name:蛋白名称;gene name:蛋白相应的基因名称;fold change:差异表达倍数;p
‑
value:p值;up/down:上调/下调(癌/癌旁)。
[0061]
实施例2
[0062]
本实施例通过gepia数据库(gepia数据库是基于tcga癌症大数据分析的统计数据库)验证表6中23个差异的蛋白(标志物)在侵袭性乳腺导管癌患者中的mrna表达水平,具体操作如下。
[0063]
步骤一~步骤四同实施例1。
[0064]
五、rna提取
[0065]
(1)在将组织在液氮中速冻,使用研磨器将组织磨碎,每管组织内加入1ml trizol后用振荡器中涡旋,在水平摇床上慢摇10min,充分裂解组织;
[0066]
(2)将trizol
‑
裂解液加入到1.5ml的无酶管中,每个样品中加入200μl氯仿,剧烈震荡15sec后,室温静置2
‑
3min,10000rcf,4℃离心15min;
[0067]
(3)将上层水相转移至新的1.5ml的无酶管中,加入500μl异丙醇,混合均匀后室温放置40min,10000rcf,4℃离心15min;
[0068]
(4)小心移除上清液体,管底可见rna白色沉淀,使用预冷的无酶水配制的75%乙醇清洗一次,10000rcf,4℃离心1min。
[0069]
(5)室温干燥rna白色沉淀,加入30
‑
60μl无酶水水溶解沉淀。
‑
80℃保存备用。
[0070]
六、实时荧光定量pcr反应(qrt
‑
pcr)
[0071]
1.rna反转录实验:
[0072]
在rnase
‑
free microtube管中配制表2所示的混合液,10μl体系:使用dnase降解样本中dna;
[0073]
表2混合液
[0074]
dnase i buffer(10x)1μlrna sample1μgdepc h2o7μldnase i1μltotal10μl
[0075]
pcr反应条件:37℃,30min。
[0076]
2. 25mm edta 1μl至混合液,65℃热激反应10min。向混合液中加入50μm 0.5μl random primer和4um 1ul dntp。
[0077]
pcr反应条件:72℃,10min,然后置于冰上。
[0078]
3.rna反转录合成cdna,反应体系如表3所示。
[0079]
表3反应体系
[0080]5×
first strand buffer4μl0.1m dtt1μlrnase inhibitior0.5μlm
‑
mlv1μldepc h2o1μltotal7.5μl
[0081]
pcr反应条件:37℃,60min;70℃,15min。
[0082]
得到的20μl cdna用depch2o稀释20倍后,
‑
20℃冰箱贮存。
[0083]
4.qrt
‑
pcr。
[0084]
按照表4设计合成引物。
[0085]
表4引物信息
[0086][0087]
[0088]
在ep管中配置如表5所示的pcr反应液。
[0089]
表5 pcr反应液
[0090]
sybr reaction buffer5μlcdna3μlprimer(r+f)0.2μldepc h2o1.8μltotal10μl
[0091]
在pcr仪上按照表6所示的条件进行qrt
‑
pcr。
[0092]
表6反应条件
[0093]
95℃10min 95℃30sec 60℃30sec40cycles72℃5min 72℃10min 4℃holding
ꢀꢀ
[0094]
5.实验结果分析:
[0095]
反应结束后确认qrt
‑
pcr的扩增曲线和熔解曲线,基因的表达量=2
‑
δδct,即δδct=(实验组目的基因的ct的平均值-实验组管家基因gapdh的ct的平均值)-(对照组目的基因的ct的平均值一对照管家基因的ct的平均值)。
[0096]
结果图2所示。由结果可知,与癌旁组织比较,lcp1、arf1、cct3、vdac1、nans、nme1、hsp90aa1、ran、ywhaz、ckap4、erh、prdx1、sfn、tubb、stip1、snrpd3、hspa8、nme2、h2afy、hspe1、hdgf、srp9和pdia3共23个基因在侵袭性乳腺癌癌组织中表达升高,具有显著性差异(p<0.05)。
[0097]
实施例3
[0098]
kaplan
‑
meier数据库筛选实施例2中的23个蛋白在侵袭性乳腺癌患者中的生存期。
[0099]
根据上述分析,我们通过kaplan
‑
meier数据库分析,结果发现,乳腺癌患者中上述23个基因表达越高,乳腺癌患者的无复发生存期(relapse
‑
free survival,rfs)越短,如图3所示。
[0100]
实施例4
[0101]
qrt
‑
pcr方法验证上述差异的基因在侵袭性乳腺癌中表达水平。
[0102]
通过在2例乳腺癌癌组织与癌旁组织中,采用qrt
‑
pcr实验验证发现,与各自癌旁组织比较,2例乳腺癌组织中,共有14个基因:lcp1、cct3、nans、nme1、hsp90aa1、ran、ywhaz、erh、prdx1、stip1、hspa8、h2afy、hspe1和pdia3表达升高,*p<0.05,**p<0.01,***p<0.001为显著性差异,如图4所示。
[0103]
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1