杯芳烃衍生化的超分子大环主体化合物、其制备方法及其应用
1.本发明属于有机合成领域,涉及一类水溶性吡啶基超分子杯、其制备方法及其应用。
背景技术:
2.杯芳烃是由苯酚单体经过亚甲基在酚羟基的邻位连接形成的大环低聚物,其结构形似希腊圣杯(calixcrater)而被称为杯芳烃,其命名通常称为杯[n]芳烃,其中n代表形成大环的苯酚单体的数目(通常n=4,6,8),最常见的是杯[4]芳烃和杯[6]芳烃。
[0003]
在杯芳烃分子中,上沿由苯环的对位取代基构成,下沿一般由规则排列的酚羟基组成,具有亲水性,中间是由苯环构成的疏水的富电子空腔,相比于前两代超分子主体,杯芳烃主要有以下几个优点:
[0004]
1.杯芳烃合成便捷,原料价廉易得,便于研究的开展;
[0005]
2.具有较大的分子量,因而熔点高,化学稳定性好,毒性比较低;
[0006]
3.容易进行衍生化,其结构决定了上沿苯环对位取代基、下沿酚羟基以及苯环之间的亚甲基可进行选择性修饰,从而调节其溶解度、空腔大小等物化性质;
[0007]
4.疏水空腔针对不同的客体分子能够进行调节,可络合多种类型的小分子化合物;
[0008]
5.构象丰富,存在各种不同的构象,也可以通过化学修饰和温度、ph等条件调节以固定需要的构象。
[0009]
超分子杯的空腔可适应更多类型的客体分子,因此水溶性超分子杯的合成逐渐受到研究者的关注,超分子杯空腔的构建往往伴随π
‑
π堆积,因而导致主体分子的水溶性差。
技术实现要素:
[0010]
为了解决现有技术问题,本发明的目的在于克服已有技术存在的不足,提供一种杯芳烃衍生化的超分子大环主体化合物、其制备方法及其应用,该类化合物具有较好的水溶性,并且能在水中选择性的识别亲水小分子。本发明水溶性较好的超分子的制备方法,在水溶性超分子杯的上缘引入了吡啶基团,增加了空腔的深度,减缓了客体的进出交换,实现了对亲水小分子的识别。
[0011]
为达到上述目的,本发明采用如下技术方案:
[0012]
一种杯芳烃衍生化的超分子大环主体化合物,其具有至少四层芳香结构,能溶解在水中,并具有能容纳客体分子的疏水空腔结构,还能在水中选择性识别亲水小分子,其结构为如下超分子杯1和超分子杯2中的至少一种结构:
[0013]
分子杯1的结构式为:
[0014][0015]
分子杯2的结构式为:
[0016][0017]
优选地,当本发明杯芳烃衍生化的超分子大环主体化合物具有分子杯1的结构时,该化合物具有深空腔,空腔主体部分为苯并咪唑基团,上缘连有氮原子在4号位的吡啶基团,下缘为羧酸钠盐,在水中与客体分子形成“花瓶”构象,将客体分子包裹于超分子杯的空腔中。
[0018]
优选地,当本发明杯芳烃衍生化的超分子大环主体化合物具有分子杯2的结构时,该化合物具有深空腔,空腔主体部分为苯并咪唑基团,上缘连有氮原子在3号位的吡啶基团,下缘为羧酸钠盐,在水中与客体分子形成“花瓶”构象,将客体分子包裹于超分子杯的空腔中。
[0019]
一种本发明杯芳烃衍生化的超分子大环主体化合物的制备方法,以间苯二酚或其衍生物为起始反应原料,制备水溶性吡啶基超分子杯化合物,在下缘通过氧化反应和水解反应引入羧酸钠盐以达到整体具有水溶性,在上缘引入通过与二胺的缩合引入不同的吡啶基团,使中间部分成为了苯丙咪唑基团,并使上缘吡啶的加入缩小空腔口径,减缓客体交换。
[0020]
优选地,本发明杯芳烃衍生化的超分子大环主体化合物的制备方法,包括如下合成步骤:
[0021]
a.采用以间苯二酚或其衍生物为原料,将不低于0℃下向原料的丙酮溶液中加入jones试剂,将反应混合物加热至室温并搅拌至少10小时;通过加入2
‑
异丙醇将反应淬灭并过滤;利用旋转蒸发仪浓缩滤液得到固体,并将固体分别用丙酮和甲醇彻底洗涤至少3次,然后干燥处理;
[0022]
b.将在步骤a中制备的产物和二水合二氯化锡作为反应物,向在冰浴中冷却的圆底烧瓶中加入在步骤a中制备的产物,使产物悬浮在预冷至不高于0℃的乙醇中搅拌;向悬浮液中缓慢加入二水合二氯化锡和质量分数不低于20%的浓盐酸,置换氮气至少3次;然后将圆底烧瓶浸入预热至不低于110℃的油浴中,并剧烈加热回流至少4小时;将反应混合物冷却至室温,过滤,并将得到的固体用不高于0℃的浓度不高于3mol/l的盐酸溶液洗涤至少3次,再用不高于0℃的乙腈洗涤至少5次,最后用乙醚洗涤至少5次,然后干燥处理;
[0023]
c.将在步骤b中制备的产物和2
‑
(4
‑
吡啶基亚甲基)丙二腈作为反应物,用甲醇溶解在步骤b中制备的产物,并加入质量分数为25
‑
28%的氨水,得到白色沉淀物,然后使用旋转蒸发仪除去溶剂,将甲醇加入烧瓶中,同时加入2
‑
(4
‑
吡啶基亚甲基)丙二腈,在氮气下,并在不高于80℃下剧烈搅拌至少15个小时,然后过滤得到固体,将固体用甲醇洗涤至少3次,水洗涤至少2次,二氯甲烷洗涤至少1次,收集固体,并于真空下干燥;
[0024]
d.将在步骤c中制备的产物和氢氧化钠作为反应物,将在步骤c中制备的产物添加到的另外一个圆底烧瓶中,加入乙醇和四氢呋喃混合溶剂,然后在不高于0℃下加入氢氧化钠水溶液;然后将反应混合物移至不低于40℃下,并搅拌至少10小时;然后将所得固体过滤并用乙醇洗涤至少3次;再将回收的固体悬浮在的丙酮中,然后剧烈搅拌并在回流下加热至少1小时,将悬浮液冷却至室温,过滤,用丙酮洗涤,并在真空下干燥,得到白色固体超分子杯1;
[0025]
e.将在步骤b中制备的产物和2
‑
(3
‑
吡啶基亚甲基)丙二腈作为反应物,用甲醇溶解在步骤b中制备的产物,并加入质量分数为25
‑
28%的氨水,得到白色沉淀物,然后使用旋转蒸发仪除去溶剂,将甲醇加入烧瓶中,同时加入2
‑
(3
‑
吡啶基亚甲基)丙二腈,在氮气下,并在不高于80℃下剧烈搅拌至少15个小时,然后过滤得到固体,将固体用甲醇洗涤至少3次,乙腈洗涤至少2次,收集固体,并于真空下干燥;
[0026]
f.将在步骤e中制备的产物和氢氧化钠作为反应物,将在步骤e中制备的产物添加到的其他一个圆底烧瓶中,加入乙醇和四氢呋喃混合溶剂,然后在不高于0℃下加入氢氧化钠水溶液;然后将反应混合物移至不低于40℃下,并搅拌至少10小时;然后将所得固体过滤并用乙醇洗涤至少3次;再将回收的固体悬浮在的丙酮中,然后剧烈搅拌并在回流下加热至少1小时,将悬浮液冷却至室温,过滤,用丙酮洗涤,并在真空下干燥,得到白色固体超分子杯2。
[0027]
优选地,在步骤a中,在浓缩滤液时采用真空浓缩处理,真空浓缩处理的条件为温度不高于50℃,真空度0.09~0.1mpa。
[0028]
优选地,在步骤a中,采用的jones试剂浓度不低于2.5mol/l,起始反应原料和jones试剂的混合质量比例为1:10。
[0029]
优选地,在步骤b中,在步骤a中制备的产物和二水合二氯化锡的反应物混合质量比为1:120。
[0030]
优选地,在步骤c中,在步骤b中制备的产物和2
‑
(4
‑
吡啶基亚甲基)丙二腈的反应物混合质量比为1:12,氨水和甲醇的体积比为1:10。
[0031]
优选地,在步骤d中,在步骤c中制备的产物和氢氧化钠的反应物混合质量比为1:5,其中氢氧化钠水溶液的浓度不低于1mol/l,加入乙醇和四氢呋喃的体积比为1:1。
[0032]
优选地,在步骤e中,在步骤b中制备的产物和2
‑
(3
‑
吡啶基亚甲基)丙二腈的反应
物混合质量比为1:12,氨水和甲醇的体积比为1:10。
[0033]
优选地,在步骤f中,在步骤e中制备的产物和氢氧化钠的反应物混合质量比为1:5,其中氢氧化钠水溶液的浓度不低于1mol/l,加入乙醇和四氢呋喃的体积比为1:1。
[0034]
优选地,在步骤d中或者在步骤f中,在得到超分子杯1或者超分子杯2之前,进行后处理操作,包括加入大量水,加入大量二氯甲烷洗涤,加入大量乙腈洗涤,真空干燥,减压浓缩,得到超分子杯1或者超分子杯2。
[0035]
一种本发明杯芳烃衍生化的超分子大环主体化合物的应用,所述杯芳烃衍生化的超分子大环主体化合物具有可容纳客体分子的疏水空腔,能识别极性小分子,包括水污染物中含有1,4
‑
二氧六环的化合物,在识别1,4
‑
二氧六环后荧光会发生较大的变化,用来检测水中是否含有极性小分子污染物。
[0036]
本发明与现有技术相比较,具有如下显而易见的突出实质性特点和显著优点:
[0037]
1.本发明超分子杯1和超分子杯2结构新颖,具有疏水空腔,能够识别极性小分子,包括水污染物1,4
‑
二氧六环,识别1,4
‑
二氧六环后荧光会发生较大的变化,具有潜在的应用于环境污染检测的前景;
[0038]
2.本发明的合成路线工艺简便,原料易得、反应条件温和,产率高,重复性好。
附图说明
[0039]
图1为超分子杯1的核磁氢谱图。
[0040]
图2为超分子杯1的核磁碳谱图。
[0041]
图3为超分子杯1的高分辨质谱图。
[0042]
图4为超分子杯1(1mmol/l,500μl)对客体(100mmol/l,5μl)络合的对极性小分子识别核磁谱图。a)超分子杯1;b)超分子杯1与四氢呋喃;c)超分子杯1与四氢吡喃;d)超分子杯1与1,3
‑
二氧六环;e)超分子杯1与1,4
‑
二氧六环;f)超分子杯1与环氧己烷。
[0043]
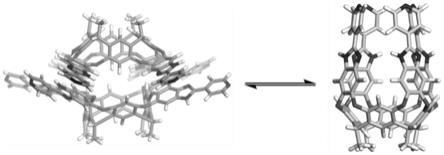
图5为超分子杯1的不同构象的快速变换图。二聚体与花瓶构象的快速变换,这一性质超分子杯1和超分子杯2都具有,此图为超分子杯1为例。
[0044]
图6为超分子杯2的核磁氢谱图。
[0045]
图7为超分子杯2的核磁碳谱图。
[0046]
图8为超分子杯2的高分辨质谱图。
[0047]
图9为超分子杯2的对极性小分子识别核磁谱图。为水溶性超分子杯2(1mmol/l,500μl)和对客体小分子(100mmol/l,5μl)的识别,从上到下的客体依次为:四氢吡喃、环氧己烷、环己醇、环己酮和硫化环戊烷。
[0048]
图10为中间产物p4的核磁氢谱图。
[0049]
图11为中间产物p3的核磁氢谱图。
[0050]
图12为超分子杯1与超分子杯主客体络合在365nm波长下的荧光对照图。
[0051]
图13为超分子杯1与超分子杯主客体络合荧光光谱谱。
具体实施方式
[0052]
以下结合具体的实施例子对上述方案做进一步说明,本发明的优选实施例详述如下:
[0053]
实施例一:
[0054]
在本实施例中,一种杯芳烃衍生化的超分子大环主体化合物,其具有四层芳香结构,能溶解在水中,并具有能容纳客体分子的疏水空腔结构,还能在水中选择性识别亲水小分子,其具有如下超分子杯1的结构式为:
[0055][0056]
一种本实施例杯芳烃衍生化的超分子大环主体化合物的制备方法,以间苯二酚或其衍生物为起始反应原料,制备水溶性吡啶基超分子杯化合物,在下缘通过氧化反应和水解反应引入羧酸钠盐以达到整体具有水溶性,在上缘引入通过与二胺的缩合引入不同的吡啶基团,使中间部分成为了苯丙咪唑基团,并使上缘吡啶的加入缩小空腔口径,减缓客体交换。其合成步骤如下:
[0057][0058]
本实施例杯芳烃衍生化的超分子大环主体化合物的制备方法,包括如下合成步骤:
[0059]
a.采用以间苯二酚或其衍生物p5(200mg,0.15mmol,1eq.)为原料,将0℃下向原料的50ml丙酮溶液中加入jones试剂(0.33ml,10eq.),将反应混合物加热至室温并搅拌10小时;通过加入5ml的2
‑
异丙醇将反应淬灭并过滤;利用旋转蒸发仪浓缩滤液得到固体,并将固体分别用50ml丙酮和50ml甲醇彻底洗涤3次,真空干燥获得p4(180mg,产率84%);
[0060]
b.将在步骤a中制备的产物p4和二水合二氯化锡作为反应物,向在冰浴中冷却的圆底烧瓶中加入在步骤a中制备的产物p4(200mg,0.13mmol,1eq.),使产物p4悬浮在预冷至0℃的20ml乙醇中搅拌;向悬浮液中缓慢加入3.6g二水合二氯化锡(16mmol,120eq.)和5ml质量分数为37.5%的浓盐酸,置换氮气3次;然后将圆底烧瓶浸入预热至110℃的油浴中,并剧烈加热回流4小时;将反应混合物冷却至室温,过滤,并将得到的固体用0℃的盐酸溶液(50ml,3mol/l)洗涤3次,再用0℃的10ml乙腈洗涤5次,最后用20ml乙醚洗涤5次,干燥后得到白色固体p3(150mg);
[0061]
c.将在步骤b中制备的产物p3和2
‑
(4
‑
吡啶基亚甲基)丙二腈作为反应物,用80ml甲醇溶解在步骤b中制备的产物p3(500mg,1eq.),并加入80ml质量分数为25
‑
28%的氨水,得到白色沉淀物,然后使用旋转蒸发仪除去溶剂,将100ml甲醇加入烧瓶中,同时加入2
‑
(4
‑
吡啶基亚甲基)丙二腈(713mg,12eq.),在氮气下,并在80℃下剧烈搅拌15小时,然后过滤得到固体,将固体用50ml甲醇洗涤3次,水洗涤2次,50ml二氯甲烷洗涤1次,收集固体,并于真空下干燥,得到p2.1(412mg,产率65%);
[0062]
d.将在步骤c中制备的产物p2.1和氢氧化钠作为反应物,将在步骤c中制备的产物p2.1(400mg,0.24mmol,1eq.)添加到的另外一个容积为50ml的圆底烧瓶中,加入30ml乙醇和四氢呋喃按照体积比为1:1进行混合的混合溶剂,然后在0℃下加入氢氧化钠水溶液(1n,1.2ml,5eq.);然后将反应混合物移至40℃下,并搅拌10小时;然后将所得固体过滤并用乙醇洗涤至少3次,每次使用20ml乙醇;再将回收的固体悬浮在的50ml丙酮中,然后剧烈搅拌并在回流下加热1小时,将悬浮液冷却至室温,过滤,用100ml丙酮洗涤,并在真空下干燥,得到白色固体超分子杯1(310mg,产率78%)。超分子杯1的结构式为:
[0063][0064]
在本实施例中,对中间产物p4进行表征,1hnmr(600mhz,dmso
‑
d6)δ12.27(s.4h),8.85(s.8h),8.29(s.4h),7.90(s.4h),5.60(s.4h),2.66(s.8h),2.24(s.8h).
13
c nmr(151mhz,dmso
‑
d6)δ174.36,155.55,154.52,140.25,136.14,126.45,122.55,116.93,33.49,32.45,27.21.
[0065]
在本实施例中,对中间产物p3进行表征,1h nmr(600mhz,dmso
‑
d6)δ7.81(s,4h),7.63(s,8h),7.22(s,4h),5.59(t,j=9.5hz,4h),4.06(d,j=7.1hz,8h),2.26(t,j=7.6hz,8h),1.19(t,j=7.1hz,12h).
[0066]
在本实施例中,对中间产物p2.1进行表征,1h nmr(600mhz,10%d2o/dmso
‑
d6,δppm)8.58(d,8h),8.07(s,8h),7.85(m,12h),7.72(s,4h),5.61(t,4h),4.05(t,8h),2.62(t,8h),2.29(t,8h),1.18(t,12h).
13
c nmr(151mhz,dmso
‑
d6/10%d2o,δppm)173.29,
155.96,150.10,149.74,136.84,135.29,135.17,125.00,124.36,117.32,60.63,50.54,33.36,32.72,27.49,18.56,14.46.hrms(esi):calcd for chemical formula c
96
h
76
n
12
o
16
:1652.5502,found:1653.56[m+h]
+
.
[0067]
在本实施例中,对最终产物超分子杯1进行表征,1h nmr(600mhz,d2o/10%dmso
‑
d6)δ8.78(d,8h),7.87
‑
7.72(m,20h),7.63(s,4h),5.67(t,4h),2.64(t,8h),2.25(t,8h).
13
c nmr(151mhz,d2o/10%dmso
‑
d6)δ183.43,166.41,157.19,150.65,149.80,141.32,137.05,125.77,122.40,118.52,111.75,39.09,37.43,35.04,29.85.hrms(esi):calcd for chemical formula c
88
h
56
n
12
o
16
:1540.4250,found:1538.41[m
‑
2h]2‑
。
[0068]
实验测试分析:
[0069]
取超分子杯1(16.29mg,10.00μmol)加入到25ml的样品瓶中,向内加入10ml的重水,超声使其全部溶解,得到澄清透明的淡黄色溶液(1mmol/l)。
[0070]
将上述溶液取500μl加入到核磁管中,再取5μl,100mmol/l的客体重水溶液加入到核磁管中,将溶液混合后在brukeravanceⅲhd 600m机器上测定298k的核磁共振氢谱,扫描的谱宽设置为为20,中心为5,扫描次数为64次。
[0071]
由于超分子杯1对极性小分子所具有的识别能力,且很多极性小分子由于其高亲水性导致在它成为环境污染物。我们将超分子杯的主客体识别特性应用与吸附环境污染物领域,利用超分子主体吸附水溶性强的污染物,来实现污染物检测功能。
[0072]
图1为超分子杯1的核磁氢谱图。图2为超分子杯1的核磁碳谱图。图3为超分子杯1的高分辨质谱图。图4为超分子杯1(1mmol/l,500μl)对客体(100mmol/l,5μl)络合的对极性小分子识别核磁谱图。a)超分子杯1;b)超分子杯1与四氢呋喃;c)超分子杯1与四氢吡喃;d)超分子杯1与1,3
‑
二氧六环;e)超分子杯1与1,4
‑
二氧六环;f)超分子杯1与环氧己烷。图5为超分子杯1的不同构象的快速变换图,二聚体与花瓶构象的快速变换参见图5。图10为中间产物p4的核磁氢谱图。图11为中间产物p3的核磁氢谱图。
[0073]
该化合物结构中主体空腔给予的高强度的屏蔽作用,客体分子的氢化学位移在核磁谱中会向高场移动,这往往会导致客体分子氢的核磁信号出现在0ppm之后,参见图4。单纯的1在水中的状态为“二聚体”与“花瓶”构象的快速变换,如附图3所示。这种构象快速变换的结果导致在核磁氢谱中无法观察到主体的大部分特征峰,参见图3中a)图谱。
[0074]
将上述溶液取500μl加入到2ml样品瓶中。再取上述超分子杯1溶液500μl与5μl,100mmol/l的1,4
‑
二氧六环客体重水溶液加入到2ml样品瓶中,置于365nm波长的紫外灯下观察,可以观察到加有客体溶液的样品瓶与没有客体溶液的样品瓶的荧光不同,见图12。
[0075]
取超分子杯1溶液取与上述超分子杯1主客体络合溶液,利用荧光光谱仪测试荧光吸收波长,发现二者有区别,这一方式能用来检测水中是否含有极性小分子污染物,见图13。
[0076]
本实施例水溶性较好的超分子的制备方法,在水溶性超分子杯的上缘引入了吡啶基团,增加了空腔的深度,减缓了客体的进出交换,能实现了对亲水小分子的识别。
[0077]
实施例二:
[0078]
本实施例与实施例一基本相同,特别之处在于:
[0079]
在本实施例中,一种杯芳烃衍生化的超分子大环主体化合物,其具有四层芳香结构,能溶解在水中,并具有能容纳客体分子的疏水空腔结构,还能在水中选择性识别亲水小
分子,其具有如下超分子杯2的结构式为:
[0080][0081]
一种本实施例杯芳烃衍生化的超分子大环主体化合物的制备方法,以间苯二酚或其衍生物为起始反应原料,制备水溶性吡啶基超分子杯化合物,在下缘通过氧化反应和水解反应引入羧酸钠盐以达到整体具有水溶性,在上缘引入通过与二胺的缩合引入不同的吡啶基团,使中间部分成为了苯丙咪唑基团,并使上缘吡啶的加入缩小空腔口径,减缓客体交换。其合成步骤如下:
[0082][0083]
本实施例杯芳烃衍生化的超分子大环主体化合物的制备方法,包括如下合成步骤:
[0084]
a.本步骤与实施例一相同;
[0085]
b.本步骤与实施例一相同;
[0086]
c.将在步骤b中制备的产物p3和2
‑
(3
‑
吡啶基亚甲基)丙二腈作为反应物,用80ml甲醇溶解在步骤b中制备的产物p3(500mg,1eq.),并加入8ml质量分数为25
‑
28%的氨水,得到白色沉淀物,然后使用旋转蒸发仪除去溶剂,将100ml甲醇加入烧瓶中,同时加入2
‑
(3
‑
吡啶基亚甲基)丙二腈(713mg,12eq.),在氮气下,并在80℃下剧烈搅拌15小时,然后过滤得到固体,将固体用50ml甲醇洗涤3次,50ml乙腈洗涤2次,收集固体,并于真空下干燥,得到p2.2
(381mg,产率60%);
[0087]
d.将在步骤c中制备的产物p2.2和氢氧化钠作为反应物,将在步骤c中制备的产物p2.2(400mg,0.24mmol,1eq.)添加到的其他一个容积为50ml的圆底烧瓶中,加入30ml乙醇和四氢呋喃按照体积比为1:1进行混合的混合溶剂,然后在0℃下加入氢氧化钠水溶液(1n,1.2ml,5eq.);然后将反应混合物移至40℃下,并搅拌10小时;然后将所得固体过滤并用乙醇洗涤3次,每次使用乙醇30ml;再将回收的固体悬浮在的50ml丙酮中,然后剧烈搅拌并在回流下加热1小时,将悬浮液冷却至室温,过滤,用100ml丙酮洗涤,并在真空下干燥,得到白色固体超分子杯2(328mg,产率82%)。超分子杯2的结构式为:
[0088][0089]
在本实施例中,对中间产物p2.2进行表征,1h nmr(600mhz,dmso
‑
d6/d2o 10%)δ9.06(s,4h),8.51(t,4h),8.16(t,4h),8.04(s,8h),7.85(s,4h),7.72(s,4h),7.39
‑
7.37(m,4h)5.62(t,4h),4.03(t,8h),1.74(m,8h).
13
c nmr(151mhz,dmso
‑
d6/d2o 10%)δ174.68,173.28,155.98,150.84,150.03,149.31,147.06,135.18,133.89,125.32,125.00,124.50,117.34,60.61,55.05,38.93,33.37,32.70,27.50,14.48.hrms(esi):calcd for chemical formula c
96
h
76
n
12
o
16
,found:1653.56[m+h]
+
.
[0090]
在本实施例中,对最终产物超分子杯2进行表征,1hnmr(600mhz,d2o/10%dmso
‑
d6)δ9.05(d,4h),8.38(t,4h),8.22(t,4h),7.83
‑
7.74(m,12h),7.61(s,4h),7.32(t,4h),5.62(t,4h),2.61(t,8h),2.18(t,8h).
13
c nmr(151mhz,d2o/10%dmso
‑
d6)δ155.78,150.39,149.85,149.40,136.48,135.26,124.84,120.19,117.27,45.30,40.04,39.93,39.90,39.79,39.65,39.51,39.37,39.23,39.09,33.01,31.23,29.13.hrms(esi):calcd for chemical formula c
88
h
56
n
12
o
16
:1540.4250,found:1538.41[m
‑
2h]2‑
.
[0091]
实验测试分析:
[0092]
取超分子杯2(16.29mg,10.00μmol)加入到25ml的样品瓶中,向内加入10ml的重水,超声使其全部溶解,得到澄清透明的淡黄色溶液(1mmol/l)。
[0093]
将上述溶液取500μl加入到核磁管中,再取5μl,100mmol/l的客体重水溶液加入到核磁管中,将溶液混合后在brukeravanceⅲhd 600m机器上测定298k的核磁共振氢谱,扫描的谱宽设置为为20,中心为5,扫描次数为64次。
[0094]
由于超分子杯2对极性小分子所具有的识别能力,且很多极性小分子由于其高亲水性导致在它成为环境污染物。我们将超分子杯的主客体识别特性应用与吸附环境污染物领域,利用超分子主体吸附水溶性强的污染物,来实现污染物检测功能。
[0095]
图5为超分子杯1的不同构象的快速变换图。二聚体与花瓶构象的快速变换,这一性质超分子杯2也具有。图6为超分子杯2的核磁氢谱图。图7为超分子杯2的核磁碳谱图。图8为超分子杯2的高分辨质谱图。图9为超分子杯2的对极性小分子识别核磁谱图。为水溶性超分子杯2(1mmol/l,500μl)和对客体小分子(100mmol/l,5μl)的识别,从上到下的客体依次为:四氢吡喃、环氧己烷、环己醇、环己酮和硫化环戊烷。
[0096]
本实施例水溶性较好的超分子的制备方法,在水溶性超分子杯的上缘引入了吡啶基团,增加了空腔的深度,减缓了客体的进出交换,实现了对亲水小分子的识别。本实施例超分子杯溶解在水中的同时又提供了一个可容纳客体分子的疏水空腔。
[0097]
综上所述,上述实施例水溶性吡啶基超分子杯的制备方法,以间苯二酚衍生物为起始原料在下缘通过氧化反应和水解反应引入羧酸钠盐以达到整体具有水溶性,在上缘引入通过与二胺的缩合引入不同的吡啶基团,一方面使中间部分成为了苯丙咪唑基团,另一方面上缘吡啶的加入缩小了空腔口径,减缓了客体交换。该制备方法路线工艺简便,原料易得,反应条件温和,产率高,重复性好。上述实施例的超分子杯化合物具有较好的水溶性,同时又提供了一个可以容纳客体分子的疏水空腔,可在水中选择性的识别亲水小分子,包括水污染物1,4
‑
二氧六环,识别1,4
‑
二氧六环后荧光会发生较大的变化,具有潜在的应用于环境污染检测的前景。
[0098]
上面结合附图对本发明实施例进行了说明,但本发明不限于上述实施例,还可以根据本发明的发明创造的目的做出多种变化,凡依据本发明技术方案的精神实质和原理下做的改变、修饰、替代、组合或简化,均应为等效的置换方式,只要符合本发明的发明目的,只要不背离本发明的技术原理和发明构思,都属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1