猪瘟、猪伪狂犬病毒二联亚单位疫苗及其制备方法与流程
1.本发明涉及兽用疫苗领域,具体地说,涉及一种猪瘟、猪伪狂犬病毒二联亚单位疫苗及其制备方法。
背景技术:
2.猪瘟(clssical swine fever,csf)是由猪瘟病毒(csfv)引起的一种急性烈性高度接触性传染病,一年四季均可发生,以病畜高热、内脏器官严重出血和高死亡率为特征,csf的爆发严重制约着养猪业的健康发展。
3.猪伪狂犬病(porcine pseudorabies,pr)是由伪狂犬病毒(pseudorabiesbvirus,prv)引起的、严重危害我国养猪业健康发展的重要传染病之一。该病毒属于疱疹毒科甲型疱疹病毒亚科的线性双链dna病毒,目前已知病毒糖蛋白有11种,其中gg为分泌蛋白,其余10种糖蛋白均锚定于病毒囊膜,在病毒感染、穿膜、融合细胞等过程中行使功能。伪狂犬病的易感范围很广,新生仔猪多为致死性感染,与其他易感物种类似,多死于中枢神经系统疾病。成年猪感染该病多表现呼吸系统疾病,大多呈隐性感染,无明显症状。猪感染prv后,自身的免疫系统受到损害,免疫力下降,因而更易继发其他疾病,如猪瘟、猪繁殖与呼吸综合征等,给猪伪狂犬病防治增加难度。
技术实现要素:
4.本发明的目的是提供一种猪瘟、猪伪狂犬病毒二联亚单位疫苗及其制备方法。
5.为了实现本发明目的,第一方面,本发明提供一种免疫原性组合物,包含猪瘟病毒e2蛋白、猪伪狂犬病毒gb蛋白和gd蛋白。
6.本发明中,e2、gb和gd蛋白的氨基酸序列分别如seq id no:1-3所示。
7.优选地,猪瘟病毒e2蛋白、猪伪狂犬病毒gb蛋白、gd蛋白是利用哺乳动物细胞(如cho细胞)表达系统制备得到的。
8.本发明的免疫原性组合物中e2、gb和gd蛋白的质量比为2:3:3~16:25:25。优选3:4:4。
9.第二方面,本发明提供一种猪瘟、猪伪狂犬病毒二联亚单位疫苗,包含所述免疫原性组合物和佐剂。
10.所述疫苗中猪瘟病毒e2蛋白的含量为20-80μg/ml,猪伪狂犬病毒gb蛋白的含量为30-125μg/ml,gd蛋白的含量为30-125μg/ml。
11.优选地,所述疫苗中猪瘟病毒e2蛋白的含量为30μg/ml,猪伪狂犬病毒gb蛋白的含量为40μg/ml,gd蛋白的含量为40μg/ml。
12.所述佐剂可以是油佐剂,优选isa 201vg。
13.所述免疫原性组合物与所述佐剂的质量比为1:1。
14.第三方面,本发明提供猪瘟、猪伪狂犬病毒二联亚单位疫苗的制备方法,包括以下步骤:
15.1)用pbs溶液将猪瘟病毒e2蛋白、猪伪狂犬病毒gb蛋白和gd蛋白分别稀释成浓度为90μg/ml、120μg/ml、120μg/ml;
16.2)将e2蛋白溶液、gb蛋白溶液和gd蛋白溶液按体积比1:1:1混匀即为抗原液;将抗原液与佐剂isa 201vg按质量比1:1配苗,在31
±
1℃条件下,以150-350r/min搅拌30-60分钟,乳化成水包油包水型疫苗。
17.借由上述技术方案,本发明至少具有下列优点及有益效果:
18.(一)本发明提供的猪瘟、猪伪狂犬病毒二联亚单位疫苗,其制备方法简单,猪瘟病毒e2蛋白、猪伪狂犬病毒gb蛋白和gd蛋白产量大、纯度高,抗原免疫性强,可有效激活机体的免疫反应,对猪瘟和猪伪狂犬病起到理想的免疫保护作用。
19.(二)本发明提供的猪瘟、猪伪狂犬病毒二联亚单位疫苗,与单价疫苗相比,可以减少人工成本、减少疫苗接种次数(一针双防),降低猪因疫苗免疫产生的应激反应,保护效果与单价疫苗相当,且中和抗体结果明显优于单价疫苗。
具体实施方式
20.以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别指明,实施例均按照常规实验条件,如sambrook等分子克隆实验手册(sambrook j&russell dw,molecular cloning:a laboratory manual,2001),或按照制造厂商说明书建议的条件。实施例1分别表达猪瘟e2、猪伪狂犬gb、gd蛋白的载体构建及免疫原性验证
21.1.表达猪瘟e2蛋白、猪伪狂犬病毒gb、gd蛋白细胞株的构建
22.1.1基因合成
23.1.1.1e2基因合成
24.参考国内外经典毒株和流行毒株e2基因,对其密码子进行优化,并在优化后的e2序列的n端添加不同的信号肽序列,并带上his标签,最终得到了3条编码e2基因序列并合成,分别标记为e2-1、e2-2、e2-3。
25.1.1.2gb基因合成
26.,从genbank上选用经典毒株和当前流行毒株的gb基因作为研究对象,通过密码子优化和修饰,并在优化后的gb序列的n端添加不同的信号肽序列,并带上his标签,最终得到了3条编码gb基因序列并合成,分别标记为gb-1、gb-2、gb-3。
27.1.1.3gd基因合成
28.从genbank上选用经典毒株和当前流行毒株的gd基因作为研究对象,通过密码子优化和修饰,并在优化后的gd序列的n端添加不同的信号肽序列,并带上his标签,最终得到了3条编码gd基因序列并合成,分别标记为gd-1、gd-2、gd-3。
29.2载体构建:采用常规重组质粒构建流程。
30.2.1细胞转染
31.参照lipofectaminetm3000产品使用说明书具体步骤如下。转染前一天,按细胞密度1.5
×
105个/ml,接种6孔板,每孔2.0ml,置于36℃-38℃,含5%co2细胞培养箱中孵育过夜;当细胞交汇度达到80%-90%时开始转染;用opti-mem培养基中稀释阳性质粒,制备dna预混液,然后添加lipofectamine
tm
3000试剂(充分混匀);用opti-mem培养基稀释lipofectamine
tm
3000试剂(充分混匀);将在每管已稀释的lipofectamine
tm
3000试剂中加
入稀释的dna(摩尔比1:1),室温孵育10-15分钟,然后逐滴均匀加入6孔板;36℃-38℃,含5%co2细胞培养箱中培养48小时,然后更换成dmem完全培养基(含0.8mg/ml g418)。
32.2.2单克隆细胞筛选
33.用选择dmem完全培养基(含0.8mg/ml g418)加压筛选。调整活细胞密度至1.0个/孔,接种96孔板,每孔200μl,置于36℃-38℃,待96孔板中单个细胞株扩增至80-100%以上时,通过elisa法检测单克隆细胞株蛋白的表达产量。将表达量数值较高的细胞消化并转移至24孔板,待24孔板长满时,取上清检测,通过elisa法检测单克隆细胞株蛋白的表达产量。
34.2.3蛋白表达
35.接种细胞于合适体积的培养基中的cho无血清培养基,细胞密度为1.0
×
105个/ml,36℃-38℃,含5%co2恒温摇床中培养,转速为100r/min;每隔24小时检测细胞密度、活力及葡萄糖含量,当葡萄糖低于2.5g/l时,补充葡萄糖至3-4g/l;发酵第4日和第9日补料,添加体积为原始培养基的10%;发酵第5日降温至32℃;第12日,收集细胞发酵液。分别纯化各细胞株表达蛋白后,命名为e1、e2、e3,b1、b2、b3,d1、d2、d3。
36.3、免疫原性测定
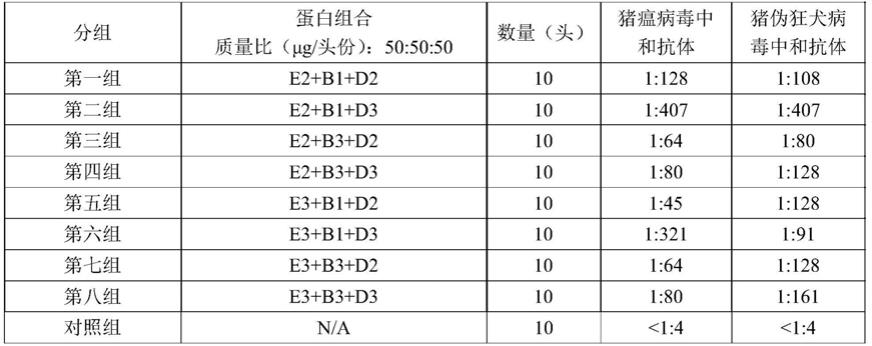
37.将上述不同猪瘟和伪狂犬病毒的蛋白片段以不同比例分别进行组合,再与isa201vg等质量混合、乳化后,制备了不同蛋白组合的疫苗样品在实验室进行km小鼠免疫实验。鉴于全部组合数据较多,本实施例给出其中部分试验分组情况,具体见表1。
38.用健康km小鼠90只,体重约20g,随机分成9组。第一组至第八组,分别免疫不同抗原组合的疫苗样品,另设10只不免疫作为对照组。免疫后21日,眼眶取血,无菌分离血清,分别测定猪瘟病毒、猪伪狂犬病毒中和抗体,试验结果见表1。
39.根据检测结果,确定中和抗体值最高的蛋白组合为猪瘟、猪伪狂犬病二联亚单位疫苗抗原组合,即e2蛋白、b1蛋白、d3蛋白的组合(第二组),最终得到编码本发明组合的猪瘟病毒e2蛋白的核酸分子(seq id no:1)、猪伪狂犬病毒gb蛋白的核酸分子(seq id no:2)、猪伪狂犬病毒gd蛋白的核酸分子(seq id no:3)。
40.表1试验分组及结果
[0041][0042]
注:“n/a”(not available)表示为不适用。
[0043]
实施例2猪瘟、猪伪狂犬病毒二联亚单位疫苗抗原比例的确定
[0044]
为确定猪瘟病毒抗原、猪伪狂犬病毒抗原的有效比例,按不同抗原含量进行配比,与isa 201vg等质量混合、乳化后,制备了8组疫苗样品在实验室进行小鼠免疫实验。
[0045]
1、疫苗制备:csfv-e2、prv-gb和prv-gd蛋白测定浓度后,按表1中蛋白含量,与无菌201佐剂(购自seppic公司)乳化制备成二联亚单位疫苗,置于4℃保存待用。
[0046]
2、免疫原性测定用健康km小鼠90只,体重约20g,随机分成9组。第一组至第八组,分别免疫不同抗原比例的疫苗,另设10只不免疫作为对照组。免疫后21日,眼眶取血,无菌分离血清,分别测定猪瘟病毒、猪伪狂犬病毒中和抗体值,每组分别取平均数作为最终结果,具体试验分组和中和抗体测定结果如表2所示。
[0047]
表2试验分组及结果
[0048][0049]
注:“n/a”(not available)表示不适用。
[0050]
从上表可以看出,各疫苗均可诱导机体产生针对猪瘟病毒、猪伪狂犬病毒中和抗体,但不同抗原配比制备的疫苗可诱导机体产生的血清中和抗体的滴度差别巨大,当e2:gb:gd质量比为20:30:30-80:125:125之间时,猪瘟病毒和伪狂犬病毒均能够产生较高的中和抗体,其中e2:gb:gd质量比为30:40:40时,猪瘟病毒和伪狂犬病毒的中和抗体能够同时达到最高值1:512。
[0051]
实施例3猪瘟、猪伪狂犬病毒二联亚单位疫苗的免疫保护效力
[0052]
用3~4周龄健康易感猪30头,根据表3进行分组,相同条件饲养。一免后14日,以相同途径与相同剂量进行二免,二免后14日进行血清中和抗体检测。免疫组5头猪连同对照猪5头,各耳后颈部肌肉注射猪瘟病毒石门系血毒1.0ml(含10
5.0
最小致死量),连续观察16日;免疫组5头猪连同对照猪5头,各滴鼻接种猪伪狂犬病毒cj株(含2
×
10
5.5
tcid
50
)2.0ml,1.0ml/鼻孔,连续观察14日。
[0053]
表3试验分组
[0054][0055]
注:“n/a”(not available)表示不适用。
[0056]
猪瘟病毒攻毒试验结果:二免后14日攻毒,连续观察16日,猪瘟e2、猪伪狂犬病二联亚单位疫苗免疫组保护率为100%;猪瘟亚单位疫苗免疫组保护率为100%。而未免疫攻毒对照组仔猪在攻毒后均出现体温反应,均伴有食欲不振、厌食甚至废食;精神萎靡、倦怠、畏寒怕冷、起卧困难、步态不稳;便秘与腹泻交替发生,产生带黏液或血丝的粪便;结膜炎,结膜充血、出血或有不正常分泌物等临床症状,5头猪全部死亡,统计攻毒对照组发病率为5/5(100%)。说明猪瘟e2、猪伪狂犬病二联亚单位疫苗和猪瘟亚单位疫苗对试验猪均具有较强的保护力而且保护效力相当,结果详见表4。
[0057]
猪伪狂犬病毒攻毒试验结果:二免后14日攻毒,连续观察14日,猪瘟e2、猪伪狂犬病二联亚单位疫苗免疫组保护率为100%;猪伪狂犬病亚单位疫苗免疫组保护率为100%。攻毒对照组在攻毒后出现体温反应,发病率为5/5(100%),并在攻毒后死亡2头试验猪。说明猪瘟e2、猪伪狂犬病二联亚单位疫苗和猪伪狂犬病亚单位疫苗对试验猪均具有坚强的保护力而且保护效力相当,结果详见表4。
[0058]
同时,从中和抗体检测情况可以看出,本发明的猪瘟、猪伪狂犬病二联亚单位疫苗免疫后获得的中和抗体远高于单独免疫猪瘟亚单位疫苗或者猪伪狂犬病亚单位疫苗的中和抗体水平。本领域公知,联苗由于多种抗原在体内发挥作用,往往存在相互干扰的情况,如何使其组合后还能获得与单苗相当的免疫效果本身就是一个技术难题,而在本发明中二者的组合取得了预料不到的协同增效作用。
[0059]
表4试验分组及结果
[0060][0061]
注:“n/a”(not available)表示不适用。
[0062]
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之做一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1