一种基于1,2,3‑三唑单元的小分子发光材料及其应用的制造方法与工艺
一种基于1,2,3-三唑单元的小分子发光材料及其应用技术领域本发明属于有机光电材料技术领域,具体涉及一种基于1,2,3-三唑单元的小分子发光材料及其应用。
背景技术:
有机电致发光器件目前已经在发光显示领域取得应用。相比聚合物发光材料而言,小分子发光材料具有制备简单,分子量确定,结构单一等优点,因此更有潜力推向更广泛的商业化应用。目前,基于小分子材料进行蒸镀或者溶液加工,制备多层器件的技术正不断地发展和进步,并取得重大的进展。目前对有机电致发光器件的研究已经取得了显著的进展。有机发光材料在电致激发的时候,产生的单线态以及三线态激子的理论比例为1:3。单线态能级的激子跃迁回基态是允许的,而三线态能级的激子跃迁回基态是禁阻的,因此,普通荧光材料的激子利用率是不高的。但是对单线态能级与三线态能级能差小的材料来说,能量略低的而且寿命较长的三线态激子可以受热激发通过反系间窜越跃迁到单线态能级上,然后发射荧光,这种荧光称为热激发延迟荧光。热激发延迟荧光材料的开发,对提高有机电致发光器件的效率起了关键的作用,而且可以避免使用磷光材料的贵金属,对于更广泛的商业化应用也具有积极意义。
技术实现要素:
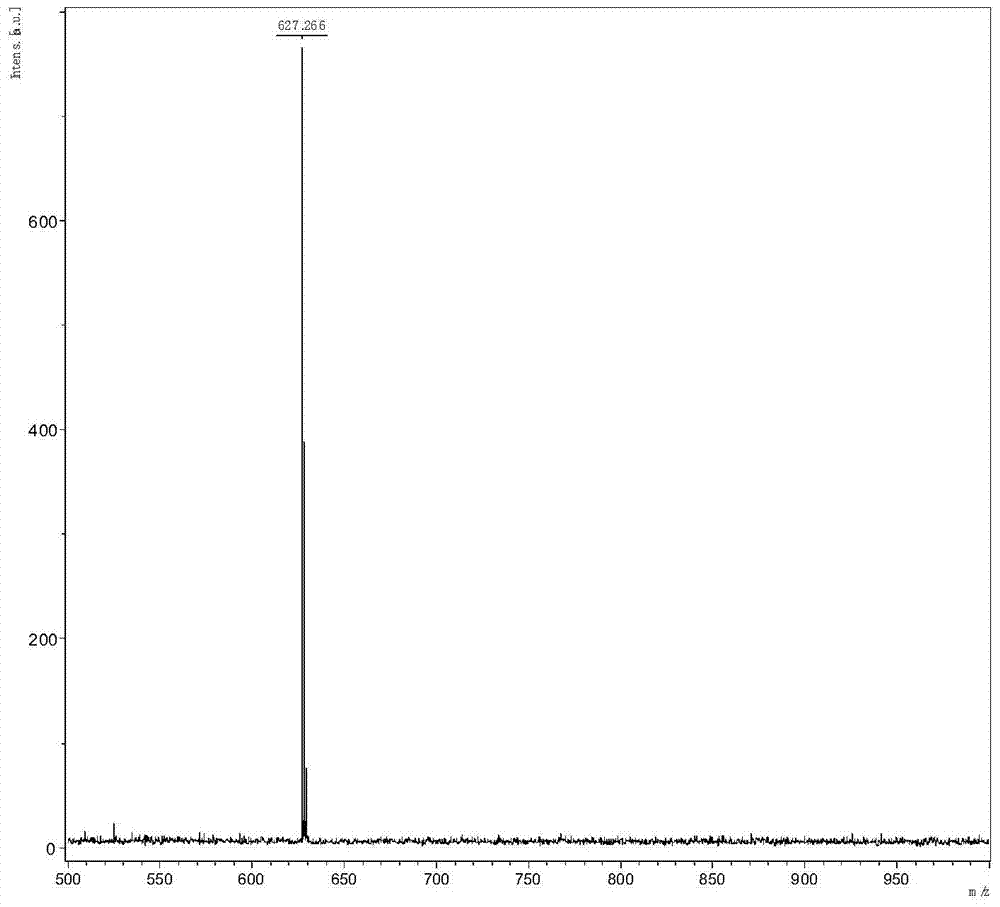
为了解决以上现有技术的缺点和不足之处,本发明的首要目的在于提供一种基于1,2,3-三唑单元的小分子发光材料。本发明的另一目的在于提供上述基于1,2,3-三唑单元的小分子发光材料在有机光电器件中的应用。本发明目的通过以下技术方案实现:一种基于1,2,3-三唑单元的小分子发光材料,所述发光材料的分子结构如下式所示:其中,Ar1和Ar2为相同或者不相同的具有如下(1)~(13)中任意一种结构式的芳香胺类基团:优选地,所述的发光材料具有如下P1~P29中任一项所示的分子结构式:上述基于1,2,3-三唑单元的小分子发光材料在有机光电器件中的应用,所述有机电致发光器件包括基板,以及依次形成在基板上的阳极层、至少一个发光层单元和阴极层;所述的发光层单元包括空穴注入层、空穴传输层、至少一个发光层和电子传输层;所述的发光层至少含有一种上述基于1,2,3-三唑单元的小分子发光材料。本发明的原理为:三唑单元的连接方式千变万化,然而目前三唑单元在有机光电领域所利用到的结构单一。因此,本发明以1,2,3-三唑为骨架单元,通过改变与其连接单元的种类、位置和数量,实现对材料分子量、π电子共轭程度以及分子内电荷转移等性质的调节。这种有机给体-受体相连接的发光材料可以实现分子内电荷转移,以及减小了单极性发光材料载流子不平衡的问题,从而简化了器件结构,以及提高了器件性能。与三唑单元连接的两个相邻单元由于位阻会发生空间扭曲,从而提高了结构的非平面性,降低了材料的堆积程度,从而抑制了材料的聚集淬灭以及激基复合物的发光。该类材料的制备简单,以芳香醛与芳香肼作为反应原料,通过一系列简单的反应,得到各种目标产物。本发明的制备方法及所得到的产物具有如下优点及有益效果:(1)本发明的新型连接方式的三唑结构的材料,具有结构单一,分子量确定,多次合成重现性好等优点,具有很高的分解温度和较低的升华温度,容易升华成高纯度的发光材料;可应用于蒸镀型有机小分子电致发光二极管中;(2)本发明的新型连接方式的三唑结构的材料具有交加的溶解性、成膜性以及薄膜形态稳定性;(3)本发明的材料结构可以通过改变连接基团的种类,从而调节材料的光色,电荷传输性能等光电器件性能;(4)本发明的材料结构可以通过调整基团连接的位置以及数量,起到调控材料的共轭长度、电子云分布、载流子传输特性和成膜性等。附图说明图1是P3、P5在二氯甲烷溶液中的吸收和发射光谱;图2和图3分别为P3和P5的MALDI-TOF-MS图;图4~6分别为实施例30以P5混杂DPEPO和P3为发光层材料的电致发光器件的电流密度-发光亮度-电压关系曲线图、电流效率-功率效率-电流密度关系曲线图和外量子效率-电流密度关系曲线图。具体实施方式下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。实施例1本实施例制备小分子发光材料P1,其反应如下式所示:具体实施步骤为:在氮气气氛下,往20mL三口烧瓶中加入中间体1(4,5-二(4-溴苯基)-2-苯基-2H-1,2,3-三唑)(1.365g,3mmol)和二苯胺(1.268g,7.5mmol),然后加入15mL1,3-二甲基-3,4,5,6-四氢-2-嘧啶酮,搅拌,待完全溶解后,往其中加入碘化亚酮(1.433g,7.5mmol)碳酸钾(2.070g,15mmol),1,3-二甲基-3,4,5,6-四氢-2-嘧啶酮1,4,7,10,13,16-六氧杂环十八烷(0.792g,3mmol),加热至190℃,反应24小时后,将反应体系降到室温,二氯甲烷萃取,用石油醚:二氯甲烷=2:1比例的洗脱剂进行硅胶柱层析,得白色固体806mg,产率42.67%。C44H33N5M/S=631.27理论值:631.27(100.0%),632.28(48.0%),633.28(11.3%),634.28(1.9%),632.27(1.8%)。C,83.65;H,5.27;N,11.09。4,5-二(4-溴苯基)-2-苯基-2H-1,2,3-三唑的合成方法参考文献(M.M.Guru,T.Punniyamurthy.J.Org.Chem.2012,77,5063),其反应如下式所示:具体实施步骤为:在250mL三口烧瓶中,将4-溴苯甲醛(9.25g,50mmol)溶于100mL甲醇溶液,在室温下搅拌至4-溴苯甲醛完全溶解。然后在氮气氛围下,缓慢往溶液中滴加苯肼(5.91mL,60mmol),滴加完毕后,有大量白色固体析出。搅拌1h后,通过旋蒸将甲醇与没有反应的苯肼蒸发出来。然后,将得到的固体在甲醇溶液中重结晶,得到产物S1,产率92.4%;在250mL单口烧瓶中,将S1(12.38g,45mmol)溶解在120mL甲苯溶液中,搅拌溶解,然后加入一水合醋酸铜(3.60g,18mmol),搅拌,并在空气氛围中加热至85℃,反应一天后停止反应,二氯甲烷萃取,用石油醚:二氯甲烷=6:1比例的洗脱剂进行硅胶柱层析,旋干后得到黄色疏松固体,烘干后得4.75g,产率为46.34%。1HNMR(400MHz,CDCl3,ppm):8.14-8.22(d,2H),7.49-7.60(m,10H),7.37-7.43(t,1H)。实施例2本实施例制备小分子发光材料P2,其反应如下式所示:具体实施步骤为:实施例1中的二苯胺换成等当量的4,4’-二叔丁基二苯胺,其他原料和步骤均同于实施例1,得白色固体产物1345mg,产率48.87%。C60H65N5M/S=855.52m/z:855.52(100.0%),856.53(65.6%),857.53(21.2%),858.53(4.7%),856.52(1.8%),857.52(1.2%)C,84.17;H,7.65;N,8.18。实施例3本实施例制备小分子发光材料P3,其反应如下式所示:具体实施步骤为:实施例1中的二苯胺换成等当量的咔唑,其他原料和步骤均同于实施例1,得白色固体产物872mg,产率46.29%。C44H29N5M/S=627.24理论值:627.24(100.0%),628.25(47.9%),629.25(11.2%),630.25(1.9%),628.24(1.8%)。C,84.19;H,4.66;N,11.16。实施例4本实施例制备小分子发光材料P4,其反应如下式所示:具体实施步骤为:实施例1中的二苯胺换成等当量的3,6-二叔丁基咔唑,其他原料和步骤均同于实施例1,得白色固体产物1527mg,产率59.78%。C60H61N5M/S=851.49理论值:851.49(100.0%),852.50(65.6%),853.50(21.2%),854.50(4.7%),852.49(1.8%),853.49(1.2%)。C,84.57;H,7.22;N,8.22。实施例5本实施例制备小分子发光材料P5,其反应如下式所示:具体实施步骤为:在氮气的氛围下,往100mL三口烧瓶中,加入中间体1(1.365g,3mmol)和吩恶嗪(6.5mmol),并加入50mL甲苯溶解,然后分别加入叔丁基醇钠、三叔丁基膦、醋酸钯。加热回流36h。停止反应后,用二氯甲烷萃取,然后用石油醚:二氯甲烷=2:1的混合溶剂作为淋洗剂进行硅胶柱层析,得到1450mg黄色产物,产率73.23%。C44H29N5O2M/S=659.23理论值:659.23(100.0%),660.24(48.0%),661.24(11.7%),662.24(2.1%),660.23(1.8%)。C,80.10;H,4.43;N,10.62;O,4.85。实施例6本实施例制备小分子发光材料P6,其反应如下式所示:具体实施步骤为:实施例5中的吩恶嗪换成等当量的吩噻嗪,其他原料和步骤均同于实施例5,得黄色固体产物1527mg,产率52.19%。C44H29N5S2M/S=691.19理论值:691.19(100.0%),692.19(49.5%),693.19(12.7%),693.18(9.1%),694.19(4.7%),692.18(1.8%),694.20(1.7%),695.19(1.1%)。C,76.38;H,4.23;N,10.12;S,9.27。实施例7本实施例制备小分子发光材料P7,其反应如下式所示:具体实施步骤为:在室温下,将1mmolP6加入到50mL单口瓶中,加入20mL醋酸和过量的30%双氧水,氧化18-24小时,抽滤,水洗,然后再用少量甲醇冲洗,干燥后以石油醚:二氯甲烷=2:1的溶剂作为淋洗剂进行硅胶柱层析,得到黄色固体产物689mg,产率91.15%。C44H29N5O4S2M/S=755.17理论值:755.17(100.0%),756.17(49.7%),757.17(13.6%),757.16(9.1%),758.17(5.2%),756.16(1.8%),758.18(1.7%),759.17(1.1%)。C,69.92;H,3.87;N,9.27;O,8.47;S,8.48。实施例8本实施例制备小分子发光材料P8,其反应如下式所示具体实施步骤为:实施例5中的吩恶嗪换成等当量的9,9’-二甲基吖啶,其他原料和步骤均同于实施例6,得黄色固体产物1184mg,产率55.44%。C50H41N5M/S=711.34理论值:711.34(100.0%),712.34(54.6%),713.34(15.3%),714.35(2.5%),712.33(1.8%)。C,84.36;H,5.81;N,9.84。实施例9本实施例制备小分子发光材料P9,其反应如下式所示:具体实施步骤为:实施例1中的4,5-二(4-溴苯基)-2-苯基-2H-1,2,3-三唑(中间体1)换成等当量的4,5-二(3-溴苯基)-2-苯基-2H-1,2,3-三唑(中间体2),其他原料和步骤均同于实施例1。得白色固体1037mg,产率54.76%。C44H33N5M/S=631.27理论值:631.27(100.0%),632.28(48.0%),633.28(11.3%),634.28(1.9%),632.27(1.8%)。C,83.65;H,5.27;N,11.09。所示中间体2的合成路线如下式所示:具体实施步骤为:实施例1中的4-溴苯甲醛换成等当量的3-溴苯甲醛,其他原料和步骤均同于实施例1,得黄色固体产物4.22g,两步反应最终产率为37.09%。实施例10本实施例制备小分子发光材料P10,其反应如下式所示:具体实施步骤为:实施例9中的二苯胺换成等当量的4,4’-二叔丁基二苯胺,其他原料和步骤均同于实施例9,得白色固体产物1444mg,产率56.22%。C60H65N5M/S=856.21m/z:855.52(100.0%),856.53(65.6%),857.53(21.2%),858.53(4.7%),856.52(1.8%),857.52(1.2%)C,84.17;H,7.65;N,8.18。实施例11本实施例制备小分子发光材料P11,其反应如下式所示:具体实施步骤为:实施例9中的二苯胺换成等当量的咔唑,其他原料和步骤均同于实施例9,得白色固体产物749mg,产率39.80%。C44H29N5M/S=627.24理论值:627.24(100.0%),628.25(47.9%),629.25(11.2%),630.25(1.9%),628.24(1.8%)。C,84.19;H,4.66;N,11.16。实施例12本实施例制备小分子发光材料P12,其反应如下式所示:具体实施步骤为:实施例9中的二苯胺换成等当量的3,6-二叔丁基咔唑,其他原料和步骤均同于实施例9,得白色固体产物1492mg,产率58.41%。C60H61N5M/S=851.49理论值:851.49(100.0%),852.50(65.6%),853.50(21.2%),854.50(4.7%),852.49(1.8%),853.49(1.2%)。C,84.57;H,7.22;N,8.22。实施例13本实施例制备小分子发光材料P13,其反应如下式所示:具体实施步骤为:实施例5中的4,5-二(4-溴苯基)-2-苯基-2H-1,2,3-三唑换成等当量的4,5-二(3-溴苯基)-2-苯基-2H-1,2,3-三唑,其他步骤和原料均同于实施例5。得到1169mg黄色产物,产率59.11%。C44H29N5O2M/S=659.23理论值:659.23(100.0%),660.24(48.0%),661.24(11.7%),662.24(2.1%),660.23(1.8%)。C,80.10;H,4.43;N,10.62;O,4.85。实施例14本实施例制备小分子发光材料P14,其反应如下式所示:具体实施步骤为:实施例13中的吩恶嗪换成等当量的吩噻嗪,其他原料和步骤均同于实施例13,得黄色固体产物1527mg,产率52.19%。C44H29N5S2M/S=691.19理论值:691.19(100.0%),692.19(49.5%),693.19(12.7%),693.18(9.1%),694.19(4.7%),692.18(1.8%),694.20(1.7%),...
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1