一种红色发光材料及其制备方法与其在白光LED器件中的应用与流程
本发明涉及发光与照明
技术领域:
,尤其涉及一种红色发光材料及其制备方法与其在白光led器件中的应用。
背景技术:
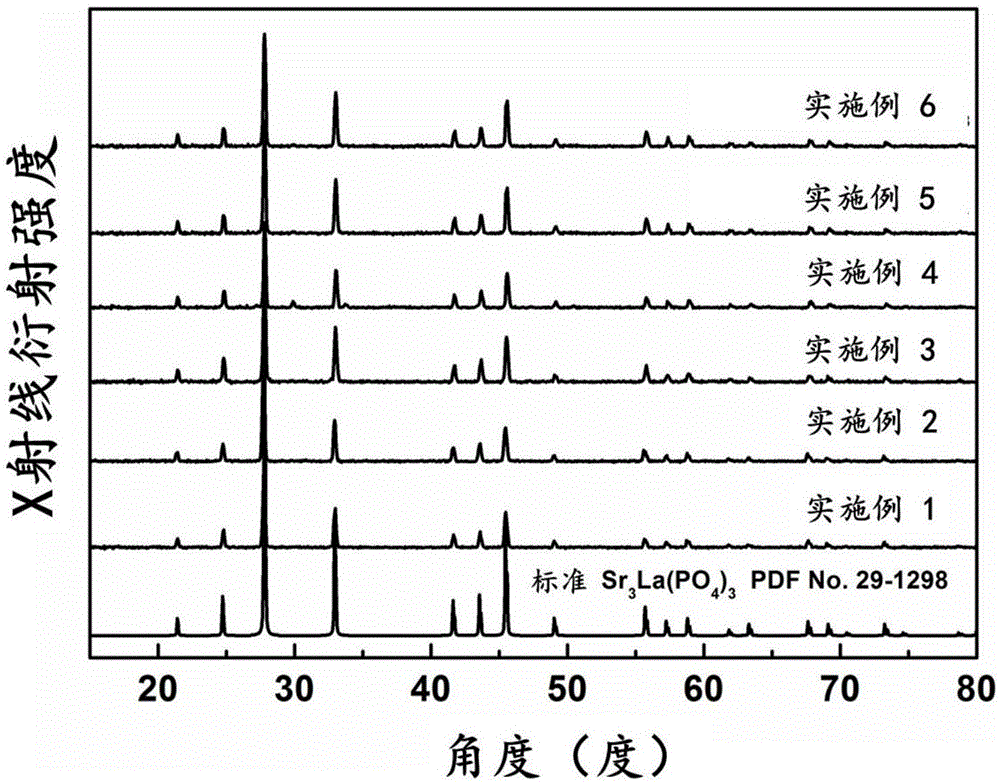
:稀土发光材料是未来新一代照明与显示技术发展不可或缺的关键材料。在照明领域,基于稀土发光材料转化的白光发光二极管(白光led)技术已引起世界各国的广泛关注,例如,目前商用的白光led是以蓝光led芯片激发黄色荧光粉产生白光,但由于光谱中缺少红光成分,白光led的显色性不高,难以满足低色温室内照明的要求。紫外光led转换红、蓝、绿三色发光材料的白光技术正迅猛发展,为了使该技术达到商品实用化要求,特别对红色发光材料的发光效率、稳定性加以改进和提高。目前商用红色发光材料主要有以下四种:(1)eu3+激活的红色荧光粉:非专利书籍1(《luminescencematerials》,1994年,第25-26页)报道,eu3+红光发射属于宇称禁阻跃迁,该类发光材料在紫外光激发下的发光效率普遍偏低。(2)eu2+激活的氮化物或氮氧化物红色发光材料,在紫外光激发下具有较高的发光效率和热稳定性,非专利文献2(《chemistryofmaterials》,2006年,18卷,第5578页)报道,该类材料需要在高温(大于1500摄氏度)、高压(约5个大气压)和厌氧环境下制备获得,制备条件较为苛刻,成本相对较高。(3)mn4+激活的氟化物红色荧光粉具有色纯度高,热稳定性好等优势,非专利文献3(《ecsjournalofsolidstatescienceandtechnology》,2016年,5(1)卷,第r3040-r3048页)报道,该类红色发光材料在合成过程中使用具有毒性的氟化物为原材料,合成产物仍有一定的毒性,对环境造成一定的危害。(4)mn2+激活的红色荧光粉:该类发光材料主要基于能量传递方式(例如eu2+与mn2+能量传递),获得高效mn2+红光发射,该类红色发光材料的种类和数量相对较多。非专利文献4(《appliedphysicsletters》,2008年,92卷,第081104页)报道,由于eu2+与mn2+的激发态能级寿命不匹配,导致eu2+→mn2+能量传递效率不高,致使mn2+的红色发光效率偏低。因此,如何提高eu2+与mn2+的能量传递效率,获得高光效的mn2+激活的红色发光材料是该类发光材料面临的巨大挑战。技术实现要素:有鉴于此,本发明的目的在于提供一种红色发光材料及其制备方法与其在白光led器件中的应用,本发明提供的红色发光材料能量传递较高、色纯度高。为了实现上述发明目的,本发明提供以下技术方案:本发明提供了一种红色发光材料,具有如下通式:m3-x-y-zre(po4)3:xeu2+,ytb3+,zmn2+;其中,m为sr、ca、mg和ba中的至少一种;re为稀土元素la、y、sc和lu中的至少一种;0<x≤0.05,0<y≤1,0<z≤1。优选地,所述红色发光材料的通式为:sr3-x-y-zla(po4)3:xeu2+,ytb3+,zmn2+、mg3-x-y-zla(po4)3:xeu2+,ytb3+,zmn2+、ba3-x-y-zy(po4)3:xeu2+,ytb3+,zmn2+、ca3-x-y-zlu(po4)3:xeu2+,ytb3+,zmn2+。优选地,所述红色发光材料的激发波长为365nm。本发明还提供了上述技术方案所述红色发光材料的制备方法,包括以下步骤:将原料研磨后,在还原气氛下,于1000~1600℃烧结3~6h,得到所述红色发光材料。优选地,所述原料包括m元素的碳酸盐、氧化物,稀土金属的氧化物,nh4h2po4,铕的氟化物或氧化物,铽的氧化物,锰的氧化物或碳酸盐。优选地,所述还原气氛包括h2/n2气氛或者co气氛。优选地,所述h2/n2气氛中h2的体积含量为10~15%。本发明还提供了上述技术方案所述红色方法材料或上述技术方案所述制备方法得到的红色发光材料在白光led器件中的应用。本发明还提供了一种白光led器件,包括所述红色发光材料。本发明提供了一种红色发光材料,具有如下通式:m3-x-y-zre(po4)3:xeu2+,ytb3+,zmn2+;其中,m为sr、ca、mg和ba中的至少一种;re为稀土元素la、y、sc和lu中的至少一种;0<x≤0.05,0<y≤1,0<z≤1。本发明在磷酸盐基质材料中掺杂eu2+、tb3+和mn2+三种发光中心,形成双敏化剂eu2+和tb3+多通道(eu2+→mn2+,tb3+→mn2+,eu2+→tb3+→mn2+),共增强mn2+发光,克服传统eu2+→mn2+单通道,能量传递效率偏低的问题。实施例的数据表明,本发明提供的红色发光材料的能量传递效率大于95%;该能量传递效率高于已报道的同类型红色发光材料的研究结果:例如:非专利文献1(《newjournalofchemistry》,2012年,36卷,第168-172页)报道,用eu2+→mn2+能量传递效率是54.6,非专利文献2(《daltontransactions》,2013年,第42卷,第5649-5654页)报道了,通过eu2+→mn2+能量传递,获得了能量传递效率约为60%的mn2+激活的红色发光材料。此外,与非专利文献1和非专利文献2比较,本发明提供的红色发光材料的发光光谱中,eu2+和tb3+的发光强度都非常低,色纯度高。本发明提供的红色发光材料的制备方法工艺简单,原料来源低廉,无污染。附图说明图1为实施例1~6制备的红色发光材料与sr3la(po4)3标准pdf卡片的xrd对比谱图;图2为实施例1制备的红色发光材料在365nm光激发下的光致发光光谱;图3为实施例2制备的红色发光材料在365nm光激发下的光致发光光谱;图4为实施例6制备的红色发光材料在365nm光激发下的光致发光光谱;图5为实施例6制备的红色发光材料分别在622nm、545nm和450nm光激发下所得的激发光谱;图6为实施例1、2、6及对比例1和2所得发光材料的荧光谱图;图7为紫外光led结合商用蓝色荧光粉、商用绿色荧光粉和实施例6红色发光材料所制备的白光led器件的电致发光光谱。具体实施方式本发明提供了一种红色发光材料,具有如下通式:m3-x-y-zre(po4)3:xeu2+,ytb3+,zmn2+;其中,m为sr、ca、mg和ba中的至少一种;re为稀土元素la、y、sc和lu中的至少一种;0<x≤0.05,0<y≤1,0<z≤1。在本发明中,所述红色发光材料的激发波长优选为365nm,进一步优选为405nm。在本发明中,所述红色发光材料的通式优选为:sr3-x-y-zla(po4)3:xeu2+,ytb3+,zmn2+、mg3-x-y-zla(po4)3:xeu2+,ytb3+,zmn2+、ba3-x-y-zy(po4)3:xeu2+,ytb3+,zmn2+、ca3-x-y-zlu(po4)3:xeu2+,ytb3+,zmn2+。在本发明的实施例中,所述红色发光材料的化学式优选为sr2.75la(po4)3:0.05eu2+,0.1tb3+,0.1mn2+;sr2.55la(po4)3:0.05eu2+,0.2tb3+,0.2mn2+;sr2.4la(po4)3:0.05eu2+,0.25tb3+,0.3mn2+;sr2.35la(po4)3:0.05eu2+,0.3tb3+,0.3mn2+;mg2.75la(po4)3:0.05eu2+,0.1tb3+,0.1mn2+;ba2.4y(po4)3:0.05eu2+,0.25tb3+,0.3mn2+;ca2.35lu(po4)3:0.05eu2+,0.3tb3+,0.3mn2+。本发明以实施例6所得的红色发光材料为例,在基质材料中掺杂金属eu2+,tb3+,mn2+,通过多通道(eu2+→mn2+,tb3+→mn2+,eu2+→tb3+→mn2+)能量传递,获得了色纯度较好的红色发光材料(红色发光占整个光谱强度的84%)。值得注意的是,本发明观察到的发光现象并非在任意基质材料中都能观测到类似现象。例如:非专利文献《inorganicchemistry》,2011,50,7846-7851,报道在bamg2al6si9o30基质材料中掺杂eu2+,tb3+,mn2+,并没有实现eu2+→tb3+→mn2+能量传递和色纯度较好的红色发光材料。非专利文献《ecsjournalofsolidstatescienceandtechnology》,2013,2(9)r213-217报道在ba3mgsi2o8基质材料中同时掺杂eu2+,tb3+,mn2+,尽管观测到了多通道(eu2+→mn2+,tb3+→mn2+,eu2+→tb3+→mn2+)共增强mn2+发光的现象,但其色纯度不高(红色发光强度仅占整个光谱强度的77%)。本发明采用xeu2+、ytb3+和zmn2+对m3-x-y-zre(po4)3中的m进行取代掺杂,三种发光中心eu2+、tb3+和mn2+的掺杂,形成双敏化剂eu2+和tb3+共增强mn2+发光,克服传统eu2+→mn2+能量传递效率偏低的问题。由于m的价态为+2,而进行取代掺杂的元素中eu2+、mn2+,与m2+的价态相同,进行取代掺杂的时候,不会影响发光材料的价态;而tb为+3价,其对m2+进行取代掺杂时,属于不等价原子替换,会影响所得发光材料的价态,使其化学价态不为0,这种情况属于化学领域的非化学计量比化合物,即化合物中化学成分与晶体结构中不同原子所占据的比例不相符合,它们的组成不符合化合价规则,不服从组成定律,组成偏离了化学计量,均匀的物相。从点阵结构上看,非化学计量化合物组成的偏离值也可能很小,已超过了x射线衍射仪器的检测极限,故不易被察觉。非化学计量比化合物很常见,由于非化学计量比化合物中各种缺陷的存在,会给材料带来许多特殊的光、电、声、磁、力和热的性质,目前一些非计量比化合物已经被广泛应用于陶瓷、超导体和电化学材料中。这种非化学计量比化合物的总化合价不一定为零,而本发明请求保护的红色发光材料即为非化学计量比化合物,基质总化合价不为零。本发明还提供了上述技术方案所述红色发光材料的制备方法,包括以下步骤:将原料研磨后,在还原气氛下,于1000~1600℃烧结3~6h,得到所述红色发光材料。在本发明中,所述原料优选包括m元素的碳酸盐、氧化物,稀土金属的氧化物,nh4h2po4,铕的氟化物或氧化物,铽的氧化物,锰的氧化物或碳酸盐。本发明的实施例中,所述研磨的时间优选为15~30min。在本发明中,所述研磨能够将原料充分的磨细并混合均匀,对后续得到目标材料提供可能。在本发明中,所述还原气氛优选包括h2/n2气氛或者co气氛。在本发明中,所述h2/n2气氛中h2的体积含量优选为10~15%。在本发明中,所述烧结的温度为1000~1600℃,进一步优选为1200~1500℃;所述烧结的时间为3~6h。本发明对进行所述烧结的装置没有特殊的限定,采用本领域技术人员熟知的加热装置即可,具体的,如高温炉。烧结结束后,本发明优选将烧结产物在空气中冷却,将冷却后物质研细,得到所述红色发光材料。本发明在还原气氛下对原料烧结能够使原料充分还原,形成目标产物。本发明提供的红色发光材料的制备方法简单,原料来源低廉,无污染。本发明还提供了上述技术方案所述红色发光材料或上述技术方案所述制备方法得到的红色发光材料在白光led器件中的应用。本发明还提供了一种白光led器件,所述白光led器件包括所述红色发光材料。在本发明中,所述白光led器件的制备方法优选包括以下步骤:(a)将商用蓝色发光材料、黄色发光材料和本发明所述红色荧光粉混合,得到白光荧光粉;(b)将所述步骤(a)得到的白色荧光粉均匀分散到硅胶中,得到胶粉混合物;(c)将所述步骤(b)得到的胶粉混合物涂敷在led芯片上,得到所述白光led器件。本发明将商用蓝色发光材料、黄色发光材料和本发明所述红色荧光粉混合,得到白光荧光粉。本发明对所述商用蓝色发光材料、黄色发光材料和本发明所述红色发光材料的用量比没有特殊的限定,只要能够将其配制成白色荧光粉即可,具体的,如所述蓝色发光材料、黄色发光材料与本发明所述红色荧光粉的质量比优选为1:1.4:1.2。得到白色荧光粉后,本发明将所述白色荧光粉均匀分散到硅胶中,得到胶粉混合物。在本发明中,所述硅胶的质量优选为白色荧光粉质量的5~20%,进一步优选为10~15%。本发明对所述白色荧光粉分散到硅胶中的方法没有特殊的限定,只要能够使白色荧光粉均匀分散到硅胶中即可。白色荧光粉均匀分散到硅胶中后,本发明优选将均匀分散的白色荧光粉-硅胶转移至真空干燥器中,连续抽真空3~5h,得到所述胶粉混合物。得到胶粉混合物后,本发明将所述胶粉混合物涂敷在led芯片上,得到所述白光led器件。本发明对涂敷的方式没有特殊的限定,只要能够使胶粉混合物能够均匀涂敷在led芯片上即可。涂敷结束后,本发明优选将涂敷有胶粉混合物的led芯片在120℃持续烘干3~5h。下面结合实施例对本发明提供的红色发光材料及其制备方法与其在白光led器件中的应用进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。实施例1所述红色发光材料的化学式为sr3-x-y-zla(po4)3:xeu2+,ytb3+,zmn2+,其中x=0.05,y=0,z=0.3,具体表达式sr2.65la(po4)3:0.05eu2+,0.3mn3+。上述红色发光材料的制备方法:称取srco31.956g,la2o30.8145g,nh4h2po41.725g,eu2o30.04399g,tb4o70g,mnco30.1724g;将上述原料充分研磨20min,将混合后的粉末装入氧化铝坩埚或者碳坩埚中,放入高温炉中在10%h2/90%n2还原气氛下1000℃高温烧结6h,冷却取出研细,得到红色发光材料。该红色发光材料是基于eu2+→mn2+单一通道能量传递获得的红色发光材料。结果为本实施所得红色发光材料的色纯度60%(红色发光强度占整个光谱强度的60%)。实施例2所述红色发光材料的化学式为sr3-x-y-zla(po4)3:xeu2+,ytb3+,zmn2+,其中x=0.00,y=0.3,z=0.3,具体表达式sr2.4la(po4)3:0.3tb3+,0.3mn2+。上述红色发光材料的制备方法:称取srco31.772g,la2o30.8145g,nh4h2po41.725g,eu2o30g,tb4o70.2804g,mnco30.1724g;将上述原料充分研磨20min,将混合后的粉末装入氧化铝坩埚或者碳坩埚中,放入高温炉中在10%h2/90%n2还原气氛下1100℃高温烧结3h,冷却取出研细,得到红色发光材料。采用与实施例1相同的测试和计算方法,测试发现本实施例是基于tb2+→mn2+单一通道能量传递获得的红色发光材料,计算红色发光材料的色纯度为65%(红色发光强度占整个光谱强度的65%)。实施例3所述红色发光材料的化学式为sr3-x-y-zla(po4)3:xeu2+,ytb3+,zmn2+,其中x=0.05,y=0.1,z=0.1,具体表达式sr2.75la(po4)3:0.05eu2+,0.1tb3+,0.1mn2+。上述红色发光材料的制备方法:称取srco32.029g,la2o30.8145g,nh4h2po41.725g,eu2o30.04399g,tb4o70.09346g,mnco30.05748g;将上述原料充分研磨25min,将混合后的粉末装入氧化铝坩埚或者碳坩埚中,放入高温炉中在10%h2/90%n2还原气氛下1400℃高温烧结5h,冷却取出研细,得到红色发光材料。采用与实施例1相同的测试和计算方法,测试发现本实施例是基于eu2+→mn2+,tb3+→mn2+,eu2+→tb3+→mn2+三通道能量传递获得的红色发光材料,计算该红色发光材料的色纯度发光为69%。实施例4所述红色发光材料的化学式为sr3-x-y-zla(po4)3:xeu2+,ytb3+,zmn2+,其中x=0.05,y=0.2,z=0.2,具体表达式sr2.55la(po4)3:0.05eu2+,0.2tb3+,0.2mn2+。上述红色发光材料的制备方法:称取srco31.882g,la2o30.8145g,nh4h2po41.725g,eu2o30.04399g,tb4o70.1869g,mnco30.1150g;将上述原料充分研磨20min,将混合后的粉末装入氧化铝方舟中,放入高温炉中在10%h2/90%n2还原气氛下1400℃高温烧结4h,冷却取出研细,得到红色发光材料。采用与实施例1相同的测试和计算方法,测试发现本实施例是基于eu2+→mn2+,tb3+→mn2+,eu2+→tb3+→mn2+三通道能量传递获得的红色发光材料,计算该红色发光材料的色纯度为73%。实施例5所述红色发光材料的化学式为sr3-x-y-zla(po4)3:xeu2+,ytb3+,zmn2+,其中x=0.05,y=0.25,z=0.3,具体表达式sr2.4la(po4)3:0.05eu2+,0.25tb3+,0.3mn2+。上述红色发光材料的制备方法:称取srco31.772g,la2o30.8145g,nh4h2po41.725g,eu2o30.04399g,tb4o70.2337g,mnco30.1724g;将上述原料充分研磨20min,将混合后的粉末装入氧化铝坩埚或者碳坩埚中,放入高温炉中在10%h2/90%n2还原气氛下1600℃高温烧结3h,冷却取出研细,得到红色发光材料。采用与实施例1相同的测试和计算方法,测试发现本实施例是基于eu2+→mn2+,tb3+→mn2+,eu2+→tb3+→mn2+三通道能量传递的红色发光材料,计算该红色发光材料的色纯度为78%。实施例6所述红色发光材料的化学式为sr3-x-y-zla(po4)3:xeu2+,ytb3+,zmn2+,其中x=0.05,y=0.3,z=0.3,具体表达式sr2.35la(po4)3:0.05eu2+,0.3tb3+,0.3mn2+。上述红色发光材料的制备方法:称取srco31.734g,la2o30.8145g,nh4h2po41.725g,eu2o30.04399g,tb4o70.2804g,mnco30.1724g;将上述原料充分研磨20min,将混合后的粉末装入氧化铝坩埚或者碳坩埚中,放入高温炉中在10%h2/90%n2还原气氛下1200℃高温焙烧4h,冷却取出研细,得到红色发光材料。采用与实施例1相同的测试和计算方法,测试发现本实施例是基于eu2+→mn2+,tb3+→mn2+,eu2+→tb3+→mn2+三通道能量传递获得的红色发光材料,计算该红色发光材料的色纯度为84%。实施例7所述红色发光材料的化学式为mg3-x-y-zla(po4)3:xeu2+,ytb3+,zmn2+,其中x=0.05,y=0.1,z=0.1,具体表达式mg2.75la(po4)3:0.05eu2+,0.1tb3+,0.1mn2+。上述红色发光材料的制备方法:称取mgco31.159g,la2o30.8145g,nh4h2po41.7254g,eu2o30.04399g,tb4o70.09346g,mnco30.05747g;将上述原料充分研磨20min,将混合后的粉末装入氧化铝坩埚或者碳坩埚中,放入高温炉中在10%h2/90%n2还原气氛下1600℃高温烧结3h,冷却取出研细,得到红色发光材料。采用与实施例1相同的测试和计算方法,测试发现本实施例是基于eu2+→mn2+,tb3+→mn2+,eu2+→tb3+→mn2+三通道能量传递获得的红色发光材料,计算该红色发光材料的色纯度为71%。实施例8所述红色发光材料的化学式为ba3-x-y-zy(po4)3:xeu2+,ytb3+,zmn2+,其中x=0.05,y=0.25,z=0.3,具体表达式ba2.4y(po4)3:0.05eu2+,0.25tb3+,0.3mn2+。上述红色发光材料的制备方法:称取baco32.368g,y2o30.5645g,nh4h2po41.725g,eu2o30.0439g,tb4o70.2336g,mnco30.1724g;将上述原料充分研磨20min,将混合后的粉末装入氧化铝坩埚或者碳坩埚中,放入高温炉中在10%h2/90%n2还原气氛下1400℃高温烧结3h,冷却取出研细,得到红色发光材料。采用与实施例1相同的测试和计算方法,测试发现本实施例是基于eu2+→mn2+,tb3+→mn2+,eu2+→tb3+→mn2+三通道能量传递获得的红色发光材料,计算该红色发光材料的色纯度为77%。实施例9所述红色发光材料的化学式为ca3-x-y-zlu(po4)3:xeu2+,ytb3+,zmn2+,其中x=0.05,y=0.3,z=0.3,具体表达式ca2.35lu(po4)3:0.05eu2+,0.3tb3+,0.3mn2+。上述红色发光材料的制备方法:称取caco31.175g,lu2o30.9948g,nh4h2po41.725g,eu2o30.0439g,tb4o70.2803g,mnco30.1724g;将上述原料充分研磨20min,将混合后的粉末装入氧化铝坩埚或者碳坩埚中,放入高温炉中在10%h2/90%n2还原气氛下1300℃高温烧结3h,冷却取出研细,得到红色发光材料。采用与实施例1相同的测试和计算方法,测试发现本实施例是基于eu2+→mn2+,tb3+→mn2+,eu2+→tb3+→mn2+三通道能量传递获得的红色发光材料,计算该红色发光材料的色纯度为79%。对比例1所述发光材料的化学式为sr2.95la(po4)3:0.05eu2+。对比例2所述发光材料的化学式为sr2.7la(po4)3:0.3tb3+。图1为实施例1~6制备的红色发光材料与sr3la(po4)3标准pdf卡片的xrd对比谱图;从图1可以看出:本专利红色发光材料的x射线衍射峰的数目和位置与国际晶体学谱库中标准的sr3la(po4)3的衍射数据信息完全一致(pdf卡片号:29-1298)。根据物理与化学的公认的原理,可以推断本专利红色发光材料为sr3la(po4)3化合物。图2为在紫外光波长为365nm光激发下,实施例1制备的红色发光材料sr2.65la(po4)3:0.05eu2+,0.3mn2+的光致发光光谱,从图2可以看出:红色发光材料中的主要发射峰为mn2+的特征发射峰(发光波长为620nm),光谱中存在eu2+的特征绿色发射峰(发光波长为520nm),绿色发射峰的强度占红色发射峰强度的40%。图3为在紫外光波长为365nm光激发下,实施例2制备的红色发光材料sr2.4la(po4)3:0.3tb3+,0.3mn2+的光致发光光谱;从图3可以看出:红色发光材料中的主要发射峰为mn2+的特征发射峰(发光波长为620nm),光谱中存在tb3+的特征绿色发射峰(发光波长为545nm),绿光发光强度占红光发光强度的34%。图4为在紫外光波长为365nm光激发下,实施例6制备的红色发光材料sr2.35la(po4)3:0.05eu2+,0.3tb3+,0.3mn2+的光致发光光谱;从图4可以看出:红色发光材料中的主要发射峰为mn2+的特征发射峰(发光波长为620nm),光谱中存在tb3+的特征绿色发射峰(发光波长为545nm),其发光强度占红色发射峰的强度的15%;eu2+的特征发射峰位于430nm,其发光强度非常弱,仅占红色发射峰的强度的5%。与实施1和实施例2相比,实施例3的eu2+/tb3+特征发射峰强度显著降低,红色发射峰强度显著增强,eu2+→tb3+→mn2+能量传递效率提高。因此,红色发光材料的色纯度有显著提高。图5为实施例6制备的发光材料sr2.35la(po4)3:0.05eu2+,0.3tb3+,0.3mn2+,分别监测mn2+的特征发射峰(发光波长为622nm)、tb3+的特征发射峰(发光波长545nm)和eu2+的特征发射峰(发光波长为450nm)获得的激发光谱,从图5可以看出:由于监测tb3+和mn2+发射峰获得的激发光谱的光谱外型与监测eu2+发射峰获得的激发光谱的谱型基本相似,可以推断在该材料中一定存在eu2+→tb3+→mn2+能量传递。图6为实施例1、2、6及对比例1和2所得发光材料的荧光谱图,从图6可以看出:由于对比例1中的红色发光材料仅掺杂eu2+,荧光为发光波长为430nm的蓝色发光;实施例1所得的发光材料由于掺杂eu2+和mn2+,样品的发光波长为610nm和450nm(暗红色),红色发光强度占整个光谱强度的60%;对比例2中的红色发光材料由于仅掺杂tb3+,荧光为发光波长为554nm的绿色发光;实施例2所得的发光材料由于掺杂eu2+和mn2+,样品的发光波长为554nm和610nm(菊红色),红色发光强度占整个光谱强度的65%。实施例6所得的发光材料,由于掺杂eu2+、tb3+、mn2+,红色发光材料的色纯度为84%,样品中蓝色发光(eu2+,430nm),光谱中几乎探测不到,绿色发光(tb3+,554nm)仅占红色发光强度的15%。说明只有在sr3la(po4)3中掺杂eu2+、tb3+、mn2+三种发光中心后,光谱中才能表现出非常强的mn2+红色发光,同时eu2+,tb3+的发光在光谱中非常的弱(色纯度相对较高)。采用文献(《rscadavances》,2013,第3卷,24期,9311-9318页)中公开的能量传递效率计算公式η=1-is/iso;其中,η为能量传递效率,is为掺杂mn2+(或者tb3+)后eu2+的发光强度,is为未掺杂mn2+(或者tb3+)eu2+的发光强度),再结合实施例1~9所得红色发光材料的荧光强度,计算实施例1~9所得红色发光材料的eu2+→mn2+能量传递效率,结果如表1所示。从表1可以看出:在磷酸盐基质材料中掺杂eu2+、tb3+和mn2+三种发光中心,显著地提高了能量传递效率。通过优化eu2+、tb3+和mn2+三种发光中心的掺杂浓度比例,实施例6中eu2+→mn2+能量传递效率为最大值(98.4%),克服单一通道eu2+/tb3+→mn2+能量传递效率偏低的问题。表1实施例1~9所得红色发光材料的能量传递效率结果序号(实施例)123456789能量传递效率(%)80%65%96.3%97.2%97.8%98.4%83.2%88.289.4%图7为紫外光led结合商用蓝色荧光粉、商用绿色荧光粉和实施例6所得红色发光材料(其中,蓝色发光材料、黄色发光材料与本发明所述红色荧光粉的质量比优选为1:1.4:1.2)制备的白光led器件的电致发光光谱,从图7可以看出:利用本专利研发的红色荧光材料可以制备高显色性(~91)、低色温(~4436开尔文)的白光led光源器件,器件性能基本满足室内光源高显色性、低色温的照明要求。以上所述仅是本发明的优选实施方式,应当指出,对于本
技术领域:
的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1