人工合成水铁矿及其在新型光-Fenton体系中的应用方法与流程
本发明属于环境保护和治理技术领域,具体是一种人工合成水铁矿及其在新型光-fenton体系中的应用方法。
背景技术:
环境内分泌干扰物(endocrinedisruptingcompounds,edcs)是一类会影响机体内稳定性的外源有害化学物质,广泛存在于环境中。通过生物体的捕食作用,使得edcs经消化系统进入机体,破坏机体内源激素的作用机制,从而影响生物体的正常生长和繁殖。中国主要以地表水作为主要饮用水,因此,减少或去除地表水中的edcs,对于人体的生命健康非常重要。bpa是类雌性激素物质,是具有代表性的edcs,同时也是运用最广泛的化学工业品之一。它对于人体的影响是一个不断累积、不可逆的过程,具有持续性危害。因此,亟待寻求高效降解以bpa为代表的环境内分泌污染物的处理技术。
高级氧化技术(advancedoxidationprocess,aops)是一种环境友好型的深度处理技术,已被广泛用于降解水中、土壤和空气中的有机和无机污染物。其中fenton氧化技术已较为成熟且得到广泛应用,在fe2+和h2o2组成的fenton试剂中,fe2+催化h2o2产生氧化活性极高的羟基自由基(·oh),使其作用于高分子有机污染物并将其直接矿化成无毒无害的小分子物质,实现污染物的降解。但传统的fenton氧化技术存在许多缺点,如ph适用范围窄,要求一般是在酸性条件下。此外,废水反应后会产生大量的铁泥,造成铁资源的浪费,也增加了后续处理难度和成本。另外,体系中的h2o2用量较高,增加了运行成本。
光-fenton氧化技术是在fenton体系引入紫外光或可见光,提高了h2o2的利用效率,减少了fe2+的使用,大大增强传统fenton法的氧化效率,达到降低反应成本的目的。目前,光-fenton氧化技术已经应用于造纸、冶金、染料和垃圾渗滤液等难降解有机工业废水的处理。但光-fenton法也存在污水处理后铁离子后续处理的传统芬顿缺点。
因此,急需一种能克服传统fenton法ph适用范围窄、产生大量铁泥的缺陷的技术。
技术实现要素:
本发明所要解决的技术问题是提供一种人工合成水铁矿及其在新型光-fenton体系中的应用方法,该方法在中性ph、可见光照射下能加速fe3+和fe2+之间的氧化还原循环,从而加快了fe2+催化h2o2生成·oh的速率,提高了bpa的降解效率,并且减少了氧化剂h2o2的使用量。
本发明以如下技术方案解决上述技术问题:
本发明所述人工合成水铁矿的制备方法如下:
称取40.0gfe(no3)3·9h2o溶于500ml去离子水中,加入310ml浓度为1mol/l的koh溶液,继续用1mol/lkoh将溶液ph调节至7.4-7.6,剧烈搅拌1h,将所得的胶体离心处理12min,弃去上清液,用去离子水冲洗所得的固体,摇匀,离心处理12min,弃去上清液,如此重复5次后于40℃烘干,即得到人工合成水铁矿。
本发明所述加入koh溶液时以100ml/min的速度添加;所述离心处理时以4000转/分钟的速度进行离心处理。
本发明所述人工合成水铁矿在新型光-fenton体系中的应用方法,它的操作步骤如下:
(1)将目标污染物bpa置于大烧杯中;
(2)在大烧杯中加入羧酸;
(3)再加入人工合成水铁矿;
(4)在上述混合溶液中加入过氧化氢;
(5)最后加入可见光,组成水铁矿-羧酸/光-fenton体系,降解环境内分泌干扰物bpa。
步骤1)中,所述目标污染物bpa的浓度为20μmol/l。
步骤2)中,所述羧酸为乙二胺二琥珀酸(edds),其在混合体系中的浓度为0.5~2.5mmol/l。
步骤3)中,所述人工合成水铁矿在体系中的浓度为0.2~1.0g/l,并曝气使水铁矿与羧酸充分络合后,调节ph至7.0±0.1。
步骤4)中,加入的过氧化氢在体系中的浓度为0.1~1.0mmol/l。
步骤5)中,所述可见光采用金属卤化灯照射,辐照方式为内照射。
与现有技术相比,本发明具有如下优点:
1)本发明能够克服传统fenton法ph适用范围窄、产生大量铁泥的缺陷,本发明采用铁氧化物和羧酸络合后与光-fenton体系形成非均相芬顿体系,可拓宽ph值的范围,减少铁泥的产生,具有较高的吸光性。
2)本发明方法操作简便,在bpa溶液中加入羧酸,并将水铁矿加入bpa和羧酸的混合溶液里,曝气形成络合物,再通过调节ph值、加入过氧化氢、施加金属卤化灯辐照,使反应中fe2+催化h2o2生成大量氧化性能极强的·oh,·oh作用于bpa对其进行降解。
3)在使用本发明方法时不用调节ph到2~3,并且本发明因水铁矿和羧酸的加入,加速了fe3+与fe2+的氧化还原循环,加快了fe2+催化h2o2生成·oh的速率,提高了铁氧化物和h2o2的利用率,减少了氧化剂h2o2的使用量,极大地节约了试剂。
4)本发明中bpa降解率可达到85.1%,并且本发明工艺简易方便,采用的实验试剂和原料来源广,易购买,价格便宜。
附图说明
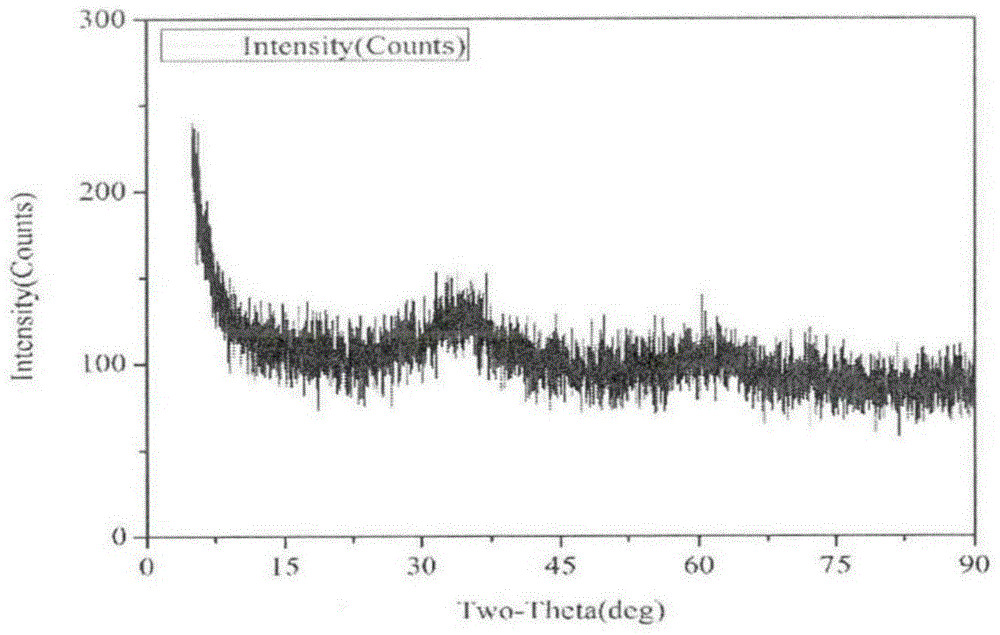
图1是本发明实施例1人工合成水铁矿的x射线衍射(xrd)分析图。
图2是本发明实施例2人工合成水铁矿在新型光-fenton体系中应用分析测定图。
图3是本发明实施例3人工合成水铁矿在新型光-fenton体系中应用分析测定图。
图4是本发明实施例4人工合成水铁矿在新型光-fenton体系中应用分析测定图。
具体实施方式
下面结合附图和具体实施例对本发明方法作进一步说明。
实施例1:
称取40.0gfe(no3)3·9h2o溶于500ml去离子水中,以100ml/min的速度加入浓度为1mol/l的koh溶液,继续用1mol/lkoh将溶液ph调节至7.5左右,剧烈搅拌1h,将所得的胶体以4000转/分钟的速度离心处理12min,弃去上清液,用去离子水冲洗所得的固体,摇匀,以4000转/分钟的速度离心处理12min,弃去上清液,如此重复5次后于40℃烘干,即得到人工合成水铁矿。
采用x射线衍射(xrd)对上述人工合成的水铁矿晶体结构进行分析。
其测定条件为:xrd采用压片法在40kv电压和100ma电流下进行,2θ/θ偶合连续扫描,0.02°步宽,扫描速度为10°/分。结果如图1所示。水铁矿出现了两个强度较弱的宽峰。xrd衍射图中衍射谱峰出现在2θ=34.65°,61.24°,其d值与2-线水铁矿(2lfh)的衍射峰一致,说明合成的水铁矿主要成分为2-线水铁矿,目前普遍接受的水铁矿化学式为fe5ho8·4h2o。
实施例2:
在2.0mmoll-1的bpa储备液中取10ml置于1l的大烧杯中,依次从50mmoll-1的edds储备液中移取10、20、30、40、50ml溶液加入到烧杯中(edds在混合体系中的浓度分别为0.5、1.0、1.5、2.0、2.5mmoll-1),然后再加0.6g水铁矿(实施例1制备得到)至烧杯中,曝气使其充分络合,稀释至接近一升,待其充分混合后,调节ph至7.0±0.1,再加入50μl的h2o2溶液(30%,密度1.13g/cm3),h2o2溶液在混合体系中的浓度为0.5mmoll-1,然后转移至1000ml容量瓶中定容,再倒入金属卤化灯光催化反应器中,照射时开始计时。在0、10、30、60、120、240、360min时刻用移液枪取1.0ml水样进行测定,结果如图2所示。
实施例3:
在2.0mmoll-1的bpa储备液中取10ml置于1l的大烧杯中,从50mmoll-1的edds储备液中移取20ml溶液加入到烧杯中(edds在混合体系中的浓度为1.0mmoll-1),然后依次加0.2、0.4、0.6、0.8、1.0g的水铁矿(实施例1制备得到)至烧杯中,曝气使其充分络合,稀释至接近一升,待其充分混合后,调节ph至7.0±0.1,再加入50μl的h2o2溶液(30%,密度1.13g/cm3),h2o2溶液在混合体系中的浓度为0.5mmoll-1,然后转移至1000ml容量瓶中定容,倒入金属卤化灯光催化反应器中,照射时开始计时。在0、10、30、60、120、240、360min时刻用移液枪取1.0ml水样进行测定,结果如图3所示。
实施例4:
在2.0mmoll-1的bpa储备液中取10ml置于1l的大烧杯中,从50mmoll-1的edds储备液中移取20ml溶液加入到烧杯中(edds在混合体系中的浓度为1.0mmoll-1),然后加0.6g的水铁矿(实施例1制备得到)至烧杯中,曝气使其充分络合,稀释至接近一升,待其充分混合后,调节ph至7.0±0.1,再依次加入10、25、50、75、100μl的h2o2溶液(30%,密度1.13g/cm3),h2o2溶液在混合体系中的浓度分别为0.1、0.25、0.5、0.75、1.0mmoll-1,然后转移至1000ml容量瓶中定容,倒入金属卤化灯光催化反应器中,照射时开始计时。在0、10、30、60、120、240、360min时刻用移液枪取1.0ml水样进行测定,结果如图4所示。
上述实施例从开始光照到反应结束,反应液在反应器中停留360min,edds的添加量具有最佳值。在0.5~1.0mmoll-1时,随着edds浓度的提高,bpa的降解率逐渐升高,当超过最佳值1.0mmoll-1时,bpa的降解率反而逐渐降低(如图2所示)。随着水铁矿的投加量逐渐升高,bpa的降解率逐渐升高,当超过最佳值0.6g/l时,bpa的降解率反而下降。随着初始h2o2的浓度的升高,bpa降解率缓慢升高,当超过最佳值0.5mmoll-1时,bpa降解率缓慢下降。最终在最佳实验条件下,bpa的降解率为85.1%。
- 还没有人留言评论。精彩留言会获得点赞!