一类含硫醚官能团的羧酸配合物杂化材料及其制备方法与流程
本发明属于材料合成领域,具体而言,涉及一种mof材料mil-125-(sch3)2及其制备方法,该mof材料具有可见光催化裂解水析氢性质。
背景技术:
相较于二氧化钛和无机半导体材料,mof材料(金属有机骨架化合物材料)由于其有机配体的可人工合成制备及性能调控特点,在光催化领域的应用前景非常值得期待。但迄今为止,mof材料做光催化剂的效率还比较低,具有可见光催化裂解水的mof材料种类还很有限。
mil-125系列mof材料是一种以钛氧八面体为金属中心,以对苯二甲酸为有机连接配体,具有四面体或八面体两种笼结构的金属有机骨架化合物材料。其作为光催化剂的研究虽然已经取得了很大的进展,尤其是mof材料作为光催化裂解水产氢,近年来这方面的研究正在兴起。但就目前的研究成果来看,mof材料作为光催化剂的效率相较于无机半导体材料来说依然很低,而且稳定性相对来说不足,所以寻找有效提升mof材料本身的可见光催化析氢效率的方法变得至关重要。
为了提高mof材料的产氢效率,对其产氢性能的研究重点已经从紫外光区转移到可见光区,大多是利用mof结构的可调性和多孔性,一种是通过对mofs材料的有机配体进行调节改性或者修饰使其可以更有效的利用可见光,另一条思路是利用mof材料的多孔性来更加有效的分散无机光催化纳米材料形成所谓的杂合材料,从而提高光催化裂解水析氢效率。
另外人们发现,在合成具有特定结构和功能的多孔材料时常常很难通过常规方法直接得到预期的mof材料。所以需要选用一种方法来规避mof合成过程中的一些意外情况的产生,以直接明确的得到自己想要的功能性mof材料。
技术实现要素:
针对上述现有技术中存在的问题,本发明提供一种含硫醚官能团的羧酸配体的mil-125系列mof材料,通过对配体的修饰来拓宽mof材料的光吸收范围使其能够响应可见光。
根据本发明的一个方面,本发明的一个目的在于提供一种具有可见光催化裂解水析氢性质的mof材料mil-125-(sch3)2,所述mof材料中的金属结点为ti(ⅳ),所述有机配体为对苯二甲酸和2,5-二甲硫醚对苯二甲酸,所述mof材料的制备采用后合成交换法(pse),交换后mof材料中配体2,5-二甲硫醚对苯二甲酸配体的含量比例为15wt%至60wt%,更优选为20wt%至50wt%,例如可以为20wt%和50wt%。
根据本发明的另一个方面,本发明的另一个目的在于提供一种具有可见光催化裂解水析氢性质的mof材料mil-125-(sch3)2的制备方法,所述制备方法包括如下步骤:
1)mil-125材料的合成
先称取对苯二甲酸于双口烧瓶中(n2保护),加入无水n,n-二甲基甲酰胺(dmf)和甲醇搅拌至溶解。之后滴加钛酸四丁酯,然后继续搅拌。然后将溶液转移到反应釜中,在130℃至160℃,优选150℃下加热10至30小时,优选为15至25小时,最优选为20小时。自然冷却后,通过离心得到白色粉末。并将得到的白色粉末在dmf中浸泡3天,每24小时用新鲜dmf代替,以消除未反应的化合物对苯二甲酸。浸泡3天后,收集的粉末进一步用甲醇洗涤以除去残留的dmf,得到mil-125材料。
2)mil-125-(sch3)2的合成
将2,5-二甲硫醚对苯二甲酸溶于无水二甲基甲酰胺(dmf)和无水甲醇的混合溶液,加入步骤1)中制备的mil-125材料超声使其分散到上述溶液中,然后转移到聚四氟乙烯内胆中,并在130至160℃,优选150℃下加热10至30小时,优选为15至25小时,最优选为24小时。自然冷却后,通过离心收集得到的mil-125-(sch3)2黄色粉末,并将得到的黄色粉末在dmf中浸泡3天,每24小时用新鲜dmf代替,以消除未反应的化合物2,5-二甲硫醚对苯二甲酸。浸泡3天后,收集的粉末进一步用甲醇洗涤四次以除去残留的dmf。制成的mil-125-(sch3)2材料需要在150℃真空下进一步干燥过夜,然后再用作活化产物。
优选地,上述步骤2)中,所述配体2,5-二甲硫醚对苯二甲酸与步骤1)中得到的mil-125材料中所含原有配体的物质的量比例为0.5:1至50:1,优选为1:1至20:1,更优选为1:1至10:1,更优选为2:1至4:1。
优选地,上述步骤2)中,所用溶剂无水dmf与无水甲醇的体积比例为1:1至30:1,优选为5:1至15:1,更优选为7:1至10:1,最优选为9:1。
有益效果
根据本发明的mofs材料mil-125-(sch3)2在可见光下具有较好的光催化活性,产氢量高,制备方法简单新颖,可控性强。
附图说明
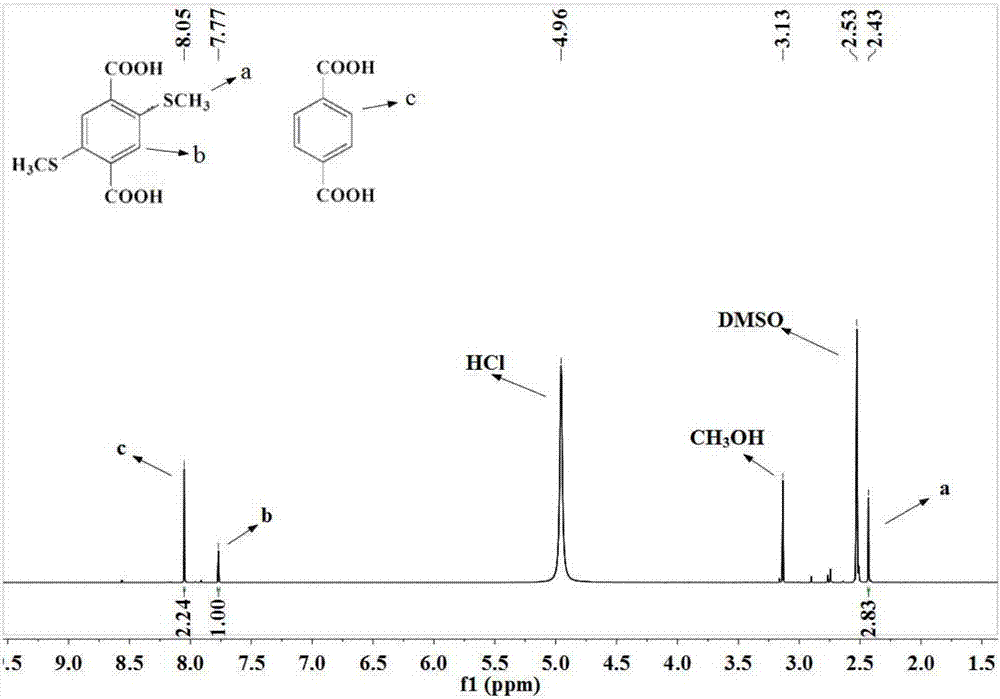
图1是根据本发明实施例1中得到的20%-mil-125-(sch3)2的核磁共振氢谱图。
图2是根据本发明实施例2中得到的50%-mil-125-(sch3)2的核磁共振氢谱图。
图3是根据本发明实施例1和2中得到的mil-125、20%-mil-125-(sch3)2、50%-mil-125-(sch3)2及催化产氢后样品的x射线粉末衍射图。
图4是根据本发明实施例2中得到的50%-mil-125-(sch3)2的透射电镜和扫描电镜照片。
图5是分别根据本发明实施例1和2中所得20%-mil-125-(sch3)2、50%-mil-125-(sch3)2、mil-125及配体2,5-二甲硫醚对苯二甲酸的红外光谱图。
图6是分别根据本发明实施例1和2中得到的mil-125材料、20%-mil-125-(sch3)2、50%-mil-125-(sch3)2及配体2,5-二甲硫醚对苯二甲酸的紫外光谱图。
图7是根据本发明实施例1和2中得到的20%-mil-125-(sch3)2、50%-mil-125-(sch3)2的光电开关测试图。
图8是根据本发明实施例1和2中得到的20%-mil-125-(sch3)2、50%-mil-125-(sch3)2加入pt作为共催化剂的及配体2,5-二甲硫醚对苯二甲酸的在420nm单色光源下的光催化产氢图。
图9是根据本发明实施例1和2中得到的20%-mil-125-(sch3)2、50%-mil-125-(sch3)2加入pt作为共催化剂的及配体2,5-二甲硫醚对苯二甲酸的在可见光下的光催化产氢图。
具体实施方式
以下,将详细地描述本发明。在进行描述之前,应当理解的是,在本说明书和所附的权利要求书中使用的术语不应解释为限制于一般含义和字典含义,而应当在允许发明人适当定义术语以进行最佳解释的原则的基础上,根据与本发明的技术方面相应的含义和概念进行解释。因此,这里提出的描述仅仅是出于举例说明目的的优选实例,并非意图限制本发明的范围,从而应当理解的是,在不偏离本发明的精神和范围的情况下,可以由其获得其他等价方式或改进方式。
优选地,上述步骤2)中,所用溶剂无水dmf与无水甲醇的体积比例为1:1至30:1,优选为5:1至15:1,更优选为7:1至10:1,最优选为9:1。当无水dmf的比例过少,例如小于1:1时,则2,5-二甲硫醚对苯二甲酸配体不能完全溶解,影响产率;当无水dmf的比例过高,例如大于30:1时,则交换效率低下,产物中2,5-二甲硫醚对苯二甲酸配体的含量不能有效提高。
优选地,上述步骤2)中,加入2,5-二甲硫醚对苯二甲酸配体的质量根据其与mil-125材料中原有配体对苯二甲酸的比例来确定。当2,5-二甲硫醚对苯二甲酸配体与原配体之间的比例为2:1时,所得产物为2,5-二甲硫醚对苯二甲酸配体含量为20wt%的mil-125-(sch3)2,优选地,当这一比例为4:1时,所得产物为2,5-二甲硫醚对苯二甲酸配体含量为50wt%的mil-125-(sch3)2。
所述配体2,5-二甲硫醚对苯二甲酸与步骤1)中得到的mil-125材料中所含原有配体的物质的量比例为0.5:1至50:1,优选为1:1至20:1,更优选为1:1至10:1,更优选为2:1至4:1。当所述物质的量比例小于0.5:1时,即配体2,5-二甲硫醚对苯二甲酸严重不足,则无法有效实现配体的交换;而当所述物质的量比例大于50:1时,即配体2,5-二甲硫醚对苯二甲酸过量,则不利于后续分离纯化步骤。
以下实施例仅是作为本发明的实施方案的例子列举,并不对本发明构成任何限制,本领域技术人员可以理解在不偏离本发明的实质和构思的范围内的修改均落入本发明的保护范围。
具体实验部分如下:具有可见光催化裂解水析氢性质的mofs材料mil-125-(sch3)2的制备方法。对于所获得样品,分别用如下仪器/技术进行表征:x射线粉末衍射仪,傅里叶红外光谱仪,紫外光谱仪,扫描电镜,透射电镜,核磁共振波谱仪。
实施例1:制备20%-mil-125-(sch3)2。
称取500mg(3mmol)的对苯二甲酸于双口烧瓶中(n2保护),加入9ml无水n,n-二甲基甲酰胺(dmf)和1ml甲醇搅拌至溶解。之后滴加0.26ml(0.75mmol)钛酸四丁酯,然后继续搅拌20min。然后将溶液转移到反应釜中,在150℃下加热20小时。自然冷却后,通过离心得到白色粉末。并将得到的白色粉末在dmf中浸泡3天,每24小时用新鲜dmf代替,以消除未反应的化合物2,5-二甲硫醚对苯二甲酸。浸泡3天后,收集的粉末进一步用甲醇洗涤四次以除去残留的dmf,得到mil-125材料。
将2,5-二甲硫醚对苯二甲酸52.0mg(0.2mmol)加入n,n-二甲基甲酰胺(dmf)(4.5ml)和无水甲醇(0.5ml)的混合溶液中。在使用前,二甲基甲酰胺(dmf)和无水甲醇需要重新蒸馏。然后将制备的mil-125材料(26.3mg,0.017mmol)分散到上述溶液中,并转移到25ml聚四氟乙烯内胆中,并在150℃下加热24小时。待反应结束后,将反应釜从干燥箱中取出,自然冷却至室温。得到的黄色的反应混合液,移入10ml离心管中,离心5min,转速5500rmp/min。离心后将得到的黄色粉末在dmf中浸泡3天,每24小时用新鲜dmf(10ml)代替溶液,以消除未反应的反应物和其他杂质。
浸泡3天后,收集的粉末进一步用甲醇洗涤四次以除去残留的dmf,得到20%-mil-125-(sch3)2。制成的样品需要在150℃真空下进一步干燥过夜,然后再用作活化产物。
图1是根据本实施例得到的20%-mil-125-(sch3)2的核磁共振氢谱图。从图1核磁中可以看出,20%-mil-125-(sch3)2结构中有配体2,5-二甲硫醚对苯二甲酸的特征峰和配体对苯二甲酸的特征峰,而且从积分比例来看配体对苯二甲酸的积分面积与配体2,5-二甲硫醚对苯二甲酸积分面积的比例为2:1,证明材料中含2,5-二甲硫醚对苯二甲酸配体的比例为20%。
本实施例得到的20%-mil-125-(sch3)2的x射线粉末衍射曲线见图3中“20%-mil-125-(sch3)2”曲线。另外图3中还给出了制备的mil-125材料和拟合的mil-125材料的x射线粉末衍射图曲线。从图中可以看出,所制得样品的衍射峰与计算机通过mil-125晶体数据模拟的粉末衍射图谱的衍射峰匹配性良好,说明合成的mofs材料与mil-125是同构型的。
图5中分别为根据实施例1和2所得20%-mil-125-(sch3)2、50%-mil-125-(sch3)2、mil-125及配体2,5-二甲硫醚对苯二甲酸的红外光谱图。从图5可以看出,在1254cm-1和2934cm-1处是配体2,5-二甲硫醚对苯二甲酸的特征吸收,在mil-125的红外谱图中不存在这两个特征吸收,而20%-mil-125-(sch3)2、50%-mil-125-(sch3)2中均存在。从而证明在合成mofs材料的过程中,配体上的甲硫醚基团保存完好。
图6中分别为根据实施例1和2得到的mil-125材料、20%-mil-125-(sch3)2、50%-mil-125-(sch3)2及配体2,5-二甲硫醚对苯二甲酸的紫外光谱图。通过对mil-125、20%-mil-125-(sch3)2、50%-mil-125-(sch3)2及配体2,5-二甲硫醚对苯二甲酸的紫外可见光吸收的测试,可以初步判定其光催化活性。在图6中可以看到:单纯的mil-125在可见光区(400nm-800nm)几乎没有吸收,而配体2,5-二甲硫醚对苯二甲酸及20%-mil-125-(sch3)2、50%-mil-125-(sch3)2在可见光区(400nm-800nm)都有很强的吸收,且两种比例的材料的吸收区域相对于配体来说都发生了蓝移,但并不影响在可见光420nm区的吸收,所以适合做可见光催化剂。
图7是根据本发明实施例1和2中得到的20%-mil-125-(sch3)2、50%-mil-125-(sch3)2的光电开关测试图。
实施例2:制备50%-mil-125-(sch3)2。
称取500mg(3mmol)的对苯二甲酸于双口烧瓶中(n2保护),加入9ml无水n,n-二甲基甲酰胺(dmf)和1ml甲醇搅拌至溶解。之后滴加0.26ml(0.75mmol)钛酸四丁酯,然后继续搅拌20min。然后将溶液转移到反应釜中,在150℃下加热20小时。自然冷却后,通过离心得到白色粉末。并将得到的白色粉末在dmf中浸泡3天,每24小时用新鲜dmf代替,以消除未反应的化合物2,5-二甲硫醚对苯二甲酸。浸泡3天后,收集的粉末进一步用甲醇洗涤四次以除去残留的dmf,得到mil-125材料。
将2,5-二甲硫醚对苯二甲酸104.0mg(0.4mmol)加入n,n-二甲基甲酰胺(dmf)(4.5ml)和无水甲醇(0.5ml)的混合溶液中。在使用前,二甲基甲酰胺(dmf)和无水甲醇需要重新蒸馏。然后将制备的mil-125材料(26.3mg,0.017mmol)分散到上述溶液中,并转移到25ml聚四氟乙烯内胆中,并在150℃下加热24小时。待反应结束后,将反应釜从干燥箱中取出,自然冷却至室温。得到的黄色的反应混合液,移入10ml离心管中,离心5min,转速5500rmp/min。离心后将得到的黄色粉末在dmf中浸泡3天,每24小时用新鲜dmf(10ml)代替溶液,以消除未反应的反应物和其他杂质。
浸泡3天后,收集的粉末进一步用甲醇洗涤四次以除去残留的dmf,得到50%-sch3-mil-125。制成的样品需要在150℃真空下进一步干燥过夜,然后再用作活化产物。
图2是根据本实施例得到的50%-mil-125-(sch3)2的核磁共振氢谱图。在图2证明材料中含2,5-二甲硫醚对苯二甲酸配体的比例为50%。
本实施例得到的50%-mil-125-(sch3)2的x射线粉末衍射图见图3中“50%-mil-125-(sch3)2”曲线。图4是根据本实施例得到的50%-mil-125-(sch3)2的透射电镜和扫描电镜照片,从图中可以看出50%-mil-125-(sch3)2的晶体形貌为类似于药片状,其直径约在200-700nm之间。
检测实施例
图7是实施例1和2中制备得到的20%-mil-125-(sch3)2、50%-mil-125-(sch3)2两种材料的光电开关(on-off)测试,光源是400-800nm的可见光,测试中每隔20s会遮光20s,从图中可以发现,当遮住光时,两种材料的光电流均立即大幅下降,在经过多个周期以后,两种材料的光电流均没有发生明显的衰减,说明这种mofs材料的光敏性非常稳定。
图8是加入pt作为共催化剂的20%-mil-125-(sch3)2、50%-mil-125-(sch3)2及配体2,5-二甲硫醚对苯二甲酸的在420nm单色光下的光催化产氢图。将50mg催化剂分散于0.01m的teoa(三乙醇胺)水溶液中加入h2ptcl6(pt1.5wt%)作为共催化剂;首先,通入n2约15分钟以除去溶液中的氧气,以420nm单色led灯为光源,测试温度为室温,通过循环冷却水保持温度,搅拌速度:300-400转。加入铂还原时开始测产氢,每1小时测一次产氢,测试时间为四个小时。从图中可以看到,材料50%-mil-125-(sch3)2最大产率可以达到1147.06μmol/(g*h),而20%-mil-125-(sch3)2最大产率也可以达到485.33μmol/(g*h)。从产氢能力上来看,该mofs的在420nm单色光源下的光催化效率都是比较高的,与已经报道的纯mofs材料(未与其他光敏剂或者半导体材料杂合)的光催化效率相对更高。而单纯的配体2,5-二甲硫醚对苯二甲酸及未加入pt共催化剂的20%-mil-125-(sch3)2几乎没有h2产生。
图9是加入pt作为共催化剂的20%-mil-125-(sch3)2、50%-mil-125-(sch3)2及配体2,5-二甲硫醚对苯二甲酸的在可见光下的光催化产氢图。将50mg催化剂分散于0.01m的teoa(三乙醇胺)水溶液中加入h2ptcl6(pt1.5wt%)作为共催化剂;首先,通入n2约15分钟以除去溶液中的氧气,以氙灯为光源(波长氛围为400-800nm),测试温度为室温,通过循环冷却水保持温度,搅拌速度:300-400转。加入铂还原时开始测产氢,每20min测一次产氢,测试时间为两个小时。从图中我们可以看到,材料50%-mil-125-(sch3)2最大产率可以达到2264.01μmol/(g*h),而20%-mil-125-(sch3)2最大产率也可以达到2394.51μmol/(g*h)。从产氢能力上来看,该mofs的在可见光下的光催化效率也是比较高的,与已经报道的纯mofs材料(未与其他光敏剂或者半导体材料杂合)的光催化效率相对更高。而配体2,5-二甲硫醚对苯二甲酸及未加入pt共催化剂的20%-mil-125-(sch3)2几乎没有h2产生。
- 还没有人留言评论。精彩留言会获得点赞!