一种自支撑FeSx电催化剂及其制备方法与应用与流程
本发明涉及电催化剂技术领域,尤其涉及一种自支撑fesx电催化剂及其制备方法与应用。
背景技术:
氨(nh3)是世界上最大的化工产品,全球年产量高达1.5亿吨。目前超过90%的合成氨都是用工业的haber-bosch法,即利用n2和h2气在高温(400-500℃),高压(150-200atm)的条件下,在铁基催化剂表面合成氨。这一过程需要消耗全球供应能源的1%,而且会产生大量的co2。与此形成鲜明对比的是,许多天然植物和细菌携带金属固氮酶,能够在环境条件活化牢固的n≡n三重键(941kj/mol),将空气中的氮气还原成氨。受到这一生物过程的启发,很多工作开始研究如何在温和的条件下将氮气还原成氨。最近,水相室温下电化学氮还原合成氨引起了广泛的研究兴趣。这一电化学过程,直接利用丰富的水资源作为氢源,而且,它可以很容易与间歇性可再生能源(如风能、太阳能或海洋能)结合起来,以提供所需的电力,因此,十分适合在一些交通不便利以及不适合建造大型化工厂的地区使用。然而,在温和的条件对n≡n键进行活化是一个重大挑战,不仅因为其非常高的键能同时也由于缺乏偶极矩,所以,这一电化学过程十分需要电催化剂的帮助。此外,在水相中电化学还原氮气(nrr)还面临着需要和电化学析氢(her)相互竞争的难题。因为这两个反应的还原电位十分接近,这就对氮还原催化剂的选择性提出了更严峻的要求。
最近报道的单原子钌(ru)基和金(au)纳米颗粒催化剂展示出了很高的氨产率和法拉第效率。但是,用合成方法复杂且价格昂贵的单原子ru和纳米颗粒au,严重的限制了其大规模使用。且其他的非贵金属催化剂材料(如:fe2o3,bi4v2o11,mos2)和碳材料虽然也得到广泛的研究,但是所报道的氨产率和法拉第效率仍然十分的低下。因此,任然迫切需要开发一种合成简单,经济且有效的非贵金属氮还原催化剂。
因此,现有技术还有待于改进和发展。
技术实现要素:
鉴于上述现有技术的不足,本发明的目的在于提供一种自支撑fesx电催化剂及其制备方法与应用,旨在解决现有金属催化剂材料合成方法复杂且价格昂贵,而非贵金属催化剂材料的氨产率和法拉第效率十分的低下的问题。
本发明的技术方案如下:
一种自支撑fesx电催化剂的制备方法,其中,包括:
提供铁基材;
对所述铁基材进行等离子体处理,所述等离子体包含h2s,在所述铁基材表面形成fesx,得到所述自支撑fesx电催化剂,其中x=0.5-2。
所述的自支撑fesx电催化剂的制备方法,其中,所述铁基材为泡沫铁、铁片或不锈钢片。
所述的自支撑fesx电催化剂的制备方法,其中,所述等离子体为h2s或h2s与惰性气体的混合气体。
所述的自支撑fesx电催化剂的制备方法,其中,所述处理的温度为25-300℃。
所述的自支撑fesx电催化剂的制备方法,其中,所述处理的时间为5-180min。
所述的自支撑fesx电催化剂的制备方法,其中,所述泡沫铁的等离子体处理在管式炉系统内石英管中进行,所述等离子体为h2s,处理过程包括:首先将泡沫铁切成1cm×2cm大小的碎片,然后放置在石英管的中心区域内;石英管在h2s等离子体处理的期间加热到160℃;持续通入50sccm的h2s进入石英管,通过真空泵将管内压力维持在600mtorr;石英管上游部分用铜线圈包裹,通过铜线圈提供60w的射频功率,在管的上游区域内产生h2s等离子体;等离子体电源为脉冲模式,每个等离子体脉冲长度为15s,整个h2s等离子体处理过程由200个h2s等离子体脉冲循环组成。
一种自支撑fesx电催化剂,其中,所述自支撑fesx电催化剂包括铁基材和所述铁基材表面的fesx,所述自支撑fesx电催化剂采用本发明所述的自支撑fesx电催化剂的制备方法制备而成。
所述的自支撑fesx电催化剂,其中,所述自支撑fesx电催化剂为自支撑fes2电催化剂。
一种本发明所述的自支撑fesx电催化剂在电化学还原氮气制氨中的应用。
有益效果:本发明提供了一种新的通过在铁基材表面进行简单的h2s等离子体处理而形成fesx氮还原催化材料。经过h2s等离子体的硫化处理,在泡沫铁表面能够形成一层fesx,并展示出了优秀的氮还原产氨的性能。用这种fesx/fe直接作为工作电极,在电位-0.30v相对可逆氢电极(rhe)时,其展现出优秀的氨产率,高达4.25×10-10mol·s-1·cm-2以及很高的法拉第效率18.1%,这些数值显著高于已经报道的非贵金属催化剂。值得注意的是,生物固氮酶的活化氮的位点位于fe-s分子簇上。它们与本发明的纯无机fesx催化剂有着相似之处,这使得本项工作更加值得关注,因为它可以为模拟天然固氮过程提供重要的帮助。
附图说明
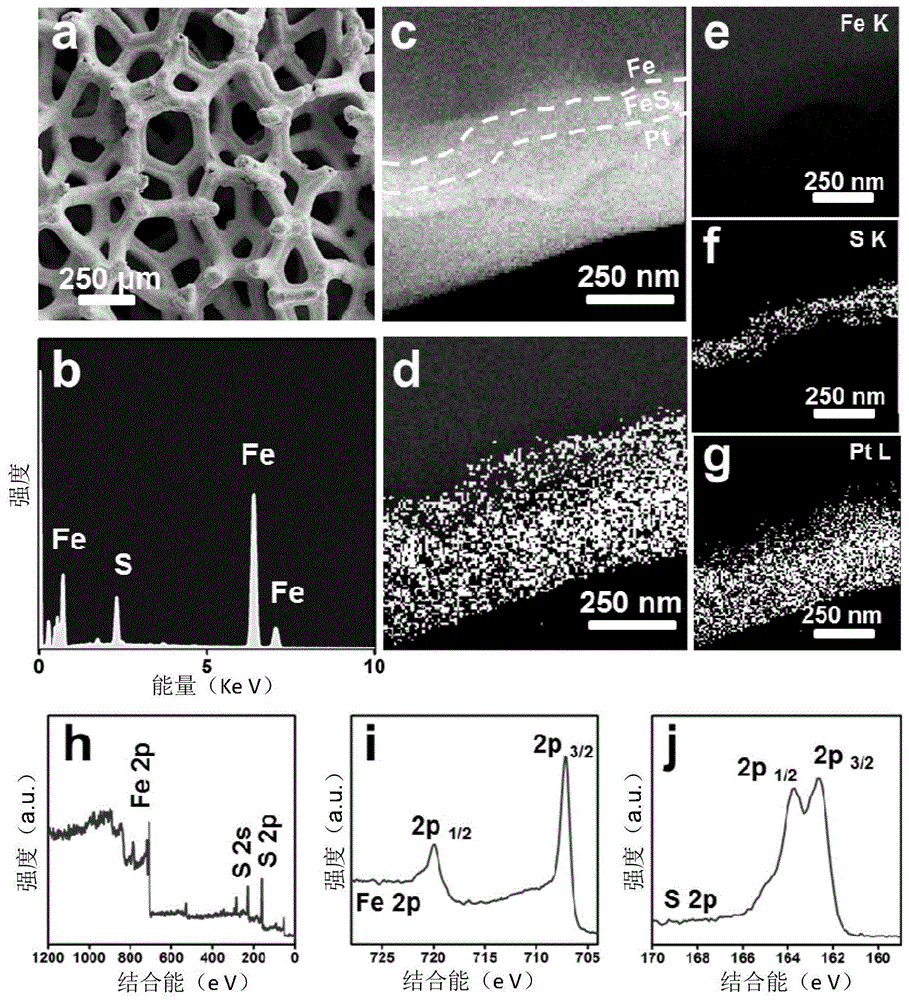
图1中(a)为实施例fesx/fe的sem图,(b)为相应的eds,(c)为横截面的stemhaddf图,(d-g)为相应的eds元素分布图,(h)为xps测量光谱,(i)为相应的高分辨光谱fe2p,(j)为相应的高分辨光谱s2p。
图2为实施例中电催化氮还原性能的表征:(a)为fesx/fe电极在氮气和氩气饱和溶液中的电化学极化曲线,插图简要说明了测量装置;(b)为恒电位测量的时间安培曲线;(c)为用靛酚蓝法测定氮还原产物的照片和吸收光谱;(b)、(c)、(d)为氨在不同电位下的产率采用相同的线色;(e)为氨的法拉第效率和δj/j氮气相对应的电位;(f)为fe、fe2o3、fesx的氨产量和法拉第效率比较。
图3为实施例中-0.30v(vs.rhe)分别在氮气和氩气饱和溶液测试得到的(a)奈奎斯特和(b)波特图;(c)为各个电位下的rnrr-1/(rnrr-1+rher-1)曲线,插图为拟合得到的等效电路。
图4为实施例中采用计时电流法,分别在氮气和氩气饱和溶液下测得的稳态电流,每个电位分别维持120s。
图5为实施例中绝对标准曲线(a,b)、靛酚蓝法(c,d)奈氏试剂法分别用来分析氨产量(e,f),watt-chrisp法用来分析肼产量。
图6为实施例中奈氏试剂法分析氨产量的照片和测定的吸收光谱。
图7为实施例中watt-chrisp法测试肼产量的照片和吸收光谱曲线。
图8为实施例中在氮气饱和和氩气饱和条件下的奈奎斯特(a,c,e,g)和波特图(b,d,f,h)。
图9为实施例中反应前后的sem和eds对比。
图10为实施例中反应前后的fesx的拉曼对比,以及合成纯的fes的拉曼对比。
图11为实施例中经过氮还原后的xps分析。
图12为实施例中循环伏安法测试fesx(a)和fe2o3(b)的曲线图,计算得到的双电层电容大小(c)。
具体实施方式
本发明提供一种自支撑fesx电催化剂及其制备方法与应用,为使本发明的目的、技术方案及效果更加清楚、明确,以下对本发明进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
本发明提供一种自支撑fesx电催化剂的制备方法,其中,包括:
提供铁基材;
对所述铁基材进行等离子体处理,所述等离子体包含h2s,在所述铁基材表面形成fesx,得到所述自支撑fesx电催化剂,其中x=0.5-2。
本发明提供了一种新的通过在铁基材表面进行简单的h2s等离子体处理而形成fesx氮还原催化材料。经过h2s等离子体的硫化处理,在铁基材表面能够形成一层fesx,并展示出了优秀的氮还原产氨的性能。用这种fesx/fe直接作为工作电极,在电位-0.30v相对可逆氢电极(rhe)时,其展现出优秀的氨产率,高达4.25×10-10mol·s-1·cm-2以及很高的法拉第效率18.1%,这些数值显著高于已经报道的非贵金属催化剂。值得注意的是,生物固氮酶的活化氮的位点位于fe-s分子簇上。它们与本发明的纯无机fesx催化剂有着相似之处,这使得本项工作更加值得关注,因为它可以为模拟天然固氮过程提供重要的帮助。
优选地,所述铁基材为泡沫铁、铁片或不锈钢片。更优选地,所述铁基材为泡沫铁。优秀的多孔率利于电催化,因为它们可以快速扩散活性物质,促进电解液的有效渗透,显著扩大电化学反应的表面积。
优选地,所述等离子体为h2s或h2s与惰性气体(如氩气等)的混合气体。
优选地,所述处理的温度为25-300℃。更优选地,所述处理的温度为150-170℃(如160℃)。本发明选择这个温度进行等离子体处理,是为了限制硫在铁中扩散,从而限制其硫化深度。
优选地,所述处理的时间为5-180min。更优选地,所述处理的时间为40-60min(如50min)。本发明等离子体处理上述时间,最终能够在铁基材表面形成一层均匀厚度的fesx。
具体地,所述泡沫铁的等离子体处理在管式炉系统内石英管中进行,所述等离子体为h2s,处理过程包括:首先将泡沫铁切成1cm×2cm大小的碎片,然后放置在石英管的中心区域内;石英管在h2s等离子体处理的期间加热到160℃;持续通入50sccm的h2s进入石英管,通过真空泵将管内压力维持在600mtorr;石英管上游部分用铜线圈包裹,通过铜线圈提供60w的射频功率,在管的上游区域内产生h2s等离子体;等离子体电源为脉冲模式,每个等离子体脉冲长度为15s,整个h2s等离子体处理过程由200个h2s等离子体脉冲循环组成。
本发明还提供了一种自支撑fesx电催化剂,其中,所述自支撑fesx电催化剂包括铁基材和所述铁基材表面的fesx,采用本发明所述的自支撑fesx电催化剂的制备方法制备而成。
本发明中,所述自支撑fesx电催化剂可以为自支撑fes2电催化剂。
本发明还提供了一种所述的自支撑fesx电催化剂在电化学还原氮气制氨中的应用。
下面通过实施例对本发明进行详细说明。
1、h2s等离子体处理泡沫铁(制备fesx/fe电极):在自制管式炉系统内石英管中进行h2s等离子体处理。首先将商业泡沫铁切成1cm×2cm大小的碎片,然后样品被放置在石英管的中心区域内。管在等离子体处理的期间需要加热到160℃。持续通入50sccm的h2s(3%ar稀释)进入石英管,通过真空泵将管内压力维持在600mtorr。石英管上游部分用铜线圈包裹,通过铜线圈提供60w的射频功率(13.56mhz),在管的上游区域内产生h2s等离子体。等离子体电源为脉冲模式,以避免管过热。每个等离子体脉冲长度为15s,整个硫化过程由200个h2s等离子体脉冲循环组成。
2、电化学氮还原测试:如图2a所示,整个测试在双室电解槽内进行,双室中间用nafion211交换膜阻隔。在实验之前,nafion薄膜要经过预处理,连续浸入5%双氧水溶液和超纯水中,80℃维持1小时。电化学数据用chi604e工作站在三电极体系下测试。pt作为对电极,hg/hgo作为参比电极,电解液为0.1mkoh水溶液。所有展示的电位都经过ir修正,都对应到了可逆氢电极(rhe),电化学极化曲线通过恒电位计时安培法得到,在每一个电位维持120s从而达到稳态电流。为了表征氮还原,纯的氮气(99.999%,1atm)持续的通向水溶液中的工作电极,在收集数据之前先通上30分钟的氮气。作为比较,氩气(99.999%,1atm)代替氮气,其他所有测试和氮气中的一样。
3、电化学阻抗测试(eis):测试的频率为0.1hz到10khz,偏压分别设置为-0.14,-0.22,-0.30,-0.38和-0.42vvs.rhe,交流振幅为5mv,阻抗拟合用zview软件。
4、制备fe2o3/fe电极:将泡沫铁在空气中600℃加热1h就能在泡沫铁表面得到fe2o3。
实验结果如下:
经过h2s等离子体处理后,整个泡沫铁的颜色发生了均匀的变化,说明fesx在fe上的覆盖是完全均匀的,说明这个等离子体硫化过程很容易放大。之后对fesx/fe的微观结构进行了扫描电子显微镜(sem)测试。图1a,b展示了典型的sem图和相应的能量色散x射线谱(eds)。h2s等离子体处理后,多孔泡沫结构完整,表面fesx层均匀光滑。优秀的多孔率和表面均匀的转化成fesx对于电催化都是很重要的,因为它们可以快速扩散活性物质,促进电解液的有效渗透,显著扩大电化学反应的表面积。
对表面的fesx层进一步进行了横截面扫描透射电镜(stem)测试。为了准备stem样品,首先在fesx/fe表面沉积一层pt保护层。图1c展示了fesx层的大角度环形暗场(haadf)stem图片。图1d-g展示了通过eds获取的相应的元素分布。这些结果清楚的显示,在泡沫铁表面均匀的形成了一层约70nm厚的fesx。用x射线光电子能谱学(xps)进一步调查fesx层的成分。图1h展示的是xps的全谱,图1i,j展示了fe2p和s2p的高分辨谱线。fe的光谱在707.3(2p3/2)和720.0ev(2p1/2)显示一对自旋轨道的峰值,s的光谱在162.5(2p3/2)和163.7ev(2p1/2)显示出一对自旋轨道的峰值,这些结合能的数值同fes2的相一致,说明表面形成的fesx可能是fes2。同时,对fe和s2p谱线峰面积的积分可以得知s/fe的原子比列为2.03±0.03,表明形成的是fes2。拉曼光谱测量(图11)进一步表明,形成的fes2是黄铁矿-白铁矿混合型fes2,类似于使用h2s等离子体原子层沉积fes2,但没有观察到元素s的拉曼信号。
在0.1m的koh溶液,及21℃的室温下用双室电解槽对fesx的电催化氮气还原进行了三电极测试。fesx/fe直接用作工作电极,纯的氮气持续的通向电解液。为了研究其与电化学析氢的竞争过程,用纯的氩气替代氮气用作对照组。电化学极化曲线通过阶梯增长电位(-0.14到-0.42vvs.rhe),每个电位保持120s来达到稳态电流(图4)。然后,利用稳态电流的值生成氮气或和氩气鼓泡下测量的极化曲线如图2a所示。发现在氮气下产生的电流密度(j氮气)要大于在氩气下产生的电流密度(j氩气),特别是在电位从-0.22到-0.38v(vs.rhe)的区间。假设氩气鼓泡下的电流应该与电化学析氢对应,假设电化学析氢和氮还原是两个独立的竞争过程,上面的两条曲线之间的差别(δj=j氮气-j氩气)就应该对应于氮还原。结果显示,当电位在-0.30v(vs.rhe)时,电流密度的差异达到最大-138μa/cm2,在氮气鼓泡的条件下,这个数值占总电流密度的比例高达19.1%。高比列的δj/j氮气意味着,有很大一部分阴极电流用来还原氮气。
氮还原的产物(如nh3和n2h4)用以下方法进行量化。首先为了获得足够数量的产品进行定量分析,把fesx/fe电极在一定的恒定电位下偏压20h,然后收集fesx电极侧的电解液,分析累积的产品数量。将这个过程在各个恒电势-0.14,-0.22,-0.30,-0.38和-0.42v(vs.rhe)分别反复进行,同时记录在这20h中,电流密度随电势的变化。如图2b所示,电流密度随着时间的推移保持相当的恒定,这表明fesx/fe电极具有很好的电催化稳定性。同时,电流密度可忽略的微小变化也表明反应产物的生成速率是恒定的,因此可以用总生成量除以总反应时间来计算产物的生成速率。氨作为氮还原的主要产物,分别通过靛酚蓝法和奈氏试剂法来定量分析。图2c展示了用靛酚蓝法测得的照片和吸收光谱曲线,相应的绝对校准曲线如图5所示,可以得到反应产物溶液中氨的浓度。同样,奈氏试剂法所测得的照片和吸收光谱如图9所示,绝对校准曲线如图5所示。通过绝对校准曲线所得的氨浓度可以用于计算fesx电催化剂在不同电位下氨的产率。如表1所示,这两种方法得到的数值非常相似(相差在4%以内),因此简单地使用它们的的平均值用作氨的产率。图2d绘图氨产量对应相应电位的曲线(参见表2),可以看出在电位-0.30v(vs.rhe)时,其氨的产率达到最大4.25×10-10mol·s-1·cm-2。这个氨的产率相当的高,基本上是最近报道的最佳值之一(表3)。本实施例也计算了氨的法拉第效率,如图2e所示,在电位-0.30v(vs.rhe)时,法拉第效率高达18.1%,这个值也是目前报道最好值之一。(表3)。除此之外,图2e还展示了法拉第效率与δj/j氮气之间的比较,通过对比,可以发现δj/j氮气只比产氨法拉第效率高出(0.3~2.7%),表明相对其他还原产物,电化学还原中,催化剂对氨具有很高的选择性。事实上,还用watt-chrisp分光光度法量化n2h4的产量(图5和图7),发现n2h4是主要的副产物,这样就解释了法拉第效率与δj/j氮气之间得微小误差来源(参见表2)。综上所述,等离子体处理制备的fesx在环境条件下拥有很好的电催化还原氮气制氨性能,氨产率很高,法拉达效率高,而且稳定性也好。
为了深入了解电催化机理,在氩气和氮气饱和溶液中分别对fesx/fe电极进行了电化学阻抗谱(eis)测量。图3a、b显示了在-0.30v(vs.rhe)时的奈奎斯特和波特曲线。尼奎斯特图显示两种情况下均为单半圆,但氮气饱和的情况下半圆直径小于氩气饱和的情况;波特图在0.1hz-10khz频率范围内显示出了单峰,同时氮气饱和的峰值频率大于氩气饱和的峰值频率。其他电位也观测到相似的结果(图8),单个奈奎斯特半圆和波特峰表示在0.1hz-10khz频率范围内,具有单个等效电荷传递过程,这表明电化学氮还原与析氢的确存在反应速率竞争关系,或许可以将他们看做两个并列过程。因此,采用稍作修改的等效电路对氮气饱和溶液中的eis数据进行拟合,如图3c插图所示,其中电荷转移电阻(rct)分为rher和rnrr两种反应通道并联,rher值仅取氩气饱和溶液中没有发生氮还原的eis数据。拟合结果详见表4。进一步计算每个电位下的rnrr-1/(rnrr-1+rher-1)值,并将其与氮还原电流的百分比相对应。如图3c所示,rnrr-1/(rnrr-1+rher-1)表现出和δj/j氮气相同的趋势(图2e),这表明直流和交流电测试下具有很好的一致性。
进一步对氮还原后fesx的表面成分进行了材料表征。如图9所示,经过氮还原后,fesx/fe电极的表面形貌基本保持不变。然而,拉曼光谱表明,fesx表面的晶体结构改为马基诺矿fes经过氮还原之后(图10),这个结论也得到xps的验证,发现fe2p和s2p的峰位转向马基诺矿fes(图11)。因此,马基诺矿fes很可能是实际的电催化剂。此外,xps光谱还显示在氮还原后,催化剂表面存在含氮物质(图11):观察到的n1s结合能为399.6ev,可能对应在催化剂表面形成的氮氢化合物(如nhx或nxhy)。
最后,还比较了fesx与fe2o3的氮还原性能,fe2o3是最近报道的一种很好的氮还原电催化剂。在同种泡沫铁表面通过氧化的方式得到fe2o3催化剂,通过测试可以得到fesx/fe电极和fe2o3/fe电极的表面积基本相同(图12)。采用相同的测量过程,得到fe2o3电催化剂的最大氮气产率和法拉达效率,如图2f所示。注意,纯泡沫铁没有显示出任何可测量的氨产物。事实上,fe2o3催化剂显示一个还不错的氨产量,为4.25×10-10mol·s-1·cm-2(-0.3vvs.rhe),以及法拉第效率2.2%,这些数值和之前的报道相一致。然后这些数值明显低于本实施例中的fesx催化剂。
表1、靛酚蓝法和奈氏试剂法氨产量的对比以及平均值,单位量级为10-10mol·s-1·cm-2
表2、氨和肼的产量,法拉第效率
表3、fesx/fe同其他催化剂的性能对比
表4、eis的拟合结果,双电层电容(cdl)通过
综上所述,本发明提供了一种简单、经济有效的等离子体硫化方法来制备一种新型的自支撑fesx电催化剂,当在环境条件下应用于电催化还原氮时,这种fesx/fe电极证明显示优秀的氨产量,为4.25×10-10mol·s-1·cm-2和很高的法拉第效率18.1%,显著优于其他非贵金属催化剂。考虑到等离子体硫化方法合成的fesx/fe具有良好的性能和较低的成本,在电化学氨合成中具有广阔的应用前景。此外,fesx催化剂在某种程度上与生物固氮酶中的fe-s簇相似,这可能为模仿自然氮气固氮过程提供重要的见解。
应当理解的是,本发明的应用不限于上述的举例,对本领域普通技术人员来说,可以根据上述说明加以改进或变换,所有这些改进和变换都应属于本发明所附权利要求的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!