二氧化碳共流体的制作方法
本申请要求于2017年4月25日提交的美国实用新型专利申请第15/496,268号和于2017年4月25日提交的美国实用新型专利申请第15/496,237号的优先权,并且还要求于2016年4月29日提交的美国临时申请第62/329,586号和于2016年4月29日提交的美国临时申请第62/329,535号的权益,以上提及的申请的全部公开内容通过引入并入本文。
本公开内容涉及用于在加热、通风、空调和制冷(hvac&r)系统中与二氧化碳制冷剂一起使用的共流体(co-fluid)。
背景技术:
该部分提供了与本公开内容相关的背景信息,所述背景信息不一定是现有技术。
由于二氧化碳(r744)具有仅为1的低的全球变暖潜能值(gwp)并且根本没有消耗臭氧潜能值(odp为零),因此与氢氟烷、氢氟烯烃和其他不太环保的制冷剂相比,其成为优异的环境友好的制冷剂。然而,将二氧化碳液化所需的压力证明太高而不能用于常规的加热和冷却系统。为了避免制冷循环中的高压力,可以将二氧化碳与所谓的共流体或共流体的混合物一起使用。
在使用二氧化碳和共流体的hvac&r系统的操作中,二氧化碳制冷剂被吸收到共流体中并从共流体中解吸出来。例如,二氧化碳在压缩和流过冷凝器或吸收器期间被吸收并且压力降低。随后流过膨胀装置和蒸发器需要一部分二氧化碳制冷剂的期望释放(解吸)。
在使用二氧化碳作为制冷剂的共流体系统中通常已观察到吸收速率倾向于比解吸速率更快。这种速率不同可能潜在地导致操作加热和冷却系统时的问题。可能没有足够的时间使合适的热流动至冷却所需的蒸发器。另外,由于速率差异而可能在共流体中积聚二氧化碳,导致系统效率低或者甚至不能操作。一直需要提供更高的解吸速率以改善冷却系统的操作的共流体。
技术实现要素:
本部分提供了本公开内容的大致概述,而并非其全部范围或其所有特征的全面公开。
提供了用于制冷循环的二氧化碳/共流体混合物,其中由共流体交替地吸收和解吸二氧化碳。所述混合物包含50重量%至99重量%的共流体和1重量%至50重量%的二氧化碳。合适的共流体选自烷氧基化的羧酸酰胺类,其中酰胺是环状或非环状的。已发现n-2,5,8,11-四氧杂十二烷基-2-吡咯烷酮及其同系物表现出在较低温度下高的解吸速率的有利特性。
提供了包含共流体作为润滑剂的泵或压缩机,其用于依次包括压缩机、吸收器(absorber或resorber)、膨胀装置(或膨胀器)和解吸器的系统。操作制冷系统的方法包括使共流体和制冷剂环绕这样的系统循环。
适用性的其他领域从本文中提供的描述中将变得明显。在本概述中的描述和具体实例仅出于说明性目的,并且不旨在限制本公开内容的范围。
附图说明
本文描述的附图仅用于所选择的实施方案而非所有可能的实施方式的说明性目的,并不旨在限制本公开内容的范围。
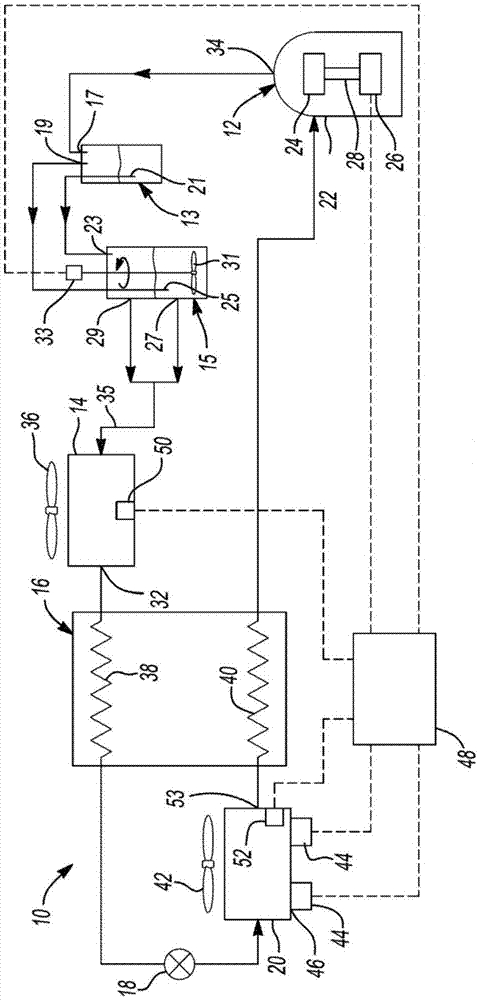
图1是根据本公开内容的原理的一种环境控制系统的示意图。
图2是可以并入图1的系统中的示例性解吸器的示意图。
图3是根据本公开内容的原理的另一种环境控制系统的示意图。
图4是根据本公开内容的原理的又一种环境控制系统的示意图。
图5是可以并入图4的系统中的发电机的示意图。
图6比较了润滑剂的解吸速率;
图7至11示出了共流体的比较解吸速率;
图12示出了共流体的二氧化碳解吸;以及
图13比较了解吸速率与共流体的解吸速率。
贯穿附图的若干视图,相应的附图标记表示相应的部件。
具体实施方式
现在将参照附图更全面地描述示例性实施方案。
提供了用于其中使用二氧化碳作为制冷剂的共流体系统的共流体。共流体是能够吸收和解吸二氧化碳制冷剂的吸收剂。使用共流体消除了对高系统压力的需要,所述高系统压力是在其他情况下改变制冷剂二氧化碳的相态所需的。
共流体选自具有以下通式的那些:
其中m为1至10;r为具有1至26个碳原子的烷基、烯基或芳基;r’为h或任选经取代的c1-6烷基;r”为h、甲基或乙基;r”’为h、甲基或乙基;并且r”和r”’中的至少一个为h;
其中m为1至10;p为1至3;r为具有1至26个碳原子的烷基、烯基或芳基;r’为h或任选经取代的c1-6烷基;r”为h、甲基或乙基;r”’为h、甲基或乙基;并且r”和r”’中的至少一个为h;
其中x为1至4;n为1至10;r’为h或任选经取代的c1-6烷基;r”为h、甲基或乙基;r”’为h、甲基或乙基;并且r”和r”’中的至少一个为h;
其中y为1至4;n为1至10;p为1至3;r’为h或任选经取代的c1-6烷基;r”为h、甲基或乙基;r”’为h、甲基或乙基;并且r”和r”’中的至少一个为h;
其中z为1至4;n为1至10;r’为h或任选经取代的c1-6烷基;r”为h、甲基或乙基;r”’为h、甲基或乙基;并且r”和r”’中的至少一个为h;和
其中z为1至4;n为1至10;p为1至3;r’为h或任选经取代的c1-6烷基;r”为h、甲基或乙基;r”’为h、甲基或乙基;并且r”和r”’中的至少一个为h。
虽然本发明不应受任何科学假设或操作理论的限制,但是式(i)至(vi)的化合物共有被认为有助于其作为用于与二氧化碳制冷剂一起使用的共流体的一般用途的化学特征。据信,羧酸酰胺(环状或开链)和聚氧化烯部分结合以提供以高速率解吸二氧化碳的组合物,该速率高于没有这些特征的同系化合物,即使同系化合物就尚未被作为共流体公开的程度而言被认为是所述发明的一部分。一般而言,具有高的解吸速率的物质由于因具有高的解吸而有望流动的操作优点而优选作为二氧化碳制冷系统中的共流体。
式(i)至(vi)的化合物的特征在于“侧链”,所述侧链具有由式中的m或n个重复单元表示的聚氧化烯结构。如果r”和r”’二者为氢(h),则该链为聚氧乙烯;如果其中一个为甲基(另一个为h),则该链为聚氧丙烯;如果其中一个为乙基,则该链为聚氧丁烯。因为重复单元m和n的范围为1至10,所以还可以提供包含聚氧乙烯、聚氧丙烯和聚氧丁烯的组合的所谓的混嵌聚氧化烯链。换言之,该式应被理解为允许至多10个重复单元,其中各重复单元独立地基于环氧乙烷、环氧丙烷或环氧丁烷。
式(i)和(ii)的非环状酰胺“烷氧基化物”基于具有至少两个且至多27个碳原子的羧酸酰胺(因为r具有1至26个碳原子)。预期r基团的性质(尺寸、支化水平、是否存在不饱和度)会影响共流体的当量和粘度。这些是可以考虑在内的设计因素。
在所有式中,聚氧化烯链的末端羟基可选择地被任选经取代的烷基(优选易于合成的甲基)封端。尽管是本发明的一部分,但是羟基化合物(r’=h)在一些实施方案中是不太优选的,因为羟基可能导致不期望的反应性、高粘度或甚至腐蚀。封端使羟基不起作用。r’上的取代被允许到它们不会破坏作为共流体的化合物的操作的程度。在一个特定实施方案中,烷基r’经羧酸酰胺基取代,如以下描述和实施例中所示。因此,以上任一者中的r’可以为经由以下结构表示的烷基脲基或烯基脲基取代的c1-6烷基,其中r为烷基或烯基:
式(i)至(vi)的化合物在形式上是所示的羧酸酰胺或羧酸酰亚胺的烷氧基化物。(i)、(iii)和(v)的化合物可以通过酰胺/酰亚胺起始基团的直接烷氧基化来合成,因为酰胺/酰亚胺基团是反应性的并且可以打开相应的环氧烷烃的环氧乙烷环。另一方面,(ii)、(iv)和(vi)的化合物可以通过使包含连接至酰胺或酰亚胺的羟烷基部分的起始材料的游离羟基烷氧基化来制备。根据式中的p为1、2或3,该基团为羟甲基、羟乙基或羟丙基。
n(或m)为1至10的化合物可以如下来制备:使起始材料与n或m当量的氧化物反应并与每个酰胺基包含平均n个氧化物单元的多分散混合物反应。或者,它们可以以产生其中峰在具有n个氧化物单元的物质处的分子量分布的目标来合成。可以物理分离各种级分以提供其他烷氧基化分布。
但是尤其是对于较低分子量的化合物,可以更简单的是:不通过烷氧基化形成化合物,而是通过使包含n个重复单元的预先形成的单分散化合物与反应性酰胺氮反应(或者与添加至酰胺中(例如,通过与甲醛反应)的羟烷基的羟基反应)形成化合物。这通过使起始材料n-羟甲基吡咯烷酮(n-羟甲基-2-吡咯烷酮)与三乙二醇单甲醚以常规的williamson醚合成反应来说明。
在多个实施方案中,式(i)至(vi)的共流体的特征还在于以下的一者或任意者组合:参数x和y的值为2或4;参数z的值为2(意味着该结构基于琥珀酰亚胺衍生物);变量n和m为1至4;r’为甲基;r”和r”’二者均为h;r’为经烷基脲基取代的c1-3烷基。特定实施方案包括以下:
在操作中,共流体充当润滑剂以及用于制冷剂二氧化碳的载体流体。本文所述的用于冷却回路的压缩机包含任何所述的共流体作为润滑剂。
在操作中,当共流体环绕制冷或冷却回路循环时,其吸收(再吸收)和解吸制冷剂二氧化碳。在回路中的各个点处,冷却组合物包含50重量%至99重量%的共流体和1重量%至50重量%的二氧化碳。
优选的共流体具有本文公开的化学结构。在多个实施方案中,性能也依赖于还具有有利物理特性的共流体。当然,优选的共流体容易吸收和解吸用作制冷剂的二氧化碳。测量瞬时速率(基本上在零时刻的速率)以及在1分钟和2分钟时解吸的量。结果可以用于筛选潜在的候选物。
共流体还需要具有合适的粘度。在多个实施方案中,粘度在1厘沲(cst)至50厘沲、1cst至20cst、3cst至20cst、5cst至20cst、1cst至10cst、3cst至10cst的范围内。一些好的候选物的粘度相当接近10cst。在多个实施方案中,粘度有利地在5cst至15cst、8cst至12cst、或9cst至11cst的范围内。粘度太高则可能阻碍环绕冷却回路的流体流动。如果粘度太低,则可能在系统中发生密封后泄漏。以下是共流体的用途的非限制性说明。
共流体在制冷方法中的用途
基于二氧化碳作为制冷剂(“蒸气”)的代表性制冷循环如下操作。蒸气和液体(共流体)的组合在压缩机中被压缩,使压力升高并迫使一些蒸气进入液相。在压缩机下游的吸收器(resorber或absorber)中排出热。这将混合物冷却并使更多的蒸气被吸收。剩余的co2蒸气和共流体在内部热交换器中被进一步冷却。然后,冷的经完全液化的混合物穿过膨胀装置,使压力降低,使温度进一步下降,并将一些co2释放到气相中。随着混合物的温度升高,热被从制冷空间中提取到解吸器中,并且另外的co2从液相中逸出。最后,流体在内部热交换器中被进一步加热,完成循环。
二元循环环境控制系统
参照图1,提供了二元循环环境控制系统10,其可以包括压缩机12、液-气分离器13、搅拌容器(例如,搅动和/或摇动容器)15、吸收器(absorber或resorber)14、内部热交换器16、膨胀装置18和解吸器20。压缩机12可以是任何合适类型的压缩机,例如如涡旋式压缩机、回转式压缩机或往复式压缩机。压缩机12可以包括壳体22、设置在壳体22内的压缩机构24和通过曲轴28驱动压缩机构24的马达26(例如,定速马达或变速马达)。压缩机12可以是固定容量压缩机或可变容量压缩机。压缩机12可以压缩制冷剂(例如,二氧化碳、氢氟烷、氨、溴化物等)和共流体(例如,油、水、聚亚烷基二醇、多元醇酯、聚乙烯醚等)的混合物并使混合物在整个系统10中循环。共流体可以是能够吸收制冷剂的吸收剂。压缩制冷剂和共流体的混合物使该混合物的压力和温度升高,并使一些制冷剂被吸收到共流体中。
液-气分离器13可以包括入口17、第一出口(例如,气体出口)19和第二出口(例如,液体出口)21。入口17可以与压缩机12的出口34流体耦接,使得液-气分离器13接收来自压缩机12的制冷剂和共流体的经压缩混合物(例如,制冷剂蒸气和包含一些溶解的制冷剂气体的液态共流体的经压缩混合物)。液态共流体(其可以包含一些溶解的制冷剂气体)可以沉降至液-气分离器13的底部,并且未溶解的制冷剂蒸气可以保留在液-气分离器13的顶部(或者上升至液-气分离器13的顶部)(即,液态共流体的表面之上)。液态共流体可以通过第二出口21(其可以位于分离器13中的液体的表面之下)离开液-气分离器13,并且制冷剂蒸气可以通过第一出口19(其可以位于分离器13中的液体的表面之上)离开液-气分离器13。
搅拌容器15可以包括第一入口23、第二入口25、第一出口27、第二出口29和搅拌器31。第一入口23可以设置在容器15的顶端或通常设置成靠近容器15的顶端,并且可以与分离器13的第二出口21流体联接,使得来自分离器13的液态共流体通过第一入口23进入容器15。通过第一入口23进入分离器13的液态共流体可以落至容器15的底部。第二入口25可以在容器15中的液态共流体的表面之下,并且可以与分离器13的第一出口19流体联接,使得来自分离器13的制冷剂蒸气通过第二入口25进入容器15。以此方式,制冷剂蒸气在液态共流体的表面之下进入容器15,这使得进入容器15的一些制冷剂蒸气被吸收(或溶解)到液态共流体中。
搅拌器31可以为或包括叶轮(例如,一个或旋转桨或叶片)和/或摇动器,例如,设置在容器15中的液态共流体的表面之下,搅拌器31可以通过马达33来驱动,并且可以搅动或搅拌容器15中的液态共流体以进一步促进制冷剂蒸气到液态共流体中的吸收。
容器15的第一出口27可以设置在液态共流体的表面之下,使得制冷剂蒸气通过第一出口27离开容器15。容器15的第二出口29可以设置在液态共流体的表面之上,使得液态共流体(具有溶解在其中的制冷剂蒸气)通过第二出口29离开容器15。第一出口27和第二出口29都可以与导管35连通,使得来自第一出口27的液态共流体和来自第二出口29的制冷剂蒸气在导管35中合并并彼此混合(进一步促进制冷剂蒸气到液态共流体中的吸收)。
吸收器14可以为热交换器,其可以与导管35流体联接并且可以接收来自导管35的制冷剂和共流体的经压缩混合物。在不包括分离器13和容器15的系统10的配置中,吸收器14可以接收直接来自压缩机12的制冷剂和共流体的经压缩混合物。在吸收器14内,来自制冷剂和共流体的混合物的热可以被排放到例如空气或水或者一些其他介质中。在图1中所示的特定配置中,风扇36可以迫使空气穿过吸收器14以冷却吸收器14内的制冷剂和共流体的混合物。当制冷剂和共流体的混合物在吸收器14内冷却时,更多的制冷剂被吸收到共流体中。
内部热交换器16可以包括第一盘管38和第二盘管40。第一盘管38和第二盘管40为彼此传热的关系。第一盘管38可以与吸收器14的出口32流体联接,使得制冷剂和共流体的混合物可以从吸收器14的出口32流动至第一盘管38。来自流过第一盘管38的制冷剂和共流体的混合物的热可以被传递到流过第二盘管40的制冷剂和共流体的混合物。当该混合物流过第一盘管38时,更多的制冷剂可以被吸收到共流体中。
膨胀装置18可以例如为膨胀阀(例如,热膨胀阀或电子膨胀阀)或者毛细管。膨胀装置18可以与第一盘管38和解吸器20流体连通。即,膨胀装置18可以在第一盘管38下游且在解吸器20上游接收已经离开的制冷剂和共流体的混合物。当制冷剂和共流体的混合物流过膨胀装置18时,混合物的温度和压力降低。
解吸器20可以是热交换器,其接收来自膨胀装置18的制冷剂和共流体的混合物。在解吸器20内,制冷剂和共流体的混合物可以吸收例如来自空气或水的热。在图1中示出的特定配置中,风扇42可以迫使来自空间(即,待通过系统10冷却的房间或空间)的空气穿过解吸器20以使空气冷却。当制冷剂和共流体的混合物在解吸器20内被加热时,制冷剂从共流体中解吸。制冷剂和共流体的混合物可以从解吸器20的出口53流过第二盘管40并流回到压缩机12以完成循环。
一个或更多个超声换能器(即,振动换能器)44可以连接至解吸器20。如图1所示,超声换能器44可以安装至解吸器20的外表面46。在一些配置中,超声换能器44设置在解吸器20内部并与制冷剂和共流体的混合物接触(如图2所示)。超声换能器44可以为任何合适类型的换能器,其响应于电流的接收而产生振动(例如,超声振动)。例如,超声换能器44可以为压电换能器、电容换能器或磁致伸缩换能器。例如,超声换能器44的输出频率可以在约20khz至150khz(千赫兹)的范围内。超声换能器44可以(直接或间接地)向流过解吸器20的制冷剂和共流体的混合物施加或传递振动以增加制冷剂从共流体中解吸的速率。
超声换能器44可以具有任何合适的形状或设计。例如,超声换能器44可以具有长且窄的形状、平盘形状等,并且可以是柔性或刚性的。在其中超声换能器44安装至解吸器20的外表面46的配置中,解吸器20在安装超声换能器44的位置处具有最小壁厚以使超声振动的衰减最小化可以是有益的。此外,在制冷剂和共流体的混合物静止的位置处或者在制冷剂和共流体的混合物的流量降低或最小的位置处向制冷剂和共流体的混合物施加超声振动可以是有益的,因为高速流动的流体可能更难以用超声能量激发。
控制模块(或控制器)48可以与超声换能器44连通(例如,有线连通或无线连通),并且可以控制超声换能器44的操作。控制模块48可以控制供应至超声换能器44的电流(例如,通过电池和/或其他电源供应至超声换能器44的电流)的频率和振幅以控制超声换能器44产生的振动的频率和振幅。控制模块48还可以与压缩机12的马达26、膨胀装置18、搅拌器31的马达33、风扇36、风扇42和/或其他组件或子系统连通并控制它们的操作。
如上所述,向制冷剂和共流体的混合物施加超声振动使解吸速率增加。控制模块48可以控制超声换能器44的操作以控制解吸速率。例如,控制模块48可以控制马达33、风扇36、风扇42和/或超声换能器44的频率、振幅、运行时间(例如,脉冲宽度调制循坏时间)等,使得解吸速率与在膨胀装置18上游(例如,在吸收器14和容器15中)发生的制冷剂到共流体中的吸收速率匹配或几乎匹配。
在没有对制冷剂和共流体的混合物进行任何激发的情况下,吸收速率可以显著大于解吸速率。吸收速率可以根据系统10的各种操作参数(例如,压力、压缩机容量、风扇速度、系统10上的热负荷、制冷剂的类型,共流体的类型等)而变化。在一些配置中,第一传感器50和第二传感器52可以与控制模块48连通,并且可以测量指示吸收速率和解吸速率的参数。例如,第一传感器50可以为压力传感器或温度传感器,其测量吸收器14内的制冷剂和共流体的混合物的压力或温度,并且第二传感器52可以为压力传感器或温度传感器,其测量解吸器20内的制冷剂和共流体的混合物的压力或温度。通过传感器50、52测量的压力和/或温度可以指示吸收速率和解吸速率。
传感器50、52可以将压力或温度数据传送至控制模块48,并且控制模块48可以基于压力或温度数据(例如,利用查找表或方程式)确定共流体中制冷剂的浓度。控制模块48可以包括内部时钟(或与外部时钟连通),并且可以基于共流体中制冷剂的浓度在一段时间内的变化来确定吸收速率和解吸速率。控制模块48可以基于吸收速率和/或解吸速率来控制超声换能器44的操作。控制模块48还可以基于吸收速率和/或解吸速率来控制压缩机12、风扇36、风扇42和/或膨胀装置18的操作,和/或还可以控制压缩机12、风扇36、风扇42和/或膨胀装置18的操作以控制吸收速率和/或解吸速率。在一些配置中,控制模块48可以基于来自附加或替代传感器的数据和/或附加或替代操作参数来控制超声换能器44。
由于许多制冷剂到许多共流体中的速率显著快于解吸速率,因此解吸速率可以大大地限制系统10的容量。向制冷剂和共流体的混合物施加超声能量(例如,通过超声换能器44)出乎意料地解决了解吸速率慢的问题。可以表明,与用螺旋桨以400转/分钟搅动混合物相比,通过用超声能量(例如,使用一个或更多个超声换能器44)激发制冷剂和共流体的混合物,解吸速率可以增加约100%至900%(根据制冷剂类型和共流体类型)。该解吸速率的增加超过了合理的成功预期。
现在参照图3,提供了另一种二元循环环境控制系统100,其可以包括压缩机112、泵111、液-气分离器113、搅拌容器(例如,搅动和/或振动容器)115、吸收器114、内部热交换器116、膨胀装置118、解吸器120、接收器121、一个或更多个超声换能器144、和控制模块148。压缩机112、液-气分离器113、搅拌容器115、吸收器114、内部热交换器116、膨胀装置118、解吸器120、超声换能器144和控制模块148的结构和功能可以与上述的压缩机12、液-气分离器13、搅拌容器15、吸收器14、内部热交换器16、膨胀装置18、解吸器20、超声换能器44和控制模块48的结构和功能类似或相同(除了下面描述的任何例外之外)。因此,可以不再详细地描述类似的特征。
接收器121可以与内部热交换器116(例如,内部热交换器116的第二盘管140)、压缩机112和泵111流体联接。接收器121可以包括入口154、制冷剂出口156和共流体出口158。入口154可以接收来自第二盘管140的制冷剂和共流体的混合物,在接收器121内部,气态制冷剂可以与液态共流体分离。即,共流体积聚在接收器121的下部162中,而制冷剂可以积聚在接收器121的上部160中。制冷剂可以通过制冷剂出口156离开接收器121,而共流体可以通过共流体出口158离开接收器121。制冷剂出口156可以与压缩机112的抽吸配件164流体联接,使得制冷剂被吸入压缩机112中以在其中进行压缩。共流体出口158可以与泵111的入口166流体联接,使得共流体被吸入泵111中。压缩机112的出口168和泵111的出口170分别通过导管172与分离器113的入口117流体联接或者与吸收器114的入口流体联接,使得从压缩机112排出的制冷剂和从泵111排出的共流体可以在容器115中、在吸收器114中和/或在向分离器113或吸收器114供给的导管172中重新合并。
参照图4,提供了吸收循环环境控制系统200,其可以包括容器212(例如,发生器)、冷凝器214、第一膨胀装置216、蒸发器218、吸收器220、内部热交换器222、第二膨胀装置224和泵226。容器212可以包括入口228、制冷剂出口230和共流体出口232。入口228可以接收制冷剂和共流体(即,具有被吸收到共流体中的制冷剂)的混合物。
容器212可以通过任何可用的热源(例如,燃烧器、锅炉或来自另一系统或机器的废热)(未示出)来加热。在一些配置中,容器212可以从待被冷却的空间(例如,制冷机、冷冻机等内待被冷却的空间)中吸收热。当热被传递至在容器212内的制冷剂和共流体的混合物时,蒸气制冷剂从共流体中解吸,使得制冷剂可以与共流体分离。制冷剂可以通过制冷剂出口230离开容器212,并且共流体可以通过共流体出口232离开容器212。
一个或更多个超声换能器244可以连接至容器212。如图4中所示,超声换能器244可以安装至容器212的外表面234。在一些配置中,超声换能器244被设置在容器212内部并与制冷剂和共流体的混合物接触(如图5中所示)。超声换能器244的结构和功能可以与上述超声换能器44的结构和功能相似或相同。如上所述,超声换能器244产生超声振动,该超声振动被传送至制冷剂和共流体的混合物以使制冷剂从共流体中解吸的解吸速率增加。在一些配置中,超声振动可以用于产生期望量的解吸,而不需要添加来自另一个源的热。在一些配置中,超声振动和热的添加可以进一步加速解吸速率。
如上所述,控制模块248可以与超声换能器244连通并控制超声换能器244的操作以使解吸速率增加至期望的水平(例如,增加至与吸收速率匹配的水平)。控制模块248的结构和功能可以与控制模块48的结构和功能相似或相同。控制模块248可以与传感器250、252连通并且可以基于从传感器250、252接收的压力和/或温度数据控制超声换能器244的操作。传感器250可以被设置在容器212内,并且可以测量其中的制冷剂和共流体的混合物的压力或温度。传感器252可以被设置在吸收器220内,并且可以测量在其中的制冷剂和共流体的混合物的压力或温度。控制模块248还可以与泵226、膨胀装置216、膨胀装置224和/或风扇254、风扇256、风扇257连通并控制它们的操作。
冷凝器214是热交换器,其接收来自容器212的制冷剂出口230的制冷剂。在冷凝器214内,来自制冷剂的热可以被排放到例如空气或水或者一些其他介质中。在图4所示的特定配置中,风扇254可以迫使空气穿过冷凝器214以冷却冷凝器214内的制冷剂。
膨胀装置216、224可以例如为膨胀阀(例如,热膨胀阀或电子膨胀阀)或毛细管。第一膨胀装置216可以与冷凝器214和蒸发器218流体连通。蒸发器218可以接收来自膨胀装置216的膨胀的制冷剂。在蒸发器218内,制冷剂可以吸收例如来自空气或水的热。在图4中所示的具体配置中,风扇256可以迫使来自空间(即,待通过系统200冷却的房间或空间)的空气穿过蒸发器218以使空气冷却。
吸收器220可以包括制冷剂入口258、共流体入口260和出口262。制冷剂入口258可以接收来自蒸发器218的制冷剂。共流体入口260可以接收来自第二膨胀装置224的共流体。制冷剂可以在吸收器220内被吸收到共流体中。风扇257可以迫使空气穿过吸收器220以对制冷剂和共流体的混合物进行冷却并促进吸收。
与内部热交换器16一样,内部热交换器222可以包括第一盘管264和第二盘管266。第一盘管264可以接收来自容器212的共流体出口232的共流体。共流体可以从第一盘管264流过第二膨胀装置224,然后通过共流体入口260进入吸收器220中。
制冷剂和共流体的混合物可以通过出口262离开吸收器220,并且泵226可以将混合物泵送穿过第二盘管266。流过第二盘管266的制冷剂和共流体的混合物可以吸收来自流过第一盘管264的共流体的热。制冷剂和共流体的混合物可以从第二盘管266通过入口228流回容器212中。
应当理解,环境控制系统10、100、200可以用于执行冷却功能(例如,制冷或空调)或加热功能(例如,热泵)。
实施例
实施例1-与已知共流体的比较
将几种商业润滑剂与当前教导的共流体进行比较。minoil是矿物油。poe是多元醇酯。pag是聚亚烷基二醇。nmp是n-甲基吡咯烷酮。pve是聚乙烯醚。它们在相同的初始压力负荷、初始解吸压力和搅拌速率下在32°f下的解吸速率的比较绘制在图6中并且与此处所示的n-2,5,8,11-四氧杂十二烷基-2-吡咯烷酮(缩写:pyrr(eo)3me)进行比较:
在图6中,各值表示在一分钟时间内的压力增加,并且所述值为三次试验的平均值。
pyrr(eo)3me也表现出随温度的速率反转。通常,预期解吸速率在较高温度下更快而在较低温度下更慢。但是图7中的图表明解吸速率实际上在较低温度下更快。
实施例2-类似化合物的比较
a)脂族侧链和聚氧化烯侧链的比较
pyrr(eo)3me具有与氮连接的12原子链。饱和类似物,n-十二烷基-2-吡咯烷酮(简称:nddpy),也具有12原子链。它们具有相似的粘度(nddpy在40℃下=9.29cst,pyrr(eo)3me在40℃下=9.06cst),并且分子量接近。由于nddpy在5℃下凝固,所以必须在更高的温度下对其进行评估。pyrr(eo)3me具有更快的解吸速率,如图8所示。
b)羧酸酰胺与羧酸酯的比较
将pyrr(eo3me)与相应的酯化合物isov(eo)3me进行比较。虽然比较酯具有比pyrr(eo)3me更低的粘度(在所有条件相同的情况下,其将提供更快的解吸速率),但是pyrr(eo)3me具有更快的解吸速率。数据如图9所示。
c)与没有环状羧酸酰胺的化合物比较
还将pyrr(eo)3me与三乙二醇二甲醚进行比较,显示出低粘度的低分子量的聚亚烷基二醇不具有相同或更好的解吸速率。数据如图10所示,证明pyrr(eo)3me具有更快的解吸速率。图10的“二甲基甘醇醚”是三乙二醇二甲醚。
d)n-2,5,8,11-四氧杂十二烷基-己内酰胺表现出与pyrr(eo)3me相同的温度速率反转。
n-2,5,8,11-四氧杂十二烷基-己内酰胺具有7元内酰胺环而非pyrr(eo)3me的五元环。其表现出温度的速率反转,其中数据如图11所示。类似物的结构为:
e)环氧乙烷链长对二氧化碳解吸速率的影响。
图12中的图示出了不具有环氧乙烷、具有1个、2个或3个环氧乙烷添加至n-羟甲基-2-吡咯烷酮的一系列化合物解吸的瞬时速率(在0时刻的速率),如在此所示:
f)用2-吡咯烷酮环双封端的八原子链共流体的解吸速率。
在40℃下比较以下两种化合物。选择该温度是由于该化合物之一在0℃下凝固。
正如单吡咯烷酮封端的材料(在另一末端为甲基封端)一样,具有环氧乙烷和吡咯烷酮官能团二者的化合物在可比较的条件下更快地解吸二氧化碳。这可以在图13中的图中看到。
实施例3-共流体的合成
n-羟甲基-2-吡咯烷酮的制备
(该制备是对us3,073,843的略微修改)
向配备有温度计、磁搅拌器和回流冷凝器的250ml两颈圆底烧瓶中同时添加53.3g(0.63摩尔)2-吡咯烷酮、19.1g(0.64摩尔)多聚甲醛和0.2gkoh。将该混合物搅拌并加热至80℃至90℃,保持约2.5小时。然后,添加100ml热甲苯。然后过滤该溶液并使其冷却至室温。过滤所得晶体并用冷甲苯洗涤以产生64.5g(89%产率)的2-羟甲基-2-吡咯烷酮。hnmr和ftir确定了该结构。
n-羟甲基-2-己内酰胺的制备
(该制备基本上是us4,769,454的制备。)
向配备有磁搅拌器、温度计和回流冷凝器的500ml圆底烧瓶中添加113.2g(1.00摩尔)己内酰胺,将己内酰胺加热成液体,此时同时添加31g(1.0摩尔)多聚甲醛和0.7gk2co3。轻微的放热使温度升高至97℃,然而,将反应混合物保持在70℃至95℃下2.5小时。然后,在57℃下添加晶种,并将混合物在50℃下保持18小时。产生具有少量液体的白色晶体。将液体从白色晶体中倾析掉以产生138g(96%产率)的n-羟甲基-2-己内酰胺。hnmr和ftir确定了该结构。
n-2,5,8,11-四氧杂十二烷基-2-吡咯烷酮的合成
(参见us3,853,910——通过引用并入本文——关于烷基、芳基、烯基等的羟甲基-2-吡咯烷酮醚)
向配备有磁搅拌器、温度计和回流冷凝器的500ml两颈圆底烧瓶中同时添加58g(0.50摩尔)n-羟甲基-2-吡咯烷酮和246g(1.5摩尔)三乙二醇单甲醚。将该混合物冷却至约10℃并在5分钟至10分钟内添加21ml12nhcl,同时在添加期间保持温度为约10℃。然后,在搅拌的同时将混合物升温至室温并在该温度下保持2小时。在15℃至25℃下向混合物中添加40g25%naoh,然后搅拌0.5小时,产生nacl和产物的混合物。过滤掉盐,并使混合物经受真空蒸馏以除去水(27℃,在0.12托下)。更多的盐沉淀出来并停止蒸馏并过滤掉盐。在真空下通过6x3/4英寸vigreux柱将所得油蒸馏三次。在0.11托下在156℃下蒸馏出最终馏分,产生71.6g(55%产率)n-2,5,8,11-四氧杂十二烷基-2-吡咯烷酮。hnmr和ftir确定了该结构。
n-2,5,8,11-四氧杂十二烷基-己内酰胺的合成
向配备有磁搅拌器、温度计和回流冷凝器的500ml两颈圆底烧瓶中同时添加71.6g(0.50摩尔)n-羟甲基-己内酰胺和246g(1.5摩尔)三乙二醇单甲醚。将该混合物冷却至约4℃并在约15分钟内添加21ml12nhcl,同时在添加期间保持温度为约10℃。然后,在搅拌的同时将混合物升温至室温并在该温度下保持2.5小时。在15℃至25℃下向混合物中添加40g25%naoh,然后搅拌0.5小时,产生nacl和产物的混合物。使混合物经受旋转蒸发以除去水。过滤掉产生的盐,并使混合物经受直型接管(straighttakeover)真空蒸馏,收集在82℃至84℃下的顶部馏分。更多的盐沉淀出来并停止蒸馏并过滤掉盐。在真空下通过6x3/4英寸vigreux柱对所得油进行蒸馏。在0.2托下在159℃至169℃下蒸馏出主要馏分,产生80.1g(55%产率)n-2,5,8,11-四氧杂十二烷基-2-己内酰胺。hnmr和ftir确定了该结构。
1,8-双-(吡咯烷酮-1-基)-3,6-二氧杂辛烷的合成
向500ml单颈圆底烧瓶中同时添加134g(1.56摩尔)γ-丁内酯和109.5g(0.74摩尔)1,8-二氨基-3,6-二氧杂辛烷。该烧瓶配备有磁搅拌棒、h型分水器和冷凝器。在冷凝器的顶部通过firestone阀连接有氮气源。在加热混合物以使任何所得固体熔化的同时抽真空。在这之后产生真空,然后进行氮气吹扫三次。同时在氮气下,加热混合物,并在h型分水器中收集26ml水之后,将反应混合物冷却并使其经受直型接管真空蒸馏。将该物质蒸馏两次,并在0.11托下在196℃至214℃下蒸馏出最终产物馏分,产生124g产物。hnmr和ftir确定了该结构。
1,8-双-(吡咯烷酮-1-基)辛烷的合成
向500ml单颈圆底烧瓶中同时添加134g(1.56摩尔)γ-丁内酯和106g(0.74摩尔)1,8-二氨基辛烷。该烧瓶配备有磁搅拌棒、dean-stark分水器和冷凝器。在冷凝器的顶部通过firestone阀连接有氮源。在加热混合物以使任何所得固体熔化的同时抽真空。在这之后产生真空,然后进行氮吹扫四次。同时在氮气下,加热混合物,并在dean-stark分水器中收集27ml水之后,将反应混合物冷却并使其经受真空蒸馏。将该物质蒸馏两次,并在0.2托下在200℃至208℃下蒸馏出最终产物馏分,产生166g(81%产率)产物。hnmr和ftir确定了该结构。
异戊酸3,6,9-三氧杂癸基酯的合成
向配备有磁搅拌棒和dean-stark分水器的500ml单颈圆底烧瓶中同时添加53.7g(0.526摩尔)异戊酸、81.6g(0.50摩尔)三乙二醇单甲醚、0.3g对甲苯磺酸和200ml甲苯。在回流下加热混合物直至收集到8.5ml水。在冷却至室温之后,用200ml5%naoh水溶液、200ml饱和盐溶液洗涤甲苯溶液,并经硫酸钠干燥。将混合物过滤并进行旋转蒸发。进行直型接管蒸馏产生91.7g(73%产率)。产物馏分为在1.0托下在107℃至115℃下。ftir确定了该结构。
实施例4-测量二氧化碳解吸速率
将共流体(50g)添加到300mlparr反应器中,并在搅拌的同时和在研究的温度下将反应器抽空至约0.21托。停止搅拌,并使共流体沉降1分钟。除非另有说明,否则在所需压力(300psia)下将co2抽入反应器中。在最小限度的共流体搅拌下,尽可能平稳地引入co2。然后开始搅拌(400rpm),将时间标记为0分钟并记录压力速率。通常在搅拌15分钟之后记录平衡。注意,在此之前达到平衡。
然后,停止搅拌并使共流体沉降1分钟。然后,使压力迅速地但“平稳地”降低至50psi。重新开始搅拌并记录压力上升(指示co2从共流体中的释放)一段时间。瞬时速率通过在前20秒中获取测量值并通过数据拟合直线曲线来确定。
所有数据点代表至少3次实验运行。
出于说明和描述的目的提供了对实施方案的以上描述。前述描述不旨在穷举或限制本公开内容。特定实施方案的各个元件或特征通常不限于该特定实施方案,而是在可适用的情况下是可互换的并且可以用于所选择的实施方案,即使没有具体示出或描述。这些元件或特征也可以以许多方式改变。这样的变型不应被认为是偏离了本公开内容,并且所有的这些变型旨在包括在本公开内容的范围内。
- 还没有人留言评论。精彩留言会获得点赞!