电化学制造锗烷的方法与流程
本发明涉及电化学制造锗烷的方法。
背景技术:
以往,半导体器件的高速化和低耗电化通过该器件的微细化等而达到,作为用于进一步的高速化和低耗电化的技术,sige基板等的应变硅受到注目。
作为制作该sige基板时的原料,使用锗烷(geh4),预想到伴随着sige基板的使用的增加,geh4的使用量也增加。
作为这样的geh4的制造方法,例如在专利文献1中记载了以下内容:通过作为阴极使用cu合金或sn合金,能够以高的电流效率电化学制造geh4。
另外,在非专利文献1中记载了以下内容:作为在电化学制造geh4时使用的阴极,将pt、zn、ti、石墨、cu、ni、cd、pb、sn进行了筛选,结果cd或cu在电流效率和污染等方面是最佳的。
而且,在非专利文献2中公开了以下内容:作为在电化学制造geh4时使用的阴极,对许多的阴极进行了调查,结果在作为阴极使用hg的情况下氢化率成为99%以上。
在先技术文献
专利文献
专利文献1:日本特开2012-52234号公报
非专利文献
非专利文献1:turyginet.al.,inorganicmaterials,2008,vol.44,no.10,pp.1081-1085
非专利文献2:djurkovicet.al.,glanikhem.drustva,beograd,1961,vol.25/26,pp.469-475
技术实现要素:
如上述文献记载的那样的以往的电化学制造geh4的方法,例如由于在上述专利文献1的实施例中使用的阴极(mcmaster-carr公司制的青铜)难以应用通过镀敷、涂敷等而仅使表面存在有效的元素这样的方法、在上述非专利文献2中使用的阴极(hg)的毒性高等的原因而不适合作为工业性地制造geh4的方法。
本发明的一实施方式提供作为电化学制造geh4的方法在工业上有利的方法。
本发明人为了解决上述课题而进行了深入研究,结果发现根据下述制造方法等能够解决上述课题,以至于完成了本发明。
本发明的构成例如下。
[1]一种电化学制造锗烷的方法,在具有隔膜、阳极和包含金的阴极的电化学单元中,向包含锗化合物的电解液通电,在阴极使锗烷产生。
[2]根据[1]所述的制造方法,上述电解液为包含二氧化锗和离子性物质的电解液。
[3]根据[2]所述的制造方法,上述离子性物质为氢氧化钾或氢氧化钠。
[4]根据[2]或[3]所述的制造方法,上述离子性物质为氢氧化钾,上述电解液中的氢氧化钾的浓度为1~8mol/l。
[5]根据[1]~[4]的任一项所述的制造方法,上述通电时的阴极的电流密度为30~500ma/cm2。
[6]根据[1]~[5]的任一项所述的制造方法,使上述锗烷产生时的反应温度为10~100℃。
根据本发明的一实施方式,能够以工业上有利的方法、特别高的电流效率来电化学制造geh4。
附图说明
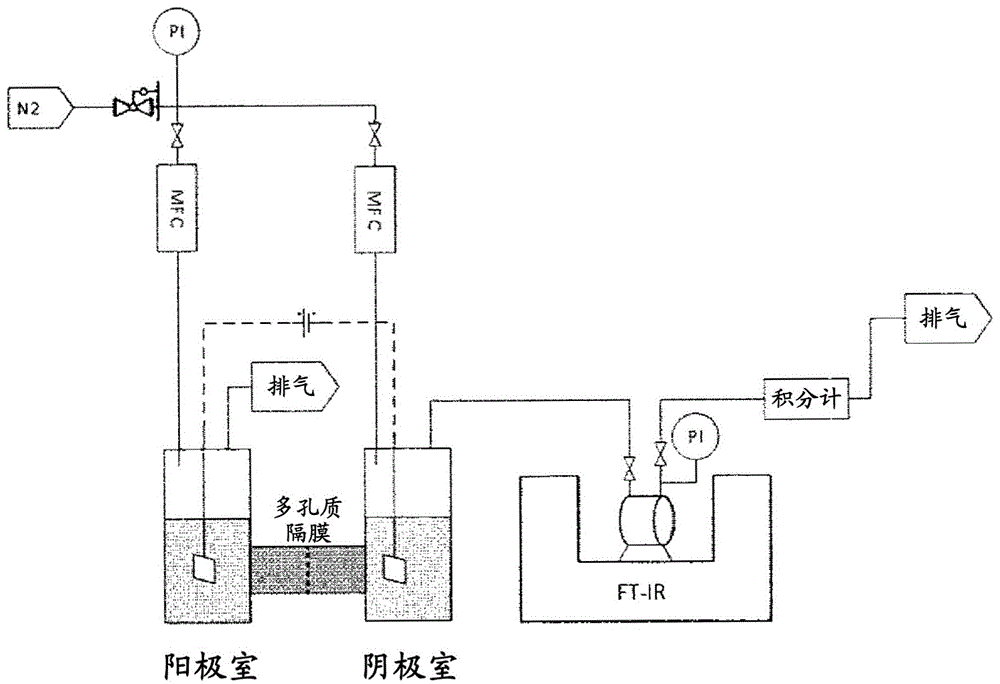
图1是在实施例中使用的装置的概略示意图。
图2是表示实施例1和比较例1的制造方法中的反应时间与电流效率的关系的图。
具体实施方式
《电化学制造geh4的方法》
本发明的一实施方式涉及的电化学制造geh4的方法(以下也称为“本方法”。),在具有隔膜、阳极和包含金的阴极的电化学单元(electrochemicalcell)中,向包含锗化合物的电解液通电,在阴极使geh4产生从而电化学制造geh4。
根据本方法,能够以工业上有利的方法、特别高的电流效率来电化学制造geh4。因此,通过使用由本方法得到的geh4,也能够在工业上有利地制造sige基板。
作为这样的工业性的反应,例如可列举如电解液容量为500~2500l、单元(cell)数为30~150个、使用的电流为100~300a这样的规模的反应。
根据本方法,能够以优选10~90%、更优选12~40%的电流效率制造geh4。
再者,上述电流效率具体而言能够利用下述实施例中记载的方法来测定。
<电化学单元>
作为上述电化学单元,如果具有隔膜、阳极和上述阴极就不特别限制,能够使用以往公知的单元。
作为该单元,可具体地列举使用隔膜将包含阳极的阳极室和包含阴极的阴极室隔开的单元等。
<阴极>
上述阴极如果包含au就不特别限制。
该阴极可以是由金属au构成的电极、由以au为主成分的au基合金构成的电极,也可以是镀敷或涂敷了金属au或au合金的电极。
作为上述镀敷或涂敷了的电极,可列举对ni等的基材镀敷或涂敷了金属au或au合金的电极等。
其中,由于金属au为高价格,因此从成本方面出发,优选为镀敷或涂敷了金属au或au合金的电极。
上述阴极的形状不特别限制,可以是板状、柱状、中空状等的任一形状。
另外,上述阴极的大小、表面积等也不特别限制。
<阳极>
作为上述阳极,不特别限制,使用以往在电化学制造geh4时所使用的阳极即可,但优选由ni、pt等导电性金属构成的电极、由以该导电性金属为主成分的合金构成的电极等,从成本的方面出发,优选由ni构成的电极。
另外,上述阳极与阴极同样地也可以使用镀敷或涂敷了上述导电性金属或包含该金属的合金的电极。
上述阳极的形状、大小、表面积等也与上述阴极同样地不特别限制。
<隔膜>
作为上述隔膜,不特别限制,使用以往在电化学单元中所使用的能够将阳极室和阴极室隔开的隔膜即可。
作为这样的隔膜,能够使用各种的电解质膜、多孔质膜。
作为电解质膜,可列举高分子电解质膜、例如离子交换固体高分子电解质膜,具体地可列举nafion(注册商标)115、117、nre-212(シグマアルドリッチ公司制)等。
作为多孔质膜,能够使用多孔质玻璃、多孔质氧化铝、多孔质二氧化钛等的多孔质陶瓷、多孔质聚乙烯、多孔质丙烯等的多孔质聚合物等。
在本发明的一实施方式中,通过隔膜将电化学单元分成阳极室和阴极室,因此能够不使在阳极产生的o2气和在阴极产生的geh4混合而将其从各自的电极室的独立的出口取出。
若o2气和geh4混合,则存在o2气与geh4发生反应从而geh4的收获率降低的倾向。
<包含锗化合物的电解液>
在本方法中,由包含锗化合物的电解液制造geh4。
该电解液优选为水溶液。
作为上述锗化合物,优选geo2。
上述电解液中的geo2的浓度,其高时反应速度变快,能够高效地合成geh4,因此优选使其为相对于溶剂、优选相对于水的饱和浓度。
为了使电解液的导电性提高、促进geo2在水中的溶解性,优选上述电解液包含离子性物质。
作为该离子性物质,能够使用在电化学上使用的以往公知的离子性物质,但从上述效果优异等方面出发,优选koh或naoh。其中,koh水溶液与naoh水溶液相比导电性优异,因此优选koh。
上述电解液中的koh的浓度优选为1~8mol/l,更优选为2~5mol/l。
若koh的浓度处于上述范围,则能够容易地得到geo2浓度高的电解液,能够以高的电流效率高效地制造geh4。
若koh的浓度小于上述范围的下限,则存在电解液的导电性变低的倾向,有时在geh4的制造中需要高电压,另外,存在geo2在水中的溶解量降低的倾向,有时反应效率降低。另一方面,若koh的浓度超过上述范围的上限,则存在作为电极、单元的材质需要耐腐蚀性高的材质的倾向,有时装置的成本变高。
<反应条件>
在本方法中,从反应速度优异、能够以高的电流效率制造geh4等方面出发,制造geh4时(上述通电时)的阴极的每单位面积的电流的大小(电流密度)优选为30~500ma/cm2,更优选为50~400ma/cm2。
若电流密度处于上述范围,则也能够不使每单位时间的geh4的产生速度和反应效率降低而适度地控制由水的电解得到的氢气的产生量。
从反应速度优异、能够以低成本制造geh4等方面出发,制造geh4时(使geh4产生时)的反应温度优选为10~100℃,更优选为15~40℃。
若反应温度处于上述范围,则也能够不使反应效率降低而适度地控制用于单元的加热的电力消耗。
制造geh4时的反应气氛(阳极室及阴极室的气相部分)不特别限制,但优选为惰性气体气氛,作为该惰性气体,优选氮气。
在本方法中,电化学单元中的上述电解液可以是使其静止的状态,也可以搅拌,也可以另行设置其他的液槽而使其循环流通。
在设置上述其他的液槽而使其循环流通的情况下,反应液浓度的变化相对变小,能够期待电流效率的稳定化,并且能够保持较高的电极表面的geo2浓度,能够期待反应速度的提高。因此,优选电化学单元中的上述电解液循环流通。
<geh4的制造装置>
在本方法中,只要使用上述电化学单元就无特别限制,能够使用除了该单元以外还具有例如如图1所示的电源、测定单元(ft-ir、压力计(pi)、积分计(integrator)等)、氮气(n2)供给路、质量流量控制器(mfc)、排气路等以往公知的构件的装置。
另外,也可以使用未图示的具有前述的循环流路等的装置。
实施例
以下,列举实施例对本发明进行具体说明,但本发明并不被这些实施例限定。
[实施例1]
使用以下的材料,制作了如图1所示的利用隔膜将阳极室和阴极室隔开的氯乙烯制电化学单元。
·阴极:0.5cm×0.5cm×厚度0.5mm的au板
·阳极:2cm×2cm×厚度0.5mm的ni板
·隔膜:ナフィオン(注册商标)nre-212(シグマアルドリッチ公司制)
·电解液:使geo2以90g/l的浓度溶解于4mol/l的koh水溶液而成的液体
·向阴极室的电解液导入量:100ml
·向阳极室的电解液导入量:100ml
·标准电极:将银-氯化银电极设置于阴极
通过将所得到的电化学单元中的阳极室及阴极室的气相部分用氮气(n2)清除后,作为电源使用北斗电工(株)制的hz-5000,以-200ma流通电流10小时,来电化学制造了geh4。此时的电流密度为348ma/cm2。
再者,在流通电流时没有控制电化学单元的温度,结果反应温度为18~23℃。
通过使用积分计对阴极室的出口气体进行测定,来测定通过反应而产生的出口气体总量(包含geh4和氢气的气体),并使用ft-ir来测定了出口气体总量中的geh4浓度。由这些测定结果算出geh4的产生量。
在某个特定的反应时间由最近1小时的geh4的产生量和施加的电量,基于下述式算出电流效率,将该电流效率作为反应时间1小时的电流效率。同样地算出了各反应时间的电流效率。将结果示于图2。
根据图2的结果,电流效率的最大值为23%。
电流效率(%)=[与产生上述产生量(mmol/min)的geh4对应的电量(c/min)×60(min)×100]/[施加的总电量(c/min)×60(min)]
[比较例1]
作为阴极使用0.5cm×0.5cm×厚度0.5mm的cu板,将施加的电流变更为以-100ma流通10小时,除此以外在与实施例1同样的条件下进行了反应。
将与实施例1同样地算出的电流效率的结果示于图2。
根据图2的结果,电流效率的最大值为18%。
- 还没有人留言评论。精彩留言会获得点赞!