面瘫复正散的质量检测方法与流程
本发明涉及中医药技术领域,具体涉及面瘫复正散的质量检测方法。
背景技术:
面瘫是面神经的非化脓性炎症所致的一种急性周围性面瘫。主要表现为患者面部表情肌瘫痪,即口角歪斜,属中医口僻(中经络证)。《内经》中称口喁、口僻,并认为口眼歪斜主要是足阳明胃经的病变。明《景岳全书·痱风》指出:“口眼喁斜有寒热之辨……然而血气无亏,则虽热未必筋缓,虽寒未必筋急,亦总由血气之衰可知也。”目前,中医界多认为本病由正气不足,腠理不密,卫外不固,络脉空虚,风邪乘虚侵袭面部经络,面部足阳明经筋失于濡养,气血痹阻,以致肌肉纵缓不收所致。但有寒热之别,寒症多有面部受凉因素,热型面瘫多因素体阳盛、寒邪入里化热、热阻阳明、少阳脉络,致经气阻滞,经筋失于濡养而发。面瘫早期的治疗十分关键,早期治疗是否恰当,直接影响日后的恢复。目前早期治疗多给予激素以减轻面神经水肿受压,减缓面神经变性。早期风热型患者多伴有感染,所以抗病毒、抗菌素的使用也是十分必要的。中药外治法治疗特发性面神经麻痹疗效显著,大多数研究者配合针灸。
周围性面瘫急性期在临床最为常见,同时急性期也是治疗周围性面瘫的黄金时段,注重此期的治疗与调护,可起到事倍功半的疗效。采用中药外用复方制剂,临床上合并针刺治疗,是治疗周围性面瘫的一个可行方案。这种治疗方法能使药物直接渗透皮肤,药效直达病灶,能促进侧支循环建立,减轻局部炎性渗出和水肿,改善神经周围微循环,具有促进局部血流,改善神经营养作用。具有见效快、疗程短、效果好、无副反应的优势。
面瘫复正散处方由三七、熟大黄、紫花地丁、厚朴、冰片5味中药配伍组成,是贵阳中医学院第二附属医院蔡伟副主任医生根据中医理论及多年临床经验凝集而成用于治疗周围性面瘫急性期及局部肿痛患者的纯中药复方外用制剂。其组成药物分别具有抗炎消肿、抑制炎性渗出、抗菌、镇痛、降低毛细血管通透性、促进组织创面修复等各方面的功效。临床上合并针刺治疗也表明,面瘫复正散对改善耳后疼痛有效,其可能机理是炎症与疼痛呈正相关性,是通过改善患者局部疼痛,使面神经炎的非特异炎性症状得到有效控制。但目前没有该药物适用的质量检测方法,难以保证制剂的稳定性和疗效。
技术实现要素:
本发明的目的是提供面瘫复正散的质量检测方法,以克服现有技术的不足。
本发明的技术方案是这样的:
面瘫复正散的质量检测方法,该面瘫复正散是这样制备的:将三七5~15份、熟大黄5~15份、紫花地丁10~20份、厚朴5~15份、冰片0.3~1份配齐,除冰片外,三七、熟大黄、紫花地丁和厚朴这四味药材经60℃减压干燥3小时,粉碎成粉末;将冰片研细,与上述粉末配研,过筛,混合,分装,即得;
该面瘫复正散的质量检测方法包括如下几项:
(1)性状:土黄色粉末;气辛,味苦;
(2)鉴别:包括三七、熟大黄、紫花地丁、厚朴的薄层色谱鉴别;
(3)检查:包括粒度、外观均匀度、水分、装量差异和微生物限度的检查;
(4)含量测定:包括人参皂苷Rg1的含量测定。
其中,三七的薄层色谱鉴别方法包括如下步骤:
分别制备供试品溶液、阴性对照溶液、对照药材溶液和对照品溶液;照薄层色谱法试验,吸取供试品溶液、阴性对照溶液、对照药材溶液和对照品溶液点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(15:40:22:10)10℃以下放置的下层溶液为展开剂,展开,取出,晾干,喷以硫酸乙醇溶液,加热至斑点显色清晰;
供试品色谱中,在与对照药材和对照品色谱相应的位置上,显相同颜色的荧光斑点,在缺三七药材的阴性样品色谱相应位置上,无此斑点。
进一步的,熟大黄的薄层色谱鉴别方法包括如下步骤:
分别制备为供试品溶液、阴性对照溶液和对照药材溶液;照薄层色谱法试验,分别取对照药材溶液、阴性对照溶液和供试品溶液,点于同一硅胶G薄层板上,以正己烷-乙酸乙酯-甲酸(27:10:2.4)为展开剂展开,取出,晾干,于365nm紫外光灯下检视;
供试品色谱中,在与对照药材同位置有相同颜色斑点,阴性对照无干扰。
进一步的,紫花地丁的薄层色谱鉴别方法包括如下步骤:
分别制备供试品溶液、阴性对照溶液和对照药材溶液;照薄层色谱法试验,吸取供试品溶液、阴性对照溶液和对照药材溶液,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯-甲酸(5:3:1)的上层溶液为展开剂,展开,取出,晾干,置于365nm紫外光灯下检视;
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,阴性对照无干扰;
进一步的,厚朴的薄层色谱鉴别方法包括如下步骤:
分别制备供试品溶液、阴性对照溶液和对照药材溶液;照薄层色谱法,分别吸取供试品溶液、阴性对照溶液和对照药材溶液,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-乙酸乙酯-甲酸(8.5:1.5:0.2)为展开剂,展开,取出,晾干,喷以香草醛硫酸溶液,加热至斑点显色清晰;
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色斑点,且阴性对照无干扰。
更进一步的,采用平皿法来进行面瘫复正散的微生物限度检查。
更进一步的,所述人参皂苷Rg1的含量测定包括如下步骤:
以本品制备供试品溶液,以人参皂苷Rg1制备对照品溶液,吸取对照品溶液与供试品溶液注入液相色谱仪进行测定,色谱条件为:以Aglient ZORBAX SB-C8(150×4.6mm,5μm)为色谱柱;以乙腈为流动相A,以水为流动相B,进行梯度洗脱;流速为1ml/min;柱温30℃;检测波长为203nm;梯度洗脱规定如下:
流动相A:0~20分钟:18%;20~30分钟:18→19%;
流动相B:0~20分钟:82%;20~30分钟:82→81%。
本发明的技术效果如下:
通过以上方法,能够制定出面瘫复正散的质量标准,从而实现对面瘫复正散的质量检测,经实验证明,以该方法为标准检测面瘫复正散,可以很好的保证制剂的稳定性,从而保证其疗效。
附图说明
图1是本发明的制备方法的工艺流程图;
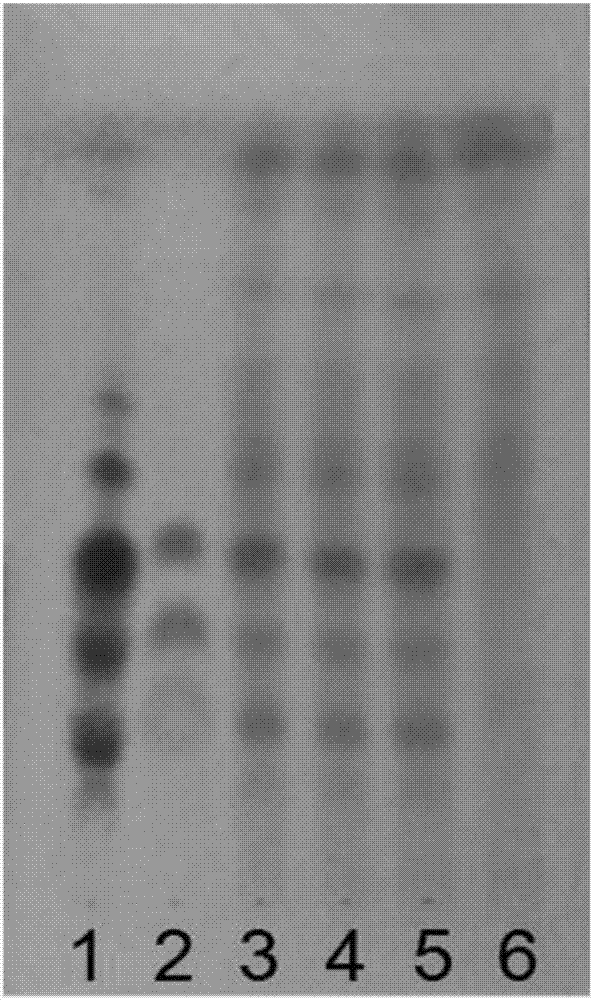
图2是本发明的三七的薄层鉴别图;图中,1、三七对照药材;2、三七皂苷R1和人参皂苷Rg1和人参皂苷Rb1混合对照品;3~5、面瘫复正散供试品(批号:20160311,20160312,20160313);6、阴性供试品(缺三七药材);
图3是熟大黄的薄层鉴别图;图中:1、熟大黄对照药材;2~4、面瘫复正散供试品(批号:20160311,20160312,20160313);5、阴性供试品(缺熟大黄药材);
图4是紫花地丁的薄层鉴别图;图中,1、紫花地丁对照药材;2~4、面瘫复正散供试品(批号:20160311,20160312,20160313);5、阴性供试品(缺紫花地丁药材);
图5是厚朴的薄层鉴别图;图中,1、厚朴对照药材;2~4、面瘫复正散供试品(批号:20160311,20160312,20160313);5、阴性供试品(缺厚朴药材);
图6是厚朴的薄层鉴别图一;图中,1、冰片对照药材;2、面瘫复正散供试品(批号:20160501);3、阴性供试品(缺冰片药材);
图7是厚朴的薄层鉴别图二;图中,1、冰片对照药材;2、面瘫复正散供试品(批号:20160501);3、阴性供试品(缺冰片药材)。
具体实施方式
下面结合附图和实施例对本发明作进一步的详细说明,但本发明的保护范围不受具体实施例的任何限制,而是由权利要求加以限定。
实施例1:
1、处方组成:三七10g 熟大黄10g 紫花地丁15g 厚朴10g冰片0.5g。
2、制备方法:如图1所示的工艺流程,将以上五味,按处方23倍量配齐,除冰片外,三七、熟大黄等四味药材经60℃减压干燥3小时,粉碎成最细粉;将冰片研细,与上述粉末配研,过筛,混合,分装,即得。装量标准:6g/袋。
3、功能主治:清热消肿、活血通络。用于周围性面瘫急性期及局部肿痛患者。
4、用法用量:外用,根据病情,选用凡士林、油脂等调匀外敷,帖敷局部穴位,每穴一贴,每日一次,1月为1疗程。根据病情需要可再重复疗程。
5、检查:按照散剂项下的有关规定(《中国药典》2015年版四部通则0115)进行检查。分别检查粒度、外观均匀度、水分、装量差异、微生物限度,应符合规定。
5.1、粒度:按照散剂“粒度”项下(通则0115)测定,应符合规定。
5.2、外观均匀度按照散剂“外观均匀度”项下(通则0115)测定,应符合规定。
5.3、水分:按照水分测定法项下第二法(《中国药典》2015年版四部通则0832)进行测定,水分不得过9.0%。
5.4、装量差异:取本品10袋,照散剂“装量差异”项下(通则0115)依法检查,装量差异限度应在±7%以内,超出装量差异限度的不得多于2袋,并不得有1袋超出限度1倍。
实验例1:
面瘫复正散的质量检测方法:
1性状:中试三批样品均为土黄色粉末;气辛,味苦。
2薄层鉴别:
2.1三七的薄层色谱研究
取本品2g,加5ml水,搅匀,再加水饱和的正丁醇50ml,超声处理1小时,滤过,滤液用120ml正丁醇饱和的水萃取,分取正丁醇层,水浴蒸干,残渣用1ml甲醇溶解,作为供试品溶液。取三七的阴性模拟制剂2g,同法制备阴性对照溶液。另取三七药材粉末0.5g,同法制成对照药材溶液。再称取人参皂苷Rg1对照品、人参皂苷Rb1对照品及三七皂苷R1对照品适量,分别用甲醇制成每1ml 含0.5mg的溶液,作为对照品溶液。照薄层色谱法(《中国药典》2015年版四部通则0502)试验,吸取上述四种溶液各5μl,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(15:40:22:10)10℃以下放置的下层溶液为展开剂,展开,取出,晾干,喷以10%的硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品色谱中,在与对照药材和对照品色谱相应的位置上,显相同颜色的斑点,在缺三七药材的阴性样品色谱相应位置上,无此斑点(见图2)。
2.2熟大黄的薄层色谱研究
取本品2g,加甲醇15ml,超声提取20min,滤过,滤液浓缩至1ml,作为供试品溶液。取缺熟大黄的阴性模拟制剂2g,同法制备阴性对照溶液。另取熟大黄对照药材粉末5g,加40ml水直火回流提取1h,滤液水浴上挥干,残渣加甲醇10ml转入锥形瓶中,超声提取10min,滤液浓缩至1ml,作为对照药材溶液。照薄层色谱法(《中国药典》2015年版四部通则0502)试验,分别取对照药材溶液3μl、阴性对照溶液、复方供试溶液各2μl,点于同一硅胶G薄层板上,以正己烷-乙酸乙酯-甲酸(27:10:2.4)为展开剂展开,取出,晾干,于365nm紫外光灯下检视。供试品色谱中,在与对照药材同位置有相同颜色斑点,阴性对照无干扰(见图3)。
2.3紫花地丁的薄层色谱研究
取本品2g,加甲醇20ml溶解,超声处理30min,滤过,滤液蒸干,残渣加纯水10ml,搅拌使溶解,滤过,滤液蒸干,残渣加乙酸乙酯1ml使溶解,作为供试品溶液。取缺紫花地丁的阴性模拟制剂2g,同法制备阴性对照溶液。另取紫花地丁对照药材1.0g,同法制成对照药材溶液。照薄层色谱法(《中国药典》2015年版四部通则0502)试验,吸取上述三种溶液各3μl,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯-甲酸(5:3:1)的上层溶液为展开剂,展开,取出,晾干,置于紫外灯(365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,阴性对照无干扰(见图4)。
2.4厚朴的薄层色谱研究
取供试品2g,取按配方比例配制的阴性对照样品2g,分别加甲醇15ml,超声30min,滤过,滤液分别作为供试品溶液和阴性对照溶液。另取厚朴对照药材粉末0.5g,加5ml甲醇,同法制成对照药材溶液;照薄层色谱法(《中国药典》2015年版四部通则0502)试验,分别吸取上述供试品溶液、阴性对照溶液各2μl,对照药材溶液5μl,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-乙酸乙酯-甲酸(8.5:1.5:0.2)为展开剂,展开,取出,晾干,喷以1%香草醛硫酸溶液,在100℃加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色斑点,且阴性对照无干扰(见图5)。
2.5冰片的薄层色谱研究
参照“TLC、GC法检测冠心苏合胶囊中的冰片”[14]中对冰片薄层色谱研究:取本品1g,加入乙酸乙酯10ml,萃取,取乙酸乙酯液,作为供试品溶液。取缺冰片阴性模拟试剂1g,同法制备阴性对照液。另取冰片对照药材1g,加乙酸乙酯制成浓度为2mg/ml的溶液,作为对照品溶液。照薄层色谱法(《中国药典》2015年版四部通则0502)试验,吸取上述三种溶液各2μl,分别点于硅胶G薄膜板上,以石油醚(30~60℃)-乙酸乙酯(9:1)为展开剂,展开,取出,晾干,喷以磷钼酸试液,热风吹至斑点显色清晰。供试品色谱中,在与对照药材色谱相应的位置上,无相应的斑点(见图6)。参照“复方消炎散中冰片和姜黄的薄层色谱鉴别”中对冰片薄层色谱研究:取本品1g,加入三氯甲烷10ml萃取,取三氯甲烷液,作为供试品溶液。取缺冰片阴性模拟试剂1g,同法制备阴性对照液。另取冰片对照药材,加乙酸乙酯制成浓度为1mg/ml的溶液,作为对照品溶液。照薄层色谱法(《中国药典》2015年版四部通则0502)试验,吸取上述三种溶液各2μl,分别点于硅胶G薄层板上,以环己烷-乙酸乙酯(17:3)为展开剂,展开,取出,晾干,喷以磷钼酸试液,热风吹至斑点显色清晰。供试品色谱中在与对照药材色谱相应的位置上,无相应的斑点(见图7)。故冰片的定性鉴别未列入本发明的质量检测方法。
实验例2:微生物限度检查法
1、供试液的制备:取本品10ml,加入不超过45℃PH7.0无菌氯化钠-蛋白胨稀释液至100ml,边加边搅拌,使供试品充分混匀,即得1:10的供试液。
2、微生物计数法:需氧菌总数计数:取1:10供试液1ml分注1个皿,1ml/皿,按《中国药典》2015版四部非无菌产品微生物限度检查:微生物计数法(通则1105)项下平皿法进行菌落计数。
霉菌和酵母菌总数计数:取1:10供试液2ml分注2个皿,1ml/皿,按《中国药典》2015版四部非无菌产品微生物限度检查:微生物计数法(通则1105)中的平皿法进行菌落计数。
3、控制菌检查:
金黄色葡萄球菌:取1:10供试液按照《中国药典》2015版四部非无菌产品微生物限度检查:控制菌检查法(通则1106)下相应控制菌检查方法进行。
铜绿假单胞菌:取1:10供试液按照《中国药典》2015版四部非无菌产品微生物限度检查:控制菌检查法(通则1106)下相应控制菌检查方法进行。
药品微生物限度检查方法适用性试验报告
培养基、稀释剂及来源:
0.9%无菌氯化钠-蛋白胨缓冲液、胰酪大豆胨琼脂、沙氏葡萄糖琼脂、胰酪大豆胨液体培养基、麦康凯液体培养基、麦康凯琼脂培养基等。(上海盛思生化科技有限公司生产,均按《中国药典》2015版相关规定配制及灭菌)。
菌种及来源:
以上菌种均为中国食品药品检定研究院派生菌种。
实验仪器:高压蒸汽灭菌器、电子天平(十分之一)、洁净室净化工作台,菌落计数器等。
结果:适用性记录及结果如下:
1、需氧菌、霉菌及酵母菌总数计数方法选择试验结果见表1;
2、需氧菌、霉菌及酵母菌总数计数方法验证回收试验见表2-4(附表记录1-3);
3、控制菌——金黄色葡萄球菌检查方法的验证结果见下表5;
4、控制菌——铜绿假单胞菌检查方法的验证结果见下表6;
表1需氧菌、霉菌及酵母菌总数计数方法选择试验结果
备注:“——”表示未做此项。
结论:
1、1:10的供试液采用平皿法(1ml/皿)大肠埃希菌、白色念珠菌、黑曲霉的回收率能达到70%以上;1:10的供试液采用平皿法(0.5ml/皿)枯草芽孢杆菌的回收率能达到70%以上,1:10的供试液采用平皿法(0.2ml/皿)金黄色葡萄球菌的回收率能达到70%以上。
2、面瘫复正散具有抑菌活性成分(如:紫花地丁、厚朴等),因此在进行微生物验证时,出现较明显的抑菌能力,尤其是对金黄色葡萄球菌的抑制效果明显,其次是对枯草芽孢杆菌有一定的抑制作用,所以采用平皿法进行,而药物对枯草芽孢杆菌的作用不是很明显,采取常规法即可。根据验证结果,综合考虑验证操作步骤,最终确定采用平皿法(1:10供试液1ml,分注5个平皿)来进行面瘫复正散的微生物限度检查。
表2需氧菌、霉菌及酵母菌总数计数方法验证回收试验记录1
注:试验组:供试液+试验菌液;供试品对照组:供试液+稀释液;菌液组:稀释液+试验菌液。
表3需氧菌、霉菌及酵母菌总数计数方法验证回收试验记录2
表4需氧菌、霉菌及酵母菌总数计数方法验证回收试验记录3
表5金黄色葡萄球菌检查方法的验证试验记录
备注:甘露醇氯化钠平板中:“+”标示有典型菌落生长;“—”标示无菌生长。
血浆凝固酶试验中:“+”标示有血浆凝固;“—”标示血浆不凝固。
“——”表示未做此项。
表6铜绿假单胞菌检查方法的验证试验记录
备注:甘露醇氯化钠平板中:“+”标示有典型菌落生长;“—”标示无菌生长。
氧化酶试验中:“+”标示纸上培养物出现粉红色—紫红色的变化;“—”标示纸上培养物不变色或仅显粉红色改变。
绿脓菌素试验中:“+”标示出现粉红色变色反应;“—”标示无粉红色出现。
“——”表示未做此项。
结论:
经本试验验证,面瘫复正散的需氧菌计数可按《中国药典》2015版四部通则1105项下平皿法(1:10供试液,0.2ml/皿)进行计数;霉菌及酵母菌总数计数可按《中国药典》2015版通则1105项下平皿法(取1:10供试液2ml分注2个皿,1.0ml/皿)计数;控制菌中金黄色葡萄球菌和铜绿假单胞菌的检查可按《中国药典》2015版通则1106项下规定的常规法进行检查。
实验例3:含量测定
人参皂苷Rg1照高效液相色谱法(《中国药典》2015年版四部通则0512)测定。
1.仪器与试药
仪器:Agilent 1260高效液相色谱仪;梅特勒-托利多AE电子分析天平(METTLER TOLEDO十万分之一)。
试药:乙腈[色谱纯,美国天地(TEDIA)有限公司];水(娃哈哈饮用纯净水,贵阳娃哈哈食品有限公司制造)。
对照品:人参皂苷Rg1对照品(供含量测定用,含量以91.7%计,批号为:110703-201530),购自中国食品药品检定研究所。
样品:面瘫复正散(批号:20160501 20160502 20160503)。
2.对照品溶液制备
对照品溶液的制备:精密称取人参皂苷Rg1对照品4.536mg,加甲醇制成每1ml含人参皂苷Rg1 0.416mg的溶液,即得。
3.色谱条件的选择:
在进行人参皂苷Rg1色谱条件选择时,参考文献,进行了色谱柱、流动相以及柱温的筛选。
3.1色谱柱的选择
不同的色谱柱对化学成分分离有一定的影响,在此考察了Diamonsil Plus C18色谱柱(250×4.6mm,5μm);Ultimate XB-C18色谱柱(250×4.6mm,5μm);Aglient ZORBAX SB-C18(250×4.6mm,5μm)及Aglient ZORBAX SB-C8(150×4.6mm,5μm)色谱柱四种,结果见表7。
表7人参皂苷Rg1色谱柱条件选择表
通过对不同色谱柱条件下色谱图进行比较,结果表明Ultimate XB-C18色谱柱峰前延,对称性差,分离度低;Diamonsil plus C18色谱柱峰展宽,峰形差;Agilent Zorbax SB-C18色谱柱峰拖尾,分离效果差;Agilent Zorbax SB-C8色谱柱峰形较好,分离度较高,因此确定Agilent Zorbax SB-C8(150×4.6mm,5μm)色谱柱为试验用柱。
3.2流动相的考察
对三种不同洗脱系统进行考察,结果见表8-10。
表8洗脱系统一
表9洗脱系统二
表10洗脱系统三
通过比较以上三种不同洗脱系统的色谱峰,其中洗脱系统一人参皂苷Rg1与其他组分峰未完全分离,分离效果差;洗脱系统二色谱峰分离较好,峰形较锐;洗脱系统三人参皂苷Rg1与其他组分峰未完全分离,且阴性有干扰,分离效果差。因此确定洗脱系统二为流动相条件。
3.3柱温的考察
分别考察了25℃、30℃、35℃时色谱分离效果。
结果表明,柱温为25℃时,人参皂苷Rg1与其他组分峰未完全分离,分离效果差;柱温为30℃、35℃对色谱峰的分离效果影响不明显,考虑到室温等情况,选择柱温为30℃。
综上,确定人参皂苷Rg1的色谱条件为Agilent Zorbax SB-C8(150×4.6mm,5μm)色谱柱;乙腈-水梯度洗脱:0~20min(18:82),21~30min(19:81);流速:1ml/min;柱温:30℃;检测波长:203nm;分析时间:30min;进样量:10μl。理论板数按人参皂苷Rg1计算应不低于4000。
当然,以上只是发明的具体应用范例,本发明还有其他的实施方式,凡采用等同替换或等效变换形成的技术方案,均落在本发明所要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!