一种基于生物膜干涉技术的安非他命检测方法与流程
本发明属于毒品检测领域,尤其是批量样本检测领域,涉及一种基于生物膜干涉技术的安非他命检测方法。
背景技术:
安非他命由盐酸麻黃素合成,能兴奋中枢神经,虽具有欣快、警觉及抑制食欲之作用,重复使用会成瘾。中毒症状包括多话、头痛、错乱、高烧、血压上升、盗汗、瞳孔放大、食欲丧失。大剂量使用引起精神错乱,思想障碍,类似妄想性精神分裂症,多疑、幻听、被害妄想等。长期使用导致器官性脑症候群,有高血压及脑中风之危险。停用之脱瘾症状包括精神呆滞、昏睡、易怒、烦躁不安、忧虑,有自杀的倾向。
目前安非他命的检测方法主要为胶体金法和色谱法。胶体金试纸条虽然检测方便,但其以吸毒人员尿液为检测对象,其灵敏度只有几百ng/ml,且每个试纸条每次只能检测一个人。色谱法虽然灵敏度高,但前处理过程时间较长,需要专门技术人员和大规模昂贵仪器。而本技术以其高灵敏度,可实现对待检人员的唾液进行毒品检测,从而避免因取尿对客体隐私的侵犯,并可实现在几分钟内进行80个样品的高通量检测。
生物膜干涉技术生物膜干涉技术(bio-1ayerinterferometry,bli)是一种实时、无需标记的快速检测技术,其原理是当生物分子结合到传感器表面形成一层生物膜层,该生物膜层对透过传感器的光的波形造成干涉现象。干涉现象以相位移动的方式被检测,可以检测结合到传感器分子数量的变化。bli技术已经成功应用于蛋白质分子间相互作用的检测,在小分子检测领域也有进一步研究。
技术实现要素:
本发明的目的是提供一种快速、高通量的检测待检人员唾液中安非他命含量的技术。所述检测方法取样方便,操作简单,检测快速,灵敏度高,在批量样品检测场合具有重要的应用价值。
本发明的目的由以下技术方案实现:
一种基于生物膜干涉技术的安非他命检测方法,包括如下步骤:
步骤(1):胶体金的制备。避光条件下,取一定体积的超纯水于磁力搅拌器上加热至80-90℃,按100:2的体积比加入氯金酸溶液继续加热至沸腾,再快速加入2%体积的柠檬酸三钠溶液,保持沸腾反应10min后,冷却至室温后,采用分光光度计检测520-530nm处的吸光度;
所述的氯金酸溶液的质量分数为1%;柠檬酸三钠溶液的质量分数为1%;
所述的胶体金的粒径为30-40nm左右,在525nm波长下有最大吸光度值;
步骤(2):金标抗体的制备。取一定体积的胶体金溶液,用碳酸钾溶液调节ph至7.2-7.4,室温搅拌10-20min;按100:1-2的体积比加入1mg/ml的安非他命单克隆抗体,室温搅拌20-30min;加入质量分数为10%的bsa溶液使其终浓度为1%;室温搅拌20-30min;4-8℃,12000rpm离心20-30min;弃上清液,留沉淀;沉淀用等体积的pbs缓冲液溶解,得到安非他命金标抗体溶液;
所述的碳酸钾溶液浓度为0.2m;安非他命单克隆抗体为购买的鼠源单克隆抗体;bsa(牛血清白蛋白)溶液封闭抗体未结合的位置;pbs缓冲液的ph为7.4;
步骤(3):光纤生物传感器的制备。将aps光纤传感器的检测端没入安非他命-bsa溶液中,室温静置20-30min;再将aps光纤生物传感器没入质量含量为10%的bsa溶液中,室温静置20-30min;再将光纤生物传感器没入蔗糖溶液中,室温静置20-30min;室温晾干,置于2~8℃干燥保存;
所述的aps光纤传感器是用无水乙醇配置的0.5-2m的aps(aminopropyls-ilane,氨基丙基硅烷)浸泡普通空白光纤传感器的检测端12小时并干燥后制得的,处理后的光纤探头表面能通过蛋白的氨基固定蛋白分子;
安非他命-bsa为安非他命完全抗原,即在bsa表面偶联了安非他命分子,可购买获得;安非他命-bsa溶液浓度为50-100μg/ml;
蔗糖溶液浓度为15%(质量含量);
步骤(4):待测样品准备。用棉签沾取待检人员下牙床内的唾液后,将棉签插入含有0.5-1ml溶液的ep管中并旋转混匀后弃掉棉签;ep管内的溶液待用;
所述的棉签为医用一次性棉签,ep管内的溶液为步骤(2)制得的安非他命金标抗体溶液,ep管内的溶液作为后续检测的样品;
步骤(5):标准曲线的制作。采用fortebiooctetred生物分子相互作用仪对梯度标准品溶液进行检测,绘制标准曲线;具体过程为①8个步骤(3)制备的光纤传感器没入pbs缓冲液中30-100s进行平衡,②平衡后的8个光纤传感器分别没入0ng/ml、1ng/ml、10ng/ml、50ng/ml、100ng/ml、200ng/ml、500ng/ml、1000ng/ml的安非他命标准品溶液中60-100s进行梯度标准品的检测,根据检测结果,绘制标准曲线,再对标准品浓度做10为底的对数转换,得出标准品浓度和检测信号之间的函数关系,③梯度标准品检测后的8个光纤传感器没入甘氨酸-盐酸缓冲液中30-100s进行再生,④再生后的光纤传感器再没入pbs缓冲液中30-100s进行平衡;
所述的具体过程可通过操作软件设置后仪器自动操作进行;甘氨酸-盐酸缓冲液的ph为1.5-2;光纤传感器经过再生后可重复使用;
步骤(6):样品检测。采用fortebiooctetred生物分子相互作用仪对步骤(4)的样品进行检测;检测过程为①步骤(5)平衡后的光纤传感器没入步骤(4)的样品中60-100s进行检测,②检测后的光纤传感器没入甘氨酸-盐酸缓冲液中30-100s进行再生,③再生后的光纤传感器再没入pbs缓冲液中30-100s进行平衡;将检测结果代入步骤(5)的函数中,即可求得样品中安非他命的浓度;
本发明的有益效果:
(1)本发明所述方法取样方便,避免检测人员在尿液取样中的不便和对待测人员隐私的侵犯。
(2)本发明所述方法检测时间短,整个检测过程仅需5min左右,且检测灵敏度最低可达到10ng/ml。
(3)本发明所述方法可同时进行批量样本的检测,最多一次可进行80个样品的检测,而整个时间仅有30min,实现高通量样品快速检测。
(4)本发明所述方法中的光纤传感器可通过再生过程重复使用,大大降低的检测的成本。
附图说明
图1为制备的胶体金的吸光度检测结果。
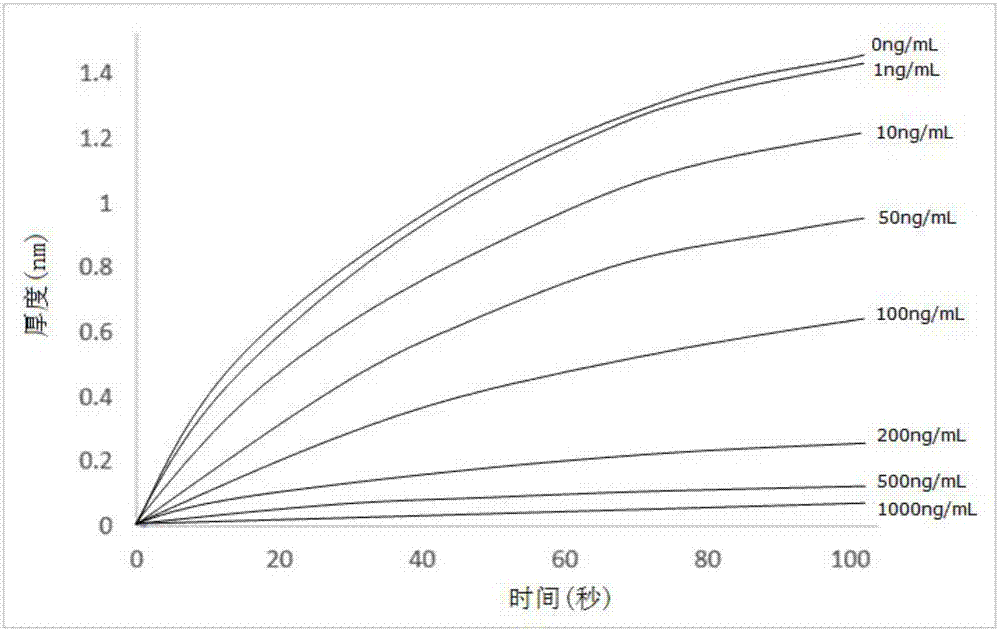
图2为8个梯度标准品的检测结果。
图3为8个梯度标准品的标准曲线。
具体实施方式
下面结合实施例和附图来详述本发明,但不限于此。
以下实施例中提到的主要试剂信息见表1;主要仪器与设备信息见表2。
表1
表2
实施例1:
(1)取100ml超纯水于磁力搅拌器上加热至90℃,加入2ml的1%氯金酸溶液继续加热至沸腾,再快速加入2ml的1%的柠檬酸三钠溶液,保持沸腾反应10min后,冷却至室温后,采用分光光度计检测,制备的胶体金的吸光度如图1所示,其λmax在525nm处,表明制备的胶体金的直径在40nm左右;
(2)取胶体金溶液100ml,用碳酸钾溶液调节ph至7.2,室温搅拌10min;加入1mg安非他命单克隆抗体,室温搅拌20min;加入2mlbsa溶液封闭抗体,室温搅拌20min;4℃,12000rpm离心20min;弃上清液,留沉淀;沉淀用100ml的ph=7.4的pbs缓冲液溶解,得到安非他命金标抗体溶液;
(3)将光纤探头浸泡用无水乙醇配置的0.5m的aps溶液中12小时后干燥获得aps光纤传感器;将其末端没入50μg/ml安非他命-bsa溶液中,室温静置20min;再将光纤生物传感器没入10%的bsa溶液中,室温静置20min;再将光纤生物传感器没入15%蔗糖溶液中,室温静置20min;室温晾干,置于4℃干燥保存;
(4)用医用一次性棉签沾取1-8号待检人员的下牙床内的唾液后,将棉签插入含有0.5ml安非他命金标抗体溶液的1.5ml的ep管中并旋转混匀后弃掉棉签;ep管内的溶液作为后续检测的样品;
(5)采用fortebiooctetred生物分子相互作用仪对梯度标准品溶液进行检测,绘制标准曲线;具体过程为①将上述制备好的8个光纤传感器没入pbs缓冲液中30s进行平衡,②平衡后的8个光纤传感器分别没入0ng/ml、1ng/ml、10ng/ml、50ng/ml、100ng/ml、200ng/ml、500ng/ml、1000ng/ml的安非他命标准品溶液中100s进行梯度标准品的检测,检测结果如图2所示,绘制标准曲线如图3所示,再对标准品浓度做10为底的对数转换,得出标准品浓度和检测信号之间的函数关系,③梯度标准品检测后的8个光纤传感器没入ph=1.5的甘氨酸-盐酸缓冲液中30s进行再生,④再生后的光纤传感器再没入ph=7.4的pbs缓冲液中30s进行平衡;
(6)采用fortebiooctetred生物分子相互作用仪上述待测样品进行检测;检测过程为①将上述平衡后的光纤传感器分别没入1-8号待检样品中100s进行检测,②检测后的光纤传感器没入ph=1.5的甘氨酸-盐酸缓冲液中30s进行再生,③再生后的光纤传感器再没入ph=7.4的pbs缓冲液中30s进行平衡;将检测结果代入步骤(5)的函数中,求得1-8号样品中安非他命的含量分别为202.31ng/ml,178.41ng/ml,>1000ng/ml,<10ng/ml,567.15ng/ml,10.53ng/ml,40.67ng/ml,369.55ng/ml;
(7)验证本实施例检测结果的真实性:以气相色谱-质谱联用技术(gc/ms)和固相萃取技术(spe)相结合测得待检人员1-8号唾液中的安非他命含量分别为231.41ng/ml,186.23ng/ml,1210.72ng/ml,1.22ng/ml,591.21ng/ml,12.11ng/ml,45.23ng/ml,381.41ng/ml,与本发明测得的结果一致。
实施例2:
(1)取100ml超纯水于磁力搅拌器上加热至90℃,加入2ml的1%氯金酸溶液继续加热至沸腾,再快速加入2ml的1%的柠檬酸三钠溶液,保持沸腾反应10min后,冷却至室温后,采用分光光度计检测,制备的胶体金的吸光度如图1所示,其λmax在525nm处,表明制备的胶体金的直径在40nm左右;
(2)取胶体金溶液100ml,用碳酸钾溶液调节ph至7.4,室温搅拌10min;加入1mg安非他命单克隆抗体,室温搅拌30min;加入2mlbsa溶液封闭抗体,室温搅拌30min;4℃,12000rpm离心30min;弃上清液,留沉淀;沉淀用100ml的ph=7.4的pbs缓冲液溶解,得到安非他命金标抗体溶液;
(3)将光纤探头浸泡用无水乙醇配置的0.5m的aps溶液中12小时后干燥获得aps光纤传感器;将其末端没入100μg/ml安非他命-bsa溶液中,室温静置30min;再将光纤生物传感器没入10%的bsa溶液中,室温静置30min;再将光纤生物传感器没入15%蔗糖溶液中,室温静置30min;室温晾干,置于4℃干燥保存;
(4)用医用一次性棉签沾取1-8号待检人员的下牙床内的唾液后,将棉签插入含有0.5ml安非他命金标抗体的1.5ml的ep管中并旋转混匀后弃掉棉签;ep管内的溶液作为后续检测的样品;
(5)采用fortebiooctetred生物分子相互作用仪对梯度标准品溶液进行检测,绘制标准曲线;具体过程为①将上述制备好的8个光纤传感器没入pbs缓冲液中60s进行平衡,②平衡后的8个光纤传感器分别没入0ng/ml、1ng/ml、10ng/ml、50ng/ml、100ng/ml、200ng/ml、500ng/ml、1000ng/ml的安非他命标准品溶液中60s进行梯度标准品的检测,检测结果如图2所示,绘制标准曲线如图3所示,再对标准品浓度做10为底的对数转换,得出标准品浓度和检测信号之间的函数关系③梯度标准品检测后的8个光纤传感器没入ph=1.5的甘氨酸-盐酸缓冲液中60s进行再生,④再生后的光纤传感器再没入ph=7.4的pbs缓冲液中60s进行平衡;
(6)采用fortebiooctetred生物分子相互作用仪上述待测样品进行检测;检测过程为①将上述平衡后的光纤传感器分别没入1-8号待检样品中60s进行检测,②检测后的光纤传感器没入ph=1.5的甘氨酸-盐酸缓冲液中60s进行再生,③再生后的光纤传感器再没入ph=7.4的pbs缓冲液中60s进行平衡;将检测结果代入步骤(5)的函数中,求得1-8号样品中安非他命的含量分别为252.15ng/ml,193.32ng/ml,>1000ng/ml,<10ng/ml,601.24ng/ml,14.21ng/ml,50.41ng/ml,396.47ng/ml;
(7)验证本实施例检测结果的真实性:以气相色谱-质谱联用技术(gc/ms)和固相萃取技术(spe)相结合测得待检人员1-8号唾液中的安非他命含量分别为231.41ng/ml,186.23ng/ml,1210.72ng/ml,1.22ng/ml,591.21ng/ml,12.11ng/ml,45.23ng/ml,381.41ng/ml,与本发明测得的结果一致。
实施例3:
(1)取100ml超纯水于磁力搅拌器上加热至90℃,加入2ml的1%氯金酸溶液继续加热至沸腾,再快速加入2ml的1%的柠檬酸三钠溶液,保持沸腾反应10min后,冷却至室温后,采用分光光度计检测,制备的胶体金的吸光度如图1所示,其λmax在525nm处,表明制备的胶体金的直径在40nm左右;
(2)取胶体金溶液100ml,用碳酸钾溶液调节ph至7.4,室温搅拌15min;加入1.5mg安非他命单克隆抗体,室温搅拌25min;加入1.5mlbsa溶液封闭抗体,室温搅拌25min;4℃,12000rpm离心25min;弃上清液,留沉淀;沉淀用100ml的ph=7.4的pbs缓冲液溶解,得到安非他命金标抗体溶液;
(3)将光纤探头浸泡用无水乙醇配置的0.5m的aps溶液中12小时后干燥获得aps光纤传感器;将其末端没入75μg/ml安非他命-bsa溶液中,室温静置25min;再将光纤生物传感器没入10%的bsa溶液中,室温静置25min;再将光纤生物传感器没入15%蔗糖溶液中,室温静置25min;室温晾干,置于4℃干燥保存;
(4)用医用一次性棉签沾取1-8号待检人员的下牙床内的唾液后,将棉签插入含有0.5ml安非他命金标抗体的1.5ml的ep管中并旋转混匀后弃掉棉签;ep管内的溶液作为后续检测的样品;
(5)采用fortebiooctetred生物分子相互作用仪对梯度标准品溶液进行检测,绘制标准曲线;具体过程为①将上述制备好的8个光纤传感器没入pbs缓冲液中100s进行平衡,②平衡后的8个光纤传感器分别没入0ng/ml、1ng/ml、10ng/ml、50ng/ml、100ng/ml、200ng/ml、500ng/ml、1000ng/ml的安非他命标准品溶液中100s进行梯度标准品的检测,检测结果如图2所示,绘制标准曲线如图3所示,再对标准品浓度做10为底的对数转换,得出标准品浓度和检测信号之间的函数关系,③梯度标准品检测后的8个光纤传感器没入ph=1.5的甘氨酸-盐酸缓冲液中100s进行再生,④再生后的光纤传感器再没入ph=7.4的pbs缓冲液中100s进行平衡;
(6)采用fortebiooctetred生物分子相互作用仪上述待测样品进行检测;检测过程为①将上述平衡后的光纤传感器分别没入1-8号待检样品中100s进行检测,②检测后的光纤传感器没入ph=1.5的甘氨酸-盐酸缓冲液中100s进行再生,③再生后的光纤传感器再没入ph=7.4的pbs缓冲液中100s进行平衡;将检测结果代入步骤(5)的函数中,求得1-8号样品中安非他命的含量分别为236.61ng/ml,195.61ng/ml,>1000ng/ml,<10ng/ml,581.31ng/ml,13.78ng/ml,42.92ng/ml,387.63ng/ml;
(7)验证本实施例检测结果的真实性:以气相色谱-质谱联用技术(gc/ms)和固相萃取技术(spe)相结合测得待检人员1-8号唾液中的安非他命含量分别为231.41ng/ml,186.23ng/ml,1210.72ng/ml,1.22ng/ml,591.21ng/ml,12.11ng/ml,45.23ng/ml,381.41ng/ml,与本发明测得的结果一致。
- 还没有人留言评论。精彩留言会获得点赞!