HPLC‑ELSD同时测定鲜冬虫夏草中4种甾醇含量的方法及应用与流程
本发明属于中药材中特定成分的定量分析检测方法领域,具体涉及一种利用hplc-elsd同时测定冬虫夏草中4种甾醇含量的方法,及其该方法在鉴别冬虫夏草真伪品中的应用。
背景技术:
冬虫夏草是麦角菌科真菌cordycepssinensis(berk.)sacc.寄生在蝙蝠蛾科昆虫幼虫上的子座和幼虫尸体的复合体。具有补肺益肾、秘精益气等功效,主治久咳虚喘、唠咳咯血、阳痿遗精、腰膝酸软,是我国传统的名贵中药材。现代药理学研究表明,冬虫夏草对人体免疫系统、循环系统、心血管系统等都是有益的。但野生冬虫夏草主产于我国青海、四川、西藏、云南等省的高寒高原草甸,生长环境特殊,野生资源有限。
近年来随着人民生活水平的提高和保健养生意识的增强,消费者对冬虫夏草的需求越来越大,造成冬虫夏草市场供不应求。目前市场上冬虫夏草产品品质参差不齐,各种伪品和虚假宣传层出不穷。最为常见的冬虫夏草伪品是其它虫草属真菌或寄生在其它昆虫体上所形成的复合体,如虫草属的亚香棒虫草、垂头虫草、蛹虫草、蝉花等。另外,以冬虫夏草为主要原材料生产的产品也应运而生。例如从新鲜冬虫夏草中分离得到菌种,采用液体发酵培养法来生产的虫草菌丝体因其产量高、价格低,已成为野生冬虫夏草的主要替代产品。但发酵虫草产品不论是在物质基础和药理活性上,与冬虫夏草均有所不同。面对市场上种类繁多的冬虫夏草产品,无论是野生冬虫夏草、冬虫夏草繁育品或者发酵冬虫夏草产品,都没有一个统一的鉴别标准,因此,开发出一种能有效鉴别冬虫夏草真伪的方法对冬虫夏草的质量评价及安全合理地使用具有重要意义。
文献《advanceddevelopmentinchemicalanalysisofcordyceps》(《journalofpharmaceutical&biomedicalanalysis》,2014,87(1434):271)报道了冬虫夏草含有多种活性成分,包括核苷、多糖、蛋白、多肽、甾醇、脂肪酸和挥发性成分。同时,目前对冬虫夏草真伪品的鉴别除了通过显微、性状、基因鉴别外,一般通过理化性质鉴别,如文献《冬虫夏草核磁特征指纹图谱建立及鉴别研究》(《世界科学技术-中医药现代化》,2014,16(11))、《冬虫夏草及其混淆品hplc指纹图谱研究及共有成分鉴定》(《中草药》,2017,48(5):991-996),但目前对冬虫夏草中的特征性成分甾醇类活性物质研究相对较少,仅有几篇文献报道采用高效液相色谱法-紫外检测器(hplc-uv)或hplc-uv-ms、gc-ms测定冬虫夏草中麦角甾醇含量,对冬虫夏草中4种甾醇同时进行定量分析鲜见报道。如文献《冬虫夏草化学成分分析》(《菌物学报》,2016,35(4):476-490)中报道采用bstfa/tms法对样品进行衍生化,虽使用gc-ms鉴定出了7种甾醇类物质,但样品需要衍生化导致样品处理过程复杂,所用试剂毒性较大,耗时长。文献《高效液相色谱法测定人工虫草中麦角甾醇的含量》(《山西医科大学学报》,2016,37(4):661-662)中报道样品采用饱和koh溶液和无水乙醇皂化之后,用环己烷提取3次,提取液用分配柱和吸附柱净化和浓缩提取液,最后使用hplc-uv分离测定麦角甾醇的量,该文献的样品处理过程复杂、耗时,且仅仅是通过hplc-uv测定了人工虫草中的麦角甾醇的含量;同样,文献《冬虫夏草(cordycepssinensis)菌丝体固体发酵粉中麦角甾醇的定量分析》(《沈阳师范大学学报》,2005,23(3):293-296)也是采用类似的方法制备样品,结果也是仅对麦角甾醇进行定量分析,且若测定冬虫夏草中胆甾醇、谷甾醇等甾醇类末端吸收物质,采用hplc-uv检测存在基线漂移不稳、响应值小、灵敏度低、重复性差等缺点。
技术实现要素:
目前未见采用hplc-elsd技术对冬虫夏草中4种甾醇物质同时进行测定的报道。因此,本发明的目的是提供一种hplc-elsd分析方法,同时测定冬虫夏草中4种甾醇类物质的含量。本发明提供的样品处理方法简单、耗时少,且提供的hplc-elsd分析检测方法所需要的分离时间短,结果稳定性好、方法可靠,可为冬虫夏草质量控制提供参考。
一方面,本发明提供了一种利用hplc-elsd同时测定冬虫夏草中4种甾醇含量的方法,其中,所述的4种甾醇分别为麦角甾醇、胆甾醇、豆甾醇和谷甾醇;
所述方法包括以下步骤:
(1)供试品溶液制备:取冬虫夏草样品,加入氢氧化钾-乙醇溶液进行回流提取;随后离心,得上清液;之后过滤,得到供试样品溶液;
(2)对照品溶液制备:取对照品麦角甾醇、胆甾醇、豆甾醇和谷甾醇,置于容量瓶中混合均匀,加入氢氧化钾-乙醇充分溶解并定容至刻度线,制成混合对照品溶液;
(3)hplc-elsd检测:检测条件:色谱柱为c18(4.6×250mm,5μm);流动相a为水,流动相b为甲酸-甲醇溶液;梯度洗脱:0-10min,3%-0%a;10-30min,0%a;30-35min,0%-3%a;将所述步骤(1)和步骤(2)所得的供试样品溶液和对照品溶液分别注入hplc-elsd联用仪,进行检测。
优选地,本发明在步骤(1)所述的供试品溶液的制备方法为:
精密称取冬虫夏草样品,按照重量体积比加入1:5-20g/ml的0.5mol/l氢氧化钾-乙醇溶液进行回流提取,提取时间为15-40min;随后离心,得上清液;之后经滤膜过滤,得到供试样品溶液。
优选地,所述流动相b为0.005%-0.2%甲酸-甲醇溶液。
进一步优选地,本发明中所述的流动相b为0.005%甲酸-甲醇溶液。
优选地,本发明在步骤(2)中所述对照品溶液的制备方法为:
精密称取标准品麦角甾醇、胆甾醇、豆甾醇和谷甾醇各20mg,置于100ml容量瓶中混合均匀,加入0.5mol/l氢氧化钾-乙醇充分溶解后制成混合对照品溶液。
进一步优选地,本发明在步骤(1)中所述供试品溶液的制备方法为:
精密称取样品粉末0.5g,按重量体积比加入10ml0.5mol/l氢氧化钾-乙醇溶液,回流30min,离心,得上清液;之后经过滤,得到供试样品溶液。
优选地,本发明所述的方法,步骤(3)中hplc-elsd检测的条件为:色谱柱:watersxbridgec18(4.6×250mm,5μm);流动相a为水,流动相b为0.005%甲酸-甲醇溶液;柱温30℃,流速1.0ml/min,梯度洗脱:0-10min,3%-0%a;10-30min,0%a;30-35min,0%-3%a;gain:6;漂移管温度:35℃。
另一方面,本发明所提供的方法可用于鉴别虫草类中药材是否为正品的冬虫夏草。
与现有技术相比,本发明的有益效果是:
(1)本发明首次采用hplc-elsd同时测定冬虫夏草中的4种甾醇类物质,且分离检测所需要的时间短,可在18min实现分离,且分离效果好、结果稳定、可靠,可为冬虫夏草的质量控制提供了参考。
(2)本发明所提供的检测甾醇类物质的方法简单,且首次对4种甾醇进行定量分析。制备样品过程耗时少,所用试剂安全。
(3)本发明首次通过冬虫夏草中甾醇类物质对虫草类中药材进行了直观的真伪鉴别,可为虫草类中药材的质量控制提供参考。
附图说明
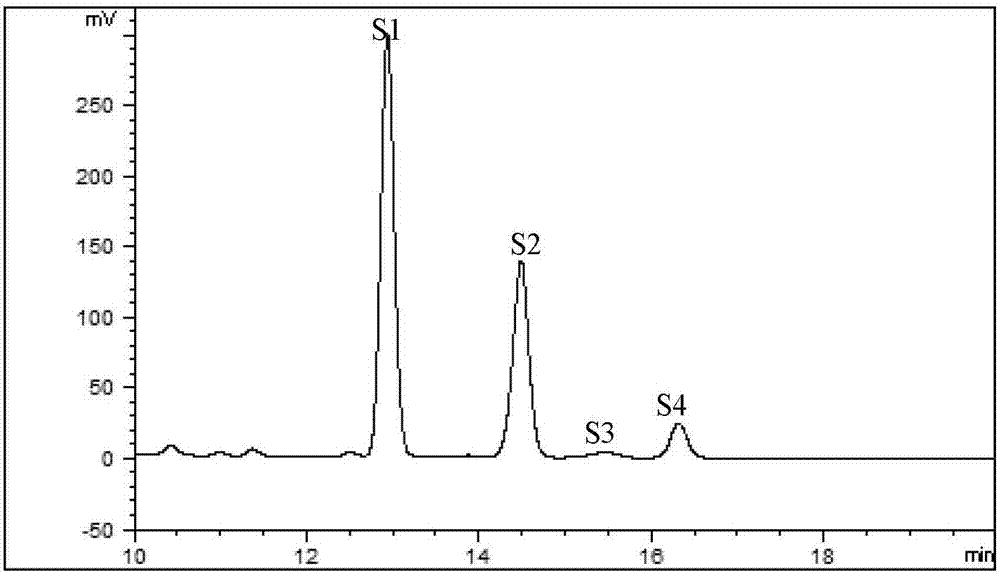
图1为混合对照品的hplc-elsd色谱图。(s1为麦角甾醇,s2为胆甾醇,s3为豆甾醇,s4为谷甾醇)。
图2为a1野生冬虫夏草hplc-elsd色谱图。
图3为a6鲜冬虫夏草hplc-elsd色谱图。
图4为a7冬虫夏草繁育品hplc-elsd色谱图。
图5为a13蝉花hplc-elsd色谱图。
图6为a14百令胶囊hplc-elsd色谱图。
图7为冬虫夏草(野生冬虫夏草和冬虫夏草繁育品)、冬虫夏草伪制品、百令胶囊和金水宝胶囊聚类分析结果图。
具体实施方式
以下提供本发明的具体实施方式,结合附图和实施例对本发明做进一步说明,给出的实施例仅为了阐述本发明,而非以任何方式限制本发明的范围。
1、样品列表
表1实验样品列表
注:本发明所指的冬虫夏草繁育品为鲜冬虫夏草冻干样品;冬虫夏草伪制品包括a10、a11、a12、a13样品。
2、样品前处理
①鲜冬虫夏草:取新鲜采收的鲜冬虫夏草,剪碎,用球磨仪将其粉碎。
②野生冬虫夏草、冬虫夏草繁育品、冬虫夏草伪制品、百令胶囊和金水宝胶囊:分别取野生冬虫夏草、冻干后的鲜冬虫夏草即冬虫夏草繁育品、冬虫夏草伪制品各10根,剪碎,于球磨罐中,用球磨仪将其粉碎,使粉末过3号筛,即可;百令胶囊和金水宝胶囊可直接过3号筛。
实施例1方法学考察
1.1仪器
高效液相色谱仪;蒸发光散射仪。
1.2溶液制备
1.2.1对照品溶液制备
称取麦角甾醇、胆甾醇、豆甾醇和谷甾醇各20.0mg,精密称定,置于100ml容量瓶中,加入0.5mol/l氢氧化钾-乙醇溶液充分溶解并定容至刻度线,即可。
1.2.2样品的制备:取冬虫夏草样品(a7)0.5g,加入10ml0.5mol/l氢氧化钾-乙醇溶液进行提取,在85℃下回流30min,离心,得上清液,经滤膜过滤,得到供试样品溶液。
1.3高效液相-蒸发光散射分析条件
色谱柱:watersxbridgec18(4.6×250mm,5μm);流动相a为水,流动相b为0.005%甲酸-甲醇溶液;进样体积为25μl,柱温30℃,流速1.0ml/min,梯度洗脱;洗脱梯度为0-10min,3%-0%a;10-30min,0%a;30-35min,0%-3%a;gain:6;漂移管温度:35℃。
1.4精密度考察
精密吸取“1.2.1”项下的混合对照品溶液,按“1.3”色谱条件下重复进样6针,进样体积为25μl,以对照品峰面积进行计算,麦角甾醇、胆甾醇、豆甾醇和谷甾醇峰面积的rsd值分别为3.19%、3.01%、2.53%、3.25%。结果表明本发明方法精密度高。
1.5重复性实验
取同一批次冬虫夏草a7样品0.5g,平行测定6份,按“1.2.2”项下方法操作,制备冬虫夏草溶液6份,每份精密吸取25μl,按“1.3”项下色谱条件操作,分别测得麦角甾醇、胆甾醇、豆甾醇和谷甾醇含量的rsd值分别为3.53%、2.99%、2.60%和3.27%。结果表明本发明方法重复性好。
1.6稳定性实验
取一份“1.2.2”项下的冬虫夏草供试品a7溶液,按“1.3”项下色谱条件操作,分别在0、2、4、6、8、12h进样,计算麦角甾醇、胆甾醇、豆甾醇和谷甾醇的含量,各物质含量的rsd分别为2.13%、3.30%、3.93%和3.08%。结果表明本方法稳定性好。
1.7标准曲线、定量限
取“1.2.1”项下含有4种甾醇的混合对照品溶液,以0.5mol/l氢氧化钾乙醇溶液稀释配成系列浓度梯度,每个浓度分别平行进样25μl,按“1.3”项下的色谱条件测定,计算峰面积,以峰面积对数值(y)为纵坐标,溶液质量对数值(x)为横坐标进行回归计算,得回归方程、相关系数与线性关系(表2)。取混合对照品溶液进行逐级稀释,进样分析,以信噪比(s/n)约为10时相应浓度确定最低定量限。结果表明在相应的线性范围内呈良好的线性关系。
表2回归方程、定量限、检测限
1.8加样回收试验
精密称定冬虫夏草a7样品6份,每份0.25g,分别准确加入4种甾醇对照品:麦角甾醇0.90mg,胆甾醇0.31mg,豆甾醇0.069mg,谷甾醇0.088mg。按“1.2.2”项下操作制备供试品溶液,按“1.3”项色谱条件测定各化合物的含量。计算各化合物的平均回收率。麦角甾醇、胆甾醇、豆甾醇和谷甾醇的平均回收率分别为100.6%、100.3%、101.4%、100.9%。
1.9样品测定
取收集的a1、a2、a3、a7、a8、a9冬虫夏草样品,分别称粉末约0.5g,精密称定,按“1.2.2”项下方法操作,制备冬虫夏草供试品溶液,按“1.3”项下色谱条件进行测定,并计算样品中4种甾醇成分的含量(见表3),对照品、野生冬虫夏草(a1)和冬虫夏草繁育品(a7)见图1、图2和图4。
表3冬虫夏草各甾醇含量
实施例2鲜冬虫夏草的hplc-elsd色谱图
2.1鲜冬虫夏草样品的制备
精密称取鲜冬虫夏草(a4、a5、a6)1.5g,加入10ml0.5mol/l氢氧化钾-乙醇溶液进行提取,在85℃下回流30min,离心,得上清液,经滤膜过滤,得到供试样品溶液。
2.2高效液相-蒸发光散射(hplc-elsd)分析条件:与实施例一“1.3”项下相同。
2.3数据处理和分析
将各供试样品溶液分别注入hplc-elsd联用仪,进行检测。各样本色谱图的保留时间和积分由工作站自动完成,以对照品出峰位置为参照,鉴定鲜冬虫夏草中麦角甾醇、胆甾醇、豆甾醇和谷甾醇各色谱峰,以干燥品计,各甾醇的含量(见表4),其中图3为鲜冬虫夏草a6的色谱图。
表4鲜冬虫夏草各甾醇含量
实施例3hplc-elsd检测方法的应用
3.1供试品溶液制备
精密称取冬虫夏草(野生冬虫夏草a1-a3、冬虫夏草繁育品a7-a9)、冬虫夏草伪制品(a10-a13)、百令胶囊(a14)和金水宝胶囊(a15)样品粉末各0.5g,分别置于50ml的玻璃瓶内,加入0.5mol/l氢氧化钾-乙醇溶液10ml,85℃回流30min。离心,得上清液。经滤膜过滤,得到供试样品溶液。
3.2高效液相-蒸发光散射(hplc-elsd)分析条件:与实施例一“1.3”项下相同。
3.3数据处理和分析
将各供试样品溶液分别注入hplc-elsd联用仪,进行检测。各样本色谱图的保留时间和积分由工作站自动完成,以对照品出峰位置为参照,鉴定冬虫夏草、冬虫夏草伪品和发酵冬虫夏草产品中麦角甾醇、胆甾醇、豆甾醇和谷甾醇各色谱峰,计算各甾醇的含量(见表5)。其中图5为蝉花a13的hplc-elsd色谱图,图6为百令胶囊a14的hplc-elsd色谱图。
表5样品中各甾醇的含量
注:“—a”表示低于定量限,“—b”表示未检出。
3.4聚类分析
将各样品的hplc-elsd数据进行积分处理后,将样品名称、出峰序列号和对应的含量导入spss软件中。点击“分析”、“分类”、“系统聚类”,聚类距离采用欧氏距离法,聚类方法采用ward法,生成聚类分析图(图7)。由图7的聚类分析图可以看出,冬虫夏草(野生和繁育品)与百令胶囊、金水宝胶囊及冬虫夏草伪制品聚成不同类,可以非常直观、方便的加以鉴别。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明构思的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!