注射用醋酸奥曲肽微球含量的测定方法与流程
本发明属于液相色谱检测领域,具体涉及注射用醋酸奥曲肽微球含量的测定方法,本方法来源于注射用醋酸奥曲肽微球进口注册标准,对注射用醋酸奥曲肽微球含量进行测定。
背景技术:
奥曲肽(octreotide)是人工合成的八肽环状化合物,其前端的四个氨基酸与天然的生长抑素十四肽前端结构相似,为生长抑素类似物。奥曲肽微球是奥曲肽的长效制剂。注射用醋酸奥曲肽微球通过臀部肌肉深部注射给药,适应症为肢端肥大症和胃肠胰内分泌肿瘤。
现有的注射用醋酸奥曲肽微球原标准含量测定方法如下:
色谱柱:用以十八烷基硅烷键合硅胶为填充剂的inertsilods-2,4.6×150mm;
流动相a:乙腈-10%四甲基氢氧化铵溶液-水(100:20:880)并用磷酸调节ph值至2.5;
流动相b:乙腈-10%四甲基氢氧化铵溶液-水(400:20:580)并用磷酸调节ph值至2.5;
流动相c:乙腈-10%四甲基氢氧化铵溶液-水(800:20:180)并用磷酸调节ph值至2.5;
流速:1.7ml/分钟;
进样体积:10μl;
检测波长:210nm;
照下表梯度洗脱:
原标准中测定方法较为复杂,推荐使用的色谱柱为日本岛津公司早期研发色谱柱,测定重现性较差、精密度较差,对主成分的洗脱能力较弱、洗脱时间长。
技术实现要素:
本发明的发明人在注射用醋酸奥曲肽微球含量的测定实践中意外发现,采用techmatec18-st色谱柱,将流动相系统由三相改为两相并调整流动相比例后,主成分峰理论板数提高,拖尾因子良好,取得了预留不到的技术效果,本发明就是基于此发现。
本发明的注射用醋酸奥曲肽微球含量测定方法,具体如下:
注射用醋酸奥曲肽微球含量的测定方法,采用液相色谱法,所述液相检测条件为:采用techmatec18-st色谱柱,用流动相a和流动相b等浓度洗脱;所述流动相a和流动相b均为乙腈、10%四甲基氢氧化铵溶液和水的混合液。
优选的,所述techmatec18-st色谱柱的具体型号参数为(4.6×250mm,5μm)。
优选的,所述流动相a的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为50-200:10-30:800-950,并用磷酸调节ph值至2.5;所述流动相b的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为300-500:10-30:500-650,并用磷酸调节ph值至2.5。
优选的,所述流动相a的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为100:20:880;所述流动相b的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为400:20:580。
优选的,所述流动相a与流动相b的体积比例为50:50,流动相流速为1-3ml/分钟。
更进一步优选的,所述流动相流速为1.7ml/分钟。
更进一步优选的,所述色谱柱的柱温为20-35℃。
更进一步优选的,所述色谱柱的柱温为30℃。
更进一步优选的,检测波长为210nm。
更进一步优选的,进样体积为10μl。
本发明的含量测定方法,对主成分的洗脱能力大大提升,方法的专属性、准确度、精密度等均符合最新标准要求。
本发明的有益效果为:
1在原标准的基础上更改色谱柱,选用性能较好的色谱柱对样品进行洗脱,增强了对样品的洗脱能力。
2流动相由原来的三相改为两相,节省资源。流动相体系改动后重现性更好,精密度更好。
3流动相比例调整后,对主成分的洗脱能力大大加强,样品快速洗脱,大大节约时间和物料成本。
附图说明
图1为注射用醋酸奥曲肽微球的原标准含量测定方法的色谱图;
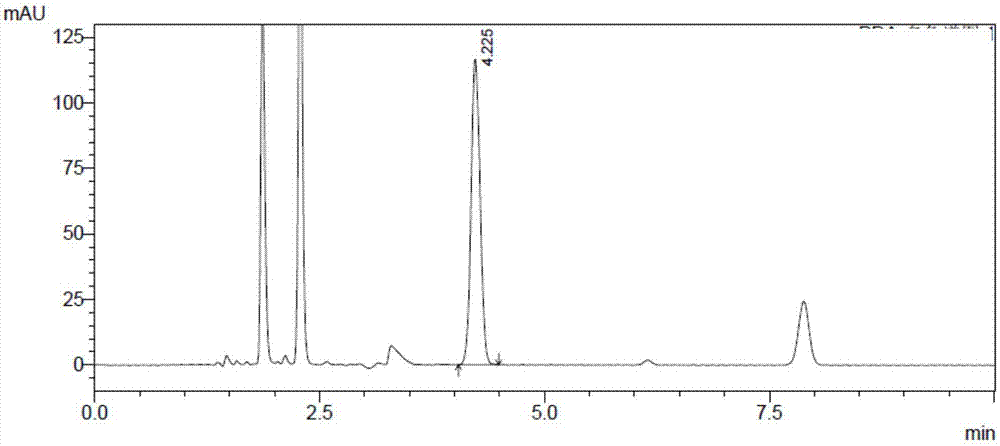
图2为注射用醋酸奥曲肽微球的本发明实施例3的含量测定方法的色谱图。
具体实施方式
为详细说明本发明之技术内容、构造特征、所达成目的及功效,以下兹例举实施例详予说明。
实施例1
注射用醋酸奥曲肽微球含量的测定方法,采用液相色谱法,所述液相检测条件为:采用techmatec18-st色谱柱,用流动相a和流动相b等浓度洗脱;所述流动相a和流动相b均为乙腈、10%四甲基氢氧化铵溶液和水的混合液。
所述techmatec18-st色谱柱的具体型号参数为(4.6×250mm,5μm)。
所述流动相a的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为50:10;800,并用磷酸调节ph值至2.5;所述流动相b的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为300:10:500,并用磷酸调节ph值至2.5。
所述流动相a与流动相b的体积比例为50:50,流动相流速为1ml/分钟。
所述色谱柱的柱温为20℃。
检测波长为210nm。
进样体积为10μl。
实施例2
与实施例1的不同之处在于,所述流动相a的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为200:30:950,并用磷酸调节ph值至2.5;所述流动相b的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为500:30:650,并用磷酸调节ph值至2.5。
流动相流速为3ml/分钟。
所述色谱柱的柱温为35℃。
检测波长为210nm。
进样体积为10μl。
实施例3
与实施例1的不同之处在于,所述流动相a的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为100:20:880;所述流动相b的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为400:20:580。
流动相流速为1.7ml/分钟。
所述色谱柱的柱温为30℃。
检测波长为210nm。
进样体积为10μl。
实施例4
与实施例1的不同之处在于,所述流动相a的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为100:20:880;所述流动相b的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为400:20:580。
流动相流速为1ml/分钟。
所述色谱柱的柱温为30℃。
检测波长为210nm。
进样体积为10μl。
实施例5
与实施例1的不同之处在于,所述流动相a的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为100:20:880;所述流动相b的乙腈:10%四甲基氢氧化铵溶液:水的体积比例为400:20:580。
流动相流速为3ml/分钟。
所述色谱柱的柱温为30℃。
检测波长为210nm。
进样体积为10μl。
实验例1注射用醋酸奥曲肽微球的含量不同测定方法的比较
以实施例1-5的方法对注射用醋酸奥曲肽微球进行含量测定,结果如表1和表2。图1为注射用醋酸奥曲肽微球的原标准含量测定方法的色谱图,图2为注射用醋酸奥曲肽微球的本发明实施例3的含量测定方法的色谱图。
本发明的注射用醋酸奥曲肽微球的本发明的含量测定方法与原标准含量测定方法相比,保留时间、理论板数和拖尾因子都得到了良好改善,
表1本发明三个实施例的注射用醋酸奥曲肽微球的含量测量方法比较
从表1并结合图1看出,实施例1-5中均能较好的分离主成分,其中实施例3为最优。
表2本发明实施例3和原标准的注射用醋酸奥曲肽微球的含量测量方法比较
从表2并结合图1、图2看出,实施例3显著优于原标准含量测量方法。
综上所述,仅为本发明之较佳实施例,不以此限定本发明的保护范围,凡依本发明专利范围及说明书内容所作的等效变化与修饰,皆为本发明专利涵盖的范围之内。
- 还没有人留言评论。精彩留言会获得点赞!