用于EAB生物传感器的硫醇化芳香族阻断结构的制作方法
本申请要求2016年12月13日提交的申请号为62/433,368的美国临时申请的优先权,其全部公开内容在此通过引用并入本文。
背景技术:
尽管汗液在生物感测应用上,特别是通过可穿戴装置而具有许多人体工程学优势,但与血液、尿液和唾液相比,汗液仍然是未充分利用的。与其他非侵入性生物流体进行更密切的比较后,优势甚至可能超出人体工程学:汗液可能提供卓越的分析物信息。汗液中含有许多存在于血液和间质液中的相同的分析物和分析物浓聚物。
然而,在历史上,许多难题使汗液一直不能在优选的临床生物流体中占据一席之地。这些难题包括样品体积非常小(nL至μL)、由于蒸发而导致浓聚物未知、大分析物被过滤和稀释、新旧汗液混合、以及被皮肤表面污染的可能性。最近,可穿戴汗液取样和感测装置的快速发展已经解决了几个历史难题。然而,这种最近的进展也限于在例如运动应用中发现的高出汗率(>1纳升/分钟/腺体)下取样的高浓度分析物(μM至mM)。随着汗液生物感测向检测低浓度大分析物(nM至pM和更低)发展,进展将变得更具挑战性。
特别地,许多用于检测较大分子的已知传感器技术不适合用于需要允许在佩戴者皮肤上连续使用的传感器的可穿戴汗液感测。这意味着需要复杂的微流体操作、添加试剂、使用货架期限有限的组成部分(例如抗体)、或设计用于一次性使用的传感器的传感器样式不适合于进行汗液感测。相比之下,基于适体的电化学(“EAB”)传感器技术(例如美国专利号7,803,542和8,003,374中公开的多捕获EAB传感器)提供了稳定可靠的生物电传感器,该生物电传感器对汗液中的靶标分析物敏感。类似地,2017年6月23日提交的申请号为62/523,835的美国临时申请(其全部内容通过引用并入本文)提出了也用于所公开的发明的对接适体EAB传感器。
在汗液感测装置中使用EAB传感器的一个困难是当暴露于汗液介质时EAB感测元件的长期稳定性相对较差。这种不稳定性的一个原因是硫醇盐键(例如通常用于将适体感测元件和阻断剂基团附接到金电极上)降解的趋势,特别是在存在询问电流的情况下。因此,如本文所公开的,提供了一种解决方案,该方案改善了电极与附接的适体感测元件和阻断剂基团之间的硫醇盐键的稳定性。
技术实现要素:
本发明提供了配置用于基于适体的电化学生物传感器的自组装单层(SAM),该基于适体的电化学生物传感器允许感测装置检测生物流体样品中的浓度非常低的靶标分析物。所公开的发明的实施方式包括SAM,该SAM通过在传感器电极与公开的阻断剂基团之间或在传感器电极与经公开的结合剂分子的适体感测元件之间的持久硫醇盐键而在汗液中具有改善的长期稳定性。本发明的实施方式还包括阻断剂基团,该阻断剂基团被配置为在传感器电极上形成密集堆积且持久的SAM。
附图说明
根据以下详细描述和附图,将进一步理解本发明的目的和优点,其中:
图1表示先前公开的EAB传感器的适体感测元件。
图2描绘了用于所公开的发明的实施方式的分子。
图3描绘了所公开的发明的实施方式。
图4描绘了与所公开的发明的实施方式有关的化学反应。
图5描绘了与所公开的发明的实施方式有关的化学反应。
图6A和6B描绘了用于所公开的发明的实施方式的示例性合成反应。
图7描绘了用于所公开的发明的实施方式的示例性分子。
图8描绘了用于所公开的发明的实施方式的示例性分子。
图9描绘了用于所公开的发明的实施方式的示例性分子。
图10描绘了用于所公开的发明的实施方式的示例性分子。
图11描绘了用于所公开的发明的实施方式的示例性分子。
图12描绘了用于所公开的发明的实施方式的示例性分子。
图13A、13B和13C描绘了用于所公开的发明的实施方式的示例性分子。
定义
如本文所用,“汗液”是指主要是汗液(例如外分泌腺汗液或顶浆分泌腺汗液)的生物流体,并且还可以包括生物流体(例如汗液和血液、或汗液和间质液)的混合物,只要生物流体混合物的平流运输(例如,流动)主要由汗液驱动。
如本文所用,“生物流体”可以指人类任何生物流体,包括但不限于汗液、间质液、血液、血浆、血清、泪液和唾液。对于如本文一般讨论的汗液感测应用,生物流体的含义较窄,即,在从皮肤排出时主要由间质液或汗液组成的流体。
“连续监测”是指装置提供至少一次汗液测量或者提供随时间而变化的多次汗液测量的能力,该至少一次汗液测量通过连续或多次收集并且感测该测量来确定。
“时间顺序保证”是指在可以对从身体排出的新汗液分析物进行测量的速率方面确保对汗液中的分析物的测量的取样速率或取样间隔。时间顺序保证还可包括确定传感器功能、潜在的被先前产生的分析物污染、潜在的被其他流体污染、或潜在的被其他测量污染源污染对测量的影响。时间顺序保证可以抵消体内的时间延迟(例如,众所周知,分析物在血液中出现与在间质液中出现之间存在5到30分钟的滞后时间),但得到的取样间隔(下文定义)与滞后时间无关,此外,这个滞后时间为在体内的,因此,对于上文定义并且在此解释的时间顺序保证,该滞后时间不适用。
“汗液刺激”是任何外部刺激直接或间接导致产生汗液,施加的外部刺激用来刺激汗液。汗液刺激的一个实例是施用汗液刺激物,例如毛果芸香碱或卡巴胆碱。如果正慢跑对象是为了刺激汗液而慢跑,则进行刺激汗液的慢跑是唯一的汗液刺激。
“汗液产生率”是汗腺本身产生汗液的速率。汗液产生率通常通过来自每个腺体的流速(纳升/分钟/腺体)来测量。然后,在某些情况下,将测量结果乘以进行了汗液取样的汗腺的数量。
“测得的”可以意味着精准或精确的定量测量,并且可以包括更广泛的含义,例如,测量某物的相对变化量。测得的也可以暗示二元测量,例如“是”或“否”类型测量。
“分析物”是指由汗液感测装置测量的物质、分子、离子或其他物质。
“EAB传感器”是指配置有多个适体感测元件的基于适体的电化学生物传感器,在流体样品中存在靶标分析物的情况下,该生物传感器产生表明分析物捕获的信号,并且该信号可以被添加到其它这样的感测元件的信号中,使得可以达到表明靶标分析物存在的信号阈值。这种传感器可以是专利号为7,803,542和8,003,374的美国专利(“多捕获适体传感器”(MCAS))或申请号为62/523,835的美国临时申请(“对接适体传感器”(DAS))中公开的形式。
“分析物捕获型复合物”是指在靶标分析物存在下经历构型变化并且能够用于具有分析物特异性的传感器的适体、低聚物或其他合适的分子或复合物,例如蛋白质、聚合物、分子印迹聚合物、多肽和聚糖。可以通过添加由核苷酸碱基组成的一条或多条引物段来修饰这些分子或复合物。
“适体”是指一种分子,该分子在与分析物结合时经历构象变化,并且该分子满足本文所述的感测方法的一般操作原理。此类分子是例如天然的或经修饰的DNA、RNA或XNA寡核苷酸序列、spiegelmer、肽适体和affimer。修饰可以包括用非天然核酸碱基替换适体序列内的天然碱基、用非天然序列替换天然序列、或改善传感器功能的其他合适的修饰。
“生物识别元件”是指与靶标分析物分子相互作用并且可以官能化作为生物传感器的一部分的适体或其他分子,包括但不限于蛋白质、聚合物、分子印迹聚合物、多肽和聚糖。
“适体感测元件”是指官能化以与电极一起起作用,从而检测靶标分析物的存在的分析物捕获型复合物。此类官能化可包括用可氧化还原部分标记适体,或将硫醇结合分子、对接结构或其他组成部分附接到适体。在电极上官能化的多个适体感测元件包括EAB传感器。
“灵敏度”表示在每单位被测量参数变化中传感器输出的变化。该变化在传感器的范围内可以是恒定的(线性的),或者可以是变化的(非线性的)。
“信号阈值”是指由多个适体感测元件产生的、表明靶标分析物的存在的信号开启(signal-on)指示的组合强度。
“自组装单层”(SAM)是指通过自限性结合反应而粘附到EAB电极的分子层,即每个开放的表面分子将仅与一个引入的气体分子反应。因此,可以以极大的精确度沉积单独层,使得在电极上能够形成每层厚约1埃的若干层(例如3至50层)以形成阻挡表面。
具体实施方式
所公开的发明的实施方式至少应用于测量汗液、间质液或其他生物流体中的至少一种分析物的任何类型的汗液感测装置。此外,所公开的发明的实施方式应用于以时间顺序保证的采样率或采样间隔来测量样品的感测装置。所公开的发明的实施方式应用于可以采取各种形式的感测装置,所述形式包括贴片、带子、带条、衣服的部分、可穿戴设备或当汗液样品被运输到皮肤表面时可靠地使取样和感测技术与汗液样品紧密接近的任何合适的机构。虽然所公开的发明的一些实施方式利用粘合剂将所述装置保持在皮肤附近,但装置也可以由保持装置固定抵靠皮肤的其他机构(例如带子或嵌入头盔)保持。所公开的发明的某些实施方式将传感器显示为简单的单独元件。应当理解,许多传感器需要两个或更多个电极、参考电极、或在本文的描述中未捕获的附加支持技术或特征。传感器优选本质上是电性的,但也可以包括光学、化学、机械或其他已知的生物感测机制。传感器可以二重的、三重的或更多重的,以提供改进的数据和读数。所公开的发明的某些实施方式示出了作为感测装置的子组件以及该装置中用于各种应用中所必需的更多的子组件,所述更多子组件是显而易见的(例如电池),而出于简洁和更加关注发明方面的目的,这些组件并未在图中明确示出或在所公开的发明的实施方式中描述。
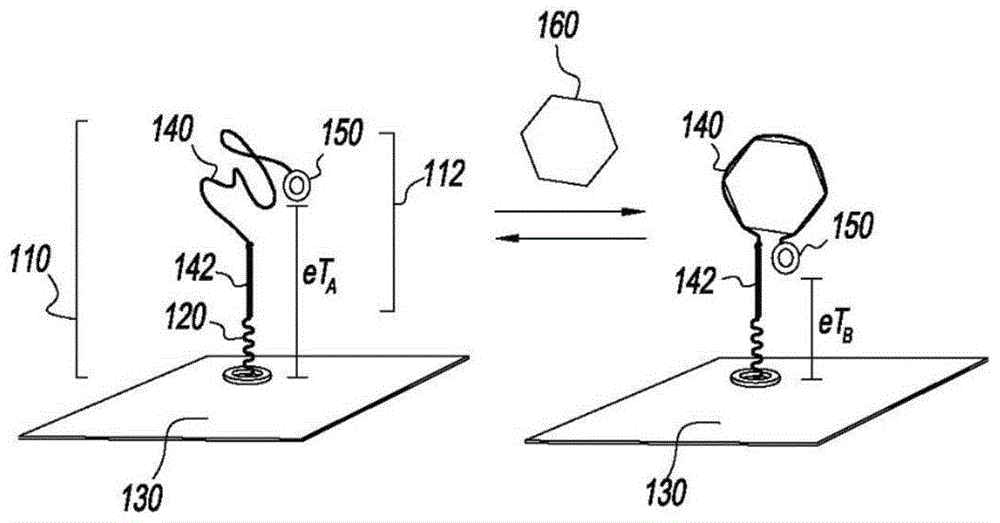
如2017年3月21日提交的PCT/US17/23399(通过引用全部内容并入本文)中所公开的,用于汗液连续感测的EAB传感器被配置为在存在主要是连续的或持续流动的汗液样品的情况下随时间提供稳定的传感器响应。例如,多捕获EAB传感器包括多个单独的适体感测元件,如图1所示,所述适体感测元件可以通过在靶标分析物与适体相互作用时捕获和释放靶标分析物来重复检测分子靶标的存在。感测元件包括分析物捕获型复合物140,分析物捕获型复合物140具有与引物142共价键合的第一末端。引物142与硫分子(硫醇)120键合,硫分子120又与金电极基底130共价键合。在其它实施方式(未示出)中,适体可以通过乙二胺四乙酸(EDTA)应变与电极结合,以改善难以感测的环境(例如汗液生物流体)中的粘附。感测元件还包括氧化还原部分150,氧化还原部分150可以与适体140共价键合或通过连接部分与适体140结合。在不存在靶标分析物的情况下,适体140处于第一构型,并且氧化还原部分150相对于电极130处于第一位置。当汗液感测装置使用方波伏安法(SWV)询问感测元件时,感测元件产生第一电信号eTA。
选择适体140以与靶标分析物160特异性相互作用,使得当适体捕获靶标分析物分子时,适体经历部分地破坏第一构型并形成第二构型的构象变化。因此,靶标分析物160的捕获使氧化还原部分150相对于电极130移动到第二位置。现在当汗液感测装置询问感测元件时,感测元件产生可与第一电信号区分的第二电信号eTB。在纳秒、毫秒、秒或更长的间隔(“恢复间隔”)之后,适体140释放靶标分析物160,并且适体返回到第一构型,这会在感测元件被询问时产生相应的第一电信号。
为了启用适体感测元件,通过添加钝化剂进一步制备电极表面以产生阻止表面上的非特异性吸附的阻断剂基团。如果不防止,污染电极表面的非特异性分子将导致感测元件在存在分析物的情况下记录较弱的信号,从而提高传感器的检测下限。通过用羟基封端的烷烃硫醇处理表面来完成电极钝化,所述羟基封端的烷基硫醇粘附到电极上并在空间上阻挡(原本)未覆盖的区域。参见Lai,Plaxco,et al.2007。通常用于形成阻断剂基团的钝化剂是短链单硫醇,例如6-巯基、1-己醇(MCH)和3-巯基丙酸(MPA),所述短链单硫醇通过从溶液中自发吸附到金表面上形成自组装单层(SAM)吸附物。
EAB传感器的主要限制是它们在汗液生物流体存在下的长期稳定性相对较差。尽管EAB传感器技术在本领域中是相对熟知的,但是很少有从业者系统地研究这种类型的传感器在汗液中的稳定性或者如何可以改善稳定性。参见Phares,White,et al.2009。因此,所公开的发明提供了一种用以改善EAB传感器在诸如汗液的生物流体中的长期稳定性的解决方案。
EAB传感器稳定性相对较差的一个原因是它们依赖于硫醇化适体和阻断剂基团的自组装。虽然这种自组装单层易于制造,但由于硫醇部分从电极表面逐渐解吸附,它们表现出低的长期稳定性。结果,适体感测元件和硫醇阻断剂基团均倾向于与电极解离,使得EAB传感器随着时间的推移而无效或效率较低。这种解吸附可能是由瞬时氧化事件和应用还原电位来询问传感器而引起的,两者都削弱了金-硫醇键。参见Poirier,Tarlov,et al.,1994;Flynn,Tran,et al.,2003。证据表明,硫醇根据以下任一反应而从金中解吸附:
方程式1:2RS-Au→2RSH+2Au→RSSR+2Au
方程式2:RS-Au+H2O+O3→RSO3H+HO-Au
根据方程式1,作为二硫化物的硫醇可以形成稳定但可逆的复合物,该复合物抵抗与电极表面的即时再附接。类似地,根据方程式2,作为磺酸盐的硫醇不会吸附到金表面,因此可以容易地除去。除了这种优先的化学途径之外,还显示金表面上的SAM在高温(>40℃)和高盐浓度(>0.3M)下变得不太稳定。参见Li,Jin,et al.,2002。
EAB传感器的稳定性在理论上可以通过使用较长链硫醇栓在适体感测元件上并充当阻断剂基团来改善,参见Ulman,A.,1996,然而,使用较长链硫醇会减弱在分析物捕获时由适体感测元件产生的电子转移(并因此减弱信号)。因此,相反,如本文所公开的,本发明的实施方式使用多个硫醇(例如三己基硫醇)使适体感测元件和阻断剂基团锚定到电极上。参见Li,Jin,et al.,2002;Sakata,Maruyama,et al.,2007;Phares,N.,et al.,2009。用柔性三己基硫醇分子锚定的适体感测元件表现出增强的稳定性,保留其原始信号的75%并在缓冲液中储存50天后保持优异的信号传导性质。所公开的方法还保持EAB传感器的稳定性,而不会减少电子传输或另外在使用期间降低传感器性能。
在基于适体的传感器的稳定性中,另一个重要因素是烷烃硫醇阻断剂基团的物理结构。如文献中所示,具有多个可用的附接位点显著提高了硫醇化吸附物膜的稳定性。因此,在所公开的发明的实施方式中,常规的单硫醇阻断剂基团(例如MCH)被带有多个硫醇的分子取代。具体而言,一种替代性的阻断分子是4,5-双(硫烷基甲基)苯-1,2-二醇(参见图2;包括其异构体)、以及具有以下性质的类似分子:1)成对的邻甲烷硫醇基团;2)由6个碳组成的芳环;3)1至4个酚羟基(无论位置如何)。此类分子还可用于将适体感测元件栓在电极上。
基于芳香族二硫醇的SAM的吸附物分子在金电极基底上形成紧密堆积且有序的结构,假设为2×2层叠层结构。通过多个金-硫相互作用、分子间范德华键、和在单层之内以及芳香族部分之间的氢键使有序结构稳定。参考图3,描绘了EAB生物传感器的一部分,该部分包括所公开的多硫醇结合剂和阻断剂基团。生物传感器包括电极320,其中具有多个结合剂分子370,该多个结合剂分子370将多个阻断剂基团380附接到电极。阻断剂基团彼此相互作用以在电极上形成密集堆积、有序且稳定的SAM,这增强了可附接到电极或附接到SAM的多个适体感测元件(未示出)的功能。
这种有希望改善EAB传感器长期稳定性的芳香族二硫醇阻断剂基团的特征如下:首先,4,5-双(硫烷基甲基)苯-1,2-二醇中的两个近端硫醇基团提供两个用于附接到金表面的键合部分。已知多个硫配体促进硫栓住的膜的稳定性,此外,熵驱动的螯合作用倾向于改善均相有机金属配合物如二硫醇基团的稳定性。再者,即使没有栓住的分子,π-π堆叠相互作用也应该为阻断剂基团稳定性提供额外的焓和熵贡献。第三,游离酚羟基应提供进一步使表面稳定的氢键,并产生两性双层。参见图4。
此外,鉴于涉及形成分子间二硫化物的解吸附途径将需要使四个或更多个栓住的硫原子同时解吸附(这是低概率事件),这些途径对二硫醇阻断剂基团不太重要。此外,对于二硫醇阻断剂基团来说,这种相互作用是可逆的。参见图5。
所提出的阻断剂基团分子的最终益处是它足够小以致不降低电子转移和适体信号传导。所提出的较小尺寸的阻断剂分子允许更密集地放置在电极上,并且提供给分子从其附接点扩散出来的自由空间较小。迄今为止,在本领域中忽略了使用像4,5-双(硫烷基甲基)苯-1,2-二醇这样的小分子,因为小分子被认为太不稳定而不能用于EAB传感器,尽管它们具有与电子转移和信号传导相关的理想特性。然而,利用如公开的具有芳香性质的、短而稳定的SAM(其改善电导率并降低电阻)将极大地改善电子转移特性。同样,任何并入有共轭系统的接头部分,无论长度如何,都会增强电子传递,从而增强信号。
以下示例性合成通常适用于所公开的发明所考虑的二硫醇基团,并且可用于以许多不同官能团使开环碳官能化。将示例性合成分解为使用乙酸钯(II)(Pd(OAc)2)作为催化剂将芳环上的第4和第5个碳乙酰化的C-H官能化步骤。一旦使用已知的合成方法官能化,乙酸酯基团可以转化为多个官能团,但是出于本发明的目的,乙酸酯仅被还原成羟基。
示例性合成步骤1。参考图6A,该步骤是Pd(OAc)2催化的苯乙酰化。作为催化剂的Pd(OAc)2和作为氧化剂的(二乙酰氧基碘)苯(PhI(OAc)2)的组合使苯环中的C-H键官能化。将(1,2-亚苯基)二甲硫醇(1当量)和Pd(OAc)2(10mol%)、PhI(OAc)2(2.2当量)溶解在乙酸(AcOH)和乙酸酐(Ac2O)(1:1)中。将所得混合物在80℃下搅拌1至3小时。通过蒸发溶剂和柱色谱法实现终产物的纯化和分离,从而允许产物分离。通过使用已知的分析方法,包括核磁共振成像、质子和碳质谱,证实了纯化的产物4,5-双(硫烷基甲基)-1,2-亚苯基。该步骤的理想产率为77%。
示例性合成步骤2。参考图6B,该步骤是使用低摩尔浓度的氢氧化锂(LiOH)在环境温度下还原乙酸酯基团。在25℃下,将0.2M LiOH水溶液添加到4,5-双(硫烷基甲基)-1,2-亚苯基二乙酸酯(1当量)的四氢呋喃(THF)溶液中,并将混合物搅拌1至2小时。接着,用H2O(LiOH的5倍量)淬灭反应混合物。然后用乙酸乙酯(EtOAc)萃取两相反应混合物,并使用硫酸镁(MgSO4)干燥合并的有机层,然后浓缩。用色谱法分离和纯化得到4,5-双(硫烷基甲基)苯-1,2-二醇的终产物。该反应步骤的理想产率为92%。
可以替代地配制所公开的稳定性增强的二硫醇阻断剂基团/适体系链。例如,可能的替代形式包括以下:4,5-双(硫烷基)苯-1,2-二醇,参见图7;4,5-双(硫烷基)戊-1-醇,参见图8;3,4-双(硫烷基甲基)苯酚,参见图9;5,6-双(硫烷基)癸烷-1,10-二醇,参见图10;5,7-双(硫烷基甲基)-6-丁醇十一烷-1,11-二醇,参见图11;1,2-二巯基戊-5-醇;和5,6-二巯基癸-1,10-二醇。
在另一种替代实施方式中,阻断剂基团/适体系链可包含含有芳香族部分(例如苄基)的支化三硫醇。参见图12。几种更复杂的排布也是可能的。例如,该分子可包括具有芳香族部分的多硫醇。可以将该分子放置在电极表面上而无需进一步修饰以起到阻断剂基团的作用,或者如寡核苷酸合成领域的技术人员所熟悉的,可以使用亚磷酰胺化学物质将该分子掺入适体DNA中以起到系链的作用。
在另一种替代实施方式中,所公开的自组装单层可以附接到由替代材料(例如石墨、碳纳米管或具有石墨烯表面特征的其他碳基材料)组成的电极。此类技术先前已在申请号为62/559,857的美国临时申请中公开,其通过引用全部内容并入本文。对于在生物流体感测装置上的用途,虽然由替代材料构成的电极可以提供优于金电极的优点,但是将组件可靠地附接到替代材料是重大的问题。附接化学物质随预期电极材料的性质而大不相同,并且材料可能显示出干扰EAB感测元件的功能的额外化学性质。因此,本文公开的适应性自组装单层提供了将分子层附接到各种碳基电极材料的有效手段,使得这些材料能够用于EAB生物传感器。
图13A至图13C描绘了用于产生产物的一系列合成反应,所述产物在与多个这样的分子组合并在EAB传感器电极表面上官能化时用作所公开发明的示例性实施方式。参考图13C,终产物1-甲醇-2,4,5-苯三甲硫醇1300可以沉积在电极上以形成具有许多所需特征的SAM。例如,阻断剂基团1300具有多个硫醇基团,所述硫醇基团可用于形成与电极表面的持久键1310或与其他组件(例如适体感测元件)的持久键1312。而且,芳环1330允许单独的SAM分子通过π-π堆叠相互作用。这些π-π键使阻挡剂基团排列成规则且紧密堆积的表面,从而形成致密的层,该致密的层转而将显示出电极表面非特异性阻垢性得以改善,以及EAB组件对电极的粘附性得以改善。尺寸相对小的阻断剂基团1300还用于使硫醇基团保持更靠近分子的主体,这产生更小的分子足迹,这也使得分子更密集地堆积在电极上。
图13A至图13C中描绘的示例性合成不限于1-甲醇-2,4,5-苯三甲硫醇,而是可以使用类似的方法来制备以烷基链、芳环、不同官能团和其他硫醇的其他组合为特征的SAM组件。在本发明的范围内也考虑由这些物质组成的SAM。例如,SAM组件可包括允许点击化学反应的官能团,例如叠氮基团。点击化学反应可以使各种化合物能够稳健附接,从而能够针对特定应用定制SAM属性。参见2017年9月18日提交的申请号为62/559,857的美国临时申请,其通过引用全部内容并入本文。
在另一种实施方式中,单独的阻断剂基团被配置成通过交联反应彼此相互作用。除了具有硫醇以将阻断剂基团结合到电极表面之外,每个阻断剂基团还包括硫醇附接点,该硫醇附接点用于附接使单独的阻断剂基团交联的官能团或包括这些官能团的碳链分支。例如,图13C中所示的1-甲醇-2,4,5-苯三甲硫醇在1312位置配置有多硫醇,该多硫醇能够与其他阻断剂基团交联。与π-π键的作用类似,使单独的阻断剂基团交联引起SAM有效地形成大分子,该大分子将显示出改善的对非特异性吸附的抗性,以及通过更好地粘附到电极上而改善的稳定性。
对于使用交联的阻断剂基团的SAM的组装,交联的官能团将存在于电极上但在SAM自组装期间不起反应。一旦SAM已经附接到电极表面,交联的官能团可以通过光子暴露、温度变化、引入自由基物质、或聚合物化学物质领域中已知的其他机制来活化。可替换地,可以在根据组装期望的SAM所需的多个步骤中添加官能团或其他组分。
促进这种交联的合适官能团化学物质的一些实例包括环氧树脂、聚醚、聚酯、聚氨酯、乙烯基、乙酸烯丙酯、烯丙基氰、氰基丁烷和丙烯酸酯。用作单独的阻断剂基团的单体的实例包括但不限于苯乙烯、丙烯酸和乙烯基吡咯烷酮。在其他实施方式中,阻断剂基团可以是多用途的,并且除了用于通过附接接头或适体感测元件使SAM官能化的附接点之外,还包括用于交联的附接点。这种多功能阻断剂基团将采用正交化学,使得交联附接点不会与官能化附接点相互作用。
- 还没有人留言评论。精彩留言会获得点赞!