一种天花粉或含天花粉为原料制备的药物的含量测定方法与流程
本发明涉及一种天花粉或含天花粉为原料制备的药物的含量测定方法。
背景技术:
天花粉是历史悠久、使用广泛的中药,具有清热生津、排脓消肿的功效。天花粉蛋白具有引产、抗肿瘤的功效。2005年版《中华人民共和国药典(一部)》收载的天花粉为葫芦科植物栝楼tri-chosantheskirilowiimaxim.或双边栝楼trichosanthesuniflorahao的干燥根,主产于河南、山东、江苏、贵州、安徽等地。目前全国各地所用天花粉的原植物很多,不同植物来源的天花粉的疗效不完全一样,某些伪品还有一定的不良反应。
目前报道的天花粉的检测方法较多,如鲁建江,天花粉多糖的提取及含量测定,天津药学,2001年4月第13卷第2期,从天花粉中提取多糖并测定其含量。方法:用水提醇沉法提取天花粉多糖,用酚-硫酸比色法测定多糖含量。该实验证明天花粉多糖含量不是很高,提取方法有待进一步改进。彭朝霞,hplc测定天花粉中葫芦素b的含量,中国现代应用药学杂志2009年11月第26卷第11期,由于葫芦素b具有较大毒性,其毒性反应是与其剂量密切相关的。该文献公开了检测天花粉中葫芦素b的方法,有文献报道采用氨基酸作为天花粉中的检测指标,如:曹敏,等,薄层色谱法鉴别天花粉及其相似品的氨基酸,传统医药,正品天花粉在瓜氨酸和丙氨酸对照品色谱相应结果位置上显相同的紫红色斑点,大苞栝楼的根则在丙氨酸对照品色谱处无相应斑点。杨玉琴,等,不同产地天花粉药材中瓜氨酸的含量,时珍国医国药2009年第20卷第6期,对15个不同产地的天花粉药材进行瓜氨酸含量测定,在含量上有一定差异,但贵州天花粉中瓜氨酸含量较高,且生长周期越长瓜氨酸含量就越高。
天花粉中含有较多的氨基酸成分,已有检测方法的有瓜氨酸、γ-氨基丁酸(刘文,天花粉中瓜氨酸与γ-氨基丁酸的含量测定),采用柱前衍生反相高效色谱峰进行检测,样品处理过程较复杂。此外,色氨酸也是植物体内生长素生物合成重要前体物质,在高等植物中普遍存在,同时,色氨酸被广泛应用于饲料中(宋吉英,hplc法测定玉米蛋白粉和乳猪教槽料中色氨酸的含量)采用0.0085mol/l乙酸钠:甲醇(95:5)。
技术实现要素:
本发明的技术方案是提供了一种天花粉或含天花粉为原料制备成药物的含量测定方法。
本发明提供一种天花粉或含天花粉为原料制备成药物的含量测定方法,它是采用hplc指谱图谱检测,其操作步骤如下:
a、供试品溶液的制备:
取待检样品,加入稀乙醇,超声处理20min-40min,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液,即得;
b、参照物溶液的制备:
取色氨酸对照品适量,精密称定,加稀乙醇溶液,即得;
c、分别精密吸取参照物溶液与供试品溶液注入液相色谱仪,以乙腈、水为流动相进行洗脱,其色谱条件为:
以苯基-己基硅烷键合硅胶为填充剂;以乙腈-水(4-10:90-96)为流动相;流速为:0.8-1.2ml/min;柱温25-35℃;检测波长为224nm;理论板数按色氨酸峰计应不低于3000。
进一步优选地,所述的药物包括天花粉药材、天花粉标准汤剂、天花粉配方颗粒。
进一步优选地,a步骤超声条件为:功率600w,频率40khz;超声时间20min。
其中,c步骤所述的苯基-己基硅烷键合硅胶填充剂柱长为250mm,内径为4.6mm,粒度为5μm。
其中,所述的天花粉药材含量测定方法为:
a、供试品溶液的制备取本品粉末(过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,称定重量,超声处理20分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过即得;
b、色谱条件与系统适用性试验以苯基-己基硅烷键合硅胶为填充剂(柱长为250mm,内径为4.6mm,粒度为5μm);以乙腈-水(4:96)为流动相;检测波长为224nm。理论板数按色氨酸峰计算应不低于3000;
c、对照品溶液的制备取色氨酸对照品适量,精密称定,加稀乙醇制成每1ml含10μg的溶液,即得;
d、测定法精密吸取供试品溶液10μl,注入液相色谱仪,测定,即得。
其中,所述的天花粉标准汤剂含量测定方法为:
a、供试品溶液的制备取本品粉末约0.1g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,称定重量,超声处理30分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过即得;
b、对照品溶液的制备取色氨酸对照品适量,精密称定,加稀乙醇制成每1ml含10μg的溶液,即得;
c、色谱条件与系统适用性试验以苯基-己基硅烷键合硅胶为填充剂(柱长为250mm,内径为4.6mm,粒度为5μm);以乙腈-水(5:95)为流动相;检测波长为224nm。理论板数按色氨酸峰计算应不低于3000;
d、测定法精密吸取供试品溶液10μl,注入液相色谱仪,测定,即得。
本发明首次确定天花粉药材、天花粉标准汤剂、天花粉配方颗粒中有色氨酸成分;采用高效液相色谱的方法将天花粉药材、天花粉标准汤剂、天花粉配方颗粒中色氨酸分开,进行测定;建立天花粉药材、汤剂、配方颗粒中色氨酸的检测方法。
本发明选择苯基-己基硅烷键合硅胶为填充剂的色谱柱,改变了惯用的十八烷基硅烷键合硅胶为填充剂的色谱柱,以色氨酸的分离情况为指标,苯基-己基硅烷键合硅胶为填充剂的色谱柱较十八烷基硅烷键合硅胶为填充剂的色谱柱分离效果更好,色氨酸峰峰形更好,流动相组分的比例更简单。
本发明检测天花粉中色氨酸的含量,操作性强、样品处理过程简单、流动相简单,重复性高,检测时间短。
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
图1色氨酸紫外吸收光谱图
图2流动相1:10%乙腈-90%水
图3流动相2:8%乙腈-92%水
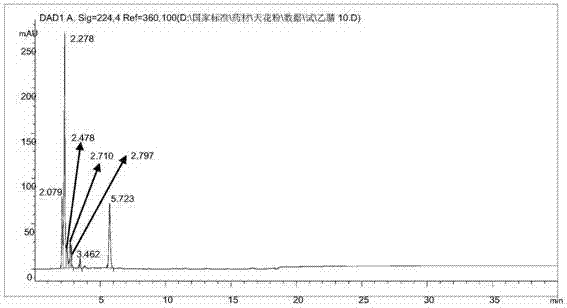
图4流动相3:4%乙腈-96%水
图5不同柱温考察结果
图6不同流速考察结果
图7提取溶剂考察结果
图8提取方式考察结果
图9提取时间考察结果
图10进样量考察
图11天花粉药材专属性考察
图12色氨酸标准曲线图
图13不同仪器考察
图14色谱柱耐用性考察结果
图15流动相1:10%乙腈-90%水
图16流动相1:8%乙腈-92%水
图17流动相1:5%乙腈-95%水
图18色氨酸紫外吸收光谱图
图19柱温考察结果
图20流速考察结果
图21提取溶剂考察结果
图22提取方式考察结果
图23提取时间考察结果
图24溶剂加入量考察
图25进样量考察
图26天花粉标准汤剂专属性考察
图27色氨酸标准曲线图
图28不同仪器考察
图29色谱柱耐用性考察结果
具体实施方式
实施例1本发明天花粉药材含量测定方法
色谱条件与系统适用性试验以苯基-己基硅烷键合硅胶为填充剂(柱长为250mm,内径为4.6mm,粒度为5μm);以乙腈-水(4:96)为流动相;检测波长为224nm。理论板数按色氨酸峰计算应不低于3000。
对照品溶液的制备取色氨酸对照品适量,精密称定,加稀乙醇制成每1ml含10μg的溶液,即得。
供试品溶液的制备取本品粉末(过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,称定重量,超声处理20分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过即得。
测定法精密吸取供试品溶液10μl,注入液相色谱仪,测定,即得。
实施例2本发明天花粉药材含量测定方法学考察
1仪器
安捷伦1200型高效液相色谱仪、岛津20ad型高效液相色谱仪、岛津20at型高效液相色谱仪;
电子天平:me204e/02、ms205du、xp26(梅特勒-托利多仪器有限公司);
超纯水机:细胞型1810a(上海摩勒科学仪器有限公司);
超声波清洗器:kq5200db型(600w,40khz;昆山市超声仪器有限公司);
色谱柱:agilentpheny-hexyl4.6×250mm5μm、dikmapheny-hexyl4.6×250mm5μm、菲罗门pheny-hexyl4.6×250mm5μm
2试剂与药材
色氨酸对照品(中国药品生物制品检定所,批号:140686-201303,含量以99.9%计)。
乙腈(sigma公司,色谱纯);水为超纯水,其它试剂均为分析纯。
3拟定试验条件
3.1色谱条件与系统适用性试验
以苯基-己基硅烷键合硅胶为填充剂(柱长为250mm,内径为4.6mm,粒度为5μm)。
3.2对照品溶液制备
取色氨酸对照品适量,精密称定,加稀乙醇制成每1ml含10μg的溶液,即得。
3.3供试品溶液制备
取本品粉末(批号:010442-1801001,过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,称定重量,超声处理20分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
3.4测定法
精密吸取供试品溶液10μl,注入液相色谱仪,测定,即得。
4色谱条件选择与系统适用性考察
4.1检测波长确定
在以上拟定的试验条件基础上,利用二极管阵列检测器对色氨酸进行全波段扫描,确定天花粉药材中色氨酸的含量测定波长为224nm,见图1。
4.2流动相选择
在以上拟定的试验条件基础上,考察了流动相1(10%乙腈:90%水)、流动相2(8%乙腈:92%水)、流动相3(4%乙腈:96%水)的洗脱效果,分别见图2-4。
由图可知,当乙腈:水(4:96)时,色氨酸峰峰形更好,故选择乙腈:水(4:96)作为天花粉药材含量测定的流动相。
4.3柱温考察
在以上拟定的试验条件基础上,分别对柱温为25℃、30℃、35℃时进行考察。以色氨酸分离度、理论塔板数、拖尾因子等作为评价指标。见图5,表1。
表1不同柱温的分析结果
结果表明,当柱温为25℃、30℃、35℃时,色谱图峰形、分离效果均符合要求。
4.4流速考察
在以上拟定的实验条件基础上,分别对流速为0.8ml/min、1.0ml/min、1.2ml/min时进行了考察,以色氨酸色谱峰的分离度、理论塔板数、拖尾因子等作为评价指标。见图6,表2。
表2不同流速分析结果
结果表明,当流速为0.8ml/min、1.0ml/min、1.2ml/min时,色谱图峰形、分离效果均符合要求。
综上所述,天花粉药材含量测定色谱条件与系统适应性试验确定为:以苯基-己基硅烷键合硅胶为填充剂(柱长为250mm,内径为4.6mm,粒度为5μm);以乙腈-水(4:96)为流动相;检测波长为224nm。理论板数按色氨酸峰计应不低于3000。
5供试品溶液制备考察
5.1提取溶剂考察
取本品粉末(批号:010442-1801001,过三号筛)约0.5g,精密称定,置具塞锥形瓶中,分别用甲醇、50%甲醇、乙醇、稀乙醇进行提取,分别精密加入25ml,密塞,称定重量,超声处理(功率600w,频率40khz)20分钟,放冷,再称定重量,用提取溶剂补足减失的重量,摇匀,滤过,取续滤液,即得。分别精密吸取供试品溶液各10μl,注入液相色谱仪,见图7。计算不同溶剂提取下色氨酸的含量,结果见表3。
表3提取溶剂考察结果
结果表明,稀乙醇的提取效率最高,峰形最好,因此选择稀乙醇作为天花粉药材检测色氨酸的提取溶剂。
5.2提取方式考察
取本品粉末(批号:010442-1801001,过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,密塞,称定重量,分别对供试品提取方法为回流、超声时进行考察,提取时间20分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。分别精密吸取供试品溶液各10μl,注入液相色谱仪,见图8。分别计算不同提取方式色氨酸的含量。结果见表4。
表4提取方式考察结果
结果表明,超声提取所得色氨酸含量与回流提无显著差异,故选择操作简捷的超声提取。
5.3提取时间考察
取本品粉末(批号:010442-1801001,过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,密塞,称定重量,超声处理(功率600w,频率40khz),分别对供试品提取20分钟、30分钟、40分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。分别精密吸取供试品溶液各10μl,注入液相色谱仪,见图9。分析计算不同提取时间下色氨酸含量,结果见表5。
表5提取时间考察结果
结果表明,当提取时间为20分钟时,即可充分提取。故供试品提取时间确定为20分钟。
5.4进样量考察
取本品粉末(批号:010442-1801001,过三号筛)约0.5g,精密称定,置具塞锥形瓶中,分别精密加入稀乙醇25ml,密塞,称定重量,超声处理20分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,即得。分别精密吸取供试品溶液5μl、10μl、15μl,注入液相色谱仪,即得,见图10。以色氨酸分离度、理论塔板数、拖尾因子等作为评价指标,见表6。
表6进样量考察性能指标
结果表明,当溶剂加入量为10μl时,色谱图峰形较好,峰面积适中。故溶剂加入量确定为10μl。
综上所述,天花粉药材含量测定供试品制备方法确定为:取本品粉末(过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,密塞,称定重量,超声处理20分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,即得。
天花粉标准汤剂含量测定供试品测定方法确定为:精密吸取供试品溶液10μl,注入液相色谱仪,即得。
6天花粉药材含量测定方法
色谱条件与系统适用性试验以苯基-己基硅烷键合硅胶为填充剂(柱长为250mm,内径为4.6mm,粒度为5μm);以乙腈-水(4:96)为流动相;检测波长为224nm。理论板数按色氨酸峰计算应不低于3000。
对照品溶液的制备取色氨酸对照品适量,精密称定,加稀乙醇制成每1ml含10μg的溶液,即得。
供试品溶液的制备取本品粉末(过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,称定重量,超声处理20分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过即得。
测定法精密吸取供试品溶液10μl,注入液相色谱仪,测定,即得。
7方法学考察
7.1专属性实验
按拟定方法制备对照品溶剂、供试品溶液及阴性对照溶液,进行检测。结果见图11。
结果表明,阴性溶液色谱图对待测峰的测定无干扰,表明该方法专属性好。
7.2精密度考察
取对照品溶液连续进样6次,记录色氨酸的峰面积,计算rsd值,结果见表7。
表7精密度考察结果
结果表明,精密度考察中色氨酸的峰面积rsd值为0.29%,表明仪器进样精密度良好。
7.3线性关系
分别精密吸取色氨酸对照品溶液(10.20μg/ml,纯度99.9%)各1μl、2μl、5μl、10μl、15μl、20μl,注入液相色谱仪,得到峰面积,以进样量(x,μg)为横坐标,峰面积(y)为纵坐标绘制响应曲线,结果见表8、图12。
表8色氨酸标准曲线分析结果
结果表明:色氨酸进样量范围在0.0102~0.2040μg时,线性关系为y=63.4321x-0.9110,r2=0.9996。表明进样量在0.0102~0.2040μg时,呈良好的线性关系。
7.4重复性
取本品粉末(批号:010442-1801001,过三号筛)约0.5g,精密称定6份,由同一操作人员按照确定的方法制成供试品溶液,计算6份供试品的色氨酸含量,结果见表9。
表9重复性实验结果
结果表明,色氨酸含量的rsd值为0%,表明本方法重复性良好。
7.5中间精密度
7.5.1不同仪器考察
在以上拟定的实验条件基础上,精密称取本品粉末(批号:010442-1801001,过三号筛)两份,制备供试品溶液,分别在安捷伦1260、安捷伦1200、岛津20at型高效液相色谱仪上进行考察(色谱柱均为agilentpheny-hexyl4.6×250mm5μm)。计算色氨酸含量,所得结果,见图13,表10。
表10不同仪器实验结果
结果表明,在安捷伦1260、安捷伦1200、岛津20at型高效液相色谱仪进行考察,色氨酸的含量测定结果rsd值为9.54%,说明本方法中间精密度良好。
7.5.2不同人员和时间考察
在以上拟定的实验条件基础上,由不同人员(a、b)在不同时间(t1、t2)分别精密称取本品粉末(批号:010442-1801001,过三号筛),制备供试品,进行测定。计算所得色氨酸含量结果,见表11。
表11不同人员与时间考察结果
结果表明,不同人员在不同时间检测,色氨酸的含量测定结果rsd值为0%,本方法中间精密度良好。
7.6加样回收率
取已知含量的供试品粉末(批号:010442-1801001,过三号筛,色氨酸的含量0.047%)约0.25g,共6份,精密称定,分别精密加入一定量的色氨酸对照品(0.1045μg/ml,纯度:99.9%),按拟定的方法进行供试品溶液的制备并测定,计算回收率,结果见表12。计算公式如下。
表12加样回收实验结果
结果表明,回收率平均值为105.07%,结果的rsd值为0.68%,本方法准确度良好。
7.7耐用性考察
7.7.1色谱柱耐用性考察
在以上拟定的实验条件基础上,分别对色谱柱为agilentpheny-hexyl4.6×250mm5μm、dikmapheny-hexyl4.6×250mm5μm、菲罗门pheny-hexyl4.6×250mm5μm进行考察。见图14,表13。
表13色谱柱耐用性考察结果
结果表明,不同色谱柱的分析色谱指标良好,6个测量结果的rsd值为11.84%,本方法色谱柱耐用性良好。
7.7.2稳定性实验
取本品粉末(批号:010442-1801001,过三号筛)约0.5g,精密称定,制备供试品溶液,分别在0h、3h、6h、12h、15h、24h测定色氨酸峰面积,结果见表15。
表15色氨酸稳定性实验结果
结果表明,在本实验条件下,色氨酸含量的rsd值为0.30%,供试品溶液在24小时内稳定性良好。
7.8样品含量测定验证
以天花粉药材为供试品,按拟定的方法制备供试品溶液并测定,记录峰面积,计算色氨酸的含量,结果见表16。
表1623批天花粉药材含量结果
试验例3本发明天花粉标准汤剂含量测定
1仪器与试药
1.1仪器
高效液相色谱仪:安捷伦1200型高效液相色谱仪、安捷伦1260型高效液相色谱仪、岛津20ad型高效液相色谱仪;
电子天平:me204e/02、ms205du、xp26(梅特勒-托利多仪器有限公司);
超纯水机:细胞型1810a(上海摩勒科学仪器有限公司);
超声波清洗器:kq5200db型(600w,40khz;昆山市超声仪器有限公司);
色谱柱:agilentpheny-hexyl4.6×250mm5μm、dikmapheny-hexyl4.6×250mm5μm、菲罗门pheny-hexyl4.6×250mm5μm;
1.2试药
色氨酸对照品(中国药品生物制品检定所,批号:140686-201303,含量以99.9%计)
乙腈(sigma公司,色谱纯);水为超纯水,其它试剂均为分析纯。
2天花粉标准汤剂拟定试验条件
2.1色谱条件与系统适用性试验
以苯基-己基硅烷键合硅胶为填充剂(柱长为250mm,内径为4.6mm,粒度为5μm);以乙腈-水(5:95)为流动相,检测波长为224nm,理论板数按色氨酸峰计算应不低于3000。
2.2对照品溶液制备
取色氨酸对照品适量,精密称定,加稀乙醇制成每1ml含10μg的溶液,即得。
2.3供试品溶液制备
取本品粉末(批号:thfbt180201)约0.1g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,称定重量,超声处理20分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.4测定法
精密吸取供试品溶液10μl,注入液相色谱仪,测定,即得。
3色谱条件选择与系统适用性考察
3.1流动相选择
在以上拟定的实验条件基础上,考察了流动相1(10%乙腈:90%水)、流动相2(8%乙腈:92%水)、流动相3(5%乙腈:95%水)的分类效果,分别见图15-17。
由图可知,当乙腈:水(5:95)时,色氨酸峰峰形更好,故选择乙腈:水(5:95)作为天花粉标准汤剂含量测定的流动相。
3.2检测波长确定
在以上拟定的试验条件基础上,利用二极管阵列检测器对色氨酸进行全波段扫描,见图18。
结果表明,通过对光谱图的分析,确定检测波长224nm。
3.3柱温考察
在以上拟定的实验条件基础上,分别对柱温为25℃、30℃、35℃时进行考察。以色氨酸分离度、理论塔板数、拖尾因子等作为评价指标。见图19、表17。
表17不同柱温的分析结果
结果表明,当柱温为25℃、30℃、35℃时,色谱图峰形、分离效果均符合要求。
3.4流速考察
在以上拟定的实验条件基础上,分别对流速为0.8ml/min、1.0ml/min、1.2ml/min时进行了考察,以色氨酸色谱峰的分离度、理论塔板数、拖尾因子等作为评价指标。见图20,表18。
表18不同流速分析结果
结果表明,当流速为0.8ml/min、1.0ml/min、1.2ml/min时,色谱图峰形、分离效果均符合要求。
综上所述,天花粉标准汤剂含量测定色谱条件与系统适应性试验确定为:以苯基-己基硅烷键合硅胶为填充剂(柱长为250mm,内径为4.6mm,粒度为5μm);以乙腈-水(5:95)为流动相;检测波长为224nm。理论板数按色氨酸峰计算应不低于3000。
4供试品溶液制备考察
4.1提取溶剂考察
取本品粉末(批号:thfbt180201)约0.1g,精密称定,置具塞锥形瓶中,分别用甲醇、乙醇、稀乙醇、水进行提取,分别精密加入25ml,密塞,称定重量,超声处理(功率600w,频率40khz)20分钟,放冷,再称定重量,用提取溶剂补足减失的重量,摇匀,滤过,取续滤液,即得。分别精密吸取供试品溶液各10μl,注入液相色谱仪,见图21。计算不同溶剂提取下色氨酸的含量,结果见表19。
表19提取溶剂考察结果
结果表明,稀乙醇的提取效率最高,峰形最好,因此选择稀乙醇作为天花粉标准汤剂检测色氨酸的提取溶剂。
4.2提取方式考察
取本品粉末(批号:thfbt180201)约0.1g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,密塞,称定重量,分别对供试品提取方法为回流、超声时进行考察,提取时间20分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。分别精密吸取供试品溶液各10μl,注入液相色谱仪,见图22。分别计算不同提取方式色氨酸的含量。结果见表19。
表19提取方式考察结果
结果表明,超声提取所得色氨酸含量较回流提取高,但无显著差异,故选择操作简捷的超声提取。
4.3提取时间考察
取本品粉末(批号:thfbt180201)约0.1g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,密塞,称定重量,超声处理(功率600w,频率40khz),分别对供试品提取20分钟、30分钟、40分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。分别精密吸取供试品溶液各10μl,注入液相色谱仪,见图23。分析计算不同提取时间下色氨酸含量,结果见表20。
表20提取时间考察结果
结果表明,当提取时间为30分钟时,即可充分提取。故供试品提取时间确定为30分钟。
4.4溶剂加入量考察
取本品粉末(批号:thfbt180201)约0.1g,精密称定,置具塞锥形瓶中,分别精密加入稀乙醇10ml、25ml、50ml,密塞,称定重量,超声处理30分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,即得。分别精密吸取供试品溶液10μl,注入液相色谱仪,即得,见图24。以色氨酸峰面积、分离度、理论塔板数、拖尾因子等作为评价指标,见表21。
表21溶剂加入量考察性能指标
结果表明,当溶剂加入量为25ml时,色谱图峰形较好,峰面积适中。故溶剂加入量确定为25ml。
4.5进样量考察
取本品粉末(批号:thfbt180201)约0.1g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,密塞,称定重量,超声处理30分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,即得。分别精密吸取供试品溶液5μl、10μl、15μl,注入液相色谱仪,即得,见图25。以色氨酸分离度、理论塔板数、拖尾因子等作为评价指标,见表22。
表22进样量考察性能指标
结果表明,在进样量为10μl时,色谱图峰形较好,峰面积适中。故进样量确定为10μl。
综上所述,天花粉标准汤剂含量测定供试品制备方法确定为:取本品粉末约0.1g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,密塞,称定重量,超声处理30分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,即得。
天花粉标准汤剂含量测定供试品测定方法确定为:精密吸取对照品溶液和供试品溶液各10μl,注入液相色谱仪,即得。
5天花粉标准汤剂含量测定方法
色谱条件与系统适用性试验以苯基-己基硅烷键合硅胶为填充剂(柱长为250mm,内径为4.6mm,粒度为5μm);以乙腈-水(5:95)为流动相;检测波长为224nm。理论板数按色氨酸峰计算应不低于3000。
对照品溶液的制备取色氨酸对照品适量,精密称定,加稀乙醇制成每1ml含10μg的溶液,即得。
供试品溶液的制备取本品粉末约0.1g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,称定重量,超声处理30分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过即得。
测定法精密吸取供试品溶液10μl,注入液相色谱仪,测定,即得。
6方法学考察
6.1专属性实验
按拟定方法制备供试品溶液及阴性对照溶液,进行检测。结果见图26。
结果表明,阴性溶液色谱图对待测峰的测定无干扰,表明该方法专属性好。
6.2精密度考察
取对照品溶液连续进样6次,记录色氨酸的峰面积,计算rsd值,结果见表23。
表23精密度考察结果
结果表明,精密度考察中色氨酸的峰面积rsd值为0.71%,表明仪器进样精密度良好。
6.3线性关系
分别精密吸取色氨酸对照品溶液(10.20μg/ml,纯度99.9%)各1μl、2μl、5μl、10μl、20μl、25μl,注入液相色谱仪,得到峰面积,以进样量(x,μg)为横坐标,峰面积(y)为纵坐标绘制响应曲线,结果见表24、图27。
表24色氨酸标准曲线分析结果
结果表明:色氨酸进样量范围在0.0102~0.2549μg时,线性关系为y=5835.8163x+8.4481,r2=0.9997。表明进样量在0.0102~0.2549μg时,呈良好的线性关系。
6.4重复性
取本品粉末(批号:thfbt180201)0.1g,精密称定6份,由同一操作人员按照确定的方法制成供试品溶液,计算6份供试品的色氨酸含量,结果见表25。
表25重复性实验结果
结果表明,色氨酸含量的rsd值为1.13%,表明本方法重复性良好。
6.5中间精密度
6.5.1不同仪器考察
在以上拟定的实验条件基础上,精密取本品粉末(批号:thfbt180201)0.1g,精密称定两份,分别在安捷伦1260、安捷伦1200、岛津20at型高效液相色谱仪上进行考察(色谱柱均为agilentpheny-hexyl4.6×250mm5μm)。计算色氨酸含量,所得结果,见图28、表26
表26不同仪器实验结果
结果表明,在安捷伦1260、安捷伦1200、岛津20at型高效液相色谱仪进行考察,色氨酸的含量测定结果rsd值为5.37%,说明本方法中间精密度良好。
6.5.2不同人员和时间考察
在以上拟定的实验条件基础上,由不同人员(a、b)在不同时间(t1、t2)取本品粉末(批号:thfbt180201)0.1g,分别精密称取两份,制备供试品,进行测定。计算所得色氨酸含量结果,见表27。
表27不同人员与时间考察结果
结果表明,不同人员在不同时间检测,色氨酸的含量测定结果rsd值为1.77%,本方法中间精密度良好。
6.6加样回收率
取已知含量的供试品(批号:thfbt180201,色氨酸的含量0.149%)约0.05g,共6份,精密称定,分别精密加入一定量的色氨酸对照品(0.1045μg/ml,纯度:99.9%),按拟定的方法进行供试品溶液的制备并测定,计算回收率,结果见表28。计算公式如下:
表28加样回收实验结果
结果表明,回收率平均值为95.48%,结果的rsd值为0.83%,本方法准确度良好。
6.7耐用性考察
6.7.1色谱柱耐用性考察
在以上拟定的实验条件基础上,分别对色谱柱agilentplusphenly-hexyl4.6×250mm5μm;dikmapheny-hexyl4.6×250mm5μm、菲罗门pheny-hexyl4.6×250mm5μm进行考察。见图29,表29。
表29色谱柱耐用性考察结果
结果表明,不同色谱柱的分析色谱指标良好,6个测量结果的rsd值为3.05%,本方法色谱柱耐用性良好。
6.7.2稳定性实验
取同一供试品溶液(批号:thfbt180201),分别在0h、2h、6h、12h、18h、24h测定色氨酸峰面积,结果见表30。
表30色氨酸稳定性实验结果
结果表明,在本实验条件下,色氨酸含量的rsd值为1.37%,供试品溶液在24小时内稳定性良好。
6.8含量验证
以天花粉标准汤剂冻干粉为供试品,按拟定的方法制备供试品溶液并测定,记录峰面积,计算色氨酸的含量,结果见表31。
表3123批天花粉标准汤剂色氨酸含量
7检测天花粉配方颗粒
用此方法对天花粉配方颗粒进行检测,结果见表。
表32三批天花粉配方颗粒含量检验结果
结论:此方法可以用于检测天花粉配方颗粒。
- 还没有人留言评论。精彩留言会获得点赞!