一种测定脂蛋白残粒胆固醇的浓度的试剂盒及制备方法与流程
本发明涉及生物技术领域,尤其涉及一种测定脂蛋白残粒胆固醇的浓度的试剂盒及制备方法。
背景技术:
脂蛋白残粒(remnantlipoprotein,rlp)又称富含甘油三酯(triglyceride,tg),脂蛋白残粒(trl)是乳糜微粒(chylomicron,cm)和极低密度脂蛋白(verylowdensitylipoprotein,vldl)经脂蛋白酯酶(lipoproteinlipase,lpl)水解逐渐失去甘油三酯、磷脂、脂蛋白a,apoa)和apoc后,转变成的富含胆固醇、胆固醇脂和apoe的较小颗粒。
近年来,随着对脂蛋白残粒的深入了解,rlp测定的临床意义日趋受重视。大量研究表明,浓度在动脉粥样硬化性疾病及动脉粥样相关的疾病(如ⅱ型糖尿病、ⅲ型高脂血症和慢性肾功能衰竭及肥胖患者)中显著增加。另外,从人动脉粥样斑块中分离的脂蛋白在结构上与富含tg脂蛋白残粒相似。因此,血清或血浆脂蛋白残粒胆固醇(rlp-c)水平升高是动脉粥样硬化性疾病和冠心病(coronaryheart、disease,chd)以及与动脉粥样硬化性有关的代谢性疾病的重要危险因素。所以,准确、快速测定rlp非常重要。常规方法中采用胶乳微球直接偶联rlp-c抗体,我公司采用该方法发现灵敏度和线性范围均较差。因此,应该提供一种新的技术方案解决上述问题。
技术实现要素:
本发明的目的是:提供一种灵敏度高,重复性好的一种测定脂蛋白残粒胆固醇的浓度的试剂盒及制备方法。
为实现上述目的,本发明采用的技术方案是:
一种测定脂蛋白残粒胆固醇的浓度的试剂盒,包括试剂r1和试剂r2,所述试剂r1的各组分及浓度包括:
所述试剂r2包括第二缓冲液、保存液、偶联有rlp-c单克隆抗体-生物素-链霉亲和素的胶乳微球,所述第二缓冲液的浓度为8.05-27.30g/l,所述保存液的各组分及浓度包括:
n,n-二羟乙基甘氨酸1.26-9.83g/l
稳定剂0.5-2.0g/l
第二防腐剂0.8-2.0ml/l
胶乳微球偶联物的各组份及浓度包括:
胶乳微球0.01-3.0%
生物素5-20g/l
链霉亲和素5-20g/l
脂蛋白残粒胆固醇单克隆抗体0.05-3.0g/l
1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐0.005-0.3g/l。
进一步的技术方案:
所述试剂r1中的第一缓冲液a、第一缓冲液b以及试剂r2中的第二缓冲液均为pbs缓冲液、hepes缓冲液、mes缓冲液、tris缓冲液、甘氨酸缓液中的一种或几种的组合。
优选的,所述第一缓冲液a为二水合磷酸二氢钠、第一缓冲液b为十二水合磷酸氢二钠,第二缓冲液为2-(n-吗啉)乙磺酸一水合物。
所述试剂r1和r2中的防腐剂为叠氮钠、proclin-950、proclin-300、硫柳汞中的一种或几种的组合。
所述试剂r2中稳定剂为牛血清白蛋白、酪蛋白、明胶、甘露醇中的一种或几种的组合。
优选的,所述试剂r2中稳定剂为牛血清白蛋白。
胶乳微球所选粒径为90-280nm,其表面修饰基团为羧基或氨基中的一种。
所述试剂r1ph在6.80-8.00之间,试剂r2ph在6.30-8.50之间。
生物素结合rlp-c单克隆抗体比例为1:1-3:1之间,链霉亲和素结合生物素-rlp-c单克隆抗体比例为0.5:1-4:1之间。
测定脂蛋白残粒胆固醇的浓度的试剂盒的制备方法,其特征在于:包括如下步骤,
a)、试剂r1制备;
在配液罐中先加入适量纯化水于磁力搅拌器上,调节搅拌器转速至200-300rpm,使搅拌保持匀速状态,以0.8-3.2g/l标准,边搅拌边投入第一缓冲液a,以8.75-24.31g/l的标准投入第一缓冲液b,搅拌5-30分钟至物料完全溶解,溶液清澈透明配液罐底部无沉淀后,调节ph值到6.80-8.00之间,之后以5.8-20.0g/l标准,投入氯化钠,待物料完全溶解后再按照上述投料方式分别以40-120g/l、0.8%-2.0%的标准,依次投入peg6000、第一防腐剂,投料完成后,继续搅拌5-30分钟至全部物料完全溶解,溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放在成品罐中,进行标识;
b)、试剂r2制备;
b1、缓冲液配制,在配液罐中先加入适量纯化水于磁力搅拌器上,打开磁力搅拌器电源开关,调节搅拌子至中档转速,使溶液保持中速转动状态,以8.05-27.30g/l的标准,边搅拌边投入第二缓冲液,搅拌5-30分钟至物料完全溶解,溶液清澈透明配液罐底部无沉淀后,调节ph值到6.30-8.50之间,继续搅拌5-30分钟至溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放在成品罐中,进行标识;
b2、保存液配制,在配液罐中先加入适量纯化水于磁力搅拌器上,调节搅拌子至中档转速,使溶液保持中速转动状态,以1.26-9.83g/l的标准边搅拌边投入n,n-二羟乙基甘氨酸,搅拌5-30分钟至物料完全溶解,调节ph值到6.30-8.50之间,之后以0.5-2.0g/l标准,投入稳定剂,待物料完全溶解后,再以0.8-2.0ml/l标准,投入第二防腐剂,继续搅拌5-30分钟至全部物料完全溶解,溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放备用,进行标识;
b3、胶乳微球抗体偶联物的制备,胶乳微球所选粒径为90-280nm,其表面修饰基团为羧基或氨基中的一种将胶乳微球以缓冲液稀释到0.01-3.0%的浓度,再以1:1比例与链霉亲和素结合,将脂蛋白残粒胆固醇单克隆抗体以反应液稀释到0.05-3.0g/l的浓度,与生物素按3:1-1:1的比例结合后,加入到含有链霉亲和素的微球中,混匀,链霉亲和素结合生物素-rlp-c单克隆抗体比例为0.5:1-4:1之间,将1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐以反应液溶解到0.005-0.3g/l的浓度,边摇匀边滴加入上述混合溶液中,室温反应100-140分钟,加入牛血清白蛋白封闭,振荡混匀,室温反应80-100分钟,将混合液以14000rpm的转速离心15-45分钟,吸去上清液,加入保存液,超声重悬,重复离心清洗3次,最后一次离心去上清液后,加入保存液,超声重悬,将制备好的r2装入成品罐中,进行标识。
由于上述技术方案的应用,本发明与现有技术相比具有如下优点:
本发明的测定脂蛋白残粒胆固醇的浓度的试剂盒,采用胶乳微球连接链霉亲和素1:1,rlp-c单克隆抗体连接生物素1:2,二者再以1:1混合反应,可明显改善重复性和灵敏度,线性范围可做到0.1-8mg/l。
附图说明
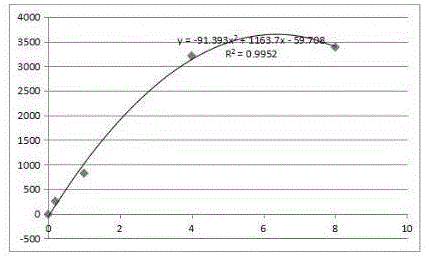
图1是本发明实施例4中r2试剂未采用级联放大偶联的定标曲线图。其中x轴表示标准品浓度,y轴表示吸光度。
图2是本发明实施例4中r2试剂采用级联放大偶联的定标曲线图。其中x轴表示标准品浓度,y轴表示吸光度。
具体实施方式
下面结合具体实施例对本发明作进一步描述:
实施例1:
一种测定脂蛋白残粒胆固醇的浓度的试剂盒,包括试剂r1和试剂r2,所述试剂r1的各组分及浓度包括:作为第一缓冲液a的二水合磷酸二氢钠,其浓度为0.8g/l,作为第一缓冲液b的十二水合磷酸氢二钠,其浓度为24.31g/l,作为第一电解质的氯化钠,其浓度为5.8g/l,作为第一高分子促进剂的peg6000,其浓度为40g/l,以及作为第一防腐剂的proclin-950,其浓度为2.0%。
所述试剂r2包括第二缓冲液、保存液、偶联有rlp-c单克隆抗体-生物素-链霉亲和素的胶乳微球,所述第二缓冲液为2-(n-吗啉)乙磺酸一水合物,其浓度为8.05g/l;所述保存液包括:浓度为9.83g/l的n,n-二羟乙基甘氨酸、作为稳定剂的牛血清白蛋白,其浓度为0.5g/l的,作为第二防腐剂的proclin-950,其浓度为0.8ml/l;胶乳微球偶联物的各组份及浓度包括:浓度为3.0%的胶乳微球,浓度为5g/l的生物素,浓度为5g/l的链霉亲和素,浓度为0.05g/l的脂蛋白残粒胆固醇单克隆抗体以及浓度为0.005g/l的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐。
以上测定测定脂蛋白残粒胆固醇的浓度的试剂盒的制备方法,包括如下步骤,
a)、试剂r1制备;
在配液罐中先加入适量纯化水于磁力搅拌器上,调节搅拌子至中档转速,使溶液保持中速转动状态,边搅拌边投入浓度为0.8g/l二水合磷酸二氢钠和浓度为24.31g/l的十二水合磷酸氢二钠,搅拌30分钟至物料完全溶解,溶液清澈透明配液罐底部无沉淀后,调节ph值为6.8,之后投入浓度为5.8g/l的氯化钠,待物料完全溶解后,再按照上述投料方式依次投入peg6000和proclin-950,以上两者的浓度分别为40g/l和2.0%,投料完成后,继续搅拌5分钟至全部物料完全溶解,溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放在成品罐中,进行标识;
b)、试剂r2制备;
b1、缓冲液配制,在配液罐中先加入适量纯化水于磁力搅拌器上,打开磁力搅拌器电源开关,调节搅拌子至中档转速,使溶液保持中速转动状态,以8.05g/l的标准,边搅拌边投入2-(n-吗啉)乙磺酸一水合物,搅拌5分钟至物料完全溶解,溶液清澈透明配液罐底部无沉淀后,调节ph值为6.30,继续搅拌5分钟至溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放在成品罐中,进行标识;
b2、保存液配制,在配液罐中先加入适量纯化水于磁力搅拌器上,调节搅拌子至中档转速,使溶液保持中速转动状态,以9.83g/l的标准边搅拌边投入n,n-二羟乙基甘氨酸,搅拌5分钟至物料完全溶解,调节ph值为6.30,之后以0.5g/l标准,投入牛血清白蛋白,待物料完全溶解后,再以0.8ml/l标准,投入proclin-950,继续搅拌30分钟至全部物料完全溶解,溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放备用,进行标识;
b3、胶乳微球抗体偶联物的制备,胶乳微球所选粒径为90nm,其表面修饰基团为羧基,将胶乳微球以缓冲液稀释到3.0%的浓度,再以1:1比例与链霉亲和素结合,将脂蛋白残粒胆固醇单克隆抗体以反应液稀释到0.05g/l的浓度,与生物素按2:1的比例结合后,加入到含有链霉亲和素的微球中,混匀,链霉亲和素结合生物素-rlp-c单克隆抗体比例为1:1,将1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐以反应液溶解到0.005g/l的浓度,边摇匀边滴加入上述混合溶液中,室温反应100分钟,加入牛血清白蛋白封闭,振荡混匀,室温反应80分钟,将混合液以14000rpm的转速离心15分钟,吸去上清液,加入保存液,超声重悬,重复离心清洗3次,最后一次离心去上清液后,加入保存液,超声重悬,将制备好的r2装入成品罐中,进行标识。
实施例2
一种测定脂蛋白残粒胆固醇的浓度的试剂盒,包括试剂r1和试剂r2,所述试剂r1的各组分及浓度包括作为第一缓冲液a的二水合磷酸二氢钠,其浓度为3.2g/l,作为第一缓冲液b的十二水合磷酸氢二钠,其浓度为8.75g/l,作为第一电解质的氯化钠,其浓度为20.0g/l,作为第一高分子促进剂的peg6000,其浓度为80g/l,作为第一防腐剂的proclin-300,其浓度为0.8%,所述试剂r2包括第二缓冲液、保存液、偶联有rlp-c单克隆抗体-生物素-链霉亲和素的胶乳微球,所述第二缓冲液为2-(n-吗啉)乙磺酸一水合物,其浓度为27.30g/l;所述保存液包括:浓度为5.0g/l的n,n-二羟乙基甘氨酸、作为稳定剂的酪蛋白,其浓度为2.0g/l的,作为第二防腐剂的proclin-300,其浓度为2.0ml/l;胶乳微球偶联物的各组份及浓度包括:浓度为0.01%的胶乳微球,浓度为20g/l的生物素,浓度为20g/l的链霉亲和素,浓度为3.0g/l的脂蛋白残粒胆固醇单克隆抗体以及浓度为0.3g/l的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐。
以上测定脂蛋白残粒胆固醇的浓度的试剂盒的制备方法,包括如下步骤,
a)、试剂r1制备;
在配液罐中先加入适量纯化水于磁力搅拌器上,调节搅拌子至中档转速,使溶液保持中速转动状态,边搅拌边投入浓度为3.2g/l二水合磷酸二氢钠和浓度为8.75g/l的十二水合磷酸氢二钠,搅拌5分钟至物料完全溶解,溶液清澈透明配液罐底部无沉淀后,调节ph值为7.3,之后投入浓度为20g/l的氯化钠,待物料完全溶解后,再按照上述投料方式依次投入peg6000和proclin-300,以上两者的浓度分别为80g/l和0.8%,投料完成后,继续搅拌30分钟至全部物料完全溶解,溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放在成品罐中,进行标识;
b)、试剂r2制备;
b1、缓冲液配制,在配液罐中先加入适量纯化水于磁力搅拌器上,打开磁力搅拌器电源开关,调节搅拌子至中档转速,使溶液保持中速转动状态,以27.3g/l的标准,边搅拌边投入2-(n-吗啉)乙磺酸一水合物,搅拌30分钟至物料完全溶解,溶液清澈透明配液罐底部无沉淀后,调节ph值到7,继续搅拌18分钟至溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放在成品罐中,进行标识;
b2、保存液配制,在配液罐中先加入适量纯化水于磁力搅拌器上,调节搅拌子至中档转速,使溶液保持中速转动状态,以5.0g/l的标准边搅拌边投入n,n-二羟乙基甘氨酸,搅拌18分钟至物料完全溶解,调节ph值为7,之后以2.0g/l标准,投入酪蛋白,待物料完全溶解后,再以2.0ml/l标准,投入proclin-300,继续搅拌18分钟至全部物料完全溶解,溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放备用,进行标识;
b3、胶乳微球抗体偶联物的制备,胶乳微球所选粒径为190nm,其表面修饰基团为氨基,将胶乳微球以缓冲液稀释到0.01%的浓度,再以1:1比例与链霉亲和素结合,将脂蛋白残粒胆固醇单克隆抗体以反应液稀释到3.0g/l的浓度,与生物素按3:1的比例结合后,加入到含有链霉亲和素的微球中,混匀,链霉亲和素结合生物素-rlp-c单克隆抗体比例为4:1,将1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐以反应液溶解到0.3g/l的浓度,边摇匀边滴加入上述混合溶液中,室温反应120分钟,加入酪蛋白封闭,振荡混匀,室温反应60分钟,将混合液以14000rpm的转速离心30分钟,吸去上清液,加入保存液,超声重悬,重复离心清洗3次,最后一次离心去上清液后,加入保存液,超声重悬,将制备好的r2装入成品罐中,进行标识。
实施例3
一种测定脂蛋白残粒胆固醇的浓度的试剂盒,包括试剂r1和试剂r2,所述试剂r1的各组分及浓度包括作为第一缓冲液a的二水合磷酸二氢钠,其浓度为2g/l,作为第一缓冲液b的十二水合磷酸氢二钠,其浓度为16g/l,作为第一电解质的氯化钠,其浓度为12g/l,作为第一高分子促进剂的peg6000,其浓度为120g/l,作为第一防腐剂的硫柳汞,其浓度为1.0%,所述试剂r2包括第二缓冲液、保存液、偶联有rlp-c单克隆抗体-生物素-链霉亲和素的胶乳微球,所述第二缓冲液为2-(n-吗啉)乙磺酸一水合物,其浓度为16.80g/l;所述保存液包括:浓度为1.26g/l的n,n-二羟乙基甘氨酸、作为稳定剂的甘露醇,其浓度为1.2g/l的,作为第二防腐剂的叠氮钠,其浓度为1.5ml/l;胶乳微球偶联物的各组份及浓度包括:浓度为1.5%的胶乳微球,浓度为13g/l的生物素,浓度为13g/l的链霉亲和素,浓度为1.5g/l的脂蛋白残粒胆固醇单克隆抗体以及浓度为0.15g/l的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐。
以上测定脂蛋白残粒胆固醇的浓度的试剂盒的制备方法,包括如下步骤,
a)、试剂r1制备;
在配液罐中先加入适量纯化水于磁力搅拌器上,调节搅拌子至中档转速,使溶液保持中速转动状态,边搅拌边投入浓度为2g/l二水合磷酸二氢钠和浓度为16g/l的十二水合磷酸氢二钠,搅拌18分钟至物料完全溶解,溶液清澈透明配液罐底部无沉淀后,调节ph值为8.0,之后投入浓度为12g/l的氯化钠,待物料完全溶解后,再按照上述投料方式依次投入peg6000和硫柳汞,以上两者的浓度分别为120g/l和1.0%,投料完成后,继续搅拌18分钟至全部物料完全溶解,溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放在成品罐中,进行标识;
b)、试剂r2制备;
b1、缓冲液配制,在配液罐中先加入适量纯化水于磁力搅拌器上,打开磁力搅拌器电源开关,调节搅拌子至中档转速,使溶液保持中速转动状态,以16.8g/l的标准,边搅拌边投入2-(n-吗啉)乙磺酸一水合物,搅拌18分钟至物料完全溶解,溶液清澈透明配液罐底部无沉淀后,调节ph值到7,继续搅拌30分钟至溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放在成品罐中,进行标识;
b2、保存液配制,在配液罐中先加入适量纯化水于磁力搅拌器上,调节搅拌子至中档转速,使溶液保持中速转动状态,以1.26g/l的标准边搅拌边投入n,n-二羟乙基甘氨酸,搅拌30分钟至物料完全溶解,调节ph值为8.5,之后以1.2g/l标准,投入甘露醇,待物料完全溶解后,再以1.5ml/l标准,投入叠氮钠,继续搅拌5分钟至全部物料完全溶解,溶液清澈透明,配液罐底部无沉淀,定容至最终体积;
溶解完的配液按照微孔过滤器操作规程,通过微孔滤膜过滤,过滤后的溶液存放备用,进行标识;
b3、胶乳微球抗体偶联物的制备,胶乳微球所选粒径为280nm,其表面修饰基团为羧基将胶乳微球以缓冲液稀释到1.5%的浓度,再以1:1比例与链霉亲和素结合,将脂蛋白残粒胆固醇单克隆抗体以反应液稀释到3g/l的浓度,与生物素按1:1的比例结合后,加入到含有链霉亲和素的微球中,混匀,链霉亲和素结合生物素-rlp-c单克隆抗体比例为0.5:1,将1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐以反应液溶解到0.15g/l的浓度,边摇匀边滴加入上述混合溶液中,室温反应140分钟,加入甘露醇封闭,振荡混匀,室温反应100分钟,将混合液以14000rpm的转速离心40分钟,吸去上清液,加入保存液,超声重悬,重复离心清洗3次,最后一次离心去上清液后,加入保存液,超声重悬,将制备好的r2装入成品罐中,进行标识。
实施例4
本发明一种测定脂蛋白残粒胆固醇的浓度的试剂盒的应用,其工作原理是:一分子链霉亲和素可以高度特异性地与四分子生物素结合,两者之间的亲和力极为强烈,形成级联放大反应。检测样本中脂蛋白残粒胆固醇(rlp-c)与其相应的链霉亲和素-生物素-rlp-c抗体在溶液中相遇,采用级联放大反应,形成抗原-抗体复合物,使乳胶颗粒发生凝集,产生浊度变化。该浊度变化的高低在足量抗体存在时与样本中rlp-c的含量成正比,在340nm波长下,通过与已知浓度的校准品比较,可定量检测出样品中rlp-c的含量。
具体测定结果比较如下:
r2试剂采用胶乳微球直接偶联rlp-c单克隆抗体试剂盒,使用标准品进行定标,结果如表1所示,定标曲线如图1所示。
表1、r2试剂未采用级联放大偶联,胶乳微球直接偶联rlp-c单克隆抗体定标结果:
结果解析:如图1和表1所示,线性范围可做到0.1-8mg/l,浓度大于4mg/l时出现hook效应。
r2试剂采用胶乳微球间接偶联rlp-c单克隆抗体试剂盒,使用标准品进行定标,结果如表2所示,定标曲线如图2所示。
表2、r2试剂采用级联放大偶联,胶乳微球间接偶联rlp-c单克隆抗体定标结果:
结果解析:如图2和表2所示,线性范围可做到0.1-8mg/l。
实施例5
精密度cv检测:
r2试剂采用胶乳微球直接偶联rlp-c单克隆抗体试剂盒,随机取3份份临床血清样本,使用全自动生化分析仪对同一样本重复检测10次,检测结果如表3所示。
表3:检测样本的脂蛋白残粒胆固醇含量(10次)及变异系数
结果解析:精密度cv较大,基本>5%。
r2试剂采用胶乳微球间接偶联rlp-c单克隆抗体的试剂盒,随机取3份临床血清样本,使用全自动生化分析仪对同一样本重复检测10次,检测结果如表4所示。
表4:检测样本的脂蛋白残粒胆固醇含量(10次)及变异系数
结果解析:精密度cv明显改善,4%以内。
结论:采用胶乳微球间接偶联rlp-c单克隆抗体的试剂盒,即胶乳微球连接链霉亲和素1:1,rlp-c单克隆抗体连接生物素1:2,二者再以1:1混合反应,可明显改善重复性和灵敏度,线性范围可做到0.1-8mg/l。
以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明所述原理的前提下,还可以作出若干改进或替换,这些改进或替换也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!