复合荧光基底、复合荧光基底的制备方法以及应用与流程
本发明涉及食品中非法添加剂检测的技术领域,尤其涉及罗丹明b的检测的技术领域,具体而言,涉及复合荧光基底、复合荧光基底的制备方法以及应用。
背景技术:
如今用于食品中非法添加剂检测的仪器分析技术主要有光谱技术,包括紫外-可见吸收光谱法(μv-vis)、原子吸收光谱法(aas)等;色谱分析最常用的是高效液相、气相色谱法,气相色谱一质谱联用技术(gc-ms);电化学技术主要应用的是高效毛细管电泳法(ce)。这些方法的精密度能够满足实验的要求,最低检测限也可满足痕量分析需要,但是却存在着适用范围窄、设备昂贵、操作复杂、成本高等问题;并且大多数色谱分析需要专门的检测仪器,对检测人员的要求也高,所以不适合大批量现场快速检测。在快速检测方面,有根据固相萃取原理开发出来的快速检测法,但该法主要是根据肉眼观察固相萃取柱上的红色条带进行判断,易出现假阳性,准确度低,检测灵敏度也不高。因此,在食品中建立一种对非法添加剂能进行快速可靠的新型检测方法至关重要。
分子印迹聚合物(molecularlyimprintedpolymer,简称mip)为具有特异性识别和选择性吸附的聚合物。分子印迹固相萃取(molecularlyimprintedsolidphaseextraction,简称mispe)是近年发展起来的一种新型样品前处理技术,它利用mip的特异选择性吸附机理制备固相萃取材料,由于mip对模板分子具有特异选择性和亲合性,而且其受酸、碱、有机溶剂和加热等环境因素影响很小,可以克服食品样品体系复杂、预处理程序烦琐等不利因素,实现复杂食品样品基体中低浓度目标物的分离富集,提高固相萃取的净化效果及分析检测方法的灵敏度和准确性。
采用mip对目标物进行检测时首先需要对样品进行预处理,即首先通过溶剂溶解样品表面的目标物,经过滤、离心后进行萃取,得到含有目标物的有机液,然后将有机液通过填充有mip材料的固相流动柱,使得有机液中的目标物被mip材料吸附,然后进行检测。可见,采用mip对目标物进行检测需要大量的预处理时间,且预处理过程操作复杂、重现性差。
技术实现要素:
本发明的主要目的在于提供复合荧光基底、复合荧光基底的制备方法以及应用,以解决现有技术中分子印迹聚合物测试样品中的目标物时对样品的预处理时间过长且预处理过程复杂的技术问题。
为了实现上述目的,根据本发明的一个方面,提供了一种复合荧光基底。该复合荧光基底包括凝胶和附着在所述凝胶的孔隙表面的分子印迹聚合物材料。
首先,本发明的复合荧光基底用于进行固体表面荧光光谱检测,具有简单快速、灵敏度高的优点。其次,利用mip材料专一性强的特点,解决了荧光光谱范围较宽无法准确确定是哪种物质的缺点,在实际检测过程中对待测样品能进行更多地富集。再者,抗干扰性能较强,能够快速地对待测样品进行痕量定性检测。同时,凝胶具有三维网状结构,能够提供较大的比表面积来附着mip材料;由于基底具有凝胶,而凝胶具有粘性且为固状,当凝胶与mip材料协同作用时,不仅能够通过切取的方式随取随用,而且还能通过擦拭待测样品表面的方式快速富集目标物,并利用固体表面荧光可直接测定固体样品的优势,快速取样和测试,与现有技术相比,无需对样品进行复杂的预处理即可实现对目标物的快速检测。
进一步地,所述凝胶为pva凝胶;所述分子印迹聚合物为罗丹明b分子印迹聚合物。pva(聚乙烯醇)凝胶易获取且状态稳定,由此,实现对罗丹明b(表示为rhb,下同)的快速检测。
进一步地,所述罗丹明b分子印迹聚合物与pva的质量比为(0.05-1):(0.2-1);还包括四硼酸钠(分子式:na2b4o7·10h2o)。罗丹明b分子印迹聚合物的含量过高,可能会影响pva凝胶的稳定性;罗丹明b分子印迹聚合物过低,则富集目标物的能力较差。由此,罗丹明b分子印迹聚合物在pva凝胶中分布均匀且所得复合荧光基底对目标物的富集能力强。采用四硼酸钠为助凝剂,能够快速获得稳定的pva凝胶。
进一步地,pva与四硼酸钠的质量比为(1-5):(0.4-2)。经验证,当pva与四硼酸钠的质量比为(1-5):(0.4-2)时,所得复合荧光基底的荧光信号最好。
为了实现上述目的,根据本发明的另一个方面,还提供了一种复合荧光基底的制备方法,包括以下步骤:
(1)获取包括凝胶前驱体和分子印迹聚合物材料的混合溶液;
(2)加入使凝胶前驱体凝胶化成凝胶的助凝剂,搅拌至形成凝胶,即得到复合荧光基底。
本发明的复合荧光基底的制备方法的工艺非常简单,所需合成时间短,所得复合荧光基底稳定性好,具有适宜的硬度和粘度,可快速取样和测试,无需对样品进行复杂的预处理即可实现对目标物的快速检测。
进一步地,所述凝胶为pva凝胶,所述助凝剂为四硼酸钠;所述分子印迹聚合物为罗丹明b分子印迹聚合物。
进一步地,步骤(1)具体包括:首先获取pva溶液,然后将罗丹明b分子印迹聚合物加入到所述pva溶液中;所述pva溶液中pva的质量分数为4%-10%;混合溶液中pva的充分溶解和均匀分散有助于pva的凝胶,与pva和分子印迹聚合物材料直接共混的工艺相比,通过先先获取pva溶液、后分散分子印迹聚合物,可以避免分子印迹聚合物对pva溶解度的影响,从而获得快速获得稳定的凝胶。
进一步地,所述四硼酸钠被配置成溶液后加入到pva溶液中,pva与四硼酸钠的质量比为(1-5):(0.4-2)。通过将四硼酸钠溶解后再加入,可以使四硼酸钠快速均匀地分布于pva溶液中,有助于获得快速获得各处性能一致的基底。
进一步地,所述罗丹明b分子印迹聚合物的制备以sio2为载体、甲基丙烯酸(表示为:maa,下同)为功能单体、乙二醇二甲基丙烯酸(表示为:egdma,下同)为交联剂、乙腈为致孔剂和2,2’-偶氮二异丁腈(表示为:aibn,下同)为引发剂。由此,获得印迹位点明显高于传统分子印迹聚合物的表面分子印迹聚合物材料(surfacemolecularimprintedpolymer,简称smip)。
为了实现上述目的,根据本发明的另一个方面,还提供了一种罗丹明b的检测方法,包括步骤:
(1)切取复合荧光基底,所述复合荧光基底为上述的复合荧光基底或采用上述的制备方法制备得到的复合荧光基底,所述分子印迹聚合物为罗丹明b分子印迹聚合物;
(2)将切取的复合荧光基底对待测样品表面进行擦拭;
(3)对擦拭后的复合荧光基底进行固体表面荧光检测,即得到待测样品表面的罗丹明b浓度。
可见,采用本发明的复合荧光基底或本发明的制备方法制备得到的荧光基底,通过擦拭的方式即可快速富集待测样品中的目标物,然后通过故乡荧光光谱即可快速检测出待测样品表面的目标物浓度,与传统方法相比,无需对待测样品进行复杂的预处理,实现快速、高效、精确的检测。
进一步地,所述擦拭的具体过程如下:首先在待测样品表面喷洒溶剂,然后使所述复合荧光基底隔着无尘纸在待测样品表面进行擦拭。由此,不仅可以快速富集目标物,而且还能避免杂质对测试结果产生影响。
可见,本发明的复合荧光基底、复合荧光基底的制备方法以及应用能够可快速取样和测试,无需对样品进行复杂的预处理即可实现对目标物的快速检测。
下面结合附图和具体实施方式对本发明做进一步的说明。本发明附加的方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
构成本发明的一部分的附图用来辅助对本发明的理解,附图中所提供的内容及其在本发明中有关的说明可用于解释本发明,但不构成对本发明的不当限定。在附图中:
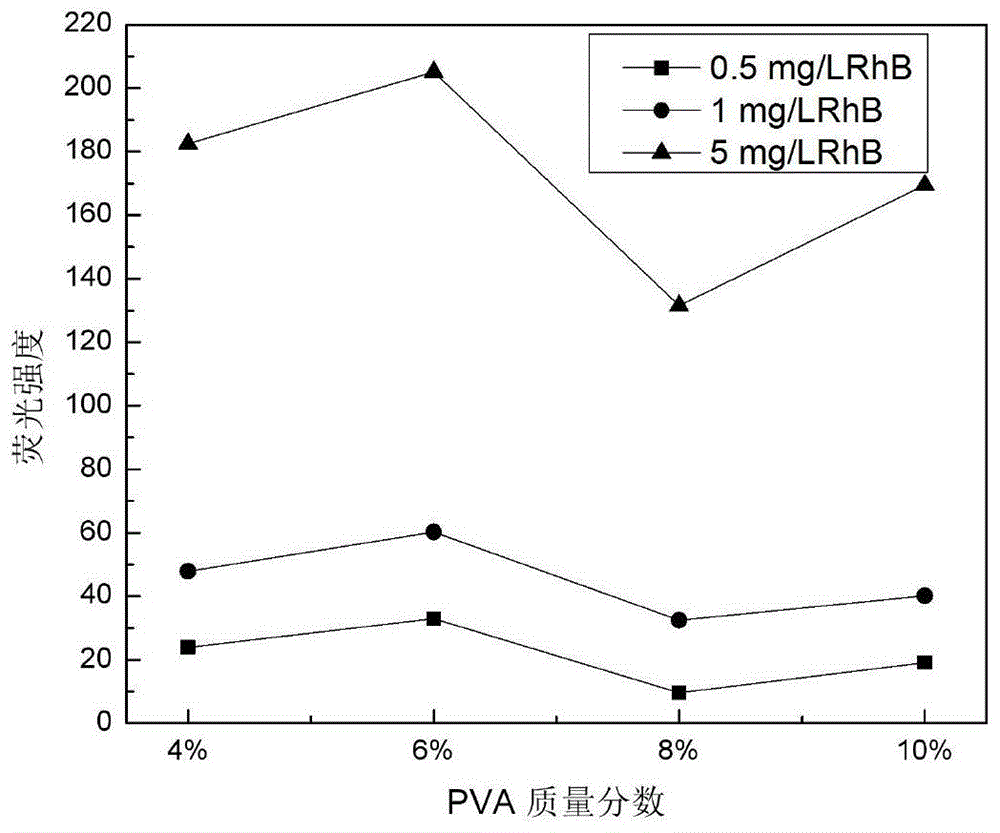
图1为实施例1-5的复合荧光基底(表示为rhb-smips-pva凝胶基底,下同)的荧光测试结果。
图2为实施例3、实施例6-8的rhb-smips-pva凝胶基底的荧光测试结果。
图3为实施例3、实施例9-12的rhb-smips-pva凝胶基底的荧光测试结果。
图4为实施例3的rhb-smips-pva凝胶基底对不同浓度的rhb溶液的荧光测试结果,其中,曲线a-k分别对应于10mg/l、8mg/l、6mg/l、4mg/l、2mg/l、1mg/l、0.8mg/l、0.6mg/l、0.4mg/l、0.2mg/l、0.1mg/l的rhb溶液。
图5为实施例3的rhb-smips-pva凝胶基底和对照例1的pva凝胶基底对不同浓度的rhb溶液的荧光测试结果。
图6为实施例3的rhb-smips-pva凝胶基底和对照例1的pva凝胶基底对不同浓度的rh6g溶液的荧光测试结果。
图7为实施例3的rhb-smips-pva凝胶基底对不同色素的荧光测试结果。
图8为实施例3的rhb-smips-pva凝胶基底检测辣椒粉表面rhb的检测结果,其中,曲线a-e分别为0.5mg/lrhb浸泡的辣椒粉、1mg/lrhb浸泡的辣椒粉、5mg/lrhb浸泡的辣椒、10mg/lrhb浸泡的辣椒粉、未浸泡的辣椒粉。
图9是sio2-kh570的sem照片,内置图为局部放大图。
图10是洗脱前的rhb-smips的sem照片。
图11是洗掉模板分子rhb后的rhb-smips的sem照片,内置图为局部放大图。
图12是对照例1的pva凝胶基底的sem照片。
图13是实施例3的rhb-smips-pva凝胶基底的sem照片,内置图为局部放大图。
具体实施方式
下面结合附图对本发明进行清楚、完整的说明。本领域普通技术人员在基于这些说明的情况下将能够实现本发明。在结合附图对本发明进行说明前,需要特别指出的是:
本发明中在包括下述说明在内的各部分中所提供的技术方案和技术特征,在不冲突的情况下,这些技术方案和技术特征可以相互组合。
此外,下述说明中涉及到的本发明的实施例通常仅是本发明一部分的实施例,而不是全部的实施例。因此,基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都应当属于本发明保护的范围。
关于本发明中术语和单位。本发明的说明书和权利要求书及有关的部分中的术语“包括”、“具有”以及它们的任何变形,意图在于覆盖不排他的包含。
实施例1
称取0.2g的pva溶于10ml超纯水中得到质量分数为2%的pva溶液,接着称取0.05g的罗丹明b分子印迹聚合物(rhb-smips)粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva的混合溶液与0.4ml的四硼酸钠溶液混合,通过实验发现该质量比的pva溶液与四硼酸钠溶液混合后无法成胶。
实施例2
称取0.4g的pva溶于10ml超纯水中得到质量分数为4%的pva溶液,接着称取0.05g的rhb-smips粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva混合溶液与0.4ml的四硼酸钠溶液混合,用玻璃棒搅拌直至形成具有良好可变形功能的凝胶,即得到rhb-smips-pva凝胶基底。
实施例3
称取0.6g的pva溶于10ml超纯水中得到质量分数为6%的pva溶液,接着称取0.05的rhb-smips粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva的混合溶液与0.4ml的四硼酸钠溶液混合,用玻璃棒搅拌直至形成具有良好可变形功能的凝胶,即得到rhb-smips-pva凝胶基底。
实施例4
称取0.8g的pva溶于10ml超纯水中得到质量分数为8%的pva溶液,接着称取0.05g的rhb-smips粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva的混合溶液与0.4ml的四硼酸钠溶液混合,用玻璃棒搅拌直至形成具有良好可变形功能的凝胶,即得到rhb-smips-pva凝胶基底。
实施例5
称取1g的pva溶于10ml超纯水中得到质量分数为10%的pva溶液,接着称取0.05g的rhb-smips粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva的混合溶液与0.4ml的四硼酸钠溶液混合,用玻璃棒搅拌直至形成具有良好可变形功能的凝胶,即得到rhb-smips-pva凝胶基底。
分别配置0.5mg/l、1mg/l、5mg/l的rhb标准溶液,将其滴在实施例1-5的,即得到rhb-smips-pva凝胶基底上后进行荧光检测,测试结果如图1所示,可以发现当pva质量比为6%时,荧光信号最好。
实施例6
称取0.6g的pva溶于10ml超纯水中得到质量分数为6%的pva溶液,接着称取0.005g的rhb-smips粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva的混合溶液与0.4ml的四硼酸钠溶液混合,用玻璃棒搅拌直至形成具有良好可变形功能的凝胶,即得到rhb-smips-pva凝胶基底。
实施例7
称取0.6g的pva溶于10ml超纯水中得到质量分数为6%的pva溶液,接着称取0.01g的rhb-smips粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva的混合溶液与0.4ml的四硼酸钠溶液混合,用玻璃棒搅拌直至形成具有良好可变形功能的凝胶,即得到rhb-smips-pva凝胶基底。
实施例8
称取0.6g的pva溶于10ml超纯水中得到质量分数为6%的pva溶液,接着称取0.1g的rhb-smips粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva的混合溶液与0.4ml的四硼酸钠溶液混合,用玻璃棒搅拌直至形成具有良好可变形功能的凝胶,即得到rhb-smips-pva凝胶基底。
分别配置0.5mg/l、1mg/l、5mg/l的rhb标准溶液,将其滴在实施例3、实施例6-8的rhb-smips-pva凝胶基底后进行荧光检测,测试结果如图2所示,可以发现当rhb-smips粉末添加量为0.05g时,荧光信号最好。
实施例9
称取0.6g的pva溶于10ml超纯水中得到质量分数为6%的pva溶液,接着称取0.05g的rhb-smips粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva的混合溶液与0.2ml的四硼酸钠溶液混合,用玻璃棒搅拌直至形成具有良好可变形功能的凝胶,即得到rhb-smips-pva凝胶基底。
实施例10
称取0.6g的pva溶于10ml超纯水中得到质量分数为6%的pva溶液,接着称取0.05g的rhb-smips粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva的混合溶液与0.6ml的四硼酸钠溶液混合,用玻璃棒搅拌直至形成具有良好可变形功能的凝胶,即得到rhb-smips-pva凝胶基底。
实施例11
称取0.6g的pva溶于10ml超纯水中得到质量分数为6%的pva溶液,接着称取0.05g的rhb-smips粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva的混合溶液与0.8ml的四硼酸钠溶液混合,用玻璃棒搅拌直至形成具有良好可变形功能的凝胶,即得到rhb-smips-pva凝胶基底。
实施例12
称取0.6g的pva溶于10ml超纯水中得到质量分数为6%的pva溶液,接着称取0.05g的rhb-smips粉末加入到1mlpva溶液中,搅拌使其均匀分散,得到混合溶液。然后称取0.4g的四硼酸钠溶于10ml超纯水中得到四硼酸钠溶液。取1ml的rhb-smips和pva的混合溶液与1ml的四硼酸钠溶液混合,用玻璃棒搅拌直至形成具有良好可变形功能的凝胶,即得到rhb-smips-pva凝胶基底。
分别配置0.5mg/l、1mg/l、5mg/l的rhb标准溶液,将其滴在实施例3、实施例9-12的rhb-smips-pva凝胶基底上后进行荧光检测,测试结果如图3所示。图3中的横坐标为pva溶液与四硼酸钠溶液的体积比,对应的质量比分别为3:0.4、3:0.8、3:1.2、3:1.6、3:2。从图3可以看出,pva溶液与四硼酸钠溶液的体积比为10:4(质量比为3:0.8)时,荧光信号最好。
为了检测本发明的rhb-smips-pva凝胶基底对rhb的最低检出限,配置了0.1-10mg/l浓度梯度的rhb溶液,分别取5ul该溶液滴加在0.03g的实施例3的rhb-smips-pva凝胶基底上,待吸附完全后,进行荧光检测。检测结果如图4所示,可以看出该rhb-smips-pva凝胶基底能检测到浓度为0.1mg/l的rhb溶液中的rhb。对比赵晨等人所制备的罗丹明b的分子印迹聚合物(赵晨,贾光锋,陆文总,等.罗丹明b表面分子印迹聚合物制备及其荧光检测[j].食品科学,2014,35(20):236-241)能检测到的最低浓度也为0.1mg/l的rhb,可见,本发明的rhb-smips-pva凝胶基底中凝胶不仅没有影响rhb-smips的专一性,而且显著提升了检测速度。
为了验证rhb-smips-pva凝胶基底对rhb吸附的专一性,我们选取了与rhb结构类似的染料,即罗丹明6g(rh6g)作为对照。由于rh6g的分子结构与rhb非常相似,在水溶液中都具有强烈的荧光,其荧光波长范围也接近于rhb,所以经常对rhb的检测造成干扰。具体过程如下:
首先进行实施例3的对照例,即对照例1,区别在于对照例1中不含有rhb-smips。接着分别用对照例1的pva凝胶基底和实施例3的rhb-smips-pva凝胶基底去吸附浓度分别为10mg/l、20mg/l、40mg/l、50mg/l、80mg/l的rhb和rh6g溶液,最后进行荧光检测,检测结果如图5和图6所示。
rhb-smips的特异性可以通过增强因子α来确定:
α=im/in
式中:im表示实施例3的rhb-smips-pva凝胶基底测出的荧光信号强度,in表示对照例1的pva凝胶基底测出的荧光信号强度。
转化为增强因子后的测试结果见表1。
表1
从表1中rhb及rh6g的α值可以看出,rhb的α值一直大于rh6g的α值,说明mip材料在凝胶中对于rhb的吸附起到了显著的效果。
同时,由于市场上的食品中往往会添加类似于rhb的其他红色染料,从而对rhb的检测造成干扰,我们选取常用于食品染色,与rhb颜色相似,在rhb检测过程中进行干扰的日落黄(sunsetyellow)、苏丹ⅰ(sudanⅰ)、苏丹ⅳ(sudanⅳ)作为对比。图7中显示了在相同浓度10mg/l下,对照例1的pva凝胶基底和实施例3的rhb-smips-pva凝胶基底对rhb、日落黄、苏丹ⅰ、苏丹ⅳ的吸附作用。可以看出,在有mip材料的凝胶基底中,rhb的信号相较于其他三种色素有明显的增强。
我们同样通过计算增强因子来对结果进行评估,结果如表2所示。
表2
从表2中可以看出,rhb的增强因子最高,而其他色素的增强因子几乎等于1,这意味着实施例3的rhb-smips-pva凝胶基底对rhb的抗干扰能力很强。
为了验证上述rhb-smips-pva凝胶基底能够很好地运用于实际样品的检测,进行如下测试:分别称取0.5g的辣椒粉浸泡在0.5mg/l、1mg/l、5mg/l、10mg/l的rhb溶液中制备成加标样,烘干备用。在待测样品上喷洒适量的酒精,取0.03g的实施例3的rhb-smips-pva凝胶基底隔着无尘纸在待测样品表面反复擦拭,对样品上的rhb富集,最后将采样后的基底放置在固体支架上进行荧光检测。测试结果如图8所示,可以看出,该方均能检测到实际样品上最低至0.5mg/kg的rhb。对比荫硕焱等人在2015年对市场上干辣椒及辣椒粉中罗丹明b含量的调查与分析(荫硕焱,贺巍巍,蒋定国,等.干辣椒及辣椒粉中罗丹明b含量的调查与分析[j].中国食品卫生杂志,2015,27(3):297-301)可以发现,本发明的rhb-smips-pva凝胶基底的最低检出限在市场上实际样品中的rhb检出含量范围内。并且相较于其运用超高效液相色谱-质谱/质谱联用仪繁琐的预处理方法,本发明的rhb-smips-pva凝胶基底能在几分钟内实现样品的采样与检测,节省了大量时间。
上述实施例的rhb-smips的制备方法如下:
取1.5g的sio2粒子与50ml无水甲苯加入锥形瓶中,超声20min,室温下磁力搅拌1h.。将5mlkh570(硅烷偶联剂)逐滴加入锥形瓶,在锥形瓶中通入氮气排尽空气后密封,磁力搅拌15个小时。将经过kh570改性后的sio2用无水甲苯洗涤后离心,再用无水乙醇洗涤多次后离心,得到sio2-kh570。另取一个锥形瓶,向其中加入10ml乙腈、2mgrhb、94ulmaa,室温氮气保护下磁力搅拌12h。然后继续向里面加入24mgsio2-kh570、0.875mlegdma、15mgaibn,75℃氮气保护下磁力搅拌24h,得到rhb-smips。用甲醇洗涤rhb-smips,多次超声后离心直至将rhb洗掉。洗脱后的rhb-smips烘干,碾碎成粉末状。
图9是sio2-kh570的sem照片,可以看出经过kh570的表面改性后,使其表面覆盖了硅烷偶联剂的有机官能团。图10是洗脱前的rhb-smips的sem照片,可以看出通过一系列交联作用,在sio2表面覆盖了一层有机物。图11是洗掉模板分子rhb后的rhb-smips的sem照片,可以看出材料中形成了很多空腔,留下了rhb的结合位点。
图12是对照例1的pva凝胶基底的sem照片,可以看到pva凝胶基底具有网状结构,可为基底的吸附作用提供很高的比表面积。图13是实施例3的rhb-smips-pva凝胶基底的sem照片,可以看到rhb-smips均匀地嵌在了pva凝胶中,在对rhb进行特异性吸附时起到了至关重要的作用。
以上对本发明的有关内容进行了说明。本领域普通技术人员在基于这些说明的情况下将能够实现本发明。基于本发明的上述内容,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都应当属于本发明保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!