一种凝固酶检测试纸的制备方法与流程
本发明属于体外诊断试剂
技术领域:
,具体涉及一种凝固酶检测试纸的制备方法。
背景技术:
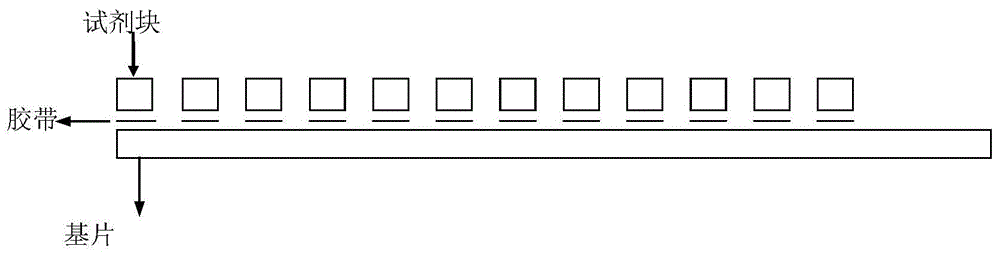
:细菌性阴道病(bv)是由多种细菌所致的无阴道粘膜炎症表现的临床综合征,临床上发病人数远远高于滴虫性阴道炎、真菌性阴道炎。由于bv与早产、绒毛膜羊膜炎、产后子宫内膜炎等产科及多种妇科疾病有关,因此越来越受到临床医生及学者的广泛重视。近年来的研究发现,引起阴道细菌感染的细菌有两大类,一类是由厌氧菌和兼性厌氧菌引起,临床上称细菌性阴道病(bv);另一类是由需氧型菌引起,临床上称需氧阴道炎(av)(是比利时著名妇产科专家donders于2002年正式报道的一种下生殖道感染),女性下生殖道多数为此两类细菌性感染,也是妇科门诊的常见病和多发病,此外常见的下生殖道感染主要还有外阴阴道假丝酵母菌病(vvc)、滴虫性阴道炎(tv)等。细菌性阴道病(bv)易感染粪肠球菌、大肠埃希氏菌等需氧菌。而正常阴道是以乳酸杆菌为优势菌的正常微生物群,阴道ph<4.5,当患有需氧菌性阴道炎时,阴道乳酸杆菌减少而需氧菌繁殖导致阴道壁粘膜具有充血、水肿、脓性分泌物的炎性特征。细菌预成酶是细菌在生长繁殖过程中合成的一系列与生长代谢有关的酶类,这些酶类能分解多种底物,并且在有氧环境中较长时间的保留其活性。不同种属的细菌,其预成酶的种类不同。bv其主要预成酶为唾液酸苷酶,av其主要预成酶为β-葡萄糖醛酸苷酶和凝固酶。bv的主要致病菌为粪肠球菌、大肠埃希氏菌,而大肠埃希菌代谢可产生凝固酶。目前国际公认的av的诊断主要采用gilbert提出的,经过tempera等学者修订的综合诊断方法,其诊断标准为:①常阴道黄色分泌物;②阴道ph升高>5.0;③分泌物有异味,koh试验阴性;④阴道分泌物高倍镜检发现大量白细胞;⑤donderav评分>1分。其中,av评分为必备指标,但av评分十分复杂,需综合阴道分泌物中乳酸杆菌分级、白细胞数量以及中毒白细胞所占比例、背景菌落数等指标,此法不适于在临床常规检验,特别是医院门诊等的使用。近年来,人们越来越重视对阴道疾病的研究,厌氧菌和兼性厌氧菌阴道炎患者阴道微生态环境均处于异常状态,其阴道微生态环境失衡特点主要表现为易感染粪肠球菌、大肠埃希氏菌等需氧菌,而乳酸杆菌等优势菌缺失明显并伴有阴道ph值升高(ph>6.0),所以大部分阴道炎都是由这些致菌菌群之间的比例失调引起的内源性感染。此外,在国内的临床中,粪肠球菌和大肠埃希氏菌在阴道炎中感染率极高。而凝固酶鉴定阴道分泌物中需氧菌群,具有很高的敏感度和专属的特异性,特别是针对粪肠球菌和大肠埃希氏菌等需养菌群有一定的诊断意义。技术实现要素:本发明的目的是提供一种凝固酶检测试纸的制备方法,制备的检测试纸具有检测速度快,灵敏度高、特异性好的优势,与类似产品相比操作简单,适宜普及。为了实现上述目的,本发明的技术方案具体如下:一种凝固酶检测试纸的制备方法,包括以下步骤:步骤1、浸液的制备所述浸液包括底物、缓冲溶液、稳定剂和分散剂;将所述底物溶解到含有缓冲溶液、稳定剂和分散剂的溶液中,得到所述浸液;所述底物为甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐、甘氨酰-精氨酸-β-萘胺、香豆素衍生物或伞形酮衍生物;所述缓冲溶液为tris-hcl缓冲液、磷酸二氢钾-氢氧化钠缓冲液或硼酸-硼砂缓冲液;所述稳定剂为蔗糖、海藻糖、葡萄糖、乳糖、半乳糖或阿拉伯糖;所述分散剂为pvp-k30、pvp-k90、peg-2000、peg-4000和peg-6000中的一种或多种;步骤2、检测试纸的制备用步骤1制备的浸液采用浸渍干燥机自动化干燥方法浸润滤纸,制备得到所述检测试纸;浸渍干燥机温度设定:浸液:开机后将设备温度主加热设定60-80℃,副加热设定60℃,待主机加热温度达到60-80℃,各干燥室温度≥60℃时开始浸液;浸渍干燥机走速设定:7.0-11.0hz;步骤3、显色液的制备所述显色液包括显色剂、稳定剂和分散剂;所述显色剂、稳定剂和分散剂溶解到硫酸溶液或蒸馏水中,制备得到所述显色液;所述显色剂为二甲氨基肉桂醛、对二甲氨基苯甲醛、固蓝b盐、固红b盐、固蓝bb盐、固蓝rr盐、固红t或者固红tr;所述稳定剂为tritonx-100或者tritonx-200;所述分散剂为pvp-k30或者pvp-k90;所述显色液配合所述检测试纸共同检测分泌物中的凝固酶成分。在上述技术方案中,所述步骤2的具体步骤如下:步骤1、按开机流程将浸渍干燥机打开,将设备温度主加热设定60-80℃,副加热设定60℃,待主机加热温度达到60-80℃,各干燥室温度达到≥60℃时开始浸液;步骤2、将浸液使用的滤纸进行悬挂,浸液槽安装好;步骤3、将步骤1配制好的浸液倒入浸渍槽中,浸液量应在浸渍槽的1/2处,然后将剩余的浸液倒入盛药瓶中,调节浸液注入的速度,将盛药瓶密封;步骤4、开启走纸开关,用压纸轮将滤纸浸入浸液中,记录浸液位置高度;浸渍干燥机走速设定:7.0-11.0hz;步骤5、浸液烘干过程注意观察浸液剂量,干燥室温度符合要求;步骤6、浸液的滤纸全部从干燥室走出,关闭走纸开关,将滤纸做好标识,放入装有干燥剂的自封袋中并放入干燥器中待用。在上述技术方案中,所述主加热设定为65℃-75℃。在上述技术方案中,所述底物为甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐、甘氨酰-精氨酸-β-萘胺、甘氨酰-精氨酸-7-氨基-4-甲基香豆素、z-甘氨酰-精氨酸-对硝基苯胺或者甘氨酰-精氨酸-7-氨基-4-甲基伞形酮。在上述技术方案中,所述底物的浓度为1.0-10.0mg/ml,缓冲溶液的浓度为100-500mm、ph为5.0-10.0,稳定剂的浓度为1.00-20.00mg/ml,分散剂的浓度为1.00-20.00mg/ml。在上述技术方案中,所述缓冲溶液的浓度为200-400mm、ph为6.0-9.0。在上述技术方案中,步骤3中所述显色剂的浓度为1.0-5.0mg/ml,稳定剂的浓度为1.0-5.0mg/ml,分散剂的浓度为1.0-5.0mg/ml,硫酸溶液的浓度为0.1-3.0mg/ml。在上述技术方案中,检测体系ph值为6.0-9.0在上述技术方案中,所述滤纸的类型为7218型滤纸、31et型滤纸、3mm型滤纸、319型滤纸或者526型滤纸。本发明的有益效果是:本发明提供的凝固酶检测试纸的制备方法,所用浸液中缓冲体系为反应提供一个良好的中性至弱碱性反应环境;分散剂pvp-k30、pvp-k90、peg-2000peg-4000、peg-6000单独或联合使用可以增加试纸的分散能力,有助于颜色的均匀分布;稳定剂蔗糖、海藻糖、葡萄糖、乳糖、半乳糖、阿拉伯糖等可以保护样本中的酶类物质,提高检测的准确度;所用显色液中tritonx-100或tritonx-200;pvp-k30或pvp-k90,为试纸提高均匀度及稳定性提供一个良好的反应环境;本发明提供的一种凝固酶检测试纸的制备方法,采用浸渍干燥机自动化干燥方法制备检测试纸,浸渍干燥方式具有便捷、省时、可自动化的优势,有效控制试纸制备过程中人工误差带来的影响,浸渍干燥机主副加热,对温度全面进行监控,温度设定在规定的范围内,可以大大减少试纸批次之间的误差,保证试纸制备的准确性、稳定性及均一性。本发明依据甘氨酰-精胺酸-4-甲氧基-2-萘胺在凝固酶的水解作用下,产生4-甲氧基-2-萘胺,产物与肉桂醛类反应显色为原理,检测分泌物样本中凝固酶浓度,呈色深度与凝固酶活性成正比。本发明中试剂配制简便,使用方便,容易操作,检测时不需要显微镜等特殊设备,通过外加显色液的方式,检测时样品与试纸块接触,37℃温浴8-10min,试纸块由无色或浅黄色变为红色、紫红色、紫色,即判定为凝固酶阳性。本发明具有检测速度快,灵敏度高、特异性好的优势,与类似产品相比操作简单,适宜普及。本发明制备的凝固酶检测试纸可作为需氧性细菌性阴道炎(av)辅助评判指标,目前临床上av感染患者的临床症状体征和tv患者极为相似,若不明确诊断,易造成误诊,又因两者致病菌的抗生素敏感性不同,从而造成久治不愈,增加患者精神疾苦和医疗负担。现将国内外用于av诊断方法多数为镜检法,操作费时且存在误判或漏检的可能,因此将β-葡萄糖醛酸苷酶与凝固酶联合检测应用,可以大大提高分泌物检测结果的准确性,经大量临床实验证实,有形成分(如粪肠球菌和大肠埃希氏菌)镜下不宜观察,即使分辨率极高的电子设备也会造成一定误判,且与凝固酶、β-葡萄糖醛酸苷酶试纸之间并无完全对应关系,所以凝固酶试纸优势在于可以有效快速高灵敏的检测分泌物中凝固酶的含量,并联合β-葡萄糖醛酸苷酶检测结果及人工镜检,三者之间相互佐证,相辅相成,联合评判,对临床诊断具有重大意义。该方法操作简便快速,准确性高,不需要显微镜等特殊设备(采用荧光底物时需要荧光仪或紫外灯),在加热的情况下,8-10min内即可出结果;检测结果客观可靠,根据颜色变化判断结果,大大减少了检测人员主观因素的影响;操作简单,无需长时间的经验积累,易于推广应用,适于临床常规,特别是医院门诊的使用。附图说明下面结合附图和具体实施方式对本发明作进一步详细说明。图1为本发明制备的凝固酶检测试纸成品的结构示意图。图2为本发明采用浸渍干燥机自动化干燥方法制备检测试纸的干燥过程示意图。具体实施方式本发明的发明思想为:本发明的目的是提供一种凝固酶检测试纸的制备方法,本发明制备的检测凝固酶测定干化学试纸,包括分散在试纸块中固化的底物和外加的显色剂,所述底物为甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐、甘氨酰-精氨酸-β-萘胺、香豆素衍生物或伞形酮衍生物。所述固化的试纸块:即将底物先溶解于带缓冲液能力和辅助试剂的溶液中,形成浸液,将浸液浸润滤纸,进行干燥制备。所述浸液干燥的温度范围为60℃-80℃,最佳范围在65℃-75℃。所述带缓冲液能力的浸液的缓冲液ph范围在5.0-10.0,最佳范围在6.0-9.0,缓冲液浓度在100-500mm,最佳范围在200-400mm,经过裁切即成为一步法凝固酶检测干化学试纸块,用胶带将试纸块固定到基片聚苯乙烯材质白瓷片上得到检测试纸成品,其结构示意图参见图1。所述辅助试剂可以是稳定剂及分散剂。所述外加的显色液是所含对二甲氨基肉桂醛、对二甲氨基苯甲醛、固蓝b盐、固红b盐、固蓝bb盐、固蓝rr盐、固红t、固红tr等试剂水溶液,配合凝固酶干化学试纸共同诊断分泌物中凝固酶成分。凝固酶(coagulase)是一种能使含有枸橼酸钠或肝素抗凝剂的人或兔血浆发生凝固的酶类物质,促使血液凝固后可以保护病原菌不被吞噬或免受抗体等的作用。主要产生于葡萄球菌、鼠疫耶尔森菌、念珠菌等。凝固酶试纸检测原理(以甘氨酰-精胺酸-4-甲氧基-2-萘胺为底物举例):反应底物甘氨酰-精胺酸-4-甲氧基-2-萘胺在tris-hcl(ph=8.5)缓冲溶液中,在凝固酶的作用下水解生成4-甲氧基-2-萘胺,4-甲氧基-2-萘胺与二甲氨基肉桂醛反应生呈紫色或紫红色,呈色浓度与酶的活性成正比。若不显色或者呈现浅色标记为阴性,反之标记为阳性;若呈现阳性,则指示可能av感染(av的主要致病菌粪肠球菌、埃希氏大肠杆菌产生凝固酶gadp)。这种凝固酶干化学试纸条的简易测定方法为:取稀释的样本,滴加一滴在试纸块上,于37℃温浴8-10min后,外加一滴显色液,可观察凝固酶试纸块的的颜色变化,试纸块由无色/浅黄色变为红色、紫红色、紫色(不同重氮盐显色存在不同),即判定为凝固酶阳性。本发明优选所采用的技术方案是:浸液:缓冲溶液可以是200-400mm的tris-hcl缓冲液、磷酸二氢钾-氢氧化钠缓冲液或者硼酸-硼砂缓冲液;反应底物可以是1.0-10.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐、甘氨酰-精氨酸-β-萘胺、香豆素衍生物或伞形酮衍生物;优选所述底物为1.0-10.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐、甘氨酰-精氨酸-β-萘胺、甘氨酰-精氨酸-7-氨基-4-甲基香豆素、z-甘氨酰-精氨酸-对硝基苯胺或者甘氨酰-精氨酸-7-氨基-4-甲基伞形酮。辅助试剂稳定剂可以是1.00-20.00mg/ml蔗糖、海藻糖、葡萄糖、乳糖、半乳糖、阿拉伯糖;辅助试剂分散剂可以是1.00-20.00mg/mlpvp-k30、pvp-k90、peg-2000、peg-4000和peg-6000中的一种或多种;检测体系ph值为6.0-9.0;显色液:显色液主成分可以是1.0-5.0mg/ml二甲氨基肉桂醛、对二甲氨基苯甲醛、固蓝b盐、固红b盐、固蓝bb盐、固蓝rr盐、固红t或固红tr;其他反应试剂稳定剂成分可以是1.0-5.0mg/mltritonx-100或者tritonx-200;其他反应试剂分散剂成分可以是1.0-5.0mg/mlpvp-k30或者pvp-k90;溶液可以是0.1-3.0mg/ml硫酸溶液或蒸馏水;滤纸类型:7218型滤纸、31et型滤纸、3mm型滤纸、319型滤纸及526型滤纸等。配方优势分析:浸液中:缓冲体系为反应提供一个良好的中性至弱碱性反应环境;分散剂pvp-k30、pvp-k90、peg-2000、peg-4000和peg-6000单独或联合使用可以增加试纸的分散能力,有助于颜色的均匀分布;稳定剂蔗糖、海藻糖、葡萄糖、乳糖、半乳糖、阿拉伯糖等可以保护样本中的酶类物质,提高检测的准确度;显色液中:1.0-5.0mg/mltritonx-100或tritonx-200;1.0-5.0mg/mlpvp-k30或pvp-k90,为试纸提高均匀度及稳定性提供一个良好的反应环境;凝固酶检测试纸干燥方法为浸渍干燥机自动化干燥方法:浸渍干燥机温度设定:浸液:开机后将设备温度主加热设定60-80℃,副加热设定60℃,待主机加热温度达到60-80℃,各干燥室温度≥60℃左右时开始浸液;采用浸渍干燥机自动化干燥方法制备凝血酶检测试纸参见图2:具体包括以下步骤:步骤1、按开机流程将浸渍干燥机打开,将设备温度主加热设定60-80℃,副加热设定60℃,待主机加热温度达到60-80℃,各干燥室温度达到≥60℃时开始浸液;步骤2、将浸液使用的滤纸进行悬挂,浸液槽安装好;步骤3、将步骤1配制好的浸液倒入浸渍槽中,浸液量应在浸渍槽的1/2处,然后将剩余的浸液倒入盛药瓶中,调节浸液注入的速度,将盛药瓶密封;步骤4、开启走纸开关,用压纸轮将滤纸浸入浸液中,记录浸液位置高度;浸渍干燥机走速设定:7.0-11.0hz;步骤5、浸液烘干过程注意观察浸液剂量,干燥室温度符合要求;步骤6、浸液的滤纸全部从干燥室走出,关闭走纸开关,将滤纸做好标识,放入装有干燥剂的自封袋中并放入干燥器中待用。优选所述主加热设定为65℃-75℃。浸渍干燥方式具有便捷、省时、可自动化的优势,有效控制试纸制备过程中人工误差带来的影响,浸渍干燥机主副加热,对温度全面进行监控,温度设定在规定的范围内,可以大大减少试纸批次之间的误差,保证试纸制备的准确性、稳定性及均一性。浸渍干燥机走速设定:7.0-11.0hz。走速的设定是根据试纸在验证过程中逐步确认,走速的快慢会影响试纸的干燥程度,对试纸的外观及准确度有一定影响。显色液则按照配方进行配制即可。本发明的凝固酶检测试纸可作为需氧性细菌性阴道炎(av)辅助评判指标,目前临床上av感染患者的临床症状体征和tv患者极为相似,若不明确诊断,易造成误诊,又因两者致病菌的抗生素敏感性不同,从而造成久治不愈,增加患者精神疾苦和医疗负担。现将国内外用于av诊断方法多数为镜检法,操作费时且存在误判或漏检的可能,因此将β-葡萄糖醛酸苷酶与凝固酶联合检测应用,可以大大提高分泌物检测结果的准确性,经大量临床实验证实,有形成分(如粪肠球菌和大肠埃希氏菌)镜下不宜观察,即使分辨率极高的电子设备也会造成一定误判,且与凝固酶、β-葡萄糖醛酸苷酶试纸之间并无完全对应关系,所以凝固酶试纸优势在于可以有效快速高灵敏的检测分泌物中凝固酶的含量,并联合β-葡萄糖醛酸苷酶检测结果及人工镜检,三者之间相互佐证,相辅相成,联合评判,对临床诊断具有重大意义。该方法操作简便快速,准确性高,不需要显微镜等特殊设备(采用荧光底物时需要荧光仪或紫外灯),在加热的情况下,8-10min内即可出结果;检测结果客观可靠,根据颜色变化判断结果,大大减少了检测人员主观因素的影响;操作简单,无需长时间的经验积累,易于推广应用,适于临床常规,特别是医院门诊的使用。本发明依据甘氨酰-精胺酸-4-甲氧基-2-萘胺在凝固酶的水解作用下,产生4-甲氧基-2-萘胺,产物与肉桂醛类反应显色为原理,检测分泌物样本中凝固酶浓度,呈色深度与凝固酶活性成正比。本发明中试剂配制简便,使用方便,容易操作,检测时不需要显微镜等特殊设备,通过外加显色液的方式,检测时样品与试纸块接触,37℃温浴8-10min,试纸块由无色或浅黄色变为红色、紫红色、紫色,即判定为凝固酶阳性。本发明具有检测速度快,灵敏度高、特异性好的优势,与类似产品相比操作简单,适宜普及。实施案例一:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml二甲氨基肉桂醛;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例二:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-β-萘胺;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml二甲氨基肉桂醛;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例三:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-7-氨基-4-甲基香豆素;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml二甲氨基肉桂醛;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例四:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/mlz-甘氨酰-精氨酸-对硝基苯胺;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml二甲氨基肉桂醛;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例五:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-7-氨基-4-甲基伞形酮;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml二甲氨基肉桂醛;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例六:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml对二甲氨基苯甲醛;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例七:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml固蓝b盐;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例八:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml固蓝bb盐;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例九:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml固红b盐;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例十:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml固蓝rr盐;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例十一:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml固红t盐;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例十二:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml固红tr盐;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例十三:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;3.0mg/ml蔗糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:31et型滤纸配套显色液:1.5mg/ml二甲氨基肉桂醛;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃左右时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例十四:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:3mm型滤纸配套显色液:1.5mg/ml二甲氨基肉桂醛;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃左右时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例十五:凝固酶检测试纸的制备浸液:300mmtris-hcl缓冲液;5.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;3.0mg/ml海藻糖;3.0mg/mlpeg-6000;ph值为8.5;滤纸类型:319型滤纸配套显色液:1.5mg/ml二甲氨基肉桂醛;2.0mg/mltritonx-100;4.0mg/mlpvp-k90;1000ml蒸馏水;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定80℃,副加热设定60℃,待主机加热温度达到80℃,各干燥室温度达到60℃左右时开始浸液;浸渍干燥机走速设定:10.0hz。实施案例十六:凝固酶检测试纸的制备浸液:200mm磷酸二氢钾-氢氧化钠缓冲液;1.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;20.0mg/ml葡萄糖;20.0mg/mlpvp-k30;ph值为6.5;滤纸类型:7218型滤纸配套显色液:5mg/ml二甲氨基肉桂醛;5.0mg/mltritonx-200;1.0mg/mlpvp-k30;1000ml0.1mg/ml硫酸溶液;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定65℃,副加热设定60℃,待主机加热温度达到65℃,各干燥室温度达到60℃左右时开始浸液;浸渍干燥机走速设定:7.0hz。实施案例十七:凝固酶检测试纸的制备浸液:400mm硼酸-硼砂缓冲液;10.0mg/ml甘氨酰-精氨酸-4-甲氧基-β-萘胺盐酸盐;10.0mg/ml乳糖;10.0mg/mlpeg-2000;ph值为9.0;滤纸类型:526型滤纸配套显色液:5mg/ml二甲氨基肉桂醛;5.0mg/mltritonx-200;1.0mg/mlpvp-k30;1000ml3.0mg/ml硫酸溶液;凝固酶试纸浸渍干燥机自动化干燥方法:开机后将设备温度主加热设定75℃,副加热设定60℃,待主机加热温度达到75℃,各干燥室温度达到60℃左右时开始浸液;浸渍干燥机走速设定:11.0hz。上述实施例中所用浸液和显色液中的辅助试剂还可以替换为前述限定的其他物质,这里不再一一举例。本发明实施例1制备的凝固酶的试纸性能评估①外观目测随机抽取制备试纸10条,以正常视力检查试纸外观性能指标,应符合要求:1)表面应平整、边缘无毛刺;2)测试块外观整齐、色泽均匀。10次目测结果均合格。②准确度检测取用制备的试纸对检测项目各浓度水平的参考溶液进行检测,每个浓度水平重复测定5次,阳性参考溶液不得出现阴性结果,阴性参考溶液不得出现阳性结果。(结果如表1所示)表1准确度数据测定次数阴性参考溶液阳性低值阳性高值rep1阴性弱阳性阳性rep2阴性弱阳性阳性rep3阴性弱阳性阳性rep4阴性弱阳性阳性rep5阴性弱阳性阳性③重复性检测随机抽取制备的试纸条10条,对第一个非阴性量级进行检测,所有检测结果不为阴性,第一个非阴性量级均应能准确检出。(结果如表2所示)表2检出限数据测定次数阳性低值rep1弱阳性rep2弱阳性rep3弱阳性rep4弱阳性rep5弱阳性rep6弱阳性rep7弱阳性rep8弱阳性rep9弱阳性rep10弱阳性本发明实施例2制备的凝固酶的试纸性能评估①外观目测随机抽取制备试纸10条,以正常视力检查试纸外观性能指标,应符合要求:1)表面应平整、边缘无毛刺;2)测试块外观整齐、色泽均匀。10次目测结果均合格。②准确度检测取用制备的试纸对检测项目各浓度水平的参考溶液进行检测,每个浓度水平重复测定5次,阳性参考溶液不得出现阴性结果,阴性参考溶液不得出现阳性结果。(结果如表3所示)表3准确度数据③重复性检测随机抽取制备的试纸条10条,对第一个非阴性量级进行检测,所有检测结果不为阴性,第一个非阴性量级均应能准确检出。(结果如表4所示)表4检出限数据测定次数阳性低值rep1弱阳性rep2弱阳性rep3弱阳性rep4弱阳性rep5弱阳性rep6弱阳性rep7弱阳性rep8弱阳性rep9弱阳性rep10弱阳性本发明实施例4制备的凝固酶的试纸性能评估①外观目测随机抽取制备试纸10条,以正常视力检查试纸外观性能指标,应符合要求:1)表面应平整、边缘无毛刺;2)测试块外观整齐、色泽均匀。10次目测结果均合格。②准确度检测取用制备的试纸对检测项目各浓度水平的参考溶液进行检测,每个浓度水平重复测定5次,阳性参考溶液不得出现阴性结果,阴性参考溶液不得出现阳性结果。(结果如表5所示)表5准确度数据测定次数阴性参考溶液阳性低值阳性高值rep1阴性弱阳性阳性rep2阴性弱阳性阳性rep3阴性弱阳性阳性rep4阴性弱阳性阳性rep5阴性弱阳性阳性③重复性检测随机抽取制备的试纸条10条,对第一个非阴性量级进行检测,所有检测结果不为阴性,第一个非阴性量级均应能准确检出。(结果如表6所示)表6检出限数据测定次数阳性低值rep1弱阳性rep2弱阳性rep3弱阳性rep4弱阳性rep5弱阳性rep6弱阳性rep7弱阳性rep8弱阳性rep9弱阳性rep10弱阳性本发明实施例6制备的凝固酶的试纸性能评估①外观目测随机抽取制备试纸10条,以正常视力检查试纸外观性能指标,应符合要求:1)表面应平整、边缘无毛刺;2)测试块外观整齐、色泽均匀。10次目测结果均合格。②准确度检测取用制备的试纸对检测项目各浓度水平的参考溶液进行检测,每个浓度水平重复测定5次,阳性参考溶液不得出现阴性结果,阴性参考溶液不得出现阳性结果。(结果如表7所示)表7准确度数据测定次数阴性参考溶液阳性低值阳性高值rep1阴性弱阳性阳性rep2阴性弱阳性阳性rep3阴性弱阳性阳性rep4阴性弱阳性阳性rep5阴性弱阳性阳性③重复性检测随机抽取制备的试纸条10条,对第一个非阴性量级进行检测,所有检测结果不为阴性,第一个非阴性量级均应能准确检出。(结果如表8所示)表8检出限数据本发明实施例12制备的凝固酶的试纸性能评估①外观目测随机抽取制备试纸10条,以正常视力检查试纸外观性能指标,应符合要求:1)表面应平整、边缘无毛刺;2)测试块外观整齐、色泽均匀。10次目测结果均合格。②准确度检测取用制备的试纸对检测项目各浓度水平的参考溶液进行检测,每个浓度水平重复测定5次,阳性参考溶液不得出现阴性结果,阴性参考溶液不得出现阳性结果。(结果如表9所示)表9准确度数据测定次数阴性参考溶液阳性低值阳性高值rep1阴性弱阳性阳性rep2阴性弱阳性阳性rep3阴性弱阳性阳性rep4阴性弱阳性阳性rep5阴性弱阳性阳性③重复性检测随机抽取制备的试纸条10条,对第一个非阴性量级进行检测,所有检测结果不为阴性,第一个非阴性量级均应能准确检出。(结果如表10所示)表10检出限数据测定次数阳性低值rep1弱阳性rep2弱阳性rep3弱阳性rep4弱阳性rep5弱阳性rep6弱阳性rep7弱阳性rep8弱阳性rep9弱阳性rep10弱阳性本发明实施例17制备的凝固酶的试纸性能评估①外观目测随机抽取制备试纸10条,以正常视力检查试纸外观性能指标,应符合要求:1)表面应平整、边缘无毛刺;2)测试块外观整齐、色泽均匀。10次目测结果均合格。②准确度检测取用制备的试纸对检测项目各浓度水平的参考溶液进行检测,每个浓度水平重复测定5次,阳性参考溶液不得出现阴性结果,阴性参考溶液不得出现阳性结果。(结果如表11所示)表11准确度数据③重复性检测随机抽取制备的试纸条10条,对第一个非阴性量级进行检测,所有检测结果不为阴性,第一个非阴性量级均应能准确检出。(结果如表12所示)表12检出限数据测定次数阳性低值rep1弱阳性rep2弱阳性rep3弱阳性rep4弱阳性rep5弱阳性rep6弱阳性rep7弱阳性rep8弱阳性rep9弱阳性rep10弱阳性由检测结果显示本发明中所述的试纸,外观表面应平整、测试块外观整齐、色泽均匀,具有可观察性;检测阳性参考溶液、阴性参考溶液结果准确无偏差;重复性检测具有均一性和一致性,所有检测指标测试结果均符合产品要求。本发明产品具有检测速度快、可目测验视、灵敏度高、稳定性好的优势,与类似产品相比操作简单,适宜普及。显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1