血管内皮生长因子检测试剂盒及其使用方法和应用与流程
本发明涉及免疫生物学检测领域,尤其是涉及一种血管内皮生长因子检测试剂盒及使用方法和应用。
背景技术:
:血管内皮生长因子(vascpglarendothelialgrowthfactor,vegf)是一种由亚基内及亚基间二硫键交联形成的同型二聚体糖蛋白,其分子量约为34-45kda。vegf属于血小板生长因子家族,可特异性作用于血管内皮细胞,促进血管内皮细胞的增殖,增加血管的通透性。此外,有研究证明vegf与淋巴管的增生存在显著关系,因此vegf也被认为是促进血管形成和引起炎症反应的重要细胞因子。vegf检测可用于辅助检测不同原因所引发的炎症患者的炎症进展情况,对于炎症的控制具有积极的意义,同时也可用于肿瘤的筛查、辅助诊断、治疗疗效的评估和监测、预后、以及复发的监测。传统的检测vegf的方法为板式化学发光,固相包被载体为48/96孔板等,将包被抗体直接或者通过生物素链霉亲和素系统包被到载体上,通过辣根过氧化物酶来催化底物发光,根据检测到的发光值强度判定样本中待测物含量。传统的检测方法不便于独立进行单人份的检测,并且微孔板包被抗体,反应时间长,制作流程复杂,而采用酶促发光检测,检测时间也较长,不利于检测灵敏度的提高,尤其是包被或者标记的抗体为全片段的igg抗体,与检测对象之间易存在非特异性结合。技术实现要素:基于此,有必要提供一种易于制作且有利于缩短检测时间、提高检测灵敏度和特异性的血管内皮生长因子检测试剂盒。一种血管内皮生长因子检测试剂盒,包括第一连接物连接的第一抗体片段、第二连接物包被的磁珠和发光标记物标记的第二抗体片段;所述第一连接物与所述第二连接物能够特异性结合;所述第一抗体片段和/或所述第二抗体片段为血管内皮生长因子抗体的fab片段,且所述第一抗体片段与所述第二抗体片段与血管内皮生长因子特异性结合的位点不同;所述发光标记物为直接化学发光标记物。在其中一个实施例中,所述第一连接物为异硫氰酸荧光素,所述第二连接物为抗异硫氰酸荧光素抗体;所述第一连接物与所述第一抗体片段的氨基端连接;所述第二连接物的氨基端与所述磁珠表面固定的羧基连接。在其中一个实施例中,fab片段的第一抗体片段和/或第二抗体片段是在酸性条件下使用胃蛋白酶消化处理血管内皮生长因子单克隆抗体,过柱分离后使用还原剂还原得到的。在其中一个实施例中,所述血管内皮生长因子单克隆抗体与所述胃蛋白酶的质量比为1:0.04;和/或消化处理的温度为33℃,时间为6h~24h;和/或所述还原剂为巯基乙醇。在其中一个实施例中,所述发光标记物为金刚烷、鲁米诺、异鲁米诺或吖啶酯。在其中一个实施例中,所述第一连接物与第一抗体片段的质量比为1:50,每毫克所述磁珠表面连接有20μg所述第二连接物,所述发光标记物与所述第二抗体片段的质量比为10:1。在其中一个实施例中,所述血管内皮生长因子检测试剂盒还包括校准品溶液、稀释用缓冲液、清洗液和发光底物溶液中的至少一种。同时,还有必要提供一种上述检测试剂盒的使用方法及应用。一种上述任一实施例所述的血管内皮生长因子检测试剂盒的使用方法,包括如下步骤:将所述第一连接物连接的第一抗体片段、所述第二连接物包被的磁珠与待测样本混合,孵育反应后洗涤,加入所述发光标记物标记的第二抗体片段,孵育反应后二次洗涤,加入发光底物溶液,测量光强度。在其中一个实施例中,所述孵育反应的温度是33℃,时间是10min;和/或所述第一连接物连接的第一抗体片段的浓度为1μg/ml,所述第二连接物包被的磁珠的浓度为1mg/ml,所述发光标记物标记的第二抗体片段浓度为0.5μg/ml,所述第一连接物连接的第一抗体片段、所述第二连接物包被的磁珠以及所述发光标记物标记的第二抗体片段的加入体积比为100μl:20μl:200μl。上述任一实施例所述的血管内皮生长因子检测试剂盒在使用化学发光分析仪检测中的应用。上述血管内皮生长因子检测试剂盒中用于与血管内皮生长因子特异性结合的第一抗体片段与第二抗体片段中至少一个为血管内皮生长因子抗体的fab片段,较之传统的igg全片段抗体,可有效避免fc片段的非特异性结合,因而检测特异性可显著提高;使用磁珠可以增大反应的灵敏度,并可进行独立单人份检测;使用直接化学发光标记物进行抗体片段标记,在检测时,无需加入酶促反应试剂,因而所需的检测时间短,检测效率高。该检测试剂盒易于制作,各项检测指标优异,可广泛推广使用。附图说明图1为本发明的血管内皮生长因子检测试剂盒的检测原理示意图;图2为血管内皮生长因子单克隆抗体的消化、还原过程示意图。具体实施方式为了便于理解本发明,下面将参照相关附图对本发明进行更全面的描述。附图中给出了本发明的较佳实施例。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容的理解更加透彻全面。除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的
技术领域:
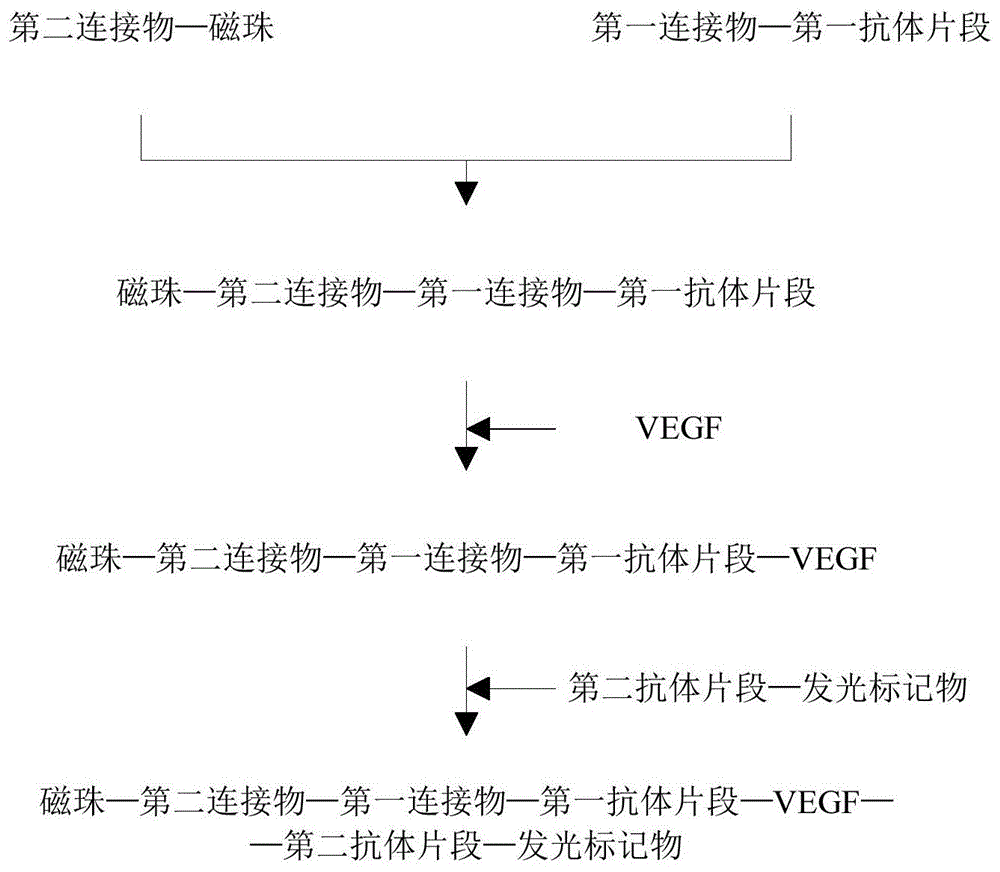
的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。本发明提供了一种血管内皮生长因子检测试剂盒,其包括第一连接物连接的第一抗体片段、第二连接物包被的磁珠和发光标记物标记的第二抗体片段。第一连接物与第二连接物能够特异性结合。第一抗体片段和/或第二抗体片段为血管内皮生长因子抗体的fab片段,且第一抗体片段与第二抗体片段与血管内皮生长因子特异性结合的位点不同。发光标记物为直接化学发光标记物。如图1所示,该检测试剂盒在使用时,第一连接物连接的第一抗体片段与第二连接物包被的磁珠可先通过能够特异性结合的第一连接物与第二连接物结合,形成磁珠-第二连接物-第一连接物-第一抗体片段的复合物;若待测样本中含有血管内皮生长因子(vegf),血管内皮生长因子可与第一抗体片段特异性结合,进而形成磁珠-第二连接物-第一连接物-第一抗体片段-vegf的复合物;接着加入发光标记物标记的第二抗体片段后,第二抗体片段会与vegf特异性结合,进而形成磁珠-第二连接物-第一连接物-第一抗体片段-vegf-第二抗体片段-发光标记物的复合物,加入反应底物(如naoh和h2o2)后即可发光检测。在一个具体示例中,第一连接物为异硫氰酸荧光素(fitc),第二连接物为抗异硫氰酸荧光素抗体。第一连接物与第一抗体片段的氨基端连接,例如可以在碱性环境下将fitc与第一抗体片段的氨基端连接。第二连接物的氨基端与磁珠表面固定的羧基连接,例如可以在酸性环境下,使用碳二亚胺将抗fitc抗体的氨基端与表面修饰固定有羧基的磁珠连接结合。在一个具体示例中,如图2所示,fab片段的第一抗体片段和/或第二抗体片段是在酸性条件下使用胃蛋白酶消化处理血管内皮生长因子单克隆抗体,过柱分离浓缩后使用还原剂还原得到的。更具体地,血管内皮生长因子单克隆抗体与胃蛋白酶的质量比为1:0.04,例如每毫克血管内皮生长因子单克隆抗体可以使用0.04毫克的胃蛋白酶进行消化处理。优选地,消化处理的温度为33℃,时间为6h。还原剂可以是但不限于巯基乙醇。在一个具体示例中,发光标记物选用金刚烷、鲁米诺、异鲁米诺或吖啶酯等。发光标记物标记的第二抗体片段可以采用戊二醛等交联剂将第二抗体片段与过量的发光标记物反应连接,后通过透析法去除多余的交联剂与发光标记物。通过方阵滴定实验对比不同配对组合,第一连接物连接的第一抗体片段的浓度优选是1μg/ml,发光标记物标记的第二抗体片段的浓度优选是0.5μg/ml。进一步,优选地,该血管内皮生长因子检测试剂盒还包括校准品溶液、稀释用缓冲液、清洗液和发光底物溶液中的至少一种。校准品溶液包括浓度分别为200pg/ml和500pg/ml的vegf纯品溶液;稀释用缓冲液优选是以bsa为主的磷酸盐缓冲液;发光底物溶液包括含4wt%氢氧化钠的缓冲液和含0.12%(v/v)h2o2的缓冲液;清洗液优选是含有表面活性剂的磷酸盐缓冲液。进一步,本发明还提供了一种上述血管内皮生长因子检测试剂盒的使用方法,其包括如下步骤:将第一连接物连接的第一抗体片段、第二连接物包被的磁珠与待测样本混合,孵育反应后洗涤,加入发光标记物标记的第二抗体片段,孵育反应后二次洗涤,加入发光底物溶液,测量光强度。在一个具体示例中,孵育反应的温度是33℃,时间是10min。优选地,第一连接物连接的第一抗体片段的浓度为1μg/ml,第二连接物包被的磁珠的浓度为1mg/ml,发光标记物标记的第二抗体片段浓度为0.5μg/ml,第一连接物连接的第一抗体片段、第二连接物包被的磁珠以及发光标记物标记的第二抗体片段的加入体积比为100μl:20μl:200μl。上述血管内皮生长因子检测试剂盒可以应用在化学发光分析仪中。该血管内皮生长因子检测试剂盒中用于与血管内皮生长因子特异性结合的第一抗体片段与第二抗体片段中至少一个为血管内皮生长因子抗体的fab片段,较之传统的igg全片段抗体,可有效避免fc片段的非特异性结合,因而检测特异性可显著提高;使用磁珠可以增大反应的灵敏度,并可进行独立单人份检测;使用直接化学发光标记物进行抗体片段标记,在检测时,无需加入酶促反应试剂,因而所需的检测时间短,检测效率高。以下结合具体实施例和对比例对本发明的血管内皮生长因子检测试剂盒及其使用方法作进一步详细地说明。以下实施例所用的部分材料、试剂和仪器说明如下:vegf单克隆抗体:来源于小鼠。抗fitc抗体:来源于小鼠。磁珠:merck粒径1.2-1.8μm/thermofisher粒径1μm。检测仪器:威海威高生物科技有限公司提供的autolumis系列。实施例1一、试剂盒的制备1.第一连接物连接的第一抗体片段的制备在酸性条件下,使用胃蛋白酶消化处理血管内皮生长因子单克隆抗体,血管内皮生长因子单克隆抗体与胃蛋白酶的质量比为1:0.04,消化处理的温度为33℃,时间为6h,过柱分离浓缩后使用巯基乙醇还原。2.第二连接物包被的磁珠的制备取10mg磁珠,用0.1mmes溶液将磁珠洗三遍后,按照磁珠:edc:抗体质量比为10:0.2:0.2的比例进行混合,20℃~28℃混匀条件下进行标记2小时,用0.01mph为3.2的pbs溶液洗涤三遍后,加入保存液置于2℃~8℃保存3.发光标记物标记的第二抗体片段的制备将1mg第二抗体片段用0.1mph为9.0的cb缓冲液稀释成1mg/ml的浓度,加入20μg异鲁米诺混匀后,加入10μl2.5%(w/v)的戊二醛,33℃混匀反应2小时,用0.01mph为3.2的pbs透析后使用。4.方阵滴定实验得到优选浓度按照下表1中的组合进行试验,以确定磁珠的浓度(a)、第一连接物连接的第一抗体片段的浓度(b)和发光标记物标记的第二抗体片段的浓度(c)。表1组合a(mg/ml)b(μg/ml)c(μg/ml)组合a(mg/ml)b(μg/ml)c(μg/ml)10.50.50.251010.50.2520.50.50.51110.50.530.50.511210.5140.510.2513110.2550.510.514110.560.5111511130.520.2516120.2580.520.513120.590.52118121二、待测样本的检测样本50μl、第二连接物包被的磁珠20μl以及含有fitc标记抗体片段的分析缓冲液100μl分别加入反应杯中,33℃反应孵育10分钟,洗涤3次后,加入吖啶酯标记的抗体片段200μl,33℃反应孵育10分钟;洗涤3次后加入底物溶液,测定发光值,根据标准曲线确定样本浓度。三、结果及分析经过检测,本发明试剂盒的线性范围为5pg/ml-1000pg/ml,当浓度小于5pg/ml时按照5pg/ml显示结果,当结果超过1000pg/ml时,显示1000pg/ml。实施例2一、试剂盒的制备使用异鲁米诺替代实施例1中的吖啶酯,其他同实施例1。二、待测样本的检测样本50μl、第二连接物包被的磁珠20μl以及含有fitc标记抗体片段的分析缓冲液100μl分别加入反应杯中,33℃反应孵育10分钟,洗涤3次后,加入异鲁米诺标记的抗体片段200μl,33℃反应孵育10分钟;洗涤3次后加入底物溶液,测定发光值,根据标准曲线确定样本浓度。三、结果及分析经过检测,本发明试剂盒的线性范围为5pg/ml-1000pg/ml,当浓度小于5pg/ml时按照5pg/ml显示结果,当结果超过1000pg/ml时,显示1000pg/ml。对比例1人血清中的类风湿因子(rf)会与包被或标记ab的fc片段结合产生假阳,选择rf有值样本使用本发明的去fc段抗体试剂盒与全片段试剂盒上进行检测。结果如表2所示,可以看出全片段抗体易受rf影响。表2进一步研究发现,接受生物素治疗的人群在生物素-链霉亲和素连接包被的磁珠体系中的检测结果易产生异常,而使用本发明的试剂盒检测结果准确。技术指标比对,结果见下表3。表3项目本发明指标现有产品指标最低检出限不高于5pg/ml不高于10pg/ml批内精密性≤6.25%≤10%批间精密性≤8.33%≤15%回收率±10%±10%线性范围5-100010-800孵育时间10min*230min*2从表3可以看出,本发明的试剂盒的各项指标较之现有产品优异。因而,本发明的试剂盒产品可以广泛推广应用在vegf检测过程中。以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1