用于检测非洲猪瘟病毒CD2v蛋白抗体的双抗原夹心免疫荧光层析试剂盒的制作方法
本发明属于兽用生物制品
技术领域:
,具体涉及一种用于检测非洲猪瘟病毒cd2v蛋白抗体的双抗原夹心免疫荧光层析试剂盒。
背景技术:
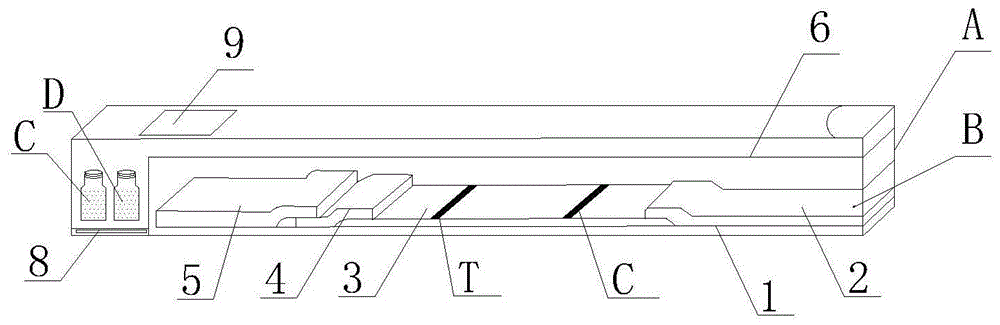
:非洲猪瘟(africanswinefever,asf)是由非洲猪瘟病毒(africanswinefevervirus,asfv)感染家猪和野猪引起猪的一种急性、热性、高度接触性传染病,临床以猪高热、食欲废绝、皮肤发绀、内脏实质器官出血、呼吸系统和神经系统功能紊乱为主要特征,被世界动物卫生组织(oie)列为必须报告的动物疫病,在我国被列为一类动物疫病。该病病程极短、死亡率高。非洲猪瘟病毒基因型众多,目前已知有24个基因型。迄今为止,该病尚无商品化的疫苗,疫情的防控主要依靠加强饲养场生物安全管理、限制生猪和猪产品跨区域流动、对疫点和疫区内所有生猪采取扑杀等措施。1921年,montgomery首次报道在肯尼亚发生非洲猪瘟疫情。2007年以来,非洲猪瘟在中东欧多个国家扩散并流行,特别是俄罗斯及其周边地区。2017年3月,俄罗斯远东地区伊尔库茨克州发生非洲猪瘟疫情,2018年8月,我国辽宁省沈阳市沈北区首次发现非洲猪瘟疫情,经核酸检测和序列比对分析发现,该毒株与俄罗斯和中东欧国家流行的格鲁吉亚毒株(georgia2007)属于同一进化支,属于基因ii型毒株。随后,在我国的河南、江苏、内蒙古、黑龙江、浙江、安徽、等多个省份(自治区、直辖市)呈现散发流行,对我国养猪业造成了数十亿元的经济损失。由于asf可给养猪业造成毁灭性打击,因此,asf疫苗研究从未间断。迄今,国际上采用基因工程手段获得了多个asfv基因缺失疫苗候选株,以及通过细胞传代致弱和从自然界分离弱毒株的方法获得了弱毒疫苗候选株,基因缺失株疫苗研究较多的是mgf和cd2v基因缺失株。国外2017年构建了cd2v缺失的ba71株(基因i型)已经充分致弱,免疫猪后存活率均100%[monteagudo,p.l.,etal.,ba71deltacd2:anewrecombinantliveattenuatedafricanswinefeverviruswithcross-protectivecapabilities.jvirol,2017.91(21).]。2019年国内构建了cd2v和mgf双基因缺失株,能使免疫猪获得100%的保护[张艳艳,等,非洲猪瘟病毒基因缺失疫苗株的构建和免疫保护特性,中国兽医学报,2019.39(8),1421-1427]。2020年国内又构建了更安全有效的非洲猪瘟病毒7基因缺失疫苗株[weiyec.,etal.,aseven-gene-deletedafricanswinefevervirusissafeandeffectiveasaliveattenuatedvaccineinpigs.scichinalifesci,2020.63(3)],在这些疫苗候选株中cd2v基因均为必缺基因,又因其为病毒的外膜蛋白并具有良好的免疫原性,使其成为建立鉴别诊断疫苗株与野毒株血清学诊断方法的首选靶抗原。我国的国情决定了现阶段应走疫苗免疫防控路线,随着疫苗的使用,鉴别疫苗株与野毒株的显得尤为重要,因此研制相关的快速诊断试剂盒十分迫切。技术实现要素:针对上述问题,本发明的目的是提供一种用于非洲猪瘟病毒抗体的大量筛查,以及将来用于cd2v基因缺失株疫苗免疫猪群中鉴别非洲猪瘟野毒株的感染的试剂盒。一种用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒,包括盒体,所述的盒体内设有cd2v抗体免疫荧光层析检测卡和装有血清稀释液的血清稀释液瓶,装有标准阳性血清的血清瓶d,装有标准有阴性血清的血清瓶e;所述的cd2v抗体免疫荧光层析检测卡包括pvc底板,所述的pvc底板上从左至右依次设有吸收垫、反应膜、结合垫和样品垫,所述的结合垫上负载有荧光标记的cd2v蛋白和荧光标记的羊抗鸡igy,所述的反应膜设有一条检测线t,一条质控线c,所述的检测线t上包被有重组cd2v蛋白,所述的质控c线上包被有羊抗鸡igy免疫球蛋白。进一步的,上述的一种用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒,所述的cd2v抗体免疫荧光层析检测卡位于卡壳内,所述的卡壳位于盒体内,所述的卡壳上设有加样孔,所述的加样孔与样品垫相对应。进一步的,上述的一种用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒,所述的盒体内设有id芯片卡、盒体外设有id芯片卡相适配的二维码。进一步的,上述的一种用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒,所述的反应膜通过下述方法制得的:用含3%蔗糖的pb分别稀释cd2v蛋白和羊抗鸡igy免疫球蛋白至浓度为1mg/ml,得检测线溶液和质控线溶液,在反应膜上划线,在膜的一端用记号笔做好质控线和检测线的标记,质控线和检测线的距离为5mm,检测t线与硝酸纤维素膜下缘的距离为10mm,划线浓度均为1μl/cm,完成后将片材放置在温度18~26℃、湿度≤30%的干燥室中干燥16~18h,干燥完迅速装到铝膜袋中,加入干燥剂,封口,2~8℃保存,待用。进一步的,上述的一种用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒,所述的结合垫的通过下述步骤制得的:1)将1mg纳米稀土荧光微球超声分散,用活化缓冲液mes稀释10倍,加入到2ml的ep管中;加入10mg的活化剂edc和10mg的活化剂nhs混匀,活化15min-30min;14000r/min,离心15min;倒掉上清液,加入1ml偶联缓冲液,然后用超声波分散均匀,边搅拌边滴加cd2v蛋白或羊抗鸡igy100μg,室温混匀1小时,加入封闭剂封闭1小时,14000r/min,离心15min,去上清,加入复溶液分散均匀,即标记好的t线标记物或c线标记物;2)将8964玻纤裁为10mm*300mm大小,将标记好的t线标记物和c线标记物,按照体积比1:10比例混合,按3μl/cm、0.02mpa采用喷金划膜仪喷至剪裁后的8964上,放置在18~26℃、湿度≤30%的干燥室中干燥16~18h,干燥完迅速装到铝膜袋中,加入干燥剂,封口,2~8℃保存,待用。进一步的,上述的一种用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒,所述的样品垫通过下述步骤制得的:配制含1%s9、0.5%曲拉通、0.05%叠氮钠的tris样品垫工作液;按40ml/张rb65玻纤投料,每张用滚轮铺均匀,37℃干燥24h,用切刀裁为23mm*300mm大小,装到铝膜袋中,加入干燥剂,封口待用。进一步的,上述的一种用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒,所述的血清稀释液为含0.8wt%s21、0.03wt%proclin300的0.01m的ph7.4磷酸盐缓冲液。进一步的,上述的一种用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒,所述的标准阳性血清通过下述步骤制得的:1)取新西兰大白兔,体重2-3kg;第一次免疫,用注射器吸取弗式完全佐剂、与重组cd2v蛋白等比例混合的乳化液1m1,大腿内侧肌肉注入0.5ml;间隔2周后,进行第二次免疫,同样剂量和部位注射弗氏不完全佐剂与重组cd2v蛋白等比例混合的乳化液1m1,间隔7-10天后,从耳静脉采血0.5-1.0ml,分离血清,采用酶联免疫吸附方法检测血清效价,抗体效价可达到1:100以上;2)采用心脏采血法采血,待析出血清后进行分离,3000r/min离心15min,取上清,加入终浓度为0.01%的硫柳汞防腐,分装后,-20℃保存。进一步的,上述的一种用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒,所述的标准阴性血清通过下述步骤制得的:取清洁级实验猪作为采血用猪,采血前体况较好,体温、食欲、大小便正常,未免疫任何疫苗和无其他疾病,消毒后,前腔静脉采血,分离血清,加入万分之一的硫柳汞防腐;以0.5ml分装于无菌管中,-20℃保存。进一步的,上述的一种用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒,所述的重组cd2v蛋白通过下述步骤制得的:1)抗原制备1.1)非洲猪瘟cd2v蛋白的表达根据genbank中非洲猪瘟cd2v基因序列,设计合成了下述一对引物:上游引物cd2v-f:5'-gacgcggccgcatgatatacttatttttttaata-3'(seqidno.1)下游引物cd2v-r:5'-gtcggatccttagtggtggtggtggtggtggggaaatgggttgagtggttgt-3'(seqidno.2)1.2)上游引物cd2v-f下划线部分为引入的酶切位点noti;下游引物cd2v-r下划线部分引入的酶切位点为bamhi,同时为了cd2v表达蛋白的纯化在下游引物引入了6个组氨酸,其编码碱基caccaccaccaccaccac(seqidno.3);2)非洲猪瘟cd2v蛋白的纯化cho-cd2v细胞株在37℃,5%co2培养箱内大规模无血清悬浮培养3d,离心收集细胞,弃上清,用pbs洗涤重悬细胞,超声裂解,12000rpm离心,收集上清,进行sds-page分析,使用镍离子亲和层析柱蛋白纯化,纯化后,经sds-page、westernblotting鉴定,获取到单一条带,并具备较好的免疫原性。与现有技术相比,本发明具有以下有益效果:1、本发明公开了一种检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析方法,可用于非洲猪瘟病毒抗体的大量筛查以及将来用于cd2v缺失株免疫猪群中鉴别非洲猪瘟野毒株的感染。2、本发明提供的技术方案检测灵敏度高,最低检出限为1.25tu/ml。3、本发明提供的技术方案精密度高,变异系数小于10%。附图说明图1是本发明提供的试剂盒结构示意图;图2是本发明提供的试剂卡结构示意图;图3是本发明提供的带卡壳试剂卡结构示意图;图4是本发明提供的cd2v蛋白的sds-page电流图;图5是本发明提供的cd2v蛋白的westernblotting鉴定结果。具体实施方式下面结合具体实施方式,对本发明的权利要求做进一步的详细说明,但不构成对本发明的任何限制,任何人在本发明权利要求范围内所做的有限次的修改,仍在本发明的权利要求保护范围之内。除有特别说明,本发明中所用各种试剂、原料均为可以从市场上购买或者通过公知的方法制得的产品。实施例1本发明提供的一种用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒,参阅图1,包括盒体a,所述的盒体a内设有cd2v抗体免疫荧光层析检测卡b和装有血清稀释液的血清稀释液瓶c,装有标准阳性血清的血清瓶d,装有标准有阴性血清的血清瓶e;所述的cd2v抗体免疫荧光层析检测卡b包括pvc底板1,所述的pvc底板1上从左至右依次设有吸收垫2、反应膜3、结合垫4和样品垫5,所述的结合垫4上负载有荧光标记的cd2v蛋白和荧光标记的羊抗鸡igy,所述的反应膜3设有一条检测线t,一条质控线c,所述的检测线t上包被有重组cd2v蛋白,所述的质控c线上包被有羊抗鸡igy免疫球蛋白。更为具体地说,所述的cd2v抗体免疫荧光层析检测卡b位于卡壳6内,所述的卡壳6位于盒体a内,所述的卡壳6上设有加样孔7,所述的加样孔7与样品垫5相对应。为了方便检测和记录检测信息,所述的盒体a内设有id芯片卡8、血清稀释液瓶9,盒体a外设有id芯片卡8相适配的二维码10。实施例2上述试剂盒的制备方法包括以下步骤:将带有nc膜的pvc底板1平铺于工作台面上,分别粘贴结合垫4、样品垫5和吸收垫2,采用切条机切成4.0mm宽的试纸条,将每一试纸条装入塑料卡壳内,将每一试剂卡置于铝膜袋中,并加入1g干燥剂1包,热合封口,即为免疫荧光层析检测卡。具体地说:1)包被膜通过下述方法制得的:用含3%蔗糖的pb(0.01mph7.4)分别稀释cd2v蛋白和igy至浓度为1mg/ml为检测线和质控线溶液,在硝酸纤维膜上划线,在膜的一端用记号笔做好质控线和检测线的标记,质控线和检测线的距离为5mm,t线与硝酸纤维素膜下缘的距离为10mm,划线浓度均为1μl/cm。完成后将片材放置在温度(18~26)℃、湿度≤30%的干燥室中干燥过夜(16~18)h,干燥完迅速装到铝膜袋中,加入干燥剂,封口,(2~8)℃保存,待用。2)结合垫通过下述方法制得的:将1mg纳米稀土荧光微球超声分散,用活化缓冲液mes稀释10倍,加入到2ml的ep管中;加入10mg的活化剂edc和10mg的活化剂nhs,混匀,活化15min-30min;14000r/min,离心15min;倒掉上清液,加入1ml偶联缓冲液,然后用超声波分散均匀,边搅拌边滴加cd2v蛋白或羊抗鸡igy100μg,室温混匀1小时,加入封闭剂封闭1小时,14000r/min,离心15min,去上清,加入复溶液分散均匀,即标记好的t线和c线标记物。将玻纤纤维膜裁为10mm*300mm大小,将标记好的t线和c线标记物,按照1:10(v:v)比例混合,按3μl/cm、0.02mpa采用喷金划膜仪喷至剪裁后的8964上,放置在温度(18~26)℃、湿度≤30%的干燥室中干燥过夜(16~18)h,干燥完迅速装到铝膜袋中,加入干燥剂,封口,(2~8)℃保存,待用。3)样品垫通过下述方法制得的:配制含1%s9、0.5%曲拉通、0.05%叠氮钠的tris(0.01mph8.0)样品垫工作液;按40ml/张rb65玻纤投料,每张用滚轮铺均匀,37℃干燥24h,用切刀裁为23mm*300mm大小,装到铝膜袋中,加入干燥剂,封口待用。4)吸收垫的制备吸水纸裁成将吸水纸裁为25mm*300mm大小,待用。5)血清稀释液的配置含0.8%s21、0.03%proclin300的0.01m的ph7.4磷酸盐缓冲液6)上述的抗原制备方法:6.1)非洲猪瘟cd2v蛋白的表达根据genbank中asfv(genbank:mk333181.1)cd2v基因核苷酸序列人工合成,并设计合成1对引物,采用pcr方法从asfvdna中扩增出cd2v基因片段,将其克隆到表达载体pires-egfp(购自美国clontech公司),构建了重组质粒pires-cd2v,测序验证后提取重组质粒并转染cho-k1细胞(购自中国科学院典型培养物保藏委员会细胞库),用含6μg/ml浓度嘌呤霉素的细胞培养液进行加压筛选,2周后对细胞克隆取少量提取核酸进行pcr鉴定,鉴定正确的细胞克隆再进行2-3轮单细胞克隆获得稳定表达cd2v基因的细胞株命名为cho-cd2v细胞株。设计的引物为:cd2v-f5'-gacgcggccgcatgatatacttatttttttaata-3'((seqidno.1)cd2v-r5'-gtcggatccttagtggtggtggtggtggtggggaaatgggttgagtggttgt-3'(seqidno.2);下划线部分为引入的酶切位点,cd2v-f为asfvcd2v基因上游扩增引物,引入的酶切位点为noti;cd2v-r为asfvcd2v基因下游扩增引物,引入的酶切位点为bamhi,同时为了cd2v表达蛋白的纯化在下游引物引入了6个组氨酸的编码碱基,其caccaccaccaccaccac(seqidno.3),cd2v基因序列和引物均由生工生物工程(上海)股份有限公司合成。6.2)非洲猪瘟cd2v蛋白的纯化cho-cd2v细胞株在37℃,5%co2培养箱内大规模悬浮培养3d,离心收集细胞,弃上清,用pbs洗涤重悬细胞,超声裂解(超声5s,间隔5s,共10min),12000rpm离心,收集上清,进行sds-page分析。蛋白纯化时使用镍离子亲和层析柱,纯化后,经sds-page、westernblotting鉴定,获取到单一条带,并具备较好的抗原性。使用bca法测定纯化后蛋白含量,标准品浓度及其对应的od值见表1。纯化后cd2v蛋白的od值为1.917,与标准品比较后,其浓度为1.5mg/ml。表17)标准asfv阳性血清及标准asfv阴性血清的制备在免疫荧光层析检测方法建立过程中,为了建立试剂盒的有效性验证、阴阳性判断标准和避免人为操作误差制备了阴阳性标准血清。本发明研制了标准asfv抗体阳性对照血清和标准asfv抗体阴性对照血清,用于实验条件的优化和检测结果的判定。7.1)标准阳性血清的制备取新西兰大白兔(购自广东省实验动物中心),体重2-3kg。第一次免疫,用注射器吸取弗式完全佐剂(fca)(购自美国sigma公司)与重组cd2v蛋白等比例混合的乳化液1m1,大腿内侧肌肉注入0.5ml。间隔2周后,进行第二次免疫,同样剂量和部位注射弗式不完全佐剂(购自美国sigma公司)与重组cd2v蛋白等比例混合的乳化液1m1,间隔7-10天后,从耳静脉采血0.5-1.0ml,分离血清,采用酶联免疫吸附方法检测血清效价,抗体效价可达到1:10000以上。采用心脏采血法采血,待析出血清后进行分离,3000r/min离心15min,取上清,加入终浓度为0.01%的硫柳汞防腐,分装后,-20℃保存。7.2)标准阴性血清的制备取清洁级实验猪(购自南方医科大学实验动物中心)作为采血用猪,采血前体况较好,体温、食欲、大小便正常,未免疫任何疫苗和无其他疾病。消毒后,前腔静脉采血,分离血清,加入万分之一的硫柳汞防腐。以0.5ml分装于无菌管中,-20℃保存。为了更好理解本发明,本发明试剂盒的检测原理采用双抗原夹心法,样本滴加到试剂的加样孔中,在毛细效应下进行层析,样本中的asfv-ab与结合垫上荧光标记的cd2v蛋白结合,扩散至测试区,被包被于硝酸纤维膜的cd2v蛋白捕获,并形成复合物聚集于测试区;测试区荧光强度与样品中的病毒抗体浓度成正比,通过免疫层析定量分析仪根据定标曲线将该荧光信号值转换成样本中抗体浓度;c线为质控线,荧光强度达到设定的有效值后证明试剂有效。为了便于本领域技术人员使用本发明提供的试剂盒,本发明制备的试剂盒进行检测方法。1)撕开cd2v抗体免疫荧光层析检测卡铝箔袋封口,取出检测卡,水平放置。2)用移液枪吸取待测样本20μl加入血清稀释液中,混匀。3)吸取混合后样本100μl,加入到检测卡加样孔中,吸取及加样时注意不要产生明显气泡。具体操作方法如下:(方法一/方法二可供选择测试)方法一:快速测试:选择“快速测量”模式,把对应项目的ic卡放到检测仪读卡区,点击批次,仪器自动读取ic卡信息,待检测卡室温反应10min后,平稳插入仪器卡槽(加样孔端朝卡槽进口),推入到底,点击“测量”选项,开始检测,显示并打印结果;方法二:标准测试:选择“标准测量”模式,把对应项目的ic卡放到检测仪读卡区,点击批次,仪器自动读取ic卡信息,将检测卡平稳插入仪器的卡槽中(加样孔端朝卡槽进口),推入到底,点击“测量”选项,仪器自动计时,计时结束,自动测试显示并打印结果。2.检测结果分析1)检测阳性对照血清(pc)的od值与阴性对照血清(nc)的荧光强度值之比必须大于2.0时,检测被认为有效。pc/nc≥2.1阳性cutoff=nc*2.1其中nc=阴性对照血清t/c值pc=阳性对照血清t/c值2)平行检测时,最终使用t/c值为两个平行测试的平均值。当血清样本的t/c值低于阳性cutoff值时,该样本为asfvcd2v抗体阴性。当血清样本的t/c值高于阴性cutoff值是,该样本为asfvcd2v抗体阳性。3)线性范围将asfv阳性血清用阴性血清分别稀释到0、10、20、40、80、160、320、640、1280tu/ml;进行检测,每浓度重复测试2次;反应10min后,将试纸放入免疫层析定量分析仪中,读取t/c值,通过内置标准曲线进行曲线拟合和浓度的计算。测试结果显示:试剂在检测0~640tu/ml的cdv线性拟合关系较好,r>0.9900,当cdv浓度增加到1280tu/ml时,线性拟合r值小于0.9900。因此本检测的最大检测范围可以达到640tu/ml。在0~640tu/ml浓度范围内,该试剂盒剂量反应曲线log(y)=0.543log(x)–1.018,r=0.9988(r2=0.9976),参阅图3。4、最低检出限将阴性血清,重复测试20次,计算t/c均值,将其代入剂量-反应曲线中,得出本方法的最低检出限为1.25tu/ml。5、精密度将asfv阳性血清用阴性血清分别稀释到20、80、320tu/ml,用本方法检测卡每浓度重复测试10次,计算测试浓度的变异系数。结果表2所示,由此可以看出,本试剂盒检测的变异系数均小于10%(三个浓度分别为8.45%、5.64%和5.85%),见表2,因此本检测方法具有较高的精密度。表2质控品浓度变异系数质控ⅰ20tu/ml9.65%质控ⅱ80tu/ml7.25%质控ⅲ320tu/ml4.36%综上所述,本发明的内容并不局限在上述的实施例中,相同领域内的专业人员可以在本发明的技术指导思想之内可以轻易提出其他的实施例,但这种实施例都包括在本发明的范围之内。序列表<110>广州敏捷生物技术有限公司<120>用于检测非洲猪瘟病毒cd2v抗体的双抗原夹心免疫荧光层析试剂盒<160>3<170>siposequencelisting1.0<210>1<211>34<212>dna<213>2ambystomalateralexambystomajeffersonianum<400>1gacgcggccgcatgatatacttatttttttaata34<210>2<211>52<212>dna<213>2ambystomalateralexambystomajeffersonianum<400>2gtcggatccttagtggtggtggtggtggtggggaaatgggttgagtggttgt52<210>3<211>18<212>dna<213>2ambystomalateralexambystomajeffersonianum<400>3caccaccaccaccaccac18当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1