细胞成像计数装置的制作方法
1.本技术涉及微流道装置技术领域,尤其涉及一种细胞成像计数装置。
背景技术:
2.细胞已经成为基础科研、医学临床及制药等行业常规的研究对象,而细胞计数和活率分析几乎成了必不可少的工作,如何快速精确低成本的进行细胞计数成为首要问题。
3.目前,市场上常规的细胞计数方法主要有两类:图像法和库尔特法,操作如下:
4.1)、图像法:研究者将细胞染色后,加入到专用的一次性塑料细胞计数板中,把一次性塑料计数板放置到细胞计数仪内进行拍照,根据照片中细胞的着色情况比较准确判断出细胞的死活,从而分别计算出死、活细胞的浓度和总数;此方法速度较快,检测结果较准确,但每次计数后,存放样品的一次性塑料细胞计数板直接被抛弃,国内每年被抛弃的一次性塑料计数板达到上千万片,导致严重的白色塑料污染,又引发高昂使用成本。
5.2)、库尔特法:研究者将细胞样品处理为单细胞混悬液,把细胞悬液加入毛细管或者微流芯片。细胞逐一通过电场产生电讯号,通过电讯号的强弱来判断细胞的大小并计数细胞的数量。但每次计数完成后,都要花费大量时间清洗毛细管和微流芯片,清洗用的鞘液也会产生大量废液,处理不好则污染环境;如果细胞悬液制备不理想则极易堵塞毛细管。
技术实现要素:
6.本技术提供一种细胞成像计数装置,以解决相关技术中的至少部分问题。
7.本技术提供的一种细胞成像计数装置,包括底座、盖板、安装在底座上的第一基体以及安装在盖板上的第二基体;其中所述第二基体设有加样孔;所述细胞成像计数装置还包括形成于第一基体和第二基体之间的微流通道;其中:
8.所述盖板与所述底座活动连接;当所述盖板带动第二基体向所述底座上的第一基体靠近时第一基体与第二基体之间形成所述微流通道;所述微流通道与加样孔一一对应,所述微流通道与对应的所述加样孔连通。
9.可选的,还设有转轴;所述盖板通过所述转轴转动安装在底座上。通过这样设置,通过转动连接的方式能够更为方便的清洁掉或擦掉第一基体和第二基体上的样品残留。
10.可选的,所述底座包括上表面,其中所述上表面设有两第一凸起块;所述第一凸起块上设有安装孔;所述转轴的两端分别转动安装在所述安装孔内。通过这样设置可以使得盖板转动安装在底座的上方。
11.可选的,还包括位于盖板和底座之间的阻尼器。通过这样设置,盖板能够在自重的作用下比较平缓的闭合,从而避免盖板毫无阻力的砸向底座导致第一基体和/或第二基体损坏。
12.可选的,所述转轴与底座或盖板之间设有安装间隙。通过这样设置,可以使得调节器在调节微流通道高度时,第一基体和第二基体依旧能保持在大致平行的状态,确保各个微流通道的高度基本一致。
13.可选的,所述第一基体上设有第一平面;所述第二基体设有与第一平面一一对应的第二平面;当第二基体向第一基体靠近时,所述第一平面形成微流通道的底壁,所述第二平面形成微流通道的顶壁。通过这样设置,形成的微流通道方便对样品进行分析、拍照和成像。
14.可选的,所述第一基体的上表面上设有第一凸起部;所述第一平面位于第一凸起部的上表面;
15.和/或,所述第二基体的下表面上设有第二凸起部;所述第二平面位于第二凸起部的下表面。
16.通过这样设置,才能通过凸出于第一基体的上表面的第一平面和/或凸出于第二基体的下表面的第二平面利用表面张力的原理将样品约束住,从而形成一个个微流通道。
17.可选的,所述第一基体包括设置在其上表面上的凹槽;所述第一平面位于凹槽的底壁。
18.所述第二基体的下表面上设有第二凸起部;所述第二平面位于所述第二凸起部的下表面。
19.通过这样设置,能够通过第二平面利用表面张力将样品约束住,从而形成一个个微流通道。
20.可选的,所述第一平面与第一基体的上表面共面;
21.所述第二基体的下表面上设有第二凸起部;所述第二平面位于所述第二凸起部的下表面。
22.通过这样设置,能够通过第二平面利用表面张力将样品约束住,从而形成一个个微流通道。
23.可选的,所述第一基体的上表面上设有第一凸起部,所述第一平面位于所述第一凸起部的上表面;
24.所述第二平面与第二基体的下表面共面。
25.通过这样设置,能够通过第一平面利用表面张力将样品约束住,从而形成一个个微流通道。
26.可选的,所述第一平面与第一基体的上表面之间的间距不超过1mm。通过这样设置,当微流通道的底部壁为第一基体上凹槽的底壁时,该范围可以确保能够比较方便的对第一基体上的凹槽进行擦拭清洗。
27.可选的,相邻两第一平面之间的边缘间距不小于0.01mm;相邻两第二平面之间的边缘间距不小于0.01mm。通过这样设置,由于本发明中的微流通道为四面开放,因此,相邻微流通道之间设置一定的边缘间隙,能够避免不同微流通道中的样品混合。
28.可选的,所述第一平面为疏水面;所述第二平面为非疏水面或弱疏水面。通过这样设置,第一平面和第二平面之间设有一定的疏水性能差,从而可以把样品从加样孔内非常顺利的加入到微流通道内,以完成加样。
29.同时,第一平面设有良好的疏水性能,在擦拭时也能很容易的擦干净而不残留样品。
30.可选的,还设有安装在底座上的调节器;其中所述调节器用于调节微流通道高度。通过这样设置,可以根据不同大小和浓度的细胞样品来调节微流通道高度,使得该细胞计
数装置能够适应不同大小和浓度的细胞样品,从而提高检测效果。
31.可选的,所述微流通道的高度不超过10mm。通过这样设置,才能形成微流通道从而方便对样品进行分析、拍照和成像。
32.可选的,所述调节器为微米级的精密螺纹副装置,设有伸出杆;所述底座上设有一通孔,所述调节器安装在底座的下方,所述调节器的伸出杆穿过所述通孔后与盖板的下表面相抵,以使得第一基体和第二基体之间设有间隙。如此设置是因为微流通道的高度范围变化是一个非常小的范围,不超过10mm,因此,通过微米级的精密螺纹副装置可以很精确的来调整微流通道的范围;
33.同时,伸出杆与盖板的下表面相抵还能够使得第一基体和第二基体之间设有间隙,从而在第一基体和第二基体之间形成高度可调节的微流通道。
34.可选的,细胞成像计数装置还包括第三凸起块和限位部;所述第三凸起块和限位部分别设置于底座和盖板上,所述第三凸起块和限位部配合以限制盖板侧向移动。如此设置是因为,盖板和转轴之间的间隙使得盖板设有侧向移动的空间;因此,通过第三凸起块与限位部配合以限制盖板侧向移动;同时,还能使得在通过调节器调节微流通道高度时,盖板能够垂直升降,从而保证第一基体和第二基体之间一直处于平行的状态。
35.可选的,所述微流通道沿样品的移动方向依次设有加样区、检测区和排样区;加样孔的出口端与加样区连通;所述排样区的宽度沿样品的移动方向逐渐减小。通过这样设置,在盖板向上打开的过程中,使得第二平面上残留的样品,能够通过表面张力停留在排样区内,从而避免残留样品流至第二基体上。
36.可选的,所述微流通道中的顶壁和底壁平行分布。通过这样设置,可以提高微流通道中的细胞成像效果和检测精度。
37.可选的,还设有用于使得第一基体和第二基体之间设有间隙的第二凸起块;其中所述第二凸起块位于所述盖板的下表面或底座的上表面。通过这样设置,使得第一基体和第二基体之间设有间隙,从而形成高度固定的微流通道。
38.本技术提供的细胞成像计数装置中的盖板能够带动第二基体移动。通过这样设置,当微流通道里面有样品残留时,通过向上移动盖板,然后用无尘布清洁掉残留在第一基体和第二基体上的样品,确保无残留无污染,因此解决了现有的密闭式的微流芯片很难清洁样品残留的问题。
39.进一步的,本技术提供的细胞成像计数装置无需大量冲洗液来清洗微流通道,保护了环境,也提高了工作效率,克服了库尔特细胞计数法产生大量的鞘液废液和工作效率低的缺陷,同时也解决了当前图像法细胞计数中昂贵的一次性塑料细胞计数板使用成本和白色塑料污染问题。
40.应当理解的是,以上的一般描述和后文的细节描述仅是示例性和解释性的,并不能限制本技术。
附图说明
41.此处的附图被并入说明书中并构成本说明书的一部分,示出了符合本技术的实施例,并与说明书一起用于解释本技术的原理。
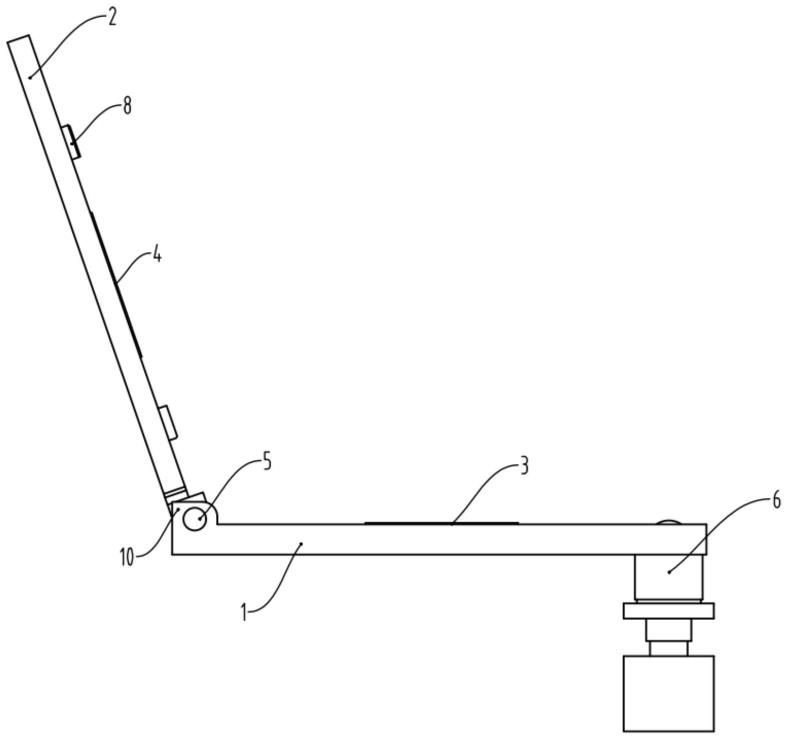
42.图1是本发明实施例一中细胞计数装置处于打开状态时的示意图;
43.图2是本发明实施例一中细胞计数装置处于关闭状态时的示意图;
44.图3是图2中细胞计数装置的俯视图;
45.图4是图3中a-a的剖视图;
46.图5是图4中的b处局部放大图;
47.图6是本发明实施例一中第一基体的俯视图;
48.图7是本发明实施例一中第一基体第一种实施方式的剖视图及其c处放大图;
49.图8是本发明实施例一中第一基体第二种实施方式的剖视图;
50.图9是本发明实施例一中第一基体第三种实施方式的剖视图及其d处放大图;
51.图10是本发明中实施例一中第二基体的俯视图;
52.图11是本发明中实施例一中第二基体的仰视图;
53.图12是本发明中实施例一中第二基体第一种实施方式的剖视图及其e处放大图;
54.图13是本发明中实施例一中第二基体第二种实施方式的剖视图。
具体实施方式
55.这里将详细地对示例性实施例进行说明,其示例表示在附图中。下面的描述涉及附图时,除非另有表示,不同附图中的相同数字表示相同或相似的要素。以下示例性实施例中所描述的实施方式并不代表与本技术相一致的所有实施方式。相反,它们仅是与如所附权利要求书中所详述的、本技术的一些方面相一致的装置和方法的例子。
56.在本技术使用的术语是仅仅出于描述特定实施例的目的,而非旨在限制本技术。除非另作定义,本技术使用的技术术语或者科学术语应当为本技术所属领域内设有一般技能的人士所理解的通常意义。本技术说明书以及权利要求书中使用的“第一”“第二”以及类似的词语并不表示任何顺序、数量或者重要性,而只是用来区分不同的组成部分。同样,“一个”或者“一”等类似词语也不表示数量限制,而是表示存在个。“多个”或者“若干”表示两个及两个以上。除非另行指出,“前部”、“后部”、“下部”和/或“上部”等类似词语只是为了便于说明,而并非限于一个位置或者一种空间定向。“包括”或者“包含”等类似词语意指出现在“包括”或者“包含”前面的元件或者物件涵盖出现在“包括”或者“包含”后面列举的元件或者物件及其等同,并不排除其他元件或者物件。“连接”或者“相连”等类似的词语并非限定于物理的或者机械的连接,而且可以包括电性的连接,不管是直接的还是间接的。
57.在本技术使用的术语是仅仅出于描述特定实施例的目的,而非旨在限制本技术。在本技术和所附权利要求书中所使用的单数形式的“一种”、“所述”和“该”也旨在包括多数形式,除非上下文清楚地表示其他含义。还应当理解,本文中使用的术语“和/或”是指并包含一个或多个相关联的列出项目的任何或所有可能组合。
58.实施例一:
59.如图1至图4所示,本技术提供一种细胞成像计数装置,包括底座1、盖板2、安装在底座1上的第一基体3以及安装在盖板2上的第二基体4。所述盖板2转动安装在底座1上。其中,第一基体3可以通过被夹持或粘接等方式安装在底座1上,并需要保持成水平状态以避免样品流出微流通道7。第二基体4可以通过被夹持或粘接的方式安装在盖板2上。第一基体3和第二基体4的材质为耐腐蚀,耐磨损,高硬度的透明材料。第一基体3和第二基体4可选为石英或玻璃。
60.如图2所示为细胞成像计数装置的关闭状态。所述细胞成像计数装置还包括形成于第一基体和第二基体之间的微流通道(结合图5所示)。所述第一基体和第二基体基本平行。将样品从加样孔40加入到微流通道7后样品能够在微流通道7内停留,然后通过相机对该微流通道7内的样品进行拍照分析,从而完成细胞计数工作。然后翻转盖板2使得细胞成像计数装置转变成如图1所示的开启状态,此时第一基体3和第二基体4之间形成大于90
°
的夹角,从而方便用无尘布清洁第一基体3和第二基体4上残留的样品,从而解决了现有的密闭式的微流芯片很难清洁样品残留的问题。另外,清洁完毕后再将盖板2向下翻转使得细胞成像计数装置还可重复使用,进而解决了当前图像法细胞计数中昂贵的一次性塑料细胞计数板使用成本和白色塑料污染问题。同时无需大量冲洗液来清洗微流通道7,保护了环境,也提高了工作效率,也解决了库尔特细胞计数法产生大量的鞘液废液和工作效率低的问题。
61.在本技术实施例中,细胞成像计数装置还包括转轴5。所述盖板2通过所述转轴5转动安装在底座1上。具体来说,所述底座1包括上表面,所述上表面设有两第一凸起块10,所述第一凸起块10上设有安装孔。所述转轴5的两端分别转动安装在所述安装孔内。通过这样设置,通过翻转盖板2的方式可以更为方便的开启或关闭所述微流通道7。
62.当然,在其他实施例中,盖板2还能够通过滑动或升降的方式安装在底座1上,从而也能够打开或关闭所述微流通道7。
63.在本技术实施例中,细胞成像计数装置还包括设置在盖板2和底座1之间的阻尼器。通过这样设置,盖板2能够在自重的作用下比较平缓的闭合,从而避免盖板2毫无阻力的砸向底座1导致第一基体3和/或第二基体4损坏。
64.在本技术实施例中,细胞成像计数装置还包括安装在底座1上的调节器6,所述调节器6用于调节微流通道7高度。其中,调节器6可选为微米级的精密螺纹副装置,设有伸出杆。所述底座1上设有一通孔,所述调节器6安装在底座1的下方,所述调节器6的伸出杆穿过所述通孔后与盖板2的下表面相抵,以使得第一基体和第二基体之间设有间隙。如此设置是因为微流通道7的高度范围变化是一个非常小的范围,不超过10mm,因此,通过微米级的精密螺纹副装置可以很精确的来调整微流通道7的范围。通过这样设置,如果细胞样品浓度很高,则可以把微流通道7高度调低来检测,如果细胞样品浓度很低,则可以把微流通道7高度调高来检测,从而保证良好的检测效果。
65.以及,伸出杆与盖板的下表面相抵还能够使得第一基体3和第二基体4之间设有间隙,从而在第一基体3和第二基体4之间形成高度可调节的微流通道7。
66.这里需要说明的是,盖板2、转轴5和底座1之间设有一定的安装间隙,从而使得调节器6在调节微流通道7高度时,第一基体3和第二基体4依旧能保持在大致平行的状态,确保各个微流通道7的高度基本一致。
67.在本技术实施例中,细胞成像计数装置还包括第三凸起块8和限位部。所述第三凸起块8和限位部配合以限制盖板2侧向移动。所述限位部为孔类结构或槽类结构。所述第三凸起块8设置在盖板2上,所述限位部设置在底座1上。当然,在其他实施例中,所述第三凸起块还可设置在底座上,以及所述限位部设置在盖板上。如此设置是因为,盖板2和转轴5之间的间隙使得盖板2设有侧向移动的空间;因此,通过第三凸起块8与限位部配合以限制盖板2侧向移动。同时,还能使得在通过调节器6调节微流通道高度时,盖板2能够垂直升降,从而
保证第一基体3和第二基体4之间一直处于平行的状态。
68.如图6中所示的第一基体3的表面为其上表面,在其上表面上设有多个第一平面30,其中,相邻两第一平面30之间的边缘间距不小于0.01mm,从而避免不同第一平面30中的样品混合。另外,在本技术实施例中仅展示了一排第一平面30,在其他实施例中,还可设置有多排第一平面30,从而能够实现高通量的细胞计数,大幅提高技术效率。
69.如图10中所示的第二基体4的表面为其上表面,在其上表面上设有多个加样孔40的进口端。
70.如图11中所示的第二基体4的表面为其下表面,在其下表面上设有多个第二平面41和多个加样孔40的出口端。其中,所述多个加样孔40的出口端分别分布在多个第二平面41上并一一对应。其中,相邻两第二平面41之间的边缘间距不小于0.01mm,从而避免不同第二平面41中的样品混合。另外,在本技术实施例中仅展示了一排第二平面41,在其他实施例中,还可设置有多排第二平面41,从而能够实现高通量的细胞计数,大幅提高技术效率。
71.在本技术实施例中,所述第一基体3的上表面上设有第一凸起部31。和/或,所述第二基体4的下表面上设有第二凸起部42。通过这样设置,才能通过凸出于第一基体的上表面的第一平面和/或凸出于第二基体的下表面的第二平面利用表面张力的原理将样品约束住,从而形成一个个微流通道7。
72.可选的,如图7所示,第一基体3的上表面上设有多个第一凸起部31。第一凸起部31的上表面即为第一平面30。如图13所示,第二平面41与第二基体4的下表面共面。图7中的第一基体3和图13中的第二基体4配合所形成的微流通道能够通过第一平面利用表面张力将样品约束住,避免样品散开。
73.可选的,如图8所示,第一平面30与第一基体3的上表面共面。如图12所示,所述第二基体4的下表面上设有第二凸起部42。所述第二凸起部42的下表面即为第二平面41。这样图8中的第一基体3和图12中的第二基体4配合所形成的微流通道能够通过第二平面利用表面张力将样品约束住,避免样品散开。
74.可选的,如图9所示,所述第一基体3的上表面上设有多个凹槽。凹槽的底壁即为第一平面30。这样图9中的第一基体3和图12中的第二基体4配合所形成的微流通道同时通过凹槽结构和第二平面的表面张力将样品约束在微流通道7内。
75.当然,图7中的第一基体3和图12中的第二基体4也能够配合形成微流通道;并且效果更好。
76.在本技术实施例中,所述第一平面30为疏水面。所述第二平面41为非疏水面或弱疏水面。通过这样设置,第一平面30和第二平面41之间设有一定的疏水性能差,从而可以把样品从加样孔40内非常顺利的加入到微流通道7内,以完成加样。
77.同时,第一平面30设有良好的疏水性能,在擦拭时也能很容易的擦干净而不残留样品。
78.在本技术实施例中,所述微流通道的高度不超过10mm。通过这样设置,才能使得第一平面和第二平面配合形成微流通道从而方便对样品进行分析、拍照和成像。
79.结合图6和图11来看,所述微流通道7沿样品的移动方向依次设有加样区、检测区和排样区。所述加样孔40位于加样区内。样品在进入微流通道7内后主要停留在检测区内,所述排样区的宽度沿样品的移动方向逐渐减小。通过这样设置,在盖板2向上打开的过程
中,第二平面41上残留的样品能够通过表面张力停留在排样区内,从而避免残留样品流至第二基体4上。另外,为了使得在盖板2向上打开的过程中,样品能够流入排样区内,可选样品的移动方向与转轴5垂直。
80.实施例二:
81.本实施例二与实施例一的不同之处在于:本实施例二中不再设置调节器。
82.在本技术实施例中,细胞成像计数装置还包括还设有用于使得第一基体和第二基体之间设有间隙的第二凸起块。其中所述第二凸起块位于所述盖板的下表面或底座的上表面。这样当细胞成像计数装置处于关闭状态时;避免第一基体和第二基体接触,从而使得第一平面和第二平面配合形成高度固定的微流通道。
83.在不产生冲突的情况下,本技术各实施方式可互为补充。
84.本领域技术人员在考虑说明书及实践这里公开的申请后,将容易想到本技术的其它实施方案。本技术旨在涵盖本技术的任何变型、用途或者适应性变化,这些变型、用途或者适应性变化遵循本技术的一般性原理并包括本技术未公开的本技术领域中的公知常识或惯用技术手段。说明书和实施例仅被视为示例性的,本技术的真正范围和精神由下面的权利要求指出。
85.应当理解的是,本技术并不局限于上面已经描述并在附图中示出的精确结构,并且可以在不脱离其范围进行各种修改和改变。本技术的范围仅由所附的权利要求来限制。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1