一种用于多模式检测过氧化氢的光学传感器及其制备方法与应用
1.本发明属于分析检测技术领域,具体涉及一种用于多模式检测过氧化氢的光学传感器及其制备方法与应用。
背景技术:
2.过氧化氢(h2o2)是活性氧(ros)物种的主要成员。迄今为止,h2o2被公认为衰老和各种疾病进展中重要的氧化应激标志物,参与广泛的生理和病理过程。作为一种潜在的生物标志物,h2o2是在疾病发展的过程中因非吞噬细胞受到细胞外刺激物刺激时产生的。在正常生理条件下,细胞器安全范围内低浓度的h2o2可以杀死微生物,维持细胞功能的稳定且不会对人体造成伤害。然而,在病理条件下,细胞产生的高浓度的h2o2(10~50μmol/l)会导致肿瘤细胞和上皮细胞的增殖和血管生成,以抵抗外界刺激并产生抗炎反应。此外,这个过程增加了炎症相关癌症产生的可能性,研究发现在一些癌细胞中,ros可以通过激活位于细胞膜中的七种nadph氧化酶复合物来产生。内质网中的黄素酶ero1也被证明利用o2作为双电子受体产生一定量的h2o2,在该亚细胞区域提供强ros通量。因此,作为一种潜在的疾病标志物,应量化h2o2以帮助医生有效诊断与活性氧相关的疾病。
3.为了阐明ros的生物学作用,量化它们的实时水平,并研究它们的分子机制,开发有效的探针来监测ros至关重要。这样的探针可以为我们提供新的研究工具和临床诊断。目前,针对h2o2的体内或体外检测已经研制出多种探针及传感器,这些策略具有较高的灵敏度、较低的检测限和巧妙的设计。然而,以往设计的策略需要依赖大型仪器和复杂的操作,检测时间过长,无法满足高灵敏、更快速、可视化、更简单的分析检测趋势。因此,确实需要开发具有改进性能的新探针来检测ros。
4.手性纳米材料包括单个手性纳米粒子和手性纳米组件,由于其灵活且可调节的尺度、光信号和合成策略,目前已广泛应用于催化、生物传感、以及研究手性纳米材料与生物系统之间的相互作用。存在于生物体系中的氨基酸,蛋白质等都属于手性分子,其手性信号分布在紫外区,因此,当手性纳米材料的手性信号分布在可见光区时,可避免来自生物体的背景手性信号的干扰,已广泛应用于生物分析。此外,手性材料能够通过修饰化学分子或与其他材料进行自组装而形成多功能复合材料,其同时具备高灵敏、高分辨成像的优势,xu课题组报道了一种通过有机金属框架zif-8将手性材料与上传换纳米材料整合到一起的手性核壳纳米组装体,该组装体优势在于同时具有手性光学信号以及荧光信号,能够应用于活体中进行活性氧的成像和半定量检测。此外,有报道通过设计合成了一种由夹板dna链组装而成的go-au np结构,通过与活靶细胞(mcf-7)一起孵育,研究了针对靶分子的动态手性和sers活性,显示出良好的选择性和稳定性。由此可知手性纳米材料在生物分析检测中具有非常大的前景。
5.为了满足高灵敏、高精度、更快速、可视化检测的需求,光学生物传感器被广泛研究。然而,目前的光学传感器主要依赖于单一信号分析,容易受到某些物质的干扰。相比之
下,基于双信号的光学传感器,例如比率传感器,双模式传感器具有高精度的优势。更重要的是,使用不同类型信号的双模光学传感器更有利于提高灵敏度和准确度,避免来自复杂基质的干扰,显示出可观的应用。目前,已经报道了基于双模态光信号的各种检测方法,例如手性和荧光,手性和表面增强拉曼散射(sers),荧光和sers,荧光探针可在某种特定条件下对分析物产生响应,尤其是荧光传感器被广泛研究并显示出多重检测能力和优异的灵敏度等优点。另一方面。sers传感器能够反映分子振动的信息,可以很好地产生sers增强效应,用于灵敏的单分子检测,其高灵敏度、高分辨率、检测速度快和指纹图谱的优势而成为了一种重要的生物传感和痕量分析技术。因此目前已成为生物标志物超灵敏检测和疾病诊断的热门技术。近年来,基于sers和荧光的双信号光学传感器已被广泛开发用于检测应用。
技术实现要素:
6.针对以上现有技术存在的缺点和不足之处,本发明的首要目的在于提供一种用于多模式检测过氧化氢的光学传感器的制备方法。
7.本发明的另一目的在于提供通过上述制备方法得到的用于多模式检测过氧化氢的光学传感器。
8.本发明的再一目的在于提供上述用于多模式检测过氧化氢的光学传感器的应用。
9.为了实现上述发明目的,本发明采用以下技术方案:
10.一种用于多模式检测过氧化氢的光学传感器的制备方法,包括如下步骤:
11.步骤1:将haucl4溶液与水混合均匀,搅拌,接着加入银纳米颗粒(ag nps)溶液和左旋多巴(l-dope)水溶液,继续搅拌;反应液加水,离心洗涤,收集沉淀,再分散于水中,得到纳米合金粒子(uaa-ncs)胶体溶液,简称为uaa-ncs胶体溶液;
12.步骤2:在步骤1得到的uaa-ncs胶体溶液中加入十六烷基三甲基溴化铵(ctab)溶液,搅拌,接着分别加入2-甲基咪唑(2-meim)溶液和zn(no3)2溶液,反应;反应液离心分离,收集沉淀,所述沉淀即为zif-8(沸石咪唑骨架材料)包裹的海胆状纳米合金(uaa@zif-8)颗粒,简称为uaa@zif-8颗粒;uaa@zif-8颗粒经洗涤再分散在水中,得到uaa@zif-8水溶液;
13.步骤3:取步骤2得到的uaa@zif-8水溶液,加入nicl2水溶液,搅拌反应,接着在剧烈搅拌下向混合溶液中加入d型或l型的青霉胺(d/l-pen)水溶液,再逐滴加入naoh水溶液,继续搅拌反应,即获得所述的用于多模式检测过氧化氢的光学传感器。
14.进一步地,步骤1中所述的haucl4溶液的浓度为0.005~0.015mol/l;优选为0.01mol/l。
15.进一步地,步骤1中所述的银纳米颗粒的平均粒径为25~35nm,优选35nm;所述的银纳米颗粒溶液优选通过如下方法制备得到:在0.05~0.15mol/l,优选0.1mol/l nh2oh
·
hcl溶液中按体积比100:2~4,优选100:3.3加入0.05~0.15mol/l,优选0.1mol/l naoh溶液,然后向所得混合溶液以0.6~0.7ml/s,优选0.67ml/s的流速、按体积比8~10:1,优选9:1加入0.05~0.15mol/l,优选0.1mol/l agno3溶液;将反应容器倒置一次以完成混合,即获得目标产物。
16.进一步地,步骤1中所述的左旋多巴水溶液的浓度为0.005~0.015mol/l;优选为0.01mol/l。
17.进一步地,步骤1中所述的haucl4溶液、水、银纳米颗粒溶液、左旋多巴水溶液、分
散用的水的体积比为4~5:8~9:1~2:9~10:9~11;优选为4.8:8.6:1.8:9.6:10。
18.进一步地,步骤1中所述的搅拌为在14~16℃水浴中磁力搅拌,搅拌转速为100~300rpm,搅拌时间为8~12min;优选为15℃水浴中磁力搅拌,搅拌转速为200rpm,搅拌时间为10min。
19.进一步地,步骤1中所述的离心洗涤的转速为3500~4500rpm,时间为8~12min;优选的转速为4000rpm,时间为10min。
20.进一步地,步骤2中所述的十六烷基三甲基溴化铵溶液的浓度为0.005~0.015mol/l;优选为0.01mol/l。
21.进一步地,步骤2中所述的2-甲基咪唑溶液的浓度为1~2mol/l;优选为1.32mol/l。
22.进一步地,步骤2中所述的zn(no3)2溶液的浓度为22~26mmol/l;优选为24mmol/l。
23.进一步地,步骤2中所述的uaa-ncs胶体溶液、十六烷基三甲基溴化铵溶液、2-甲基咪唑溶液、zn(no3)2溶液、分散用的水的体积比为1~2:1~2:1~2:1~2:1~2;优选为1:1.5:1:1:1。
24.进一步地,步骤2中所述的反应为在35~45℃水浴中反应,反应时间为2.5~3.5h;优选为在40℃水浴中反应,反应时间为3h。
25.进一步地,步骤2中所述的离心分离的转速为5500~6500rpm,时间为8~12min;优选的转速为6000rpm,时间为10min。
26.进一步地,步骤3中所述的nicl2水溶液的浓度为0.1~0.3mol/l;优选为0.2mol/l。
27.进一步地,步骤3中所述的青霉胺水溶液的浓度为0.1~0.3mol/l;优选为0.2mol/l。
28.进一步地,步骤3中所述的naoh水溶液的浓度为0.1~0.3mol/l;优选为0.2mol/l。
29.进一步地,步骤3中所述的uaa@zif-8水溶液、nicl2水溶液、青霉胺水溶液、naoh水溶液的体积比为0.5~2:0.05~0.15:0.05~0.15:0.05~0.15;优选为1:0.1:0.1:0.1。
30.进一步地,步骤3中所述的加入nicl2水溶液后的搅拌为磁力搅拌,搅拌转速为200~400rpm,时间为25~35min;优选的搅拌转速为300rpm,时间为30min。
31.进一步地,步骤3中所述的加入naoh水溶液后的继续搅拌的时间为50~70min;优选为60min。
32.进一步地,步骤3中获得所述的用于多模式检测过氧化氢的光学传感器后,离心洗涤,水洗多次出于多余的反应物并分散在水中进行保存。
33.所述的离心洗涤的转速为3000~4000rpm,时间为8~12min;优选的转速为3500rpm,时间为10min。
34.一种用于多模式检测过氧化氢的光学传感器,通过上述制备方法得到。
35.上述用于多模式检测过氧化氢的光学传感器在多模式识别和/或定量过氧化氢中的应用。
36.进一步地,所述的应用的具体操作为:将所述的光学传感器的分散液与邻苯二胺(opd)溶液混合形成探针溶液,然后添加到待测体系中,孵育,观察颜色变化或者利用圆二
色谱仪检测系统的cd信号变化或者利用拉曼光谱仪检测邻苯二胺的特征峰信号变化,以识别和/或定量过氧化氢。
37.进一步地,所述的光学传感器的分散液的浓度为0.05~2mol/l;通过颜色变化别和/或定量过氧化氢时,浓度优选为0.05~0.15mol/l。
38.进一步地,所述的邻苯二胺溶液的浓度为0.05~0.15mol/l;优选为0.1mol/l。
39.进一步地,所述的光学传感器的分散液与邻苯二胺溶液的体积比为0.1~0.5:0.5~1.5;优选为0.2:1。
40.进一步地,所述的孵育的条件为温度为35~39℃、时间25~35min;优选为37℃、时间30min。
41.进一步地,所述的待测体系为含有过氧化氢的溶液或生物样本。
42.进一步地,所述生物样本包括但不限于活细胞、组织、血液等。
43.进一步地,所述的应用中过氧化氢的检测范围在1nmol/l到400μmol/l;优选在1nmol/l到100μmol/l。;更优选在0.1μmol/l到100μmol/l。
44.本发明的原理:本发明在多孔zif-8包裹纳米合金uaaa结构的核-壳纳米材料的表面修饰上手性纳米材料nisx-l,获得复合材料ua@zif-8-nisx,该复合材料同时具备手性信号以及拉曼“热点”,用于比色/手性/拉曼三传感模式定性定量h2o2。在h2o2存在下,随着手性材料被降解,其cd信号随h2o2的增大而减小。同时,在uaa@zif-8的催化下,在uaa@zif-8表面修饰的邻苯二胺(opd)可被h2o2快速催化,引起颜色的变化。此外,在拉曼光谱仪检测下,opd的拉曼信号也会发生变化,从而实现多模式检测h2o2。
45.本发明相对于现有技术具有如下的优点及效果:
46.(1)本发明合成了一种基于手性材料的新型sers光学传感器,其在多孔zif-8包裹uaa-ncs结构的核-壳纳米材料的表面修饰上手性纳米材料(uaa@zif-8-nisx),该光学传感器同时具有圆二信号以及拉曼信号,可用于多模式检测h2o2;
47.(2)在h2o2的存在下,光学传感器表面的手性纳米材料降解,吸附在uaa@zif-8表面的手性材料颗粒逐渐减少,在圆二色谱仪检测下,其cd信号逐渐降低最终消失;同时,uaa@zif-8纳米材料在h2o2的存在下会快速催化opd,一方面可以通过肉眼观察到明显的颜色变化,另一方面由于opd被催化,在拉曼光谱仪检测下,opd的特征峰信号会明显减弱;
48.(3)本发明所建立的方法与目前检测h2o2的技术相比,主要优势在于在高浓度目标物的存在下可以直接通过比色法进行检测,避免借助复杂仪器。此外,我们所设计的光学传感器将手性与拉曼结合,实现对h2o2的快速、可视化、和高灵敏度的检测。最重要的是,通过三模式的检测方法既提高了检测h2o2的效率也提升了检测结果的可靠性,同时扩大了检测的范围。该策略突出了手性纳米组件在ros检测中的潜力,为开发手性纳米材料用于生物医学和生物分析的工具箱开辟了一条新途径。
附图说明
49.图1为uaa@zif-8-nisx光学传感器制备过程纳米材料的透射电镜图;其中,a为uaa-ncs纳米粒子,b为uaa@zif-8纳米粒子;c为uaa@zif-8-nisx,d为uaa@zif-8-nisx用0.1mmol/l h2o2处理,手性材料降解;
50.图2为uaa@zif-8-nisx光学传感器的sers性能研究结果图;其中,a为uaa-ncs、
uaa@zif-8和uaa@zif-8-nisx的拉曼光谱,b为对应于a的641cm-1
处的拉曼增强效应比较;c为uaa@zif-8-nisx的时间依赖性拉曼光谱,d为对应于c的641cm-1
处的拉曼强度,rsd为4.188%;
51.图3为l-pen存在下制备的手性纳米材料nisx-l的tem图;
52.图4为手性纳米材料与h2o2之间的反应的验证结果图;其中,a为nisx-l的cd光谱,b为nisx-l的紫外-可见光谱,c为nisx-l和0.1mmol/l h2o2处理后的nisx-l的紫外-可见光谱,d为nisx-l和0.1mmol/l h2o2处理后的nisx-l的紫外-可见光谱;
53.图5为uaa@zif-8-nisx光学传感器对于检测策略的可行性的验证结果图;其中,a为uaa@zif-8-nisx和0.1mmol/l h2o2处理uaa@zif-8-nisx和的cd光谱,b为uaa@zif-8-nisx和0.1mmol/l h2o2处理uaa@zif-8-nisx和的sers光谱;
54.图6为uaa@zif-8-nisx光学传感器的催化性能的验证结果图;其中,a为uaa@zif-8-nisx传感器,b为0.1mmol/l opd加入h2o2在37℃下孵育30mins,c为uaa@zif-8-nisx传感器加入opd和h2o2在37℃下孵育30min;
55.图7为比色法检测h2o2的结果图;其中,a为检测系统在h2o2浓度范围为0至100μmol/l时的颜色变化(在37℃水浴中反应30mins),b为uv-vis光谱;
56.图8为圆二色谱法检测h2o2的结果图;其中,a和c为检测系统在不存在和存在不同浓度的h2o2的情况下的cd光谱,b为对应于a的h2o2的标准曲线,d为对应于b的h2o2的标准曲线(误差棒表示三次测量的标准偏差);
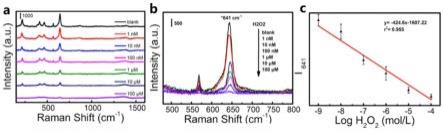
57.图9为sers法检测h2o2的结果图;其中,a为检测系统在不同浓度h2o2存在下的sers光谱;b为在450-800cm-1
范围内拉曼峰强度随h2o2浓度增加的变化情况;c为h2o2的标准曲线(误差棒表示三次测量的标准偏差);
58.图10为uaa@zif-8-nisx光学传感器的特异性研究结果图;其中,a为检测不用h2o2处理的亮场图像,b为对应于a的荧光图像,c为检测系统用opd孵育6h,h2o2孵育60min的亮场图像,d为对应于c的荧光图像。
具体实施方式
59.下面结合实施例和附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
60.实施例1:uaa@zif-8-nisx光学传感器的制备与表征
61.步骤一:银纳米颗粒(agnps)的制备
62.ag nps的合成主要参照报道的方法,首先配制0.1mmol/l的agno3溶液,另外在100ml的nh2oh
·
hcl(0.1mmol/l)溶液中加入3.3ml naoh(0.1mol/l)混合均匀,接着先在离心管中加入9ml上述混合溶液。在不搅拌的情况下,以0.67ml/s的流速向离心管中加入1ml agno3。最后,将离心管倒置一次以完成混合得到灰绿色溶液,置于4℃下避光保存。
63.步骤二:海胆状纳米合金粒子(uaa-ncs)的制备
64.参考文献adv mater 26(15)(2014)2431-9.公开的方法。首先,在25ml的烧瓶中加入4.8ml的haucl4溶液(0.01mol/l)和8.6ml的超纯水混合均匀,在15℃的低温水浴中磁力搅拌(300rpm,10min),接着加入1.8ml先前制备好的ag nps(30nm)和9.6ml l-dope(0.01mol/l)水溶液,继续低温水浴搅拌反应15mins,用水离心洗涤(4000rpm,10min),分散
于10ml水中,形成uaa-ncs溶液。
65.步骤三:zif-8包裹的海胆状纳米合金(uaa@zif-8)的合成
66.将1ml uaa-ncs胶体溶液加入1.5ml ctab(0.1mmol/l),磁力搅拌5min以混合均匀,接着分别加入1ml 2-meim(1.32mol/l)和1ml zn(no3)2(24mmol/l)并置于40℃水浴中反应3小时。这样在溶液中形成zif-8包裹的uaa-ncs结构,并通过离心(6000rpm,10min)收集以除去一些未包裹的zif-8颗粒,水洗并分散在1ml水中。
67.步骤四:表面修饰手性材料的uaa@zif-8的(uaa@zif-8-nisx)的合成
68.参考文献j am chem soc.141(49)(2019)19373-19378.公开的方法。首先在5ml烧瓶中加入1ml先前制备的uaa@zif-8水溶液,接着加入0.1ml nicl2(0.2mol/l)水溶液,磁力搅拌30min(转速为300rpm)。然后,在剧烈搅拌下向混合溶液中加入0.1ml d/l-pen(0.2mol/l)水溶液,再逐滴加入0.1ml naoh(0.2mol/l)水溶液,继续搅拌反应1小时,接着离心洗涤(3500rpm,10min),水洗2次除去多余的反应物并分散在水中。
69.用透射电镜(tem)图来观察其制备过程纳米材料的变化。结果如图1所示,从图1中的a-c可以清楚的看出,首先合成了uaaa-nps纳米材料,然后包裹上zif-8材料形成uaa@zif-8的核壳结构材料,之后再在表面修饰上手性材料,表面的mof材料被刻蚀了大部分。
70.实施例2:uaa@zif-8-nisx光学传感器的sers性能
71.uaa@zif-8-nisx光学传感器是基于mof的新型sers基底,由于mof独特的结构和性能,赋予了基底优良的性能,改善了传统sers基底的传感性能,如化学增强能力和分子富集能力。此外,由于手性材料的刻蚀,增强了拉曼“热点”,因此这种新型sers基底具有优异的拉曼增强能力。如图2中a和b所示,在相同条件下,opd在641cm-1
的拉曼信号是单一未包裹的uaaa-nps的3倍。
72.由于拉曼报告分子opd被封装在mof与手性纳米材料结构中,因此能够产生重复性良好且稳定性高的拉曼信号,时间依赖的拉曼光谱如图2中c所示。uaa@zif-8-nisx纳米材料在641cm-1
处的拉曼峰相比其他峰来说,信号强度高且在采集过程中保持良好的稳定性,相对标准偏差(rsd)为4.188%(图2中d),基于sers信号强度和探针稳定性两方面因素的考虑,我们选择641cm-1
处的峰作为h2o2检测的特征峰。
73.实施例3:uaa@zif-8-nisx光学传感器检测策略可行性的验证
74.第一步,制备单一分散的手性纳米材料nisx-l:nisx-nps的制备根据已有文章报道的方法,首先在nicl2(0.2mol/l)水溶液中加入0.1ml l-pen或d-pen(0.2mol/l)水溶液,再逐滴加入0.1ml naoh(0.2mol/l)水溶液,经过磁力搅拌反应1小时,得到分散的nisx-nps溶液。
75.nisx-l的tem图如3所示,检测结果显示其在440nm和530nm有强烈的圆二色性(cd)信号(图4中a),在490nm左右具有紫外吸收信号(图4中b)。
76.第二步,对手性纳米材料nisx-l与h2o2之间的反应进行验证:首先,在石英比色皿中加入200μl uaa@zif-8-nisx(azn)溶液和1ml opd溶液(0.1mol/l),并用移液枪混匀形成探针溶液,将500μl预定浓度的h2o2溶液(浓度为0、0.1μmol/l、1μmol/l、10μmol/l、50μmol/l、100μmol/l、200μmol/l、400μmol/l)分别加进探针溶液中,将混合物在37℃水浴中孵育30mins。在室温中观察其颜色的变化。
77.结果如图4中c和d所示,cd光谱以及紫外吸收光谱均发生了变化,说明h2o2可以将
手性材料降解,证实了该检测策略的可行性。
78.第三步,验证uaa@zif-8-nisx光学传感器对于检测策略的可行性:参考实施例1制备uaa@zif-8-nisx光学传感器并检测其圆二色性。
79.结果如图5所示,结果表明该材料同样在440nm以及530nm处有圆二信号,且加入h2o2后圆二信号减弱(图5中a)。此外,将uaa@zif-8-nisx作为sers探针,检测其加入h2o2前后的拉曼信号变化,结果如图5中b显示,由于opd被h2o2催化,其特征峰的拉曼信号减弱。
80.第四步,对纳米材料的催化性能进行验证:制备只有uaa@zif-8-nisx光学传感器存在的溶液(图6中a),以及没有光学传感器存在下h2o2和opd单独反应的空白组(图6中b)。
81.结果表明,在同样的温度时间下,反应颜色会变成深绿色(图6中的c),与没有纳米复合材料参与的空白组对比,验证了纳米材料是具有催化作用的。
82.实施例4:uaa@zif-8-nisx光学传感器的应用
83.(1)比色法检测h2o284.首先,在石英比色皿中加入200μl uaa@zif-8-nisx(azn)溶液(0.1mol/l)和1ml opd溶液(0.1mol/l),并用移液枪混匀形成探针溶液,然后将500μl预定浓度的h2o2溶液(浓度为0、0.1μmol/l、1μmol/l、10μmol/l、50μmol/l、100μmol/l、200μmol/l、400μmol/l)分别加进探针溶液中,将混合物在37℃水浴中孵育30min。在室温中观察其颜色的变化。
85.图7中a显示了不同浓度h2o2的响应情况,随着h2o2的浓度由0逐渐增加至400μmol/l,该检测系统的颜色变化情况为从无色到黄绿色。肉眼可观察到浓度低至0.1μmol/l的颜色变化。随后,我们测量了空白对照溶液以及uaa@zif-8-nisx光学传感器在检测h2o2过程的紫外吸收变化。图7中b绘制了空白对照溶液以及检测系统前后的uv-vis吸收光谱,实验数据表明,在h2o2的存在下,检测系统在430nm处会出现紫外吸收,但随着浓度变化不存在线性关系。
86.(2)圆二色谱法检测h2o287.首先,将200μl uaa@zif-8-nisx(azn)溶液(1mol/l)和1ml opd溶液(0.1mol/l)用移液枪混匀形成探针溶液,然后将500μl预定浓度的h2o2溶液(浓度为0、1nmol/l、10nmol/l、100nmol/l、1μmol/l、10μmol/l、100μmol/l)分别加进探针溶液中,将混合物在37℃水浴中孵育30min。所得溶液用于光谱测量。
88.图8中a和c绘制了检测系统溶液在不存在和存在不同浓度的h2o2的情况下的圆二光谱。实验数据表明,随着h2o2浓度的增加,检测系统在440nm和530nm处的圆二信号逐渐减弱。440nm和530nm处的圆二信号变化揭示了与h2o2浓度在0.1至100μmol/l范围内的良好线性相关性(图8中b和d)。该手性测定法的检测限(lod)为0.1μmol/l。该lod的水平与报道的用于检测h2o2的比色法和荧光法相当或更好。
89.(3)sers法检测h2o290.首先,将200μl uaa@zif-8-nisx(azn)溶液(1mol/l)和1ml opd溶液(0.1mol/l)用移液枪混匀形成探针溶液,然后将100μl预定浓度的h2o2溶液(浓度为0、0.1μmol/l、0.5μmol/l、2μmol/l、5μmol/l、10μmol/l、20μmol/l、50μmol/l、100μmol/l)分别加进探针溶液中,将混合物在37℃水浴中孵育30min。所得溶液用于sers检测。
91.结果表明,随着h2o2浓度的增加,opd报告分子的特征峰在641cm-1
的拉曼强度随h2o2浓度增加而减弱,实验结果显示信号探针的特征峰拉曼强度与h2o2浓度之间存在负相
关(图9中b),二者之间线性关系良好,其标准曲线如图9中c所示,其检测范围在1nmol/l到100μmol/l,能检测到的h2o2最低浓度水可以达到1nmol/l。
92.(4)在活细胞中可视化检测h2o293.hela细胞在含有10%热灭活胎牛血清(fbs)和100μg/ml青霉素/链霉素的培养基(dmem)中进行培养过夜,其培养条件为37℃、5%co2和95%相对湿度。将最终数量为2
×
104的细胞接种到96孔板的每个孔中,分为两组:
94.第一组:将200μl uaa@zif-8-nisx(azn)溶液(1mol/l)和1ml opd溶液(0.1mol/l)用移液枪混匀形成探针溶液,将探针(opd的终浓度为10-3
mol/l)添加到孔中,孵育30min,接着丢弃原始培养基并填充新鲜培养基,最后加入h2o2溶液再孵育60分钟;
95.第二组:将200μl uaa@zif-8-nisx(azn)溶液(1mol/l)和1ml opd溶液(0.1mol/l)用移液枪混匀形成探针溶液,将探针(opd的终浓度为10-3
mol/l)添加到孔中,孵育30min,然后丢弃原始培养基并填充新鲜培养基。
96.在共聚焦显微镜系统(leica)上以502nm的激发波长获取共聚焦激光扫描显微镜图。
97.结果如图10所示,结果表明基于手性的uaa@zif-8-nisx光学传感器所采用的探针分子opd具有荧光,当加入h2o2后,纳米材料会促使其快速催化opd,从而使其荧光明显减弱,而对于其他常见阴离子不会有荧光减弱的变化,因此该探针有望用于特异性识别活细胞中的h2o2。最初,用探针处理hela细胞。作为对照,拍摄并比较了用和不用h2o2溶液处理的hela细胞的荧光共聚焦图像。结果清楚地表明,探针在没有h2o2的情况下显示出荧光,而加入h2o2处理的探针荧光明显减弱。这些数据证明了opd作为一种敏感的荧光探针的潜力,该光学传感器可用于特异性检测细胞中h2o2。
98.上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受所述的实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1