一种可磁控响应的液相漂浮微球及制备方法
1.本发明属于磁性纳米材料技术领域,尤其涉及一种可磁控响应的液相漂浮 微球及制备方法。
背景技术:
2.目前,磁珠,不论是微米级的微球还是纳米级的纳米颗粒,由于具有良好 的磁响应性,在磁场作用下可定向运动到特定部位,可以迅速从周围介质中分 离出来,因此有着极广阔的应用前景,包括细胞分离、蛋白质分离和纯化、固 定化酶、免疫分析测定、靶向药物、dna分离与核酸杂交等领域。然而其在液 相中使用时会因为重力作用发生沉降,往往需要外界的机械力(摇晃等)来保 证其能在液相中与待作用的物质有一定的接触几率。但是因磁珠本身固有性质 (质量,体积,磁响应能力等)的不同,外界机械力的作用可能会对待作用/分 离的物质造成应力伤害/损害;也可能有些场所不便于使用震荡等力学行为。因 此,需要开发一种策略,调控磁性微球在液相中的运动行为,或调控其沉降行 为,以便于对目标物质开展便捷有效的作用,并同时减小因机械应力带来的损 伤。
3.通过上述分析,现有技术存在的问题及缺陷为:现有的磁珠在液相中需要 施加外界的机械力,应用场景受限;同时磁珠会因机械应力带来损伤,导致应 用效果不佳。
技术实现要素:
4.针对现有技术存在的问题,本发明提供了一种可磁控响应的液相漂浮微球 及制备方法。
5.本发明是这样实现的,一种可磁控响应的液相漂浮微球,所述可磁控响应 的液相漂浮微球的外层为中空玻璃微球,所述中空玻璃微球内组装有超顺磁性 磁性纳米颗粒;微球以中空玻璃微球为基底,由内到外分别为聚乙烯亚胺(pei) 层、四氧化三铁磁性纳米颗粒(mnps)层、聚乙烯亚胺(pei)层、聚丙烯酸(paa) 层、识别分子层(抗体、适配体、多肽);
6.所述可磁控响应的液相漂浮微球可同时受到浮力与磁力的调控。
7.本发明的另一目的在于提供一种所述可磁控响应的液相漂浮微球的可磁控 响应的液相漂浮微球制备方法,所述可磁控响应的液相漂浮微球的制备方法包 括:
8.采用层层自组装的方法通过hgms表面包覆聚合物层、hgms与mnps组装 以及材料修饰将超顺磁性磁性纳米颗粒组装至中空玻璃微球,得到hgms@mnps 复合材料;
9.所述hgms@mnps复合材料为可磁控响应的液相漂浮微球。
10.进一步,所述可磁控响应的液相漂浮微球制备方法包括以下步骤:
11.步骤一,通过将洁净的hgms与聚乙烯亚胺孵育,得到表面包覆pei层的带 正电的hgms;
12.步骤二,将表面带有负电的磁性纳米颗粒与修饰后的hgms进行孵育,通 过静电作用将mnps组装至hgms表面;
13.步骤三,将组装好的hgms@mnps先与pei孵育后再与聚丙烯酸孵育,得 到表面具有
大量羧基的hgms@mnps复合材料;并对所述表面具有大量羧基的 hgms@mnps复合材料进一步修饰得到可磁控响应的液相漂浮微球。
14.进一步,所述通过将洁净的hgms与聚乙烯亚胺孵育,得到带正电的hgms 包括:
15.首先,称取一定量的hgms,利用ph为8的nacl缓冲液润洗三遍,再利用 hgms漂浮的特性收集洁净的hgms;
16.其次,称取一定量聚乙烯亚胺溶解于缓冲液中,配制成浓度为1mg/ml的聚 乙烯亚胺溶液;
17.最后,将配置好的聚乙烯亚胺溶液与hgms混合摇晃孵育30min;再使用 buffer反复洗涤去除多余的反应物,再用移液枪吸出溶液后备用。
18.进一步,所述将表面带有负电的磁性纳米颗粒与修饰后的hgms进行孵育, 通过静电作用将mnps组装至hgms表面包括:
19.将带负电的磁性纳米颗粒分散于缓冲液中;将mnps溶液与hgms混合,室 温下摇晃孵育30min,再使用buffer反复洗涤去除多余的反应物,得到 hgms@mnps。
20.进一步,所述将组装好的hgms@mnps先与pei孵育后再与聚丙烯酸孵育, 得到表面具有大量羧基的hgms@mnps复合材料包括:
21.(1)称取一定量聚丙烯酸paa,溶解于ph为8的nacl缓冲液,配制成浓 度为2.4mg/ml的paa溶液;
22.(2)将制备好的hgms@mnps先于pei溶液室温下摇晃孵育30min,利用 材料的磁响应性反复洗涤去除多余的pei,再与paa溶液室温下摇晃孵育30min, 反复洗涤。
23.进一步,所述对表面具有大量羧基的hgms@mnps复合材料进一步修饰得 到可磁控响应的液相漂浮微球包括:
24.通过缩合反应/静电组装/物理吸附修饰表面具有大量羧基的hgms@mnps 复合材料。
25.本发明的另一目的在于提供一种所述可磁控响应的液相漂浮微球在液相检 测、液相分离中的应用。
26.本发明的另一目的在于提供一种所述可磁控响应的液相漂浮微球在液相催 化中的应用。
27.本发明的另一目的在于提供一种所述可磁控响应的液相漂浮微球在生物体 外检测中的应用。
28.结合上述的技术方案和解决的技术问题,请从以下几方面分析本发明所要 保护的技术方案所具备的优点及积极效果为:
29.第一、针对上述现有技术存在的技术问题以及解决该问题的难度,紧密结 合本发明的所要保护的技术方案以及研发过程中结果和数据等,详细、深刻地 分析本发明技术方案如何解决的技术问题,解决问题之后带来的一些具备创造 性的技术效果。具体描述如下:
30.本发明的可磁控响应的液相漂浮微球能同时受到浮力与磁力调控且制备过 程简单,表面的大量羧基可以用于结合各类识别分子。
31.本发明提供了一种生物体外检测的新型材料与孵育方法。本发明制备过程 简单,可以批量生产,可以降低孵育过程中对生物标志物(细胞)的损害,有 利于标志物的下游分
析。
32.本发明通过将洁净的hgms(10mg/ml)与聚乙烯亚胺(pei、1mg/ml)孵 育,得到表面包覆了pei层带正电的hgms,pei层提供可以继续吸附/结合磁响 应组分(四氧化三铁磁性纳米粒子,或者其他的磁性纳米粒子)的能力。
33.本发明将表面带有负电的磁性纳米颗粒(mnps,粒径约为20nm,15mg/ml) 与修饰后的hgms进行孵育;通过物理结合(静电吸附)将磁性纳米粒子结合 与上述复合体,使材料获得磁响应能力。
34.本发明将组装好的hgms@mnps先与pei孵育后再与聚丙烯酸(paa、 2.4mg/ml)孵育,得到表面具有大量羧基的hgms@mnps复合材料;通过外围 的进一步修饰,对所结合的磁性纳米粒子进行进一步的稳定,并且在材料表面 引入大量羧基并且可以通过缩合反应/静电组装/物理吸附修饰目标物质识别分 子(抗原,蛋白受体,适配子等)特异性结合或识别目标分子。
35.第二,把技术方案看做一个整体或者从产品的角度,本发明所要保护的技 术方案具备的技术效果和优点,具体描述如下:
36.本发明创造性的提出磁响应的可漂浮的微球概念;本发明的可磁控响应的 液相漂浮微球可被磁控,提供了不同于外界机械力的另一种方式对微球开展“操 控”。本发明所制备的微球可以用于液相(不管是水还是有机溶剂,只要比微球 密度大的液体)中的检测,分离,甚至催化等领域。
37.第三,作为本发明的权利要求的创造性辅助证据,还体现在以下几个重要 方面:
38.本发明的技术方案填补了国内外业内技术空白:在现有技术中,为了与目 标物质充分接触,磁珠往往搭配摇床或是机械震动使用,然而磁珠与目标物质 孵育的同时,剧烈的机械碰撞会使一部分目标物质被损坏,此外也有一些场景 下并不适用激烈的机械震荡。在本发明中提出了一种可磁控响应的液相漂浮微 球概念,并且成功制备,由于磁控响应的液相漂浮微球的行为同时受到磁力与 浮力的调控,本发明可以通过外加周期性的磁场,在浮力的共同的作用下,使 材料周期性运动,实现磁珠与待作用物质的充分接触为磁分离材料孵育提供了 一种新方法与思路。
附图说明
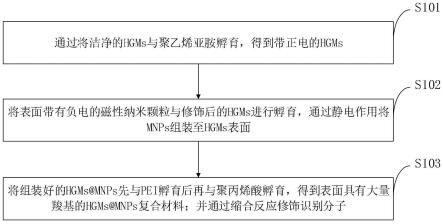
39.图1是本发明实施例提供的可磁控响应的液相漂浮微球的制备方法流程图;
40.图2是本发明实施例提供的组装前的hgms光学显微镜图;
41.图3是本发明实施例提供的组装后的hgms@mnps光学显微镜图;
42.图4是本发明实施例提供的hgms@mnps的粒径分布统计示意图;
43.图5是本发明实施例提供的单颗hgms的sem图像;
44.图6是本发明实施例提供的不同区域放大后的sem图像;
45.图7是本发明实施例提供的hgms@mnps材料表面的eds元素分析示意图;
46.图8是本发明实施例提供的未经修饰的hgms@mnps@paa共聚焦分析示意 图;
47.图9是本发明实施例提供的修饰后的hgms@mnps@paa共聚焦分析示意 图;
48.图10是本发明实施例提供的hgms@mnps与待作用物质的运动示意图;
49.图11是本发明实施例提供的hgms@mnps捕获循环肿瘤细胞后的共聚焦 图;
50.图12是本发明实施例提供的修饰后的有无磁场时的行为变化示意图;
具体实施方式
51.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例, 对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以 解释本发明,并不用于限定本发明。
52.一、解释说明实施例。为了使本领域技术人员充分了解本发明如何具体实 现,该部分是对权利要求技术方案进行展开说明的解释说明实施例。
53.本发明实施例提供的可磁控响应的液相漂浮微球的制备方法包括:
54.采用层层自组装的方法通过hgms表面包覆聚合物层、hgms与mnps组装 以及材料修饰将超顺磁性磁性纳米颗粒组装至中空玻璃微球,得到 hgms@mnps复合材料即可磁控响应的液相漂浮微球。微球以中空玻璃微球为 基底,由内到外分别为聚乙烯亚胺(pei)层、四氧化三铁磁性纳米颗粒(mnps) 层、聚乙烯亚胺(pei)层、聚丙烯酸(paa)层、识别分子层(抗体、适配体、 多肽)。
55.如图1所示,本发明实施例提供的可磁控响应的液相漂浮微球制备方法包 括以下步骤:
56.s101,通过将洁净的hgms与聚乙烯亚胺孵育,得到带正电的hgms;
57.s102,将表面带有负电的磁性纳米颗粒与修饰后的hgms进行孵育,通过 静电作用将mnps组装至hgms表面;
58.s103,将组装好的hgms@mnps先与pei孵育后再与聚丙烯酸孵育,得到 表面具有大量羧基的hgms@mnps复合材料;并通过缩合反应修饰识别分子。
59.本发明实施例提供的通过将洁净的hgms与聚乙烯亚胺孵育,得到带正电 的hgms包括:
60.首先,称取一定量的hgms,利用ph为8的nacl缓冲液润洗三遍,再利用 hgms漂浮的特性收集洁净的hgms;
61.其次,称取一定量聚乙烯亚胺溶解于缓冲液中,配制成浓度为1mg/ml的聚 乙烯亚胺溶液;
62.最后,将配置好的聚乙烯亚胺溶液与hgms混合摇晃孵育30min;再使用 buffer反复洗涤去除多余的反应物,再用移液枪吸出溶液后备用。
63.本发明实施例提供的将表面带有负电的磁性纳米颗粒与修饰后的hgms进 行孵育,通过静电作用将mnps组装至hgms表面包括:
64.将带负电的磁性纳米颗粒分散于缓冲液中;将mnps溶液与hgms混合,室 温下摇晃孵育30min,再使用buffer反复洗涤去除多余的反应物,得到 hgms@mnps。
65.本发明实施例提供的将组装好的hgms@mnps先与pei孵育后再与聚丙烯 酸孵育,得到表面具有大量羧基的hgms@mnps复合材料,并通过缩合反应修 饰识别分子包括:
66.(1)称取一定量聚丙烯酸paa,溶解于ph为8的nacl缓冲液,配制成浓 度为2.4mg/ml的paa溶液;
67.(2)将制备好的hgms@mnps先于pei溶液室温下摇晃孵育30min,利用 材料的磁响应性反复洗涤去除多余的pei,再与paa溶液室温下摇晃孵育30min, 反复洗涤即可。
68.下面结合具体实施例对本发明的技术方案作进一步说明。
69.实施例1:
70.本发明采用层层自组装的方法,将超顺磁性磁性纳米颗粒(mnps大约 20nm)组装到中空玻璃微球(hgms大约30μm),形成hgms@mnps复合材 料。具体包括如下步骤。
71.1、hgms表面包覆聚合物层:将洁净的hgms与聚乙烯亚胺poly(ethylenimine) (pei)孵育,使hgms带正电。
72.2、hgms与mnps组装:将表面带有负电的磁性纳米颗粒与修饰后的hgms 进行孵育,通过静电作用使mnps组装到hgms表面。
73.3、材料的进一步修饰:将组装好的hgms@mnps先与pei孵育后再与聚丙 烯酸poly(acrylic acid)(paa)孵育,使材料表面具有大量羧基,可通过缩合反应 修饰识别分子。
74.4、具体实验步骤方式及表征图:
75.(1)hgms表面包覆聚合物层:
76.1)称取一定量的hgms,使用nacl缓冲液(ph=8)润洗三遍除去灰尘杂 质,利用hgms漂浮的特性收集后备用。
77.2)称取一定量聚乙烯亚胺(pei,分子量24000)溶解于缓冲液中,配制成 浓度为1mg/ml的pei溶液。
78.3)将配置好的pei溶液与hgms混合摇晃孵育30min。然后使用buffer反 复洗涤除去多余的反应物,再用移液枪吸出溶液后备用。
79.(2)hgms与mnps组装:
80.1)带负电的磁性纳米颗粒(粒径大约20nm)分散于缓冲液中。
81.2)将mnps溶液与hgms混合,室温下摇晃孵育30min,然后使用buffer 反复洗涤除去多余的反应物,得到hgms@mnps。
82.(3)材料的进一步修饰:
83.1)称取一定量聚丙烯酸paa(分子量24万),溶解于nacl缓冲液(ph=8), 配制成浓度为2.4mg/ml的paa溶液,
84.2)将制备好的hgms@mnps先于pei溶液室温下摇晃孵育30min,利用材 料的磁响应性反复洗涤除去多余的pei,然后再与paa溶液室温下摇晃孵育 30min,最后反复洗涤,后备用。
85.二、应用实施例。为了证明本发明的技术方案的创造性和技术价值,该部 分是对权利要求技术方案进行具体产品上或相关技术上的应用的应用实施例。
86.应用实施例1:
87.将本发明应用实施例提供的可磁控响应的液相漂浮微球与待作用物质的离 心管,周期性的经过固定磁场上方,在这个过程中,hgms@mnps的浮力与重 力交替着占主导作用,因此hgms@mnps上下浮动,实现了与待作用物质的充 分作用。如图10所示,当hgms@mnp靠近磁铁上方时,重力占主导,微球下 降,远离磁铁上方时,磁铁上升,如此往复,实现上下浮动。
88.应用实施例2:
89.将本发明应用实施例提供的可磁控响应的液相漂浮微球用于ctcs循环肿瘤 细胞的富集与分离。
90.循环肿瘤细胞(ctcs)是从原发肿瘤组织脱落,并进入人体血液循环系统的 肿瘤细胞,是肿瘤灶转移的主要原因。ctcs所携带的生物信息对于癌症患者的 预后、治疗有着重要的指示意义,因此从外周血中富集分离ctcs具有十分重要的 意义。在此,将本发明应用于循环肿瘤细胞(ctcs)的捕获,经实验验证,表面 修饰了抗体/适配子的hgms@mnps可以成功富集分离ctcs,通过磁力与浮力共 同调控其行为,使微球与目标细胞充分接触再通过抗体结合细胞,实现ctcs的 高效富集
91.图11为hgms@mnps,捕获循环肿瘤细胞后的共聚焦图片,蓝色的是细胞 核。
92.三、实施例相关效果的证据。本发明实施例在研发或者使用过程中取得了 一些积极效果,和现有技术相比的确具备很大的优势,下面内容结合试验过程 的数据、图表等进行描述。
93.材料的表征:
94.首先对本发明的材料在不同磁场条件下的行为进行了探究,然后进行了光 学显微镜表征,sem表征观察其表面的形貌,以eds分析并验证了其表面元素 组成,最终通过共聚焦验证其表面基团并且证实在本发明的材料表面修饰识别 基团的可能性。
95.结果如下:
96.(1)物理特性
97.微球的密度通过排水法测量,具体步骤如下:
98.1)取一定量微球干燥后称取质量为m1放入干燥洁净的样品瓶里。
99.2)由于微球性质,直接加入液体微球会漂浮于液相表面,因此先将装有微 球样品瓶置于磁体上方,使微球吸附在容器底部,再加入v1体积的h2o,此时 因为微球占据了一部分体积,样品瓶里液面高度会高于正常v1体积h2o的液面 高度。
100.3)使用微量量筒量取高于正常液面高度的部分,测量其体积为v2,微球的 密度最总通过公式:v2/m1计算得出。微球的密度约为0.443g/cm3。
101.当微球远离磁场时,浮力占主导作用,微球漂浮于液相表面,当微球处于 磁体上方时,磁力占主导作用,微球下降到容器底部,当微球远离磁场时,浮 力再次发挥主要作用,微球快速上升。因此,当材料周期性的靠近远离磁场时, 就会上下往复运动,实现搅动液体的功能。
102.4)微球的行为研究
103.图12是微球有无磁场时的行为变化,可以看出,当微球置于磁场上方时会 沉降,而远离磁场时上浮。
104.(2)光学显微镜图像
105.图2代表了组装前的hgms,图3是代表组装后的hgms@mnps,图4是 hgms@mnps的粒径分布统计。从图2至图4可以看出组装前后hgms没有明 显形态变化,没有出现团聚现象,粒径分布在26μm到30μm之间,说明该材 料具有良好的分散性与均匀的粒径分布。
106.1)sem表面形貌观察
107.图5为单颗hgms的sem图像;图6为不同区域放大后的sem图像。从图 5-图6可以看出磁性纳米颗粒均匀的分布在hgms表面。
108.2)eds元素分析
109.图7是hgms@mnps材料表面的eds元素分析,可以看到fe元素的信号均 匀的分布在
材料表面,同样说明mnps成功组装到hgms表面。
110.3)共聚焦分析
111.组装paa后的材料(hgms@mnps@paa)表面带有大量的羧基,通过与氨 基的缩合反应,来引入能特异性结合ctcs的识别分子。以适配子来验证,该适 配子一端带有氨基,另一端带有cy3荧光分子(nh2-apt-cy3)具体实验步骤如 下:
112.取一定量hgms@mnps@paa分散于buffer中,加入edcl/nhs缩合剂使最 终浓度为10nm,然后4℃摇晃孵育1h,活化羧基。活化过后,加入适配子最终 浓度0.5mm,然后在室温下(25℃左右)摇晃孵育24h。
113.图8是未经修饰的hgms@mnps@paa,在共聚焦下未出现对应的荧光信号, 图9是修饰后的材料可以看到材料表面出现了明显的荧光信号,由此可以得出, 适配子被成功修饰到了材料表面。
114.以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于 此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,凡在本发明 的精神和原则之内所作的任何修改、等同替换和改进等,都应涵盖在本发明的 保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1