用于植物生长的包含脂肽的生物刺激剂组合物的制作方法
用于植物生长的包含脂肽的生物刺激剂组合物
1.本技术是申请日为2017年12月29日、申请号为“201780085143.9”、发明名称为“用于植物生长的包含脂肽的生物刺激剂组合物”的中国专利申请的分案申请,原申请是国际申请pct/fr2017/053865的中国国家阶段申请。
技术领域
2.本发明涉及用于农业以促进植物生长的生物刺激剂的领域。特别地,本发明涉及脂肽作为生物刺激剂用于植物生长的用途,以及包含脂肽的生物刺激剂组合物,用于获得这种组合物的方法和通过施用该组合物用于促进植物物质增长的方法。包被有生物刺激剂组合物的种子也是本发明的一部分。
背景技术:
3.由于世界人口的持续增长而引起的食物需求的提高是未来的真正挑战。生物刺激剂可有效地有助于这一挑战,并越来越多地用于全球农业生产中。
4.通常在最初的数周内,植物根达到养分的速度是植物初始发育和生长成功的关键参数。生物刺激剂使得能够通过提供基于天然产物的养分或通过帮助植物获取其养分来改善植物生长。
5.生物刺激剂在从种子萌发至植物成熟的整个作物生命周期中促进植物的生长和发育,它们改善了植物代谢的效率,导致收获提高和质量更好。它们提高了植物对非生物胁迫的耐受性以及植物从其中恢复的能力。它们促进了养分的同化、传递和使用。它们改善了农业生产的质量,包括含糖量、颜色和果实大小。另外,它们调节和改善了植物的含水量。最后,它们提高了土壤的某些物理化学性质并促进了田间微生物的发育。
6.使用微生物或微生物混合物用于植物的生物刺激是公知的。这些方法基于施用包含经纯化的微生物或微生物混合物的组合物,特别是包含芽孢杆菌(bacillus)菌株的此类组合物。
7.文献中描述的植物生长生物刺激剂组合物包含单独或与其他组分组合的经纯化的芽孢杆菌菌株。例如,申请wo2016/109332描述了包含芽孢杆菌属(bacillus sp.)菌株d747的生物学纯的培养物的组合物(作为ferm bp-8234提交)。申请wo2016/108976描述了包含短小芽孢杆菌(bacillus pumilus)rti菌株279的生物学纯的培养物的组合物(按照atcc以编号pta-121164提交),其可单独施用或与化学品或其他微生物剂或这二者组合施用以促进植物生长并针对植物性疾病提供保护和/或防治。
8.然而,此类组合物存在缺点。为了使组合物具有活性,期望微生物是活的并能够在植物上繁殖;然而,这些条件难以控制。另外,在促进生态解决方案的农业环境中,使用经遗传修饰的微生物菌株是有问题的。
9.本发明提供了对于该问题的解决方案。
10.实际上,本发明人出乎意料地发现了包含脂肽的组合物可用于刺激植物的生长。基于脂肽或基于包含脂肽且不包含产生该上清液的芽孢杆菌菌株的芽孢杆菌培养物上清
液的制剂具有自身活性而不需要原位产生生物刺激剂分子且不含gmo的双重优点。现有技术文献都没有描述这种包含脂肽的制剂用于刺激植物生长的用途。
11.因此,本发明提出了对于植物生长的生物刺激的创新方法。
技术实现要素:
12.本发明的第一个目的涉及至少一种脂肽作为生物刺激剂用于植物生长的用途。
13.实际上,本发明人首次通过示出经纯化脂肽的制剂的刺激作用表明了脂肽对植物生长的生物刺激作用。因此,他们提出使用脂肽作为生物刺激剂。生物刺激剂可以是从至少一种芽孢杆菌属菌株的上清液中获得的组合物、脂肽浓缩的组合物或包含经纯化脂肽的组合物。
14.因此,本发明的第二个目的涉及生物刺激植物生长的组合物,其特征在于:该组合物包含至少一种脂肽。脂肽可被纯化、浓缩或包含在排除产生细胞的芽孢杆菌属培养物的上清液中。在一个优选的实施方案中,生物刺激剂组合物对应于脂肽浓缩的组合物或包含经纯化脂肽的组合物。
15.如在此所用的,术语“上清液”是指至少一种芽孢杆菌属菌株的上清液或上清液提取物。
16.如在此所用的,术语“脂肽浓缩的组合物”是指通过浓缩至少一种芽孢杆菌属菌株的培养物上清液而获得的溶液或组合物。
17.如在此所用的,术语“包含经纯化脂肽的组合物”是指通过从包含脂肽的溶液(例如至少一种芽孢杆菌属菌株的培养物上清液或经浓缩脂肽组合物)中纯化脂肽而获得的溶液或组合物。
18.在这些不同的组合物中,脂肽的性质和量和纯度可变化。
19.如在此所定义的,“生物刺激剂组合物”是可改善植物生长的组合物(或溶液或制剂)。可适用的生长评价标准是多样的;一些标准在实验部分中描述。这涉及例如评估可归因于施用生物刺激剂组合物的对于萌发时间、根尺寸、生物质或植物高度的增长。为了验证这种制剂是否具有生物刺激性质,所述上清液可通过浇灌施用于植物的上部部分;和/或通过浇灌和/或浸泡在根水平施用;或通过包被/浸渍种子而施用。
20.芽孢杆菌属菌株因其产生脂肽的能力而被知晓。可用于本发明的芽孢杆菌菌株是天然的或经遗传修饰的菌株。
21.在一个具体实施方案中,芽孢杆菌属菌株选自枯草芽孢杆菌(bacillus subtilis)、解淀粉芽孢杆菌(bacillus amyloliquefaciens)、地衣芽孢杆菌(bacillus licheniformis)、多黏类芽孢杆菌(paenibacillus polymixa)、短小芽孢杆菌(bacillus pumilus)、苏云金芽孢杆菌(bacillus thuringiensis)、球形芽孢杆菌(bacillus sphaericus)、凝结芽孢杆菌(bacillus coagulans)、蕈状芽孢杆菌(bacillus mycoides)、贝莱斯芽孢杆菌(bacillus velenzensis)和坚强芽孢杆菌(bacillus firmus)、甲基营养型芽孢杆菌(bacillus methylotrophicus)、巨大芽孢杆菌(bacillus megaterium)、死谷芽孢杆菌(bacillus vallismortis)。
22.有利地,芽孢杆菌菌株选自枯草芽孢杆菌和解淀粉芽孢杆菌(近期被认为是贝莱斯芽孢杆菌)。在一个优选的实施方案中,枯草芽孢杆菌(b.subtilis)菌株选自atcc 6633、
atcc 21332、168、atcc 9943和ncib 3610,及其衍生物;解淀粉芽孢杆菌(b.amyloliquefaciens)菌株选自fzb42和lmg s-29032(也称为ga1),及其衍生物。
23.在另一个具体实施方案中,通过浓缩上清液获得生物刺激剂组合物。因此,经浓缩的组合物可对应于相对于所收获的上清液的至少2倍、或甚至5或10倍,优选至少20倍、且甚至更优选至少50倍的浓缩。还可通过纯化上清液中包含的脂肽来获得生物刺激剂组合物。因此,可既定性地(存在脂肽的性质)又定量地提出具有确定组成的生物刺激剂溶液。
24.根据本发明的生物刺激剂组合物还可通过其脂肽含量来限定。因此,在一个优选的实施方案中,根据本发明的脂肽制剂可包含浓度为至少10mg/l(0.001%)、20mg/l、50mg/l、100mg/l(0.01%)、200mg/l、500mg/l、1g/l(0.1%)、2g/l、5g/l(0.5%)、10g/l(1%)、20g/l、50g/l,优选1%至7%,特别是1%、2%、3%、4%、5%、6%或7%,且甚至更优选至少10%、或至少20%的脂肽,已知1%溶液对应于10g/l的浓度。
25.脂肽浓缩的组合物或包含经纯化脂肽的组合物可包含0.002%至15%的脂肽,其纯度可变化。特别地,此类组合物的脂肽纯度可大于或等于10%,优选大于或等于15%、20%、30%、40%或50%。在一个特别优选的实施方案中,这些组合物的脂肽纯度大于或等于60%,优选大于或等于70%、75%、80%、85%、90%、95%、99%或甚至100%。
26.在本发明的上下文中,在对于植物生长具有生物刺激性质的脂肽中,伊枯草菌素(iturine)、表面活性素(surfactine)、芬芥素(fengycine)、库斯塔克素(kurstakine)和罗克霉素(locillomycine)家族的脂肽特别令人感兴趣。
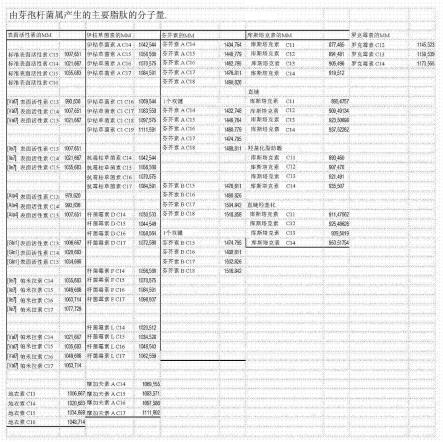
27.在一个优选的实施方案中,生物刺激剂组合物由其属于伊枯草菌素家族的分子和/或属于表面活性素家族的分子和/或属于芬芥素家族的分子和/或属于库斯塔克素家族的分子和/或属于罗克霉素家族的分子的含量来限定(参见图1中的表格)。
[0028]“伊枯草菌素家族的分子”意指伊枯草菌素a、摩加夫素(mojavensine)、抗霉枯草菌素(mycosubtiline)和杆菌霉素(bacillomycine)a、b、c、d、f和l。
[0029]“表面活性素家族的分子”意指表面活性素a、b、c、地衣素(lichenysine)和帕米拉素(pumilacidine)。
[0030]“芬芥素家族的分子”是指芬芥素a和b、制磷脂菌素(plipastatine)a和b和阿瓜斯他汀(agrastatine)。
[0031]
因此,例如,根据本发明的生物刺激剂组合物可包含0.002%至25%的脂肽,特别是1%至15%的脂肽。
[0032]
在第一个实施方案中,该组合物包含以下比例的0.002%至25%脂肽:属于伊枯草菌素家族的分子10%至90%、属于表面活性素家族的分子10%至90%、属于芬芥素家族的分子0至50%。
[0033]
在第二个实施方案中,该组合物包含以下比例的0.002%至25%脂肽:属于伊枯草菌素家族的分子0至100%、属于表面活性素家族的分子0至100%,属于芬芥素家族的分子0至100%。
[0034]
根据本发明的另一种生物刺激剂组合物可包含以下比例的0.002%至25%脂肽,优选1%至15%的脂肽:
[0035]-100%表面活性素
[0036]-100%芬芥素
[0037]-100%伊枯草菌素,尤其是抗霉枯草菌素
[0038]-伊枯草菌素和表面活性素的混合物
[0039]-抗霉枯草菌素和表面活性素的混合物
[0040]-伊枯草菌素和芬芥素的混合物
[0041]-抗霉枯草菌素和芬芥素的混合物
[0042]-表面活性素和芬芥素的混合物
[0043]-伊枯草菌素(其包含抗霉枯草菌素)、表面活性素和芬芥素的混合物。
[0044]
根据本发明的组合物还可包含由所述菌株产生的初生代谢物,例如乙偶姻、2-3丁二醇、生长素前体和/或磷酸盐增溶酶。
[0045]
在实验部分中描述了根据本发明的组合物的一些实施例。
[0046]
实施例2中描述了经浓缩的脂肽组合物。通过浓缩培养物上清液获得且包含175mg/l的伊枯草菌素,特别是伊枯草菌素,特别是抗霉枯草菌素,以及75mg/l的表面活性素a;或者700mg/l的伊枯草菌素,特别是抗霉枯草菌素,以及300mg/l的表面活性素a的组合物,显著提高了番茄植株的尺寸和这些植株地上部分中的新鲜生物质的量。这两种组合物还显著提高了小麦植株的地上部分和根部分的新鲜生物质的量。包含350mg/l的伊枯草菌素,特别是抗霉枯草菌素,以及150mg/l的表面活性素a的另一种组合物显著提高了小麦植株的地上部分和根的部分的新鲜生物质的量以及这些植株的地上部分的叶绿素含量。
[0047]
实施例3和4中描述了根据本发明的经纯化脂肽的组合物。包含经纯化的伊枯草菌素(其包含经纯化的抗霉枯草菌素)(99%)、或经纯化的芬芥素(99%)或伊枯草菌素(其包含抗霉枯草菌素)和表面活性素(79%)的混合物的组合物对根生长具有显著作用,特别是在处理番茄种子之后(参见实施例3)。
[0048]
相对比例为80%的伊枯草菌素,特别是抗霉枯草菌素和20%的表面活性素的包含30%至99%的经纯化脂肽的组合物改善了对水分胁迫的抗性,特别是对于番茄植株。组合物的这些生物刺激作用导致番茄植株在水分胁迫开始与结束之间的高度方面的增长,更好的光合效率和更好的气孔导度(参见实施例4)。
[0049]
为了促进制剂渗透到植物中,根据本发明的组合物还可包含辅料。有益地,辅料促进生物刺激剂组合物渗透至植物中。辅料的选择受所期望的作用的指导。例如,湿润剂通过扩散生物刺激剂物质来增大叶与微滴之间的接触面并确保产品保留在角质层上。油剂通过“破坏”植物上角质层蜡层的屏障来促进生物刺激剂物质的渗透;当已知油剂将以相同的方式作用于栽培植物的角质层达到减弱其对致病性真菌的天然防御时,这变成了缺点。其他辅料(例如渗透剂)是湿润剂,其浸渍蜡质角质层同时保持它们的完整性。盐也可用作辅料,特别是用于从空气中吸收水分,并因此防止干燥。最后,胶黏剂将生物刺激剂物质固定在叶上并限制淋洗作用和挥发。因此,辅料应适应于生物刺激剂物质的作用方式(根、接触、内吸或渗透)、产品制剂类型和目标植物类型(无毛或有毛叶、角质层厚度、植物阶段、气孔位置等)。
[0050]
有利地,辅料选自经填充或未经填充的聚合物表面活性剂、烷基聚葡糖苷和烷基聚葡糖苷酯、茶磺酸盐衍生物、纤维素衍生物、天然多糖、基于硅酮的乳液
……
[0051]
在另一个实施方案中,根据本发明的生物刺激剂组合物还可包含细胞,前提是这些细胞不对应于产生上清液的特定菌株。添加至制剂中的细胞可具有特定性质以增强上清
液制剂的生物刺激作用或另外的性质,包括抗真菌性质。因此,此类细胞可选自不同于用于产生上清液的菌株的芽孢杆菌属菌株,特别是选自枯草芽孢杆菌、解淀粉芽孢杆菌、地衣芽孢杆菌、多黏类芽孢杆菌、短小芽孢杆菌、苏云金芽孢杆菌、球形芽孢杆菌、凝结芽孢杆菌、蕈状芽孢杆菌、坚强芽孢杆菌、贝莱斯芽孢杆菌、甲基营养型芽孢杆菌、巨大芽孢杆菌、死谷芽孢杆菌菌株。此类细胞也可以不是芽孢杆菌类型菌株,而是类芽孢杆菌属(paenibacillus sp.)、假单胞菌属(pseudomonas sp.)(洋葱假单胞菌(pseudomonas cepacia)、荧光假单胞菌(pseudomonas fluorescens)、绿针假单胞菌(pseudomonas chioraphis)、丁香假单胞菌(pseudomonas syringae))、链霉菌属(streptomyces sp.)(灰绿链霉菌(streptomyces griseoviridis)、利迪链霉菌(streptomyces lydicus))。此类细胞也可以是酵母菌、菌根真菌或木霉属(trichoderma sp.)或腐霉属(pythium sp.)
……
[0052]
本发明的第三个目的涉及用于获得用于植物生长的生物刺激剂制剂的方法,其包括以下步骤:(i)培养至少一种芽孢杆菌属菌株,(ii)在适合于使分子分泌到上清液中的培养基中孵育,以及(iii)收获上清液。在该方法中,上清液或上清液的提取物可直接用作生物刺激剂。
[0053]
根据待培养的菌株选择孵育时间和培养基;技术人员将能够调整这些参数。
[0054]
在一个具体实施方案中,该方法中使用的芽孢杆菌菌株优选地选自芽孢杆菌属枯草芽孢杆菌、解淀粉芽孢杆菌、地衣芽孢杆菌、多黏类芽孢杆菌、短小芽孢杆菌、苏云金芽孢杆菌、凝结芽孢杆菌、蕈状芽孢杆菌、球形芽孢杆菌、贝莱斯芽孢杆菌、坚强芽孢杆菌、甲基营养型芽孢杆菌、巨大芽孢杆菌、死谷芽孢杆菌。有利地,芽孢杆菌菌株选自枯草芽孢杆菌和解淀粉芽孢杆菌菌株。在一个优选的实施方案中,枯草芽孢杆菌菌株选自atcc 6633、atcc 21332、168、atcc 9943和ncib 3610,及其衍生物;解淀粉芽孢杆菌菌株选自fzb42和lmg s-29032,及其衍生物。
[0055]
另外,该方法可包括浓缩上清液的步骤。可通过使用本领域技术人员公知的技术之一来获得制剂的浓缩。例如,可通过膜超滤、蒸发、物理化学沉淀或萃取来浓缩制剂。
[0056]
或者,该方法可包括纯化脂肽的步骤。纯化步骤产生经纯化脂肽,以产生含有不超过一种类型脂肽的溶液或产生含有不同脂肽之组合的溶液。可通过使用本领域技术人员公知的技术之一来实现脂肽的纯化。例如,可提及单独或组合使用有机溶剂(例如甲醇、乙醇、丁醇、乙酸乙酯和氯仿)的连续次序的超滤、渗滤和最终纯化步骤。或者,可通过酸沉淀或通过使用一价或二价阳离子盐(例如铵盐、镁盐、钙盐、钠盐等)来进行脂肽的纯化。
[0057]
由此获得的生物刺激剂组合物可以以粉末形式脱水,以有利于其保存、储存和运输。因此,通过使上清液粉末溶解以获得所期望浓度的目的分子(特别是脂肽),可获得如上定义的生物刺激剂组合物。
[0058]
本发明的第四个目的涉及用于促进植物生长的生物刺激方法,其由以下组成:向植物的一个或所有部分施用如上定义的生物刺激剂组合物。在一个优选的实施方案中,生物刺激剂组合物是包含经纯化脂肽的组合物。
[0059]
在一个具体实施方案中,可通过叶面处理施用生物刺激剂制剂,以便在叶面和/或根和/或果实和/或蔬菜和/或谷类物质中获得显著的增长。该处理可例如通过喷施生物刺激剂组合物来施用。
[0060]
在另一个具体实施方案中,可通过根处理施用生物刺激剂组合物,以便在叶面和/
或根和/或果实和/或蔬菜和/或谷类物质中获得显著的增长。该处理可例如通过用生物刺激剂制剂浇灌来施用。
[0061]
在另一个实施方案中,可通过种子处理施用生物刺激剂组合物,以便在叶面和/或根和/或果实和/或蔬菜和/或谷类物质中获得显著的增长。该处理可例如通过用生物刺激剂制剂包被来施用。
[0062]
本发明的另一目的涉及用本发明中定义的生物刺激剂组合物处理以获得叶物质的显著增长的观赏性鳞茎。
[0063]
本发明的另一目的涉及包被有本发明中定义的生物刺激剂组合物的种子。
[0064]
蔬菜种子的包被旨在特别地用于改善植物的初始生长。
附图说明
[0065]
图1:由芽孢杆菌属产生的主要脂肽的分子量的描述性表格。
[0066]
图2:在施用来源于芽孢杆菌属的经浓缩组合物之后番茄植株高度的测量。在施用包含以下的组合物之后测量植株高度:(模式1)来源于解淀粉芽孢杆菌上清液的组合物,其含有用于用90mg/l伊枯草菌素a、100mg/l芬芥素a和b以及60mg/l表面活性素a进行处理的终浓度;(模式2)枯草芽孢杆菌上清液组合物,其含有用于用175mg/l抗霉枯草菌素和75mg/l表面活性素a进行处理的终浓度;(模式3)枯草芽孢杆菌上清液组合物,其含有用于用700mg/l抗霉枯草菌素和300mg/l表面活性素a进行处理的终浓度。该分析揭示了所述处理对植株高度的显著作用(p=0.0029)。统计组在图上由字母a和b指示。
[0067]
图3:在施用来源于芽孢杆菌属培养物上清液的经浓缩的组合物之后番茄植株地上部分的新鲜生物质重量的测量。在施用包含以下的组合物之后测量番茄植株地上部分的新鲜生物质的重量:(模式1)来源于解淀粉芽孢杆菌上清液的组合物,其含有用于处理的90mg/l伊枯草菌素a、100mg/l芬芥素a和b和60mg/l表面活性素a的终浓度;(模式2)枯草芽孢杆菌上清液组合物,其含有用于用175mg/l抗霉枯草菌素和75mg/l表面活性素a进行处理的终浓度;(模式3)枯草芽孢杆菌上清液组合物,其含有用于用700mg/l抗霉枯草菌素和300mg/l表面活性素a进行处理的终浓度。该分析揭示了所述处理对植株高度的显著作用(p=0.0029)。统计组在图上由字母a、b和c指示。
[0068]
图4:在施用来源于芽孢杆菌属培养物上清液的经浓缩的组合物之后小麦植株的湿物质和根的增多的测量。
[0069]
在仅通过根(r)施用或通过根和叶面(r+f)施用包含以下的组合物之后测量小麦植株的地上部分和根部分的新鲜生物质的重量:(模式1)来源于解淀粉芽孢杆菌上清液的组合物,其含有用于用90mg/l伊枯草菌素a、100mg/l芬芥素a和b以及60mg/l表面活性素a进行处理的终浓度;(模式2)枯草芽孢杆菌上清液组合物,其含有用于用175mg/l抗霉枯草菌素和75mg/l表面活性素a进行处理的终浓度;(模式4)枯草芽孢杆菌上清液组合物,其含有用于用350mg/l抗霉枯草菌素和150mg/l表面活性素a进行处理的终浓度。统计组在图上由字母a和b指示对小麦植株地上部分的生物刺激作用,并且由字母a和b指示对小麦植株根部的生物刺激作用。
[0070]
图5:在施用来源于芽孢杆菌属的经浓缩组合物之后小麦植株叶绿素含量提高的测量。在仅通过根(r)施用或根和叶面(r+f)施用包含以下的组合物之后测量小麦植株地上
部分的叶绿素含量:(模式1)来自解淀粉芽孢杆菌上清液的组合物,其含有用于用90mg/l伊枯草菌素a、100mg/l芬芥素a和b以及60mg/l表面活性素a进行处理的终浓度;(模式4)来自枯草芽孢杆菌上清液的组合物,其含有用于用350mg/l抗霉枯草菌素和150mg/l表面活性素a进行处理的终浓度。统计组在图上由字母a、b和c指示。
[0071]
图6:用包含经纯化脂肽的组合物浸泡/包被处理之后番茄种子的根长度的测量。
[0072]
在施用包含以下的组合物之后测量番茄种子的根长度:(模式1)经浓缩和纯化的枯草芽孢杆菌培养物的上清液,其包含99%抗霉枯草菌素;(模式2)经浓缩和纯化的枯草芽孢杆菌培养物的上清液,其包含99%表面活性素;(模式3)经浓缩和纯化的枯草芽孢杆菌培养物的上清液,其包含99%芬芥素;(模式4)经浓缩和纯化的枯草芽孢杆菌培养物上清液的上清液,其包含79%的抗霉枯草菌素与表面活性素的混合物;将每种模式与对应于用相同体积的0.1%dmso溶液处理的对照的对照条件进行比较。统计组在图上由字母a、b指示。
[0073]
图7:在水分胁迫时期开始与结束之间用包含经纯化脂肽的组合物处理的番茄植株的生长增长的测量。
[0074]
在水分胁迫时期结束时测量番茄植株的尺寸,并与该时期开始时的尺寸进行比较,以便评估在施用包含以下的组合物之后的增长:(模式1)经浓缩和纯化至纯度为30%(脂肽质量/总干质量)的枯草芽孢杆菌培养物的上清液,且其相对比例为80%抗霉枯草菌素和20%表面活性素。以75g/ha的脂肽的比例施用该组合物;(模式2)经浓缩和纯化至纯度为30%(脂肽质量/总干质量)的枯草芽孢杆菌培养物的上清液,且其相对比例为80%抗霉枯草菌素和20%表面活性素。以150g/ha的脂肽的比例施用该组合物;(模式3)经浓缩和纯化至纯度为99%(脂肽质量/总干质量)的枯草芽孢杆菌培养物的上清液,并且其相对比例为80%抗霉枯草菌素和20%表面活性素。以150g/ha的脂肽的比例施用该组合物;将每种模式与对应于用相同体积的蒸馏水溶液处理的对照的对照条件进行比较。统计组在图上由字母a、b和c指示。
[0075]
图8:在水分胁迫时期开始与结束之间用包含经纯化脂肽的组合物处理的番茄植株的光合效率的测量。
[0076]
通过pam荧光测定法在水分胁迫的开始和结束时以及在施用包含以下的组合物之后测量光合效率:(模式1)经浓缩和纯化至纯度为30%(脂肽质量/总干质量)的枯草芽孢杆菌培养物的上清液,且其相对比例为80%抗霉枯草菌素和20%表面活性素。以75g/ha的脂肽的比例施用该组合物;(模式2)经浓缩和纯化至纯度为30%(脂肽质量/总干质量)的枯草芽孢杆菌培养物的上清液,并且其相对比例为80%抗霉枯草菌素和20%表面活性素。以150g/ha的脂肽的比例施用该组合物;(模式3)经浓缩和纯化至纯度为99%(脂肽质量/总干质量)的枯草芽孢杆菌培养物的上清液,并且其相对比例为80%抗霉枯草菌素和20%表面活性素。以150g/ha的脂肽的比例施用该组合物;将每种模式与对应于用相同体积的蒸馏水溶液处理的对照的对照条件进行比较。图a对应于水分胁迫开始时的测量,并且图b对应于水分胁迫结束时的测量。统计组在图上由字母a、b和c指示。
[0077]
图9:在水分胁迫时期的开始与结束之间用包含经纯化脂肽的组合物处理的番茄植株的气孔导度的测量。
[0078]
用气孔计分析气孔导度,以测量在水分胁迫开始与结束时和在施用包含以下的组合物之后通过叶气孔的二氧化碳(co)或水蒸汽的流量:(模式1)经浓缩和纯化至纯度为
30%(脂肽质量/总干质量)的枯草芽孢杆菌培养物的上清液,且其相对比例为80%抗霉枯草菌素和20%表面活性素。以75g/ha的脂肽的比例施用该组合物;(模式2)经浓缩和纯化至纯度为30%(脂肽质量/总干质量)的枯草芽孢杆菌培养物的上清液,并且其相对比例为80%抗霉枯草菌素和20%表面活性素。以150g/ha的脂肽的比例施用该组合物;(模式3)经浓缩和纯化至纯度为99%(脂肽质量/总干质量)的枯草芽孢杆菌培养物的上清液,并且其相对比例为80%抗霉枯草菌素和20%表面活性素。以150g/ha的脂肽的比例施用该组合物;将每种模式与对应于用相同体积的蒸馏水溶液处理的对照的对照条件进行比较。图a对应于水分胁迫开始时的测量,并且图b对应于水分胁迫结束时的测量。统计组在图上由字母a和b指示。
具体实施方式
[0079]
实施例1:生物刺激剂组合物的制备
[0080]
1.a培养物上清液的制备
[0081]
培养物上清液获得自来源于枯草芽孢杆菌atcc 6633菌株或解淀粉芽孢杆菌lmg s-29032菌株的芽孢杆菌菌株的需氧发酵过程。培养在包含碳源(葡萄糖、蔗糖、
……
)、氮源(硫酸铵、蛋白胨
……
)和微量元素的经搅拌培养基中在30℃下进行。将ph维持在值为7。在48至72小时之后收获培养物。然后将其离心或过滤以除去细胞。准备好培养物上清液以待浓缩。在该阶段时的脂肽百分比为0.05%至0.5%(重量/体积)。
[0082]
1.b经浓缩的生物刺激剂制剂的制备
[0083]-通过切向过滤
[0084]
通过使用膜的切向超滤将通过例如1.a中所示的制剂获得的培养物上清液进行浓缩,其截止阈值可以是1kda至100kda。例如,通过透过所述膜将如上所述获得的1000l培养物上清液进行浓缩,以获得体积为10至100l的渗余物。
[0085]-通过在酸性ph下沉淀
[0086]
制备经浓缩的生物刺激剂制剂的第二个实例是降低ph以便使脂肽沉淀。向所获得的上清液添加浓硫酸,例如,通过1.a中所示的制剂。在获得约1的最终ph之后,将溶液保持搅拌2至12小时。离心使得回收包含脂肽物质的沉淀(culot)。然后通过添加水和纯碱以获得7至8.5的ph值来将该沉淀溶解。例如,当从1000l培养物上清液中获得沉淀时,可以以10至100l的总体积使用该沉淀。
[0087]
在这两个制备实例之一结束时脂肽的百分比为1%至15%(重量/体积)。
[0088]
实施例2:从芽孢杆菌培养物上清液中获得的组合物对植物生长的生物刺激作用
[0089]
2.a上清液中存在的化合物的分析
[0090]
可使用分析方法验证组合物用作生物刺激剂组合物的能力。组合物中来自芽孢杆菌培养物的脂肽、初生代谢物或酶的存在的确可通过本领域技术人员已知的不同方法(特别是通过液相色谱法与质谱法联用(或lc-ms)、高效液相色谱法(hplc)或比色法)来测量。
[0091]
2.b用于评价对植物的生物刺激作用的方法
[0092]
可通过分析生长参数直接评估组合物对植物的生物刺激作用。为此,可以通过浇灌将培养物上清液或从其来源的组合物施用于植物的上部部分、根术平处,或通过浸泡种子来施用。这些施用方法也可进行组合。在生长期之后评价生物刺激作用。
[0093]
如果满足以下至少一个标准,则获得生物刺激作用:
[0094]-提高了植物尺寸(高度或粗度)
[0095]-提高了植物果实的新鲜和/或干生物质
[0096]-提高了植物地上部分的新鲜和/或干生物质
[0097]-提高了植物根的新鲜和/或干生物质
[0098]-提高了针对谷类作物的节数量、穗状花序的数量
[0099]-提高了植物根系的长度
[0100]-提高了谷类、蔬菜和/或果实的产率
[0101]-提高了叶绿素含量
[0102]-对非生物胁迫的抗性的提高:例如,在水分胁迫期间:光合效率、气孔导度等的提高。
[0103]
2.c包含脂肽的组合物对番茄植株高度之提高的作用。
[0104]
设备和方法
[0105]
测试在栽培温室中进行,以确保温度和日照的半受控条件:
[0106]-温度:白昼25℃/黑夜20℃
[0107]-光周期:14小时的白昼/10小时的黑夜
[0108]
温室的最低亮度调节为175w/m2。低于此亮度,将打开照明并补偿亮度值。超过500w/m2的亮度时遮阳物伸出,并回调至450w/m2。
[0109]
在先前在沙质农业土壤中移植的5株2叶期的番茄植株上对每种模式进行评价。在移植之前两天进行初始施肥,其中以每株番茄植株0.2g的比例提供red hakaphos 8-12-24溶液。
[0110]
考虑到200l/ha的喷雾体积,在该生物刺激剂效率测试中测试的使用方式对应于植物根部处的产物对番茄移植以及3周叶面培养之后的贡献。
[0111]
受试组合物如下:
[0112]-将解淀粉芽孢杆菌培养物的上清液浓缩20倍并稀释40倍,以获得浓度为50g/ha的脂肽,其相对比例为:伊枯草菌素家族(此处为伊枯草菌素a)为36%,且表面活性素家族(此处为表面活性素a)为24%,且芬芥素家族(此处为芬芥素a和b)为40%(模式1);
[0113]-将枯草芽孢杆菌培养物的上清液浓缩20倍并稀释40倍,以获得浓度为50g/ha的脂肽,其相对比例为:伊枯草菌素家族(此处为抗霉枯草菌素)为70%,且表面活性素家族(此处为表面活性素a)为30%(模式2);
[0114]-将枯草芽孢杆菌培养物的上清液浓缩20倍并稀释10倍,以获得浓度为200g/ha的脂肽,其相对比例为:伊枯草菌素家族(此处为抗霉枯草菌素)为70%,且表面活性素家族(此处为表面活性素a)为30%(模式3);
[0115]-用相同体积的蒸馏水处理的对照(对照模式)
[0116]
然后在栽培6周之后测量植株的高度和地上部分的新鲜生物质。通过方差分析(anova,在95%置信水平下(即5%的风险阈值)的lsd方法)处理数据,以便突出显著的作用。使用statgraphics centurion xv版本15.2.06软件进行检验。
[0117]
结果
[0118]
实验方案使得可比较来源于芽孢杆菌菌株培养物上清液的不同组合物对番茄植
株达到的高度的生物刺激作用。结果示于图1中。统计分析显示所述处理对该参数的显著作用(p=0.0029)。统计组在图上由字母a和b指示,与对照相比,所有模式都具有显著的生物刺激作用。
[0119]
图2中所示的结果显示,在6周的时期中,与未处理模式(对照模式)相比,含有用于用175mg/l抗霉枯草菌素和75mg/l表面活性素a的终浓度进行处理(模式2)和用于用700mg/l抗霉枯草菌素和300mg/l表面活性素a的终浓度进行处理(模式3)的来自枯草芽孢杆菌上清液的组合物显著提高了番茄植株的尺寸。含有用于用90mg/l伊枯草菌素a、100mg/l芬芥素a和b以及60mg/l表面活性素a的终浓度进行处理的来自解淀粉芽孢杆菌上清液的模式1的生物刺激作用远高于未处理的对照,但属于包含对照的那些的2个统计组。
[0120]
2.d脂肽组合物对番茄植株地上部分新鲜生物质之提高的作用。
[0121]
设备和方法
[0122]
实验方案与上述2.c段落中描述的方案相同。
[0123]
结果
[0124]
实验方案使得可比较来源于芽孢杆菌菌株的培养物上清液的不同组合物对番茄植株地上部分的新鲜生物质重量的生物刺激作用。结果示于图3中。统计分析显示所述处理对该参数的显著作用(p=0.0029)。
[0125]
统计组在图上由字母a、b和c指示。
[0126]
图2中所示的结果显示与未处理的模式(对照模式)相比,来自含有用于用175mg/l抗霉枯草菌素和75mg/l表面活性素a的终浓度进行处理(模式2)和用于用700mg/l抗霉枯草菌素和300mg/l表面活性素a的终浓度进行处理(模式3)的枯草芽孢杆菌上清液的组合物,使得地上部分的新鲜生物质显著提高。含有用于用90mg/l伊枯草菌素a、100mg/l芬芥素a和b以及60mg/l表面活性素a的终浓度进行处理的来自解淀粉芽孢杆菌上清液的模式1的生物刺激作用远高于未处理对照,但属于包含对照的2个统计组。
[0127]
2.e脂肽组合物对来自小麦植株的湿物质和来自小麦植株根的湿物质的产生之提高的作用
[0128]
设备和方法
[0129]
将tybalt品种的小麦种子播种在惰性基质上。使根在液体培养基中发育。当小麦植株处于1至2叶期时,将植株种植在具有砂质黏土的盆中。将盆存放在栽培室中,其中光照为16小时,且温度为19℃。
[0130]
针对每种作物和处理,种植20株植株。通过根施用处理10株植株(在图4和5中标注为r);未处理10株植株。然后,在通过根施用处理的10株植株的组中,然后通过叶面施用处理5株植株(在图4和5中标注为r+f);未处理5株植株(图4和5中标注为r)。
[0131]
通过浸润在多种产物溶液中处理小麦植株的根,并在处理之后立即栽培在具有沙质果实盆栽土的盆中。在栽培之后4周施加叶面施用,其中喷雾体积为200i/ha。在生长9周之后进行最终测量。
[0132]
用sas 7对所获得的数据进行统计学分析。用kolmogorov-smirnov检验正态性,并通过levene检验来检验方差的相等性。使正态分布的同方差变量进行用tukey作为事后检验的双向单因素anova。
[0133]
受试组合物如下:
[0134]-将解淀粉芽孢杆菌培养物的上清液浓缩20倍并稀释40倍,以获得浓度为50g/ha的脂肽,其相对比例为:伊枯草菌素家族(此处为伊枯草菌素a)为36%,表面活性素家族(此处为表面活性素a)为24%,且芬芥素家族(此处为芬芥素a和b)为40%(模式1);
[0135]-将枯草芽孢杆菌培养物的上清液浓缩20倍并稀释40倍,以获得浓度为50g/ha的脂肽,其相对比例为:伊枯草菌素家族(此处为抗霉枯草菌素)为70%,且表面活性素家族(此处为表面活性素a)为30%(模式2);
[0136]-将枯草芽孢杆菌培养物的上清液浓缩20倍并稀释20倍,以获得浓度为100g/ha的脂肽,其相对比例为:伊枯草菌素家族(此处为抗霉枯草菌素)为70%,且表面活性素家族(此处为表面活性素a)为30%(模式4);
[0137]-用相同体积的蒸馏水处理对照(对照模式)
[0138]
结果
[0139]
实验方案使得可比较来源于芽孢杆菌菌株培养物的上清液的不同组合物对小麦植株的地上部分的新鲜生物质(mf植株)以及新鲜根生物质(mf根)的重量的生物刺激作用。结果示于图4中。统计组在图上由字母a和b指示地上部分,并且a和b指示根。
[0140]-对小麦植株地上部分新鲜生物质的作用
[0141]
图4中所示的结果显示通过根和叶面施用(r+f)施用的含有用于用175mg/l抗霉枯草菌素和75mg/l表面活性素a的终浓度进行处理(模式2)和通过根施用(r)施用的含有用于用350mg/l抗霉枯草菌素和150mg/l表面活性素肽a的终浓度进行处理(模式4)的来自枯草芽孢杆菌上清液的组合物使得地上部分的新鲜生物质与未处理模式(对照模式)的地上部分的新鲜生物质相比显著提高。
[0142]
图4中所示的结果显示仅通过根(r)施用或根和叶面(r+f)施用的含有用于用90mg/l伊枯草菌素a、100mg/l芬芥素a和b以及60mg/l表面活性素a的终浓度进行处理(模式1)的来自解淀粉芽孢杆菌上清液的组合物远高于未处理对照,但属于包含对照的那些的2个统计组。对于通过根和叶面(r+f)施用而施用的模式4观察到了类似的结果。
[0143]-对小麦植株根部新鲜生物质的作用
[0144]
图4中所示的结果显示通过根和叶面(r+f)施用而施用的含有用于用175mg/l抗霉枯草菌素和75mg/l表面活性素a的终浓度进行处理(模式2)的与通过根(r)施用而施用的用于用350mg/l抗霉枯草菌素和150mg/l表面活性素a的终浓度进行处理(模式4)的来自枯草芽孢杆菌上清液的组合物使得根部的新鲜生物质与未处理模式(对照模式)的那些相比显著提高。
[0145]
图4中所示的结果显示在根和叶面水平处(r+f)施用的含有用于用90mg/l伊枯草菌素a、100mg/l芬芥素a和b以及60mg/l表面活性素a的终浓度进行处理的来自解淀粉芽孢杆菌上清液的组合物(模式1)远高于未处理的对照,但属于包含对照的那些的2个统计组。对于通过根(r)施用而施用的模式2与通过根和叶面(r+f)施用而施用的模式4,观察到了类似的结果。
[0146]
2.f脂肽组合物对小麦植株中叶绿素含量之提高的作用
[0147]
设备和方法
[0148]
实验方案与上述2.e段落中描述的方案相同。
[0149]
结果
[0150]
该实验方案使得可比较来源于芽孢杆菌菌株培养物上清液的不同脂肽组合物对小麦植株地上部分的叶绿素含量的生物刺激作用。结果示于图5中。统计组在图上由字母a、b和c指示。
[0151]
图5中所示的结果显示与未处理模式(对照模式)相比,通过根和叶面(r+f)施用而施用的含有用于处理的350mg/l抗霉枯草菌素和150mg/l表面活性素a的终浓度的枯草芽孢杆菌上清液的组合物(模式4)使得地上部分的叶绿素含量显著提高。
[0152]
这些结果还显示,通过根(r)或根和叶面(r+f)施用而施用的含有用于用90mg/l伊枯草菌素a、100mg/l芬芥素a和b以及60mg/l表面活性素a的终浓度进行处理的来自解淀粉芽孢杆菌上清液的组合物(模式1)使得地上部分的叶绿素含量与未处理模式(对照模式)的地上部分的叶绿素含量相比显著提高。
[0153]
实施例3:在浸泡/包被种子之后不同脂肽组合物对番茄种子的根尺寸的作用
[0154]
设备和方法
[0155]
该测试是在moneymaker品牌的番茄种子上进行的。预先通过将番茄种子在75/25v/v乙醇/水溶液中浸润2分钟,然后在5%漂白剂(次氯酸钠)加吐温(0.1%)中浸润30分钟,并且最后用水冲洗直至泡沫完全消失来进行消毒。
[0156]
然后将种子在具有不同纯度和浓度的脂肽溶液中浸泡1小时。
[0157]
将脂肽溶液进行浓缩(参见1.b中的方法),并且然后通过切向过滤进行纯化。
[0158]
然后将溶液在0.1%dmso中稀释以获得针对模式1为50和100μm、针对模式2为5、20和100μm、针对模式3为5、20和100μm、针对模式4为5、20和100μm的脂肽浓度。
[0159]
将种子垂直放置在培养皿中并冷藏一晚以使萌发标准化。然后,将盒置于22℃下的烘箱中,光周期为16小时。
[0160]
将蒸馏水中的0.1%dmso溶液用作实验的对照。
[0161]
每种模式在培养皿中重复5次。
[0162]
受试组合物如下:
[0163]-经浓缩和纯化的枯草芽孢杆菌培养物的上清液,其包含99%的抗霉枯草菌素(模式1);
[0164]-经浓缩和纯化的枯草芽孢杆菌培养物的上清液,其包含99%的表面活性素(模式2);
[0165]-经浓缩和纯化的枯草芽孢杆菌培养物的上清液,其包含99%的芬芥素(模式3);
[0166]-经浓缩和纯化的枯草芽孢杆菌培养物上清液,其包含79%的包含相对比例为40%抗霉枯草菌素和60%表面活性素的混合物(模式4);
[0167]-用相同体积的0.1%dmso溶液处理对照(对照)
[0168]
在将盒孵育7天之后测量根长度。用kolmogorov-smirnov检验来检验正态性,并用brown-forsythe检验或kruskal-wallis检验来检验方差的相等性。然后使变量进行具有事后student-newman-keuls检验的anova,其中p=0.05(95%置信水平或5%风险阈值)以突出显著的作用。使用sigmaplot14.0软件进行检验。统计组由字母a和b指示。
[0169]
结果
[0170]
实验方案使得可比较多种经纯化脂肽组合物对番茄种子的根长度的生物刺激作用。图6中所示的结果显示除了模式2之外,枯草芽孢杆菌上清液组合物对番茄种子根的生
长具有显著作用。统计组在图上由字母a和b指示。基于这些结果,可观察到从50μm浓度起用模式1(抗霉枯草菌素)进行处理对根长度的显著作用(p=0.028)。尽管在20μm和100μm的浓度下,用模式2(表面活性素)观察到对根长度的作用,但是它与对照条件没有统计学差异。从5μm起,模式3(芬芥素)(p=0.05)和4(抗霉枯草菌素和表面活性素的混合物)(p=0.009)观察到对根长度的生物刺激作用。
[0171]
实施例4:在水分胁迫条件下不同经纯化脂肽组合物对番茄植株的生长、光合效率和气孔导度的作用
[0172]
该测试的目的是研究在水分胁迫条件下,来自不同经浓缩和纯化的枯草芽孢杆菌上清液获得的脂肽组合物对番茄的生长、光合效率和气孔导度的作用。所研究的组合物包含不同纯度和不同浓度的脂肽。
[0173]
设备和方法
[0174]
植株材料
[0175]
该测试是根据fandango fi品牌的番茄种子进行的。
[0176]
将种子播种在幼苗斑块(klasmann peat)中。在萌发期间使水分保持接近于饱和(通过地下灌溉和喷施来提供水)。在2叶展开阶段(3周之后),将小植株移植到土壤盆中以进行测试。在移植期间,通过在移盆之前浸泡在水中来除去黏附至根上的泥炭。
[0177]
土壤和栽培盆的准备
[0178]
受试土壤是具有已知组成的沙质农业土壤。在测试之前,将其筛至10mm,然后测量干物质和保水能力。在测试开始时,每个盆含有以土壤最大保水能力(crmax)的70%浇灌的3.5kg生土。
[0179]
计算5个盆的平均重量,以使目标重量对应于crmax的70%。
[0180]
在没有水分胁迫的时期内,以相当于移盆土壤的水的crmax的70%的设定重量对盆进行浇灌。另外,供应2g/l hakaphos roude 8-12-24溶液的100ml的初始肥料。在水分胁迫之前还提供50ml该溶液。在水分胁迫期间,添加kno3和mgso4的溶液。
[0181]
水分胁迫
[0182]
在3周的水分胁迫期期间,未对盆进行浇灌,持续一周,然后使其在30%crmax大下维持一周,然后在50%crmax下维持一周。
[0183]
测试的持续时间
[0184]
将测试置于栽培温室中以确保半受控的温度和日照条件:
[0185]-温度:白昼25℃/黑夜20℃
[0186]-光周期:14小时的白昼/10小时的黑夜
[0187]
温室的最低亮度调节为175w/m2。低于此亮度,将打开照明并补偿亮度值。超过500w/m2的亮度时遮阳物伸出,并回调低于450w/m2。
[0188]
受试模式
[0189]
将不同的组合物投放三次。对于每次投放,每盆提供10ml组合物。第一次投放是在移盆时进行的,这次投放是对土壤的投放。其他投放是通过叶面喷施进行的。第二次投放是在栽培的3周之后和水分胁迫开始之前两天进行的,第三次是在水分胁迫10天之后进行的。对照模式用相同体积的蒸馏水处理。
[0190]
受试模式如下,并且每种模式包含6个重复盆。
[0191]
受试组合物如下:
[0192]-用相同体积的蒸馏水处理的对照(对照)
[0193]-纯化至纯度为30%(脂肽质量/总干质量)的经浓缩的枯草芽孢杆菌培养物的上清液,且其相对比例为80%抗霉枯草菌素和20%表面活性素。以75g/ha的脂肽的比例施用该组合物(模式1);
[0194]-纯化至纯度为30%(脂肽质量/总干质量)的经浓缩的枯草芽孢杆菌培养物的上清液,且其相对比例为80%抗霉枯草菌素和20%表面活性素。以150g/ha的脂肽的比例施用该组合物(模式2);
[0195]-纯化至纯度为99%(脂肽质量/总干质量)的经浓缩的枯草芽孢杆菌培养物的上清液,且其相对比例为80%抗霉枯草菌素和20%表面活性素。以150g/ha的脂肽的比例施用该组合物(模式3);
[0196]
测量了水分胁迫开始与结束之间植株的高度增长,水分胁迫开始和结束时的光合效率以及水分胁迫开始和结束时的气孔导度,并与对照模式进行比较。然后使变量进行anova和kruskal-wallis检验,其中p=0.05(95%置信水平或5%风险阈值)来突出显著的作用。使用statgraphics centurion xv软件-版本15.2.06来进行检验。统计组由字母a、b和c指示。
[0197]
结果
[0198]
番茄植株在水分胁迫开始与结束之间的高度增长
[0199]
将水分胁迫时期结束时的番茄植株的高度与水分胁迫时期之前的初始高度进行比较,生长增长示于图7中。模式1在统计学上与对照模式没有差异(p值=0.432)。用模式2观察到更好的生长,但是该模式在统计学上与对照模式没有差异(p值=0.124)。与对照模式相比,使用模式3观察到显著不同的增长(p值=0.008)。
[0200]
通过pam荧光测定法的光合效率
[0201]
在水分胁迫的开始时和结束时,通过pam荧光测定法测量光合效率。在胁迫下,以光合作用为代价,值(psii)降低且非光化学过程提高(热耗散和叶绿素荧光)。在图8a中,对于模式3观察到(psii)的轻微提高,但是该作用在统计学上不显著(p值=0.4932)。在图8b中,模式2(统计学上不显著的作用)和模式3(统计学上显著的作用)(p值=0.0070)观察到(psii)的提高,因此这些模式比对照条件的胁迫更小。相比于对照条件,模式1具有较低的值(psii)(统计学上不显著的作用)。
[0202]
气孔导度
[0203]
用气孔计进行气孔导度测量。该装置用于测量叶的气孔导度。气孔导度是对通过叶的气孔的二氧化碳(co2)或水蒸汽的流量的测量。气孔是在叶顶部和底部上的小孔,并且负责使co和水分从外部空气中进入和排出至外部空气中。测量的单位是毫摩尔每平方米秒(mmol/m2s)。
[0204]
在图9a中,在水分胁迫开始时,模式1和3具有最高的气孔导度值,指示了更好的气孔开放,并且因此这些模式的胁迫更小,但这种作用没有统计学显著性(p值=0.0544)。在图9b中,在水分胁迫结束时,相比于对照模式和模式1,模式2和3具有更低的值(统计学上显著的作用,p值=0.000)。对于这些模式2和3,气孔已关闭,植株更好地保持水并且对干旱更具抗性。
[0205]
这些测试使得可详细说明包含在枯草芽孢杆菌经浓缩的上清液中的脂肽作为生物刺激剂的作用机制之一,即改善对水分胁迫的抗性。还观察到剂量效应,其中无论所述上清液的脂肽纯度如何,从150g/ha及更高获得了显著作用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1